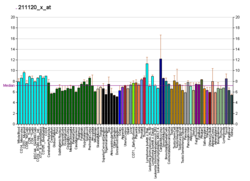
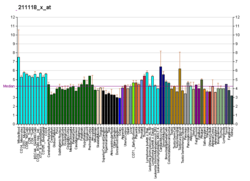
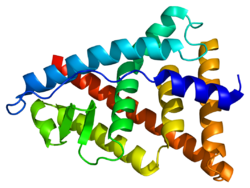
Эстрогеновый рецептор бета
| СОЭ2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ESR2 , ER-BETA, ESR-BETA, ESRB, ESTRB, Erb, NR3A2, рецептор эстрогена 2, ODG8 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | ОМИМ : 601663; МГИ : 109392; Гомологен : 1100; Генные карты : ESR2; ОМА :ESR2 – ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Рецептор эстрогена бета ( ERβ ), также известный как NR3A2 (подсемейство ядерных рецепторов 3, группа A, член 2), является одним из двух основных типов рецепторов эстрогена — ядерным рецептором , который активируется половым гормоном эстрогеном . [5] У людей ERβ кодируется геном ESR2 . [6]
Функция
ERβ является членом семейства рецепторов эстрогена и суперсемейства факторов транскрипции ядерных рецепторов . Продукт гена содержит N-концевой домен связывания ДНК и C-концевой домен связывания лиганда и локализуется в ядре, цитоплазме и митохондриях. При связывании с 17-β-эстрадиолом, эстриолом или родственными лигандами кодируемый белок образует гомодимеры или гетеродимеры с рецептором эстрогена α , которые взаимодействуют со специфическими последовательностями ДНК для активации транскрипции. Некоторые изоформы доминантно ингибируют активность других членов семейства рецепторов эстрогена. Было описано несколько альтернативно сплайсированных вариантов транскриптов этого гена, но полноразмерная природа некоторых из этих вариантов не была полностью охарактеризована. [7]
ERβ может подавлять пролиферацию клеток и противодействует действию ERα в репродуктивной ткани. [8] ERβ также может играть важную роль в адаптивной функции легких во время беременности. [9]
ERβ является мощным супрессором опухолей и играет решающую роль во многих типах рака, таких как рак предстательной железы и рак яичников . [10] [11]
Молочная железа
Мыши с нокаутом ERβ демонстрируют нормальное развитие молочных желез в период полового созревания и способны нормально лактировать . [12] [13] [14] Молочные железы взрослых девственных самок мышей неотличимы от молочных желез соответствующего возраста девственных самок мышей дикого типа. [12] Это контрастирует с мышами с нокаутом ERα , у которых наблюдается полное отсутствие развития молочных желез в период полового созревания и после него. [12] [14] Введение селективного агониста ERβ ERB -041 неполовозрелым овариэктомированным самкам крыс не вызвало никаких наблюдаемых эффектов в молочных железах, что дополнительно указывает на то, что ERβ не является маммотрофным . [15] [14] [16]
Хотя ERβ не требуется для пубертатного развития молочных желез, он может быть вовлечен в терминальную дифференциацию во время беременности , а также может быть необходим для поддержания организации и дифференциации эпителия молочной железы во взрослом возрасте. [17] [18] У старых самок мышей с нокаутом ERβ развивается тяжелое кистозное заболевание молочной железы , которое по внешнему виду похоже на постменопаузальную мастопатию , тогда как у старых самок мышей дикого типа этого не происходит. [13] Однако у мышей с нокаутом ERβ не только наблюдается дефицит сигнала ERβ в молочных железах, но и наблюдается дефицит воздействия прогестерона из-за нарушения формирования желтых тел . [13] [17] Это затрудняет приписывание предыдущих результатов сигналу ERβ молочной железы. [13] [17]
Было обнаружено, что селективный агонизм ERβ с диарилпропионитрилом (DPN) противодействует пролиферативным эффектам в молочных железах селективного агонизма ERα с пропилпиразолтриолом (PPT) у овариэктомированных самок крыс в постменопаузе. [19] [20] Аналогичным образом, повышенная экспрессия ERβ посредством лентивирусной инфекции у зрелых девственных самок крыс снижает пролиферацию молочных желез. [20] Сигнализация ERα оказывает пролиферативное действие как на нормальные линии клеток молочной железы, так и на линии клеток рака молочной железы , тогда как ERβ оказывает в целом антипролиферативное действие на такие линии клеток. [17] Однако было обнаружено, что ERβ оказывает пролиферативное действие на некоторые линии клеток молочной железы. [17]
Было обнаружено, что экспрессия ERα и ERβ в молочной железе меняется в течение менструального цикла и в состоянии овариэктомии у самок крыс. [20] В то время как у макак-резусов ERα в молочной железе снижается в ответ на повышенный уровень эстрадиола, экспрессия ERβ в молочных железах не снижается. [21] Экспрессия ERα и ERβ в молочных железах также различается в течение жизни у самок мышей . [ 22 ] Экспрессия ERα в молочной железе выше , а экспрессия ERβ в молочной железе ниже у молодых самок мышей, в то время как экспрессия ERα в молочной железе ниже, а экспрессия ERβ в молочной железе выше у старых самок мышей, а также у рожавших самок мышей. [22] Пролиферация молочной железы и чувствительность к эстрогену выше у молодых самок мышей, чем у старых или рожавших самок мышей, особенно во время пубертатного развития молочной железы. [22]
Распределение в тканях
ERβ экспрессируется многими тканями , включая матку , [23] моноциты крови и тканевые макрофаги, клетки эпителия толстой кишки и легких, а также в эпителии простаты и в злокачественных аналогах этих тканей. Кроме того, ERβ обнаруживается по всему мозгу в разных концентрациях в разных нейронных кластерах. [24] [25] ERβ также высоко экспрессируется в нормальном эпителии молочной железы, хотя его экспрессия снижается с прогрессированием рака. [26] ERβ экспрессируется во всех подтипах рака молочной железы. [27] Противоречия относительно экспрессии белка ERβ препятствовали изучению ERβ, но были получены и хорошо проверены высокочувствительные моноклональные антитела для решения этих проблем. [28]
Аномалии ERβ
Функция ERβ связана с различными сердечно-сосудистыми мишенями, включая АТФ-связывающий кассетный транспортер A1 (ABCA1) и аполипопротеин A1 (ApoA-1) . Полиморфизм может влиять на функцию ERβ и приводить к измененным реакциям у женщин в постменопаузе, получающих заместительную гормональную терапию . [29] Аномалии в экспрессии генов, связанные с ERβ, также связаны с расстройством аутистического спектра . [30]
Болезнь
Сердечно-сосудистые заболевания
Было показано, что мутации в ERβ влияют на кардиомиоциты , клетки, которые составляют большую часть сердца, и могут привести к повышенному риску сердечно-сосудистых заболеваний (ССЗ). Существует неравенство в распространенности ССЗ между женщинами до и после менопаузы, и это различие можно объяснить уровнями эстрогена. Существует много типов рецепторов ERβ, которые помогают регулировать экспрессию генов и последующее здоровье в организме, но связывание 17βE2 (естественного эстрогена) в частности улучшает сердечный метаболизм. Сердце использует много энергии в форме АТФ, чтобы должным образом перекачивать кровь и поддерживать физиологические потребности для того, чтобы жить, и 17βE2 помогает, увеличивая эти уровни АТФ миокарда и дыхательную функцию. [31]
Кроме того, 17βE2 может изменять сигнальные пути миокарда и стимулировать регенерацию миоцитов, что может помочь в ингибировании гибели клеток миоцитов. Сигнальный путь ERβ играет роль как в вазодилатации , так и в артериальной дилатации, что способствует здоровому сердечному ритму и снижению артериального давления у человека. Эта регуляция может увеличить эндотелиальную функцию и артериальную перфузию , оба из которых важны для здоровья миоцитов. Таким образом, изменения в этом сигнальном пути из-за мутации ERβ могут привести к гибели клеток миоцитов от физиологического стресса. В то время как ERα играет более глубокую роль в регенерации после гибели клеток миоцитов, ERβ все еще может помочь, увеличивая активацию эндотелиальных клеток-предшественников и последующую сердечную функцию. [32]
болезнь Альцгеймера
Генетическая изменчивость ERβ зависит как от пола, так и от возраста, а полиморфизм ERβ может привести к ускоренному старению мозга, когнитивным нарушениям и развитию патологии AD. Подобно сердечно-сосудистым заболеваниям, женщины в постменопаузе имеют повышенный риск развития болезни Альцгеймера (AD) из-за потери эстрогена, что влияет на правильное старение гиппокампа , выживание и регенерацию нейронов и метаболизм амилоида . мРНК ERβ высоко экспрессируется в гиппокампальной формации, области мозга, которая связана с памятью. Эта экспрессия способствует повышению выживаемости нейронов и помогает защитить от нейродегенеративных заболеваний, таких как AD. Патология AD также связана с накоплением амилоидного бета-пептида (Aβ). Хотя правильная концентрация Aβ в мозге важна для здорового функционирования, слишком большая концентрация может привести к когнитивным нарушениям. Таким образом, ERβ помогает контролировать уровни Aβ, поддерживая белок, из которого он происходит, белок-предшественник β-амилоида. ERβ помогает, повышая регуляцию инсулин-деградирующего фермента (IDE), что приводит к деградации β-амилоида, когда уровни накопления начинают расти. Однако при болезни Альцгеймера недостаток ERβ вызывает снижение этой деградации и увеличение накопления бляшек. [33]
ERβ также играет роль в регуляции APOE , фактора риска болезни Альцгеймера, который перераспределяет липиды по клеткам. Экспрессия APOE в гиппокампе специфически регулируется 17βE2, влияя на обучение и память у людей, страдающих болезнью Альцгеймера. Таким образом, эстрогеновая терапия с использованием ERβ-таргетного подхода может использоваться в качестве метода профилактики болезни Альцгеймера как до, так и в начале менопаузы. Взаимодействие между ERα и ERβ может приводить к антагонистическим действиям в мозге, поэтому ERβ-таргетный подход может усиливать терапевтические нейронные реакции независимо от ERα. Терапевтически ERβ может использоваться как у мужчин, так и у женщин для регуляции образования бляшек в мозге. [34]
Нейропротекторные преимущества
Синаптическая сила и пластичность
Уровни ERβ могут определять как синаптическую силу, так и нейропластичность посредством модификации нейронной структуры. Изменения в уровнях эндогенного эстрогена вызывают изменения в дендритной архитектуре гиппокампа, что влияет на нейронную сигнализацию и пластичность. В частности, более низкие уровни эстрогена приводят к уменьшению дендритных шипиков и неправильной сигнализации, что подавляет пластичность мозга. Однако лечение 17βE2 может обратить этот эффект вспять, давая ему возможность изменять структуру гиппокампа. В результате связи между дендритной архитектурой и долговременной потенциацией (LTP) ERβ может усиливать LTP и приводить к увеличению синаптической силы. Кроме того, 17βE2 способствует нейрогенезу в развивающихся нейронах гиппокампа и нейронах в субвентрикулярной зоне и зубчатой извилине взрослого человеческого мозга. В частности, ERβ увеличивает пролиферацию клеток-предшественников для создания новых нейронов и может быть увеличена в более позднем возрасте с помощью лечения 17βE2. [35] [36]
Лиганды
Агонисты
Неселективный
- Эндогенные эстрогены (например, эстрадиол , эстрон , эстриол , эстетрол )
- Натуральные эстрогены (например, конъюгированные эстрогены )
- Синтетические эстрогены (например, этинилэстрадиол , диэтилстильбэстрол )
Избирательный
Агонисты ERβ, селективные по отношению к ERα, включают:
- 20-Гидроксиэкдизон (экдистерон, 20-HE, 20-E) — фитоэкдистероид [37]
- 3β-Андростандиол (3β-диол) – эндогенный
- 8β-ВЭ 2
- АС-186
- Апигенин – фитоэстроген [38]
- Дайдзеин – фитоэстроген [38]
- DCW234
- Дегидроэпиандростерон (ДГЭА) – эндогенный
- Диарилпропионитрил (ДПН)
- ERB-79 и его активный энантиомер ERB-26
- ERB-196 (WAY-202196)
- Эртеберель (SERBA-1, LY-500307)
- FERb 033 – 62-кратная селективность для ERβ по сравнению с ERα [39]
- Генистеин – фитоэстроген; 16-кратная селективность к ERβ по сравнению с ERα [38]
- Ликиритигенин ( Менерба ) – фитоэстроген [38]
- Пендулетин – фитоэстроген [38]
- Принаберел (ERB-041, WAY-202041)
- S-Equol ((S)-4',7-изофлавандиол) – фитоэстроген; 13-кратная селективность к ERβ по сравнению с ERα [38]
- ПУТЬ-166818
- ПУТЬ-200070
- ПУТЬ-214156
Антагонисты
Неселективный
- Селективные модуляторы эстрогеновых рецепторов (например, тамоксифен , ралоксифен ) [40]
- Антиэстрогены (например, фулвестрант , ICI-164384 )
Избирательный
Антагонисты ERβ, селективные по отношению к ERα, включают:
- ПХТПП
- ( R , R )-Тетрагидрохризен (( R , R )-ТГК) – на самом деле не селективен в отношении ERα, а скорее является агонистом, а не антагонистом ERα
Сродства
| Лиганд | Другие имена | Относительное сродство связывания (ОСС, %) а | Абсолютное сродство связывания (K i , нМ) а | Действие | ||
|---|---|---|---|---|---|---|
| ЭРα | ЭРβ | ЭРα | ЭРβ | |||
| Эстрадиол | E2; 17β-Эстрадиол | 100 | 100 | 0,115 (0,04–0,24) | 0,15 (0,10–2,08) | Эстроген |
| Эстрон | E1; 17-кетоэстрадиол | 16.39 (0.7–60) | 6,5 (1,36–52) | 0,445 (0,3–1,01) | 1,75 (0,35–9,24) | Эстроген |
| Эстриол | E3; 16α-ОН-17β-E2 | 12.65 (4.03–56) | 26 (14,0–44,6) | 0,45 (0,35–1,4) | 0,7 (0,63–0,7) | Эстроген |
| Эстетрол | E4; 15α,16α-Ди-ОН-17β-E2 | 4.0 | 3.0 | 4.9 | 19 | Эстроген |
| Альфатрадиол | 17α-Эстрадиол | 20,5 (7–80,1) | 8.195 (2–42) | 0,2–0,52 | 0,43–1,2 | Метаболит |
| 16-Эпиэстриол | 16β-гидрокси-17β-эстрадиол | 7,795 (4,94–63) | 50 | ? | ? | Метаболит |
| 17-Эпиэстриол | 16α-гидрокси-17α-эстрадиол | 55,45 (29–103) | 79–80 | ? | ? | Метаболит |
| 16,17-эпиестриол | 16β-гидрокси-17α-эстрадиол | 1.0 | 13 | ? | ? | Метаболит |
| 2-гидроксиэстрадиол | 2-ОН-Е2 | 22 (7–81) | 11–35 | 2.5 | 1.3 | Метаболит |
| 2-метоксиэстрадиол | 2-МеО-Е2 | 0,0027–2,0 | 1.0 | ? | ? | Метаболит |
| 4-гидроксиэстрадиол | 4-ОН-Е2 | 13 (8–70) | 7–56 | 1.0 | 1.9 | Метаболит |
| 4-метоксиэстрадиол | 4-МеО-Е2 | 2.0 | 1.0 | ? | ? | Метаболит |
| 2-гидроксиэстрон | 2-ОН-Е1 | 2,0–4,0 | 0,2–0,4 | ? | ? | Метаболит |
| 2-метоксиэстрон | 2-МеО-Е1 | <0,001–<1 | <1 | ? | ? | Метаболит |
| 4-гидроксиэстрон | 4-ОН-Е1 | 1,0–2,0 | 1.0 | ? | ? | Метаболит |
| 4-метоксиэстрон | 4-МеО-Е1 | <1 | <1 | ? | ? | Метаболит |
| 16α-Гидроксиэстрон | 16α-ОН-Е1; 17-кетоэстриол | 2,0–6,5 | 35 | ? | ? | Метаболит |
| 2-гидроксиэстриол | 2-ОН-Е3 | 2.0 | 1.0 | ? | ? | Метаболит |
| 4-метоксиэстриол | 4-МеО-Е3 | 1.0 | 1.0 | ? | ? | Метаболит |
| Эстрадиол сульфат | E2S; Эстрадиол 3-сульфат | <1 | <1 | ? | ? | Метаболит |
| Эстрадиол дисульфат | Эстрадиол 3,17β-дисульфат | 0,0004 | ? | ? | ? | Метаболит |
| Эстрадиол 3-глюкуронид | Е2-3Г | 0,0079 | ? | ? | ? | Метаболит |
| Эстрадиол 17β-глюкуронид | Е2-17Г | 0,0015 | ? | ? | ? | Метаболит |
| Эстрадиол 3-глюк. 17β-сульфат | Е2-3Г-17С | 0.0001 | ? | ? | ? | Метаболит |
| Эстрон сульфат | E1S; Эстрон 3-сульфат | <1 | <1 | >10 | >10 | Метаболит |
| Эстрадиол бензоат | ЭБ; Эстрадиол 3-бензоат | 10 | ? | ? | ? | Эстроген |
| Эстрадиол 17β-бензоат | Е2-17Б | 11.3 | 32.6 | ? | ? | Эстроген |
| Метиловый эфир эстрона | Эстрон 3-метиловый эфир | 0,145 | ? | ? | ? | Эстроген |
| энтр -Эстрадиол | 1-Эстрадиол | 1.31–12.34 | 9.44–80.07 | ? | ? | Эстроген |
| Эквилин | 7-Дегидроэстрон | 13 (4,0–28,9) | 13.0–49 | 0,79 | 0,36 | Эстроген |
| Эквиленин | 6,8-Дидегидроэстрон | 2.0–15 | 7,0–20 | 0,64 | 0,62 | Эстроген |
| 17β-Дигидроэквилин | 7-дегидро-17β-эстрадиол | 7.9–113 | 7.9–108 | 0,09 | 0,17 | Эстроген |
| 17α-Дигидроэквилин | 7-дегидро-17α-эстрадиол | 18,6 (18–41) | 14–32 | 0,24 | 0,57 | Эстроген |
| 17β-дигидроэквиленин | 6,8-Дидегидро-17β-эстрадиол | 35–68 | 90–100 | 0,15 | 0.20 | Эстроген |
| 17α-Дигидроэквиленин | 6,8-Дидегидро-17α-эстрадиол | 20 | 49 | 0,50 | 0,37 | Эстроген |
| Δ 8 -Эстрадиол | 8,9-дегидро-17β-эстрадиол | 68 | 72 | 0,15 | 0,25 | Эстроген |
| Δ 8 - Эстрон | 8,9-Дегидроэстрон | 19 | 32 | 0,52 | 0,57 | Эстроген |
| Этинилэстрадиол | EE; 17α-Этинил-17β-E2 | 120,9 (68,8–480) | 44,4 (2,0–144) | 0,02–0,05 | 0,29–0,81 | Эстроген |
| Местранол | ЭЭ 3-метиловый эфир | ? | 2.5 | ? | ? | Эстроген |
| Моксэстрол | RU-2858; 11β-Метокси-EE | 35–43 | 5–20 | 0,5 | 2.6 | Эстроген |
| Метилэстрадиол | 17α-Метил-17β-эстрадиол | 70 | 44 | ? | ? | Эстроген |
| Диэтилстильбестрол | ДЭС; Стильбэстрол | 129,5 (89,1–468) | 219,63 (61,2–295) | 0,04 | 0,05 | Эстроген |
| Гексэстрол | Дигидродиэтилстильбэстрол | 153,6 (31–302) | 60–234 | 0,06 | 0,06 | Эстроген |
| Диенэстрол | Дегидростильбестрол | 37 (20,4–223) | 56–404 | 0,05 | 0,03 | Эстроген |
| Бензестрол (B2) | – | 114 | ? | ? | ? | Эстроген |
| Хлортрианизен | ТАСЭ | 1.74 | ? | 15.30 | ? | Эстроген |
| трифенилэтилен | ТПЭ | 0,074 | ? | ? | ? | Эстроген |
| Трифенилбромэтилен | ТПБЭ | 2.69 | ? | ? | ? | Эстроген |
| Тамоксифен | ИКИ-46,474 | 3 (0,1–47) | 3,33 (0,28–6) | 3,4–9,69 | 2.5 | СЭРМ |
| Афимоксифен | 4-гидрокситамоксифен; 4-OHT | 100,1 (1,7–257) | 10 (0,98–339) | 2,3 (0,1–3,61) | 0,04–4,8 | СЭРМ |
| Торемифен | 4-Хлоротамоксифен; 4-CT | ? | ? | 7.14–20.3 | 15.4 | СЭРМ |
| Кломифен | МРЛ-41 | 25 (19,2–37,2) | 12 | 0.9 | 1.2 | СЭРМ |
| Циклофенил | F-6066; Сексовид | 151–152 | 243 | ? | ? | СЭРМ |
| Нафоксидин | У-11,000А | 30.9–44 | 16 | 0.3 | 0.8 | СЭРМ |
| Ралоксифен | – | 41,2 (7,8–69) | 5,34 (0,54–16) | 0,188–0,52 | 20.2 | СЭРМ |
| Арзоксифен | LY-353,381 | ? | ? | 0,179 | ? | СЭРМ |
| Лазофоксифен | КП-336,156 | 10.2–166 | 19.0 | 0,229 | ? | СЭРМ |
| Ормелоксифен | Центхроман | ? | ? | 0,313 | ? | СЭРМ |
| Левормелоксифен | 6720-CDRI; NNC-460,020 | 1.55 | 1.88 | ? | ? | СЭРМ |
| Оспемифен | Деаминогидрокситоремифен | 0,82–2,63 | 0,59–1,22 | ? | ? | СЭРМ |
| Базедоксифен | – | ? | ? | 0,053 | ? | СЭРМ |
| Этакстил | ГВ-5638 | 4.30 | 11.5 | ? | ? | СЭРМ |
| ИКИ-164,384 | – | 63,5 (3,70–97,7) | 166 | 0.2 | 0,08 | Антиэстроген |
| Фулвестрант | ИКИ-182,780 | 43,5 (9,4–325) | 21,65 (2,05–40,5) | 0,42 | 1.3 | Антиэстроген |
| Пропилпиразолтриол | ППT | 49 (10,0–89,1) | 0,12 | 0,40 | 92.8 | Агонист ERα |
| 16α-LE2 | 16α-Лактон-17β-эстрадиол | 14.6–57 | 0,089 | 0,27 | 131 | Агонист ERα |
| 16α-Йодо-E2 | 16α-Йодо-17β-эстрадиол | 30.2 | 2.30 | ? | ? | Агонист ERα |
| Метилпиперидинопиразол | МПП | 11 | 0,05 | ? | ? | антагонист ERα |
| Диарилпропионитрил | ДПН | 0,12–0,25 | 6.6–18 | 32.4 | 1.7 | Агонист ERβ |
| 8β-VE2 | 8β-Винил-17β-эстрадиол | 0,35 | 22,0–83 | 12.9 | 0,50 | Агонист ERβ |
| Принаберель | ERB-041; WAY-202,041 | 0,27 | 67–72 | ? | ? | Агонист ERβ |
| ЕРБ-196 | ПУТЬ-202,196 | ? | 180 | ? | ? | Агонист ERβ |
| Эртеберел | СЕРБА-1; LY-500,307 | ? | ? | 2.68 | 0,19 | Агонист ERβ |
| СЕРБА-2 | – | ? | ? | 14.5 | 1.54 | Агонист ERβ |
| Куместрол | – | 9,225 (0,0117–94) | 64,125 (0,41–185) | 0,14–80,0 | 0,07–27,0 | Ксеноэстроген |
| Генистеин | – | 0,445 (0,0012–16) | 33,42 (0,86–87) | 2.6–126 | 0,3–12,8 | Ксеноэстроген |
| Экволь | – | 0,2–0,287 | 0,85 (0,10–2,85) | ? | ? | Ксеноэстроген |
| Дайдзейн | – | 0,07 (0,0018–9,3) | 0,7865 (0,04–17,1) | 2.0 | 85.3 | Ксеноэстроген |
| Биоханин А | – | 0,04 (0,022–0,15) | 0,6225 (0,010–1,2) | 174 | 8.9 | Ксеноэстроген |
| Кемпферол | – | 0,07 (0,029–0,10) | 2,2 (0,002–3,00) | ? | ? | Ксеноэстроген |
| Нарингенин | – | 0,0054 (<0,001–0,01) | 0,15 (0,11–0,33) | ? | ? | Ксеноэстроген |
| 8-пренилнарингенин | 8-ПН | 4.4 | ? | ? | ? | Ксеноэстроген |
| Кверцетин | – | <0,001–0,01 | 0,002–0,040 | ? | ? | Ксеноэстроген |
| Иприфлавон | – | <0,01 | <0,01 | ? | ? | Ксеноэстроген |
| Мироэстрол | – | 0,39 | ? | ? | ? | Ксеноэстроген |
| Дезоксимироэстрол | – | 2.0 | ? | ? | ? | Ксеноэстроген |
| β-ситостерин | – | <0,001–0,0875 | <0,001–0,016 | ? | ? | Ксеноэстроген |
| Ресвератрол | – | <0,001–0,0032 | ? | ? | ? | Ксеноэстроген |
| α-Зеараленол | – | 48 (13–52,5) | ? | ? | ? | Ксеноэстроген |
| β-Зеараленол | – | 0,6 (0,032–13) | ? | ? | ? | Ксеноэстроген |
| Зеранол | α-Зеараланол | 48–111 | ? | ? | ? | Ксеноэстроген |
| Талеранол | β-Зеараланол | 16 (13–17,8) | 14 | 0.8 | 0.9 | Ксеноэстроген |
| Зеараленон | ДЗЕН | 7,68 (2,04–28) | 9,45 (2,43–31,5) | ? | ? | Ксеноэстроген |
| Зеараланон | ЗАН | 0,51 | ? | ? | ? | Ксеноэстроген |
| Бисфенол А | БФА | 0,0315 (0,008–1,0) | 0,135 (0,002–4,23) | 195 | 35 | Ксеноэстроген |
| Эндосульфан | ЭЦП | <0,001–<0,01 | <0,01 | ? | ? | Ксеноэстроген |
| Кепоне | Хлордекон | 0,0069–0,2 | ? | ? | ? | Ксеноэстроген |
| о,п' -ДДТ | – | 0,0073–0,4 | ? | ? | ? | Ксеноэстроген |
| п,п' -ДДТ | – | 0,03 | ? | ? | ? | Ксеноэстроген |
| Метоксихлор | p,p' -Диметокси-ДДТ | 0,01 (<0,001–0,02) | 0,01–0,13 | ? | ? | Ксеноэстроген |
| ХПТЭ | Гидроксихлор; p,p'- OH-ДДТ | 1,2–1,7 | ? | ? | ? | Ксеноэстроген |
| Тестостерон | Т; 4-Андростенолон | <0,0001–<0,01 | <0,002–0,040 | >5000 | >5000 | Андрогены |
| Дигидротестостерон | ДГТ; 5α-андростанолон | 0,01 (<0,001–0,05) | 0,0059–0,17 | 221–>5000 | 73–1688 | Андрогены |
| Нандролон | 19-нортестостерон; 19-НТ | 0,01 | 0,23 | 765 | 53 | Андрогены |
| Дегидроэпиандростерон | ДГЭА; Прастерон | 0,038 (<0,001–0,04) | 0,019–0,07 | 245–1053 | 163–515 | Андрогены |
| 5-Андростенедиол | A5; Андростенедиол | 6 | 17 | 3.6 | 0.9 | Андрогены |
| 4-Андростенедиол | – | 0,5 | 0,6 | 23 | 19 | Андрогены |
| 4-Андростендион | А4; Андростендион | <0,01 | <0,01 | >10000 | >10000 | Андрогены |
| 3α-Андростандиол | 3α-Адиол | 0,07 | 0.3 | 260 | 48 | Андрогены |
| 3β-Андростандиол | 3β-Адиол | 3 | 7 | 6 | 2 | Андрогены |
| Андростандион | 5α-Андростандион | <0,01 | <0,01 | >10000 | >10000 | Андрогены |
| Этиохоландион | 5β-Андростандион | <0,01 | <0,01 | >10000 | >10000 | Андрогены |
| Метилтестостерон | 17α-Метилтестостерон | <0,0001 | ? | ? | ? | Андрогены |
| Этинил-3α-андростандиол | 17α-Этинил-3α-адиол | 4.0 | <0,07 | ? | ? | Эстроген |
| Этинил-3β-андростандиол | 17α-Этинил-3β-адиол | 50 | 5.6 | ? | ? | Эстроген |
| прогестерон | P4; 4-прегнедион | <0,001–0,6 | <0,001–0,010 | ? | ? | Прогестаген |
| Норэтистерон | NET; 17α-Этинил-19-NT | 0,085 (0,0015–<0,1) | 0,1 (0,01–0,3) | 152 | 1084 | Прогестаген |
| Норэтинодрелл | 5(10)-норэтистерон | 0,5 (0,3–0,7) | <0,1–0,22 | 14 | 53 | Прогестаген |
| Тиболон | 7α-Метилнорэтинодрэль | 0,5 (0,45–2,0) | 0,2–0,076 | ? | ? | Прогестаген |
| Δ 4 -Тиболон | 7α-Метилнорэтистерон | 0,069–<0,1 | 0,027–<0,1 | ? | ? | Прогестаген |
| 3α-гидрокситиболон | – | 2,5 (1,06–5,0) | 0,6–0,8 | ? | ? | Прогестаген |
| 3β-гидрокситиболон | – | 1,6 (0,75–1,9) | 0,070–0,1 | ? | ? | Прогестаген |
| Сноски: a = (1) Значения сродства связывания имеют формат «медиана (диапазон)» (# (#–#)), «диапазон» (#–#) или «значение» (#) в зависимости от доступных значений. Полные наборы значений в пределах диапазонов можно найти в коде Wiki. (2) Сродство связывания определялось с помощью исследований смещения в различных системах in vitro с меченым эстрадиолом и человеческими белками ERα и ERβ (за исключением значений ERβ из Kuiper et al. (1997), которые являются крысиными ERβ). Источники: см. страницу шаблона. | ||||||
Взаимодействия
Было показано, что бета-рецептор эстрогена взаимодействует с:
Ссылки
- ^ abc GRCh38: Ensembl выпуск 89: ENSG00000140009 – Ensembl , май 2017 г.
- ^ abc GRCm38: Ensembl выпуск 89: ENSMUSG00000021055 – Ensembl , май 2017 г.
- ^ "Human PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ "Mouse PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Kuiper GG, Enmark E, Pelto-Huikko M, Nilsson S, Gustafsson JA (июнь 1996 г.). «Клонирование нового рецептора, экспрессируемого в простате и яичниках крыс». Труды Национальной академии наук Соединенных Штатов Америки . 93 (12): 5925– 5930. doi : 10.1073/pnas.93.12.5925 . PMC 39164. PMID 8650195 .
- ^ Mosselman S, Polman J, Dijkema R (август 1996 г.). «ER beta: идентификация и характеристика нового человеческого рецептора эстрогена». FEBS Letters . 392 (1): 49– 53. Bibcode : 1996FEBSL.392...49M. doi : 10.1016/0014-5793(96)00782-X . PMID 8769313. S2CID 85795649.
- ^ «Ген Энтрез: рецептор 2 эстрогена ESR2 (бета ER)» .
- ^ Weihua Z, Saji S, Mäkinen S, Cheng G, Jensen EV, Warner M, Gustafsson JA (май 2000 г.). «Рецептор эстрогена (ER) бета, модулятор ERalpha в матке». Труды Национальной академии наук Соединенных Штатов Америки . 97 (11): 5936– 5941. Bibcode : 2000PNAS...97.5936W. doi : 10.1073/pnas.97.11.5936 . PMC 18537. PMID 10823946 .
- ^ Carey MA, Card JW, Voltz JW, Germolec DR, Korach KS, Zeldin DC (август 2007 г.). «Влияние пола и половых гормонов на физиологию и заболевания легких: уроки исследований на животных». American Journal of Physiology. Клеточная и молекулярная физиология легких . 293 (2): L272 – L278 . doi :10.1152/ajplung.00174.2007. PMID 17575008. S2CID 3175960.
- ^ Stettner M, Kaulfuss S, Burfeind P, Schweyer S, Strauss A, Ringert RH, Thelen P (октябрь 2007 г.). «Значение экспрессии рецептора эстрогена бета для антипролиферативных эффектов, наблюдаемых при использовании ингибиторов гистондеацетилазы и фитоэстрогенов при лечении рака простаты». Molecular Cancer Therapeutics . 6 (10): 2626– 2633. doi : 10.1158/1535-7163.MCT-07-0197 . PMID 17913855.
- ^ Kyriakidis I, Papaioannidou P (июнь 2016 г.). «Эстрогеновый рецептор бета и рак яичников: ключ к патогенезу и ответу на терапию». Архивы гинекологии и акушерства . 293 (6): 1161– 1168. doi :10.1007/s00404-016-4027-8. PMID 26861465. S2CID 25627227.
- ^ abc Couse JF, Korach KS (июнь 1999). «Мыши с нулевым рецептором эстрогена: чему мы научились и куда они нас приведут?». Endocrine Reviews . 20 (3): 358–417 . doi : 10.1210/edrv.20.3.0370 . PMID 10368776.
- ^ abcd Gustafsson JA, Warner M (ноябрь 2000 г.). «Эстрогеновый рецептор бета в груди: роль в чувствительности к эстрогену и развитии рака груди». Журнал стероидной биохимии и молекулярной биологии . 74 (5): 245– 248. doi :10.1016/S0960-0760(00)00130-8. PMID 11162931. S2CID 39714457.
- ^ abc Nilsson S, Gustafsson JÅ (2010). «Рецепторы эстрогена: их действия и функциональная роль в здоровье и болезни». Ядерные рецепторы . стр. 91–141 . doi :10.1007/978-90-481-3303-1_5. ISBN 978-90-481-3302-4.
- ^ Nilsson S, Gustafsson JÅ (январь 2011). «Рецепторы эстрогена: терапия, направленная на подтипы рецепторов». Клиническая фармакология и терапия . 89 (1): 44– 55. doi :10.1038/clpt.2010.226. PMID 21124311. S2CID 22724380.
- ^ Harris HA, Albert LM, Leathurby Y, Malamas MS, Mewshaw RE, Miller CP и др. (октябрь 2003 г.). «Оценка агониста бета-рецептора эстрогена в моделях заболеваний человека на животных». Эндокринология . 144 (10): 4241– 4249. doi : 10.1210/en.2003-0550 . PMID 14500559.
- ^ abcde Thomas C, Gustafsson JÅ (2019). "Рецептор эстрогена β и рак молочной железы". Cancer Drug Discovery and Development . стр. 309–342 . doi :10.1007/978-3-319-99350-8_12. ISBN 978-3-319-99349-2. ISSN 2196-9906.
- ^ Dey P, Barros RP, Warner M, Ström A, Gustafsson JÅ (декабрь 2013 г.). «Взгляд на механизмы действия рецептора эстрогена β в груди, простате, толстой кишке и ЦНС». Журнал молекулярной эндокринологии . 51 (3): T61 – T74 . doi : 10.1530/JME-13-0150 . PMID 24031087.
- ^ Song X, Pan ZZ (май 2012). «Агонист эстрогеновых рецепторов-бета диарилпропионитрил противодействует эстрогенной активности агониста эстрогеновых рецепторов-альфа пропилпиразол-триола в молочной железе овариэктомированных крыс Sprague Dawley». Журнал стероидной биохимии и молекулярной биологии . 130 ( 1– 2): 26– 35. doi : 10.1016/j.jsbmb.2011.12.018. PMID 22266284. S2CID 23865463.
- ^ abc Song, X. (2014). Рецептор эстрогена бета — отрицательный регулятор пролиферации клеток молочной железы. Диссертация и тезисы аспирантуры. 259. https://scholarworks.uvm.edu/graddis/259
- ^ Cheng G, Li Y, Omoto Y, Wang Y, Berg T, Nord M и др. (январь 2005 г.). «Дифференциальная регуляция рецепторов эстрогена (ER)альфа и ERбета в молочной железе приматов». Журнал клинической эндокринологии и метаболизма . 90 (1): 435–444 . doi : 10.1210/jc.2004-0861 . PMID 15507513.
- ^ abc Dall GV, Hawthorne S, Seyed-Razavi Y, Vieusseux J, Wu W, Gustafsson JA и др. (июнь 2018 г.). «Подтипы рецепторов эстрогена определяют пролиферативную природу молочной железы». The Journal of Endocrinology . 237 (3): 323– 336. doi : 10.1530/JOE-17-0582 . PMID 29636363.
- ^ Hapangama DK, Kamal AM, Bulmer JN (март 2015 г.). «Рецептор эстрогена β: страж эндометрия». Human Reproduction Update . 21 (2): 174–193 . doi : 10.1093/humupd/dmu053 . PMID 25305176.
- ^ Couse JF, Lindzey J, Grandien K, Gustafsson JA, Korach KS (ноябрь 1997 г.). «Распределение тканей и количественный анализ рибонуклеиновой кислоты рецептора эстрогена-альфа (ERalpha) и рецептора эстрогена-бета (ERbeta) у мышей дикого типа и мышей с нокаутом ERalpha». Эндокринология . 138 (11): 4613– 4621. doi : 10.1210/endo.138.11.5496 . PMID 9348186.
- ^ Koehler KF, Helguero LA, Haldosén LA, Warner M, Gustafsson JA (май 2005 г.). «Размышления об открытии и значении рецептора эстрогена бета». Endocrine Reviews . 26 (3): 465–478 . doi : 10.1210/er.2004-0027 . PMID 15857973.
- ^ Leygue E, Dotzlaw H, Watson PH, Murphy LC (август 1998 г.). «Измененная экспрессия РНК-мессенджера альфа- и бета-рецепторов эстрогена во время опухолей молочной железы у человека». Cancer Research . 58 (15): 3197–3201 . PMID 9699641.
- ^ Reese JM, Suman VJ, Subramaniam M, Wu X, Negron V, Gingery A и др. (октябрь 2014 г.). "ERβ1: характеристика, прогноз и оценка стратегий лечения при ERα-положительном и -отрицательном раке груди". BMC Cancer . 14 (749): 749. doi : 10.1186/1471-2407-14-749 . PMC 4196114 . PMID 25288324.
- ^ Hawse JR, Carter JM, Aspros KG, Bruinsma ES, Koepplin JW, Negron V и др. (январь 2020 г.). «Оптимизированное иммуногистохимическое обнаружение рецептора эстрогена бета с использованием двух проверенных моноклональных антител подтверждает его экспрессию в нормальных и злокачественных тканях молочной железы». Breast Cancer Research and Treatment . 179 (1): 241– 249. doi :10.1007/s10549-019-05441-3. PMC 6989344 . PMID 31571071. S2CID 203609306.
- ^ Darabi M, Ani M, Panjehpour M, Rabbani M, Movahedian A, Zarean E (январь–февраль 2011 г.). «Влияние полиморфизма рецептора эстрогена β A1730G на экспрессию гена ABCA1 в ответ на заместительную гормональную терапию в постменопаузе». Genetic Testing and Molecular Biomarkers . 15 ( 1– 2): 11– 15. doi :10.1089/gtmb.2010.0106. PMID 21117950.
- ^ Crider A, Thakkar R, Ahmed AO, Pillai A (9 сентября 2014 г.). «Нарушение регуляции рецептора эстрогена бета (ERβ), ароматазы (CYP19A1) и коактиваторов ER в средней лобной извилине у субъектов с расстройствами аутистического спектра». Molecular Autism . 5 (1): 46. doi : 10.1186/2040-2392-5-46 . PMC 4161836 . PMID 25221668.
- ^ Luo T, Kim JK (август 2016 г.). «Роль эстрогена и рецепторов эстрогена в кардиомиоцитах: обзор». Канадский журнал кардиологии . 32 (8): 1017– 1025. doi :10.1016/j.cjca.2015.10.021. PMC 4853290. PMID 26860777 .
- ^ Мука Т., Варгас К.Г., Джасперс Л., Вэнь К.Х., Дхана К., Витезова А. и др. (апрель 2016 г.). «Действие β-рецептора эстрогена на женскую сердечно-сосудистую систему: систематический обзор исследований на животных и людях». Матуритас . 86 : 28–43 . doi :10.1016/j.maturitas.2016.01.009. ПМИД 26921926.
- ^ Li R, Cui J, Shen Y (май 2014). «Мозговой пол имеет значение: эстроген в познании и болезни Альцгеймера». Молекулярная и клеточная эндокринология . 389 ( 1– 2): 13– 21. doi : 10.1016/j.mce.2013.12.018. PMC 4040318. PMID 24418360.
- ^ Zhao L, Woody SK, Chhibber A (ноябрь 2015 г.). «Эстрогенный рецептор β при болезни Альцгеймера: от механизмов к терапии». Ageing Research Reviews . 24 (Pt B): 178– 190. doi :10.1016/j.arr.2015.08.001. PMC 4661108. PMID 26307455.
- ^ Engler-Chiurazzi EB, Brown CM, Povroznik JM, Simpkins JW (октябрь 2017 г.). «Эстрогены как нейропротекторы: эстрогенные действия в контексте когнитивного старения и повреждения мозга». Progress in Neurobiology . 157 : 188– 211. doi :10.1016/j.pneurobio.2015.12.008. PMC 4985492. PMID 26891883 .
- ^ Варгас К.Г., Милич Дж., Зацирагич А., Вэнь К.Х., Джасперс Л., Нано Дж. и др. (ноябрь 2016 г.). «Функции бета-рецептора эстрогена в женском мозге: систематический обзор». Матуритас . 93 : 41–57 . doi :10.1016/j.maturitas.2016.05.014. ПМИД 27338976.
- ^ Мария Кристина Парр; Пивен Чжао; Оливер Хаупт; Сандрин Чукуэгно Нгуеу; Йонас Хенгевосс; Карл Генрих Фритцемайер; Марион Пьехотта; Нильс Шлерер; Петер Мун; Вэнь-Я Чжэн; Мин-Йонг Се; Патрик Диль (2014). «Рецептор эстрогена бета участвует в гипертрофии скелетных мышц, вызванной фитоэкдистероидом экдистероном». Молекулярное питание и исследования продуктов питания . 58 (9): 1861– 1872. doi :10.1002/mnfr.201300806. PMID 24974955.
- ^ abcdef Hajirahimkhan A, Dietz BM, Bolton JL (май 2013 г.). «Ботаническая модуляция симптомов менопаузы: механизмы действия?». Planta Medica . 79 (7): 538– 553. doi :10.1055/s-0032-1328187. PMC 3800090. PMID 23408273 .
- ^ Minutolo F, Bertini S, Granchi C, Marchitiello T, Prota G, Rapposelli S и др. (февраль 2009 г.). «Структурные эволюции салицилальдоксимов как селективных агонистов эстрогеновых рецепторов бета». Журнал медицинской химии . 52 (3): 858– 867. doi :10.1021/jm801458t. PMID 19128016.
- ^ Barkhem T, Carlsson B, Nilsson Y, Enmark E, Gustafsson J, Nilsson S (июль 1998). «Дифференциальная реакция эстрогеновых рецепторов альфа и эстрогеновых рецепторов бета на частичные агонисты/антагонисты эстрогена». Молекулярная фармакология . 54 (1): 105– 112. doi :10.1124/mol.54.1.105. PMID 9658195.
- ^ Nakamura Y, Felizola SJ, Kurotaki Y, Fujishima F, McNamara KM, Suzuki T и др. (май 2013 г.). «Экспрессия циклина D1 (CCND1) участвует в эстрогеновом рецепторе бета (ERβ) при раке простаты человека». The Prostate . 73 (6): 590– 595. doi :10.1002/pros.22599. PMID 23060014. S2CID 39130053.
- ^ Огава С., Иноуэ С., Ватанабе Т., Хирои Х., Оримо А., Хосои Т. и др. (февраль 1998 г.). «Полная первичная структура человеческого эстрогенового рецептора бета (hER бета) и его гетеродимеризация с ER альфа in vivo и in vitro». Biochemical and Biophysical Research Communications . 243 (1): 122– 126. doi :10.1006/bbrc.1997.7893. PMID 9473491.
- ^ ab Poelzl G, Kasai Y, Mochizuki N, Shaul PW, Brown M, Mendelsohn ME (март 2000 г.). «Специфическая связь рецептора эстрогена бета с белком контрольной точки сборки веретена клеточного цикла, MAD2». Труды Национальной академии наук Соединенных Штатов Америки . 97 (6): 2836– 2839. Bibcode : 2000PNAS ...97.2836P. doi : 10.1073/pnas.050580997 . PMC 16016. PMID 10706629.
- ^ Wong CW, Komm B, Cheskis BJ (июнь 2001 г.). «Оценка структуры и функции взаимодействия ER alpha и beta с коактиваторами семейства SRC. Селективные лиганды ER». Биохимия . 40 (23): 6756– 6765. doi :10.1021/bi010379h. PMID 11389589.
- ^ Leo C, Li H, Chen JD (февраль 2000 г.). «Дифференциальные механизмы регуляции ядерного рецептора рецептор-ассоциированным коактиватором 3». Журнал биологической химии . 275 (8): 5976–5982 . doi : 10.1074/jbc.275.8.5976 . PMID 10681591.
- ^ Lee SK, Jung SY, Kim YS, Na SY, Lee YC, Lee JW (февраль 2001 г.). «Два отдельных домена взаимодействия с ядерными рецепторами и трансактивационная функция коинтегратора-2, зависящая от CREB-связывающего белка». Молекулярная эндокринология . 15 (2): 241– 254. doi : 10.1210/mend.15.2.0595 . PMID 11158331.
- ^ Ko L, Cardona GR, Iwasaki T, Bramlett KS, Burris TP, Chin WW (январь 2002 г.). «Ser-884, смежный с мотивом LXXLL коактиватора TRBP, определяет селективность для ER и TR». Молекулярная эндокринология . 16 (1): 128– 140. doi : 10.1210/mend.16.1.0755 . PMID 11773444.
- ^ Jung DJ, Na SY, Na DS, Lee JW (январь 2002 г.). «Молекулярное клонирование и характеристика CAPER, нового коактиватора активации белка-1 и рецепторов эстрогена». Журнал биологической химии . 277 (2): 1229– 1234. doi : 10.1074/jbc.M110417200 . PMID 11704680.
- ^ Migliaccio A, Castoria G, Di Domenico M, de Falco A, Bilancio A, Lombardi M и др. (октябрь 2000 г.). «Комплекс андрогеновых рецепторов-эстрадиоловых рецепторов бета-Src, индуцированный стероидами, запускает пролиферацию клеток рака простаты». The EMBO Journal . 19 (20): 5406– 5417. doi : 10.1093 /emboj/19.20.5406. PMC 314017. PMID 11032808.
- ^ Slentz-Kesler K, Moore JT, Lombard M, Zhang J, Hollingsworth R, Weiner MP (октябрь 2000 г.). «Идентификация гена Mnk2 человека (MKNK2) через взаимодействие белка с рецептором эстрогена бета». Genomics . 69 (1): 63–71 . doi :10.1006/geno.2000.6299. PMID 11013076.
Дальнейшее чтение
- Pettersson K, Gustafsson JA (2001). «Роль рецептора эстрогена бета в действии эстрогена». Annual Review of Physiology . 63 : 165–192 . doi :10.1146/annurev.physiol.63.1.165. PMID 11181953.
- Warner M, Saji S, Gustafsson JA (июль 2000 г.). «Нормальная и злокачественная молочная железа: свежий взгляд с ER beta на борту». Журнал биологии и неоплазии молочной железы . 5 (3): 289– 294. doi :10.1023/A:1009598828267. PMID 14973391. S2CID 34129981.
- Saxon LK, Turner CH (февраль 2005 г.). «Эстрогенный рецептор бета: антимеханостат?». Bone . 36 (2): 185– 192. doi :10.1016/j.bone.2004.08.003. PMID 15780944.
- Halachmi S, Marden E, Martin G, MacKay H, Abbondanza C, Brown M (июнь 1994). «Эстрогеновые рецептор-ассоциированные белки: возможные медиаторы гормон-индуцированной транскрипции». Science . 264 (5164): 1455– 1458. Bibcode :1994Sci...264.1455H. doi :10.1126/science.8197458. PMID 8197458.
- Schwabe JW, Chapman L, Finch JT, Rhodes D (ноябрь 1993 г.). «Кристаллическая структура домена связывания ДНК рецептора эстрогена, связанного с ДНК: как рецепторы различают элементы своего ответа». Cell . 75 (3): 567– 578. doi :10.1016/0092-8674(93)90390-C. PMID 8221895. S2CID 20795587.
- Chen H, Lin RJ, Schiltz RL, Chakravarti D, Nash A, Nagy L и др. (август 1997 г.). «Коактиватор ядерного рецептора ACTR — это новая гистонацетилтрансфераза, которая образует мультимерный комплекс активации с P/CAF и CBP/p300». Cell . 90 (3): 569– 580. doi : 10.1016/S0092-8674(00)80516-4 . PMID 9267036. S2CID 15284825.
- Pace P, Taylor J, Suntharalingam S, Coombes RC, Ali S (октябрь 1997 г.). «Человеческий рецептор эстрогена бета связывает ДНК аналогично рецептору эстрогена альфа и димеризуется с ним». Журнал биологической химии . 272 (41): 25832– 25838. doi : 10.1074/jbc.272.41.25832 . PMID 9325313.
- Бранденбергер А.В., Ти МК, Ли Дж.Ю., Чао В., Джаффе Р.Б. (октябрь 1997 г.). «Тканевое распределение мРНК рецепторов эстрогена альфа (ER-альфа) и бета (ER-бета) у плода человека в середине беременности». Журнал клинической эндокринологии и метаболизма . 82 (10): 3509–3512 . doi : 10.1210/jcem.82.10.4400 . ПМИД 9329394.
- Enmark E, Pelto-Huikko M, Grandien K, Lagercrantz S, Lagercrantz J, Fried G и др. (декабрь 1997 г.). «Структура гена бета-рецептора человеческого эстрогена, локализация в хромосомах и паттерн экспрессии». Журнал клинической эндокринологии и метаболизма . 82 (12): 4258– 4265. doi : 10.1210/jcem.82.12.4470 . PMID 9398750.
- Vladusic EA, Hornby AE, Guerra-Vladusic FK, Lupu R (январь 1998 г.). «Экспрессия варианта РНК-мессенджера рецептора эстрогена бета при раке груди». Cancer Research . 58 (2): 210– 214. PMID 9443393.
- Ogawa S, Inoue S, Watanabe T, Hiroi H, Orimo A, Hosoi T и др. (февраль 1998 г.). «Полная первичная структура человеческого эстрогенового рецептора бета (hER beta) и его гетеродимеризация с ER alpha in vivo и in vitro». Biochemical and Biophysical Research Communications . 243 (1): 122– 126. doi :10.1006/bbrc.1997.7893. PMID 9473491.
- Alves SE, Lopez V, McEwen BS, Weiland NG (март 1998 г.). «Дифференциальная колокализация рецептора эстрогена бета (ERbeta) с окситоцином и вазопрессином в паравентрикулярных и супраоптических ядрах мозга самок крыс: иммуноцитохимическое исследование». Труды Национальной академии наук Соединенных Штатов Америки . 95 (6): 3281– 3286. Bibcode : 1998PNAS...95.3281A. doi : 10.1073/pnas.95.6.3281 . PMC 19733. PMID 9501254 .
- Brandenberger AW, Tee MK, Jaffe RB (март 1998 г.). «МРНК эстрогеновых рецепторов альфа (ER-альфа) и бета (ER-бета) в нормальных клеточных линиях яичников, серозной цистаденокарциномы яичников и рака яичников: снижение регуляции ER-бета в неопластических тканях». Журнал клинической эндокринологии и метаболизма . 83 (3): 1025– 1028. doi : 10.1210/jcem.83.3.4788 . PMID 9506768.
- Moore JT, McKee DD, Slentz-Kesler K, Moore LB, Jones SA, Horne EL и др. (июнь 1998 г.). «Клонирование и характеристика бета-изоформ рецептора человеческого эстрогена». Biochemical and Biophysical Research Communications . 247 (1): 75– 78. doi :10.1006/bbrc.1998.8738. PMID 9636657.
- Ogawa S, Inoue S, Watanabe T, Orimo A, Hosoi T, Ouchi Y, Muramatsu M (август 1998 г.). «Молекулярное клонирование и характеристика человеческого эстрогенового рецептора betacx: потенциальный ингибитор действия эстрогена у человека». Nucleic Acids Research . 26 (15): 3505– 3512. doi :10.1093/nar/26.15.3505. PMC 147730. PMID 9671811 .
- Lu B, Leygue E, Dotzlaw H, Murphy LJ, Murphy LC, Watson PH (март 1998). «Варианты мРНК рецептора эстрогена бета в тканях человека и мышей». Молекулярная и клеточная эндокринология . 138 ( 1– 2): 199– 203. doi : 10.1016/S0303-7207(98)00050-1. PMID 9685228. S2CID 54243493.
- Seol W, Hanstein B, Brown M, Moore DD (октябрь 1998 г.). «Ингибирование действия рецептора эстрогена сиротским рецептором SHP (короткий гетеродимерный партнер)». Молекулярная эндокринология . 12 (10): 1551– 1557. doi : 10.1210/mend.12.10.0184 . PMID 9773978.
- Hanstein B, Liu H, Yancisin MC, Brown M (январь 1999). «Функциональный анализ новой изоформы эстрогенового рецептора бета». Молекулярная эндокринология . 13 (1): 129– 137. doi : 10.1210/mend.13.1.0234 . PMID 9892018.
- Видал О., Киндблом Л.Г., Олссон К. (июнь 1999 г.). «Экспрессия и локализация рецептора эстрогена-бета в мышиной и человеческой кости». Журнал исследований костей и минералов . 14 (6): 923–929 . doi :10.1359/jbmr.1999.14.6.923. PMID 10352100. S2CID 85604096.
Внешние ссылки
- Эстроген+Рецептор+бета в Национальной медицинской библиотеке США Медицинские предметные рубрики (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : Q92731 (рецептор эстрогена бета) на сайте PDBe-KB .
В данной статье использован текст из Национальной медицинской библиотеки США , являющийся общественным достоянием .