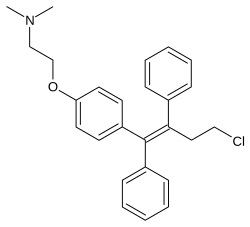
Торемифен
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / ˈ t ɔːr ə m ɪ f iː n / |
| Торговые наименования | Фарестон, другие |
| Другие имена | ( Z )-Торемифен; 4-хлортамоксифен; 4-КТ; Акаподен; CCRIS-8745; ФК-1157; ФК-1157а; ГТх-006; НК-622; НСК-613680 |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а608003 |
| Данные лицензии |
|
| Пути введения | Через рот |
| Класс наркотиков | Селективный модулятор рецепторов эстрогена |
| код АТС |
|
| Фармакокинетические данные | |
| Биодоступность | Хорошо/~100% [1] [2] |
| Связывание с белками | 99,7% [1] |
| Метаболизм | Печень ( CYP3A4 ) [5] [2] |
| Метаболиты | N-Дезметилторемифен; 4-Гидрокситоремифен; Оспемифен [3] [4] |
| Период полувыведения | Торемифен: 3–7 дней [1] Метаболиты: 4–21 день [2] [4] [1] |
| Выделение | Фекалии : 70% (в виде метаболитов) [2] |
| Идентификаторы | |
| |
| Номер CAS |
|
| CID PubChem |
|
| ИУФАР/БПС |
|
| DrugBank | |
| ChemSpider | |
| УНИИ |
|
| КЕГГ | |
| ЧЭБИ | |
| ChEMBL | |
| PDB-лиганд |
|
| Панель инструментов CompTox ( EPA ) |
|
| Информационная карта ECHA | 100.125.139 |
| Химические и физические данные | |
| Формула | С26Н28ClNО |
| Молярная масса | 405,97 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| (проверять) | |
Торемифен , продаваемый под торговой маркой Fareston, среди прочих, является лекарственным средством, которое используется для лечения рака молочной железы на поздних стадиях у женщин в постменопаузе . [4] [6] [3] Он принимается внутрь . [4]
Побочные эффекты торемифена включают приливы , потливость , тошноту , рвоту , головокружение , выделения из влагалища и вагинальное кровотечение . [5] [7] Он также может вызывать образование тромбов , нерегулярное сердцебиение , катаракту , нарушения зрения , повышение уровня печеночных ферментов , гиперплазию эндометрия и рак эндометрия . [5] Высокий уровень кальция в крови может наблюдаться у женщин с метастазами в костях . [5]
Препарат является селективным модулятором эстрогеновых рецепторов (SERM) и, следовательно, является смешанным агонистом - антагонистом эстрогеновых рецепторов (ER), биологической мишенью эстрогенов , таких как эстрадиол . [5] [7] Он оказывает эстрогенное действие на кости , печень и матку и антиэстрогенное действие на грудь . [6] [8] [9] [5] Он является производным трифенилэтилена и тесно связан с тамоксифеном . [10]
Торемифен был представлен для медицинского применения в 1997 году. [11] [12] Это был первый антиэстроген , представленный после тамоксифена в 1978 году. [13] Он доступен как дженерик в Соединенных Штатах . [14]
Медицинское применение
Торемифен одобрен для лечения метастатического рака молочной железы у женщин в постменопаузе с опухолями , положительными по рецепторам эстрогена или с неизвестным статусом . [4] [6] Это его единственное одобренное применение в Соединенных Штатах . [4] Он показывает эквивалентную эффективность тамоксифену при этом показании. [6] [15] Было обнаружено, что торемифен эффективен при лечении боли в груди и может быть более эффективным лекарством, чем тамоксифен при этом показании. [16] Он также оказывает превосходное воздействие на минеральную плотность костной ткани и липидный профиль , включая уровни холестерина и триглицеридов , по сравнению с тамоксифеном. [15] Сообщалось, что торемифен значительно улучшает симптомы гинекомастии у мужчин. [17]
Доступные формы
Торемифен выпускается в форме таблеток для приема внутрь по 60 мг . [18] [19]
Побочные эффекты
Побочные эффекты торемифена аналогичны таковым у тамоксифена. [5] Наиболее распространенным побочным эффектом являются приливы . [5] Другие побочные эффекты включают потоотделение , тошноту , рвоту , головокружение , выделения из влагалища и вагинальное кровотечение . [5] [7] У женщин с метастазами в костях может возникнуть гиперкальциемия . [5] Торемифен имеет небольшой риск тромбоэмболических событий . [5] Сообщалось о катаракте , изменении зрения и повышении уровня печеночных ферментов . [5] [7] Препарат удлиняет интервал QT и, следовательно, имеет риск потенциально фатальных аритмий . [5] Риск аритмий можно снизить, избегая использования у пациентов с гипокалиемией , гипомагниемией , уже существующим удлинением QT и у тех, кто принимает другие препараты, удлиняющие QT. [5] Поскольку торемифен оказывает эстрогенное действие на матку , он может увеличить риск гиперплазии эндометрия и рака эндометрия . [5]
Торемифен, по-видимому, безопаснее тамоксифена. [15] Он имеет более низкий риск венозной тромбоэмболии (ВТЭ) (например, тромбоэмболии легочной артерии ), инсульта и катаракты . [15] Более низкий риск ВТЭ может быть связан с тем, что тамоксифен снижает уровни антитромбина III в значительно большей степени, чем торемифен в дозе 60 или 200 мг/день. [15]
Взаимодействия
Торемифен является субстратом CYP3A4 , фермента цитохрома P450 , и, следовательно , препараты, которые индуцируют или ингибируют этот фермент, могут соответственно снижать или повышать уровень торемифена в организме. [5]
Фармакология
Фармакодинамика
Торемифен — селективный модулятор эстрогеновых рецепторов (SERM). [5] [7] [20] То есть, это селективный смешанный агонист-антагонист эстрогеновых рецепторов (ER), с эстрогенным действием в некоторых тканях и антиэстрогенным действием в других тканях. [5] [7] Препарат оказывает эстрогенное действие на кости , частичное эстрогенное действие на матку и печень и антиэстрогенное действие на грудь . [6] [8] [9] [5]
| Медикамент | Грудь | Кость | Печень | Матка | Вагина | Мозг | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Липиды | Коагуляция | ГСПГПодсказка Глобулин, связывающий половые гормоны | ИФР-1Подсказка Инсулиноподобный фактор роста 1 | Приливы | гонадотропины | |||||||||
| Эстрадиол | + | + | + | + | + | + | + | + | + | + | ||||
| «Идеальный SERM» | – | + | + | ± | ± | ± | – | + | + | ± | ||||
| Базедоксифен | – | + | + | + | + | ? | – | ± | – | ? | ||||
| Кломифен | – | + | + | ? | + | + | – | ? | – | ± | ||||
| Лазофоксифен | – | + | + | + | ? | ? | ± | ± | – | ? | ||||
| Оспемифен | – | + | + | + | + | + | ± | ± | – | ± | ||||
| Ралоксифен | – | + | + | + | + | + | ± | – | – | ± | ||||
| Тамоксифен | – | + | + | + | + | + | + | – | – | ± | ||||
| Торемифен | – | + | + | + | + | + | + | – | – | ± | ||||
| Эффект: + = Эстрогенный / агонистический . ± = Смешанный или нейтральный. – = Антиэстрогенный / антагонистический . Примечание: СЭРМ обычно повышают уровень гонадотропина у гипогонадных и эугонадных мужчин, а также у женщин в пременопаузе (антиэстрогенный), но снижают уровень гонадотропина у женщин в постменопаузе (эстрогенный). Источники: см. шаблон. | ||||||||||||||
Сродство торемифена к ER аналогично сродству тамоксифена. [6] [21] [22] В исследованиях с использованием крысиного ER торемифен имел около 1,4%, а тамоксифен около 1,6% сродства эстрадиола к ER. [23] [24] [25] [26] [27] [22] Сродство (K i ) торемифена к человеческим ER было зарегистрировано как 20,3 ± 0,1 нМ для ERα и 15,4 ± 3,1 нМ для ERβ . [20] В других исследованиях ЭР у крыс торемифен имел 3–9% сродства эстрадиола к ЭР, в то время как его метаболиты N -десметилторемифен и 4-гидрокситоремифен имели 3–5% и 64–158% сродства эстрадиола к ЭР соответственно. [28] [29] [30] Сродство другого метаболита, 4-гидрокси- N -десметилторемифена, не оценивалось. [29] 4-гидрокситоремифен показал примерно в 100 раз более высокую антиэстрогенную активность , чем торемифен in vitro в одном исследовании, [29] но не в другом. [28] Также было обнаружено, что 4-гидрокси- N -десметилторемифен является сильным антиэстрогеном in vitro . [28] Метаболиты торемифена, в частности 4-гидрокситоремифен, могут вносить значительный вклад в клиническую активность препарата. [1] [29] [28] С другой стороны, некоторые специалисты считают, что торемифен не является пролекарством . [ 31]
Торемифен очень похож на тамоксифен и разделяет большинство его свойств. [6] [8] [9] [5] Есть некоторые указания на то, что торемифен может быть безопаснее тамоксифена, поскольку он не является гепатоканцерогеном у животных и может иметь меньший потенциал генотоксичности . [ 6] [3] Однако клинические исследования не обнаружили существенных различий между торемифеном и тамоксифеном, в том числе с точки зрения эффективности , переносимости и безопасности , и, следовательно, клиническое использование торемифена было несколько ограничено. [6] [3] Считается, что торемифен обладает примерно одной третью эффективности тамоксифена ; то есть 60 мг торемифена примерно эквивалентны 20 мг тамоксифена при лечении рака молочной железы. [32]
Было обнаружено, что торемифен оказывает антигонадотропное действие на женщин в постменопаузе [33] , прогонадотропное действие на мужчин [34] , повышает уровень глобулина, связывающего половые гормоны [33], и снижает уровень инсулиноподобного фактора роста 1 примерно на 20% у женщин и мужчин в постменопаузе [35] .
Помимо своей активности в качестве SERM, 4-гидрокситоремифен является антагонистом эстроген -связанного рецептора γ (ERRγ). [36]
Фармакокинетика
Поглощение
Биодоступность торемифена точно не определена, но известно , что она хорошая и оценивается примерно в 100%. [1] [2] Уровни торемифена в устойчивом состоянии при дозировке 60 мг/день составляют от 800 до 879 нг/мл. [1] Уровни N -десметилторемифена в устойчивом состоянии с торемифеном составили 3058 нг/мл при 60 мг/день, 5942 нг/мл при 200 мг/день и 11913 нг/мл при 400 мг/день. [1] Уровни 4-гидрокситоремифена в устойчивом состоянии с торемифеном составили 438 нг/мл при 200 мг/день и 889 нг/мл при 400 мг/день. [1] Концентрации торемифена увеличиваются линейно в диапазоне доз от 10 до 680 мг. [37] [38]
Распределение
Торемифен на 99,7% связывается с белками плазмы , причем 92% связывается конкретно с альбумином , около 6% с фракцией β1 - глобулинов и около 2% с фракцией между альбумином и α1 - глобулинами . [37] [1] Кажущийся объем распределения торемифена варьировался от 457 до 958 л. [37]
Метаболизм
Торемифен метаболизируется в печени в основном с помощью CYP3A4 , а затем подвергается вторичному гидроксилированию . [2] Метаболиты торемифена включают N - десметилторемифен, 4-гидрокситоремифен и 4-гидрокси- N -десметилторемифен, среди прочих. [1] [29] [2] [39] Оспемифен (деаминогидрокситоремифен) также является основным метаболитом торемифена. [1] [4]
Устранение
Период полувыведения торемифена составляет от 3 до 7 дней у здоровых людей. [1] У людей с нарушением функции печени период полувыведения составляет 11 дней. [1] Периоды полувыведения метаболитов торемифена составляют от 5 до 21 дня для N -десметилторемифена, 5 дней для 4-гидрокситоремифена и 4 дня для оспемифена. [1] [2] [4] Считается, что длительный период полувыведения торемифена и его метаболитов обусловлен энтерогепатической рециркуляцией и высоким связыванием с белками плазмы. [1] [5] Торемифен выводится на 70% с калом в виде метаболитов. [2]
Химия
Торемифен, также известный как 4-хлоротамоксифен , является производным трифенилэтилена и близким аналогом тамоксифена . [10] Он также тесно связан с афимоксифеном (4-гидрокситамоксифен) и оспемифеном ( деаминогидрокситоремифен ). [40] [41]
История
Торемифен был представлен в Соединенных Штатах в 1997 году. [11] [12] Это был первый антиэстроген , представленный в этой стране после тамоксифена в 1978 году. [13]
Общество и культура
Общие названия
Торемифен — это общее название препарата и его МННПодсказка Международное непатентованное названиеи БАНПодсказка: одобренное британцами имя, в то время как цитрат торемифена является его USANПодсказка Соединенные Штаты Принятое названиеи ЯНПодсказка Японское принятое имяи торемифен является его DCFПодсказка: Наименование: Французская коммуна. [42] [43] [44] [45]
Названия брендов
Торемифен продается почти исключительно под торговой маркой Фарестон. [43] [45]
Доступность
Торемифен широко продается по всему миру и доступен в Соединенных Штатах , Великобритании , Ирландии , многих других европейских странах, Южной Африке , Австралии , Новой Зеландии и других странах мира. [43] [45]
Исследовать
Торемифен также оценивался как средство профилактики рака простаты и имел рабочее торговое название Акаподен. [46]
В 2007 году фармацевтическая компания GTx, Inc проводила два различных клинических испытания фазы 3 ; во-первых, клиническое испытание фазы стержня для лечения серьезных побочных эффектов андрогенной депривационной терапии (АДТ) (особенно переломов позвоночника и приливов , липидного профиля и гинекомастии ) при прогрессирующем раке простаты, и, во-вторых, клиническое испытание фазы стержня III для профилактики рака простаты у мужчин с высоким риском с высокой степенью простатической интраэпителиальной неоплазии , или ПИН. Результаты этих испытаний ожидаются к первому кварталу 2008 года [47]
NDA для первой заявки (облегчение побочных эффектов АДТ при раке предстательной железы) было подано в феврале 2009 г. [48] , а в октябре 2009 г. FDA заявило, что им потребуются дополнительные клинические данные, например, еще одно исследование фазы III. [49]
В конечном итоге разработка была прекращена, и торемифен никогда не выпускался на рынок для лечения осложнений, связанных с АДТ, или для лечения или профилактики рака предстательной железы. [50]
Торемифен может быть полезен для профилактики гинекомастии, вызванной бикалутамидом . [15]
Результаты испытаний III фазы
Двойное слепое, плацебо-контролируемое, рандомизированное, 3-летнее клиническое исследование торемифена было проведено с использованием выборки из 1260 мужчин. Средний возраст участников составил 64 года, и им была поставлена диагноз: простатическая интраэпителиальная неоплазия высокой степени (HGPIN), которая считается предраковой, хотя Томпсон и Лич считают, что PIN низкой степени также может считаться предраковой. [51]
Спонсор GTx, который разработал и провел исследование, обнаружил, что у 34,7% пациентов из группы плацебо и 32,3% пациентов из группы торемифена были случаи рака. Различий в баллах Глисона ни в одной из групп обнаружено не было. [52]
Предыдущие исследования на мышах с использованием трансгенной аденокарциномы простаты мышей (TRAMP) показали, что торемифен предотвращает пальпируемые опухоли у 60% животных. В этом исследовании торемифен использовался в качестве раннего профилактического средства, что отличает его от исследований фазы III на людях. [53]
Ссылки
- ^ abcdefghijklmnop Тарас Т.Л., Вурц Г.Т., Линарес Г.Р., ДеГрегорио М.В. (ноябрь 2000 г.). «Клиническая фармакокинетика торемифена». Клин Фармакокинетика . 39 (5): 327–34 . doi : 10.2165/00003088-200039050-00002. PMID 11108432. S2CID 26647296.
- ^ abcdefghi DeVita Jr VT, Lawrence TS, Rosenberg SA (7 января 2015 г.). Рак DeVita, Hellman и Rosenberg: принципы и практика онкологии. Wolters Kluwer Health. стр. 1126–. ISBN 978-1-4698-9455-3.
- ^ abcd Chabner BA, Longo DL (7 декабря 2011 г.). Химиотерапия и биотерапия рака: принципы и практика. Lippincott Williams & Wilkins. стр. 659–. ISBN 978-1-4511-4820-6.
- ^ abcdefgh "FARESTON (торемифен цитрат) 60 мг таблетки для приема внутрь" (PDF) . GTx, Inc . Управление по контролю за продуктами и лекарствами США. Март 2011 г.
- ^ abcdefghijklmnopqrstu Rosenthal L, Burchum J (17 февраля 2017 г.). Фармакотерапия Lehne для передовых поставщиков услуг - Электронная книга. Elsevier Health Sciences. стр. 931–. ISBN 978-0-323-44779-9.
- ^ abcdefghi Miller WR, Ingle JN (8 марта 2002 г.). Эндокринная терапия при раке молочной железы. CRC Press. стр. 55–57 . ISBN 978-0-203-90983-6.
- ^ abcdef Schiff D, Arrillaga I, Wen PY (16 сентября 2017 г.). Неврология рака в клинической практике: неврологические осложнения рака и их лечение. Humana Press. стр. 296–. ISBN 978-3-319-57901-6.
- ^ abc Morrow M, Jordan VC (2003). Управление риском рака молочной железы. PMPH-USA. стр. 192–. ISBN 978-1-55009-260-8.
- ^ abc Селективные модуляторы рецепторов эстрогена — достижения в исследованиях и применении: издание 2013 г.: ScholarlyBrief. ScholarlyEditions. 1 мая 2013 г. стр. 51–. ISBN 978-1-4901-0447-8.
- ^ ab Cano A, Calaf i Alsina J, Duenas-Diez JL (22 сентября 2006 г.). Селективные модуляторы эстрогеновых рецепторов: новый бренд многоцелевых препаратов. Springer Science & Business Media. стр. 52–. ISBN 978-3-540-34742-2.
- ^ ab Silva OE, Zurrida S (2005). Рак молочной железы: практическое руководство. Elsevier Health Sciences. стр. 355–. ISBN 0-7020-2744-8.
- ^ ab Bidlack WR, Omaye ST, Meskin MS, Topham DK (16 марта 2000 г.). Фитохимические вещества как биоактивные агенты. CRC Press. стр. 26–. ISBN 978-1-56676-788-0.
- ^ ab DiSaia PJ, Creasman WT, Mannel RS, McMeekin DS, Mutch DG (4 февраля 2017 г.). Электронная книга по клинической гинекологической онкологии. Elsevier Health Sciences. стр. 124–. ISBN 978-0-323-44316-6.
- ^ "Наличие дженерика Фарестона - Drugs.com". Drugs.com . Получено 19.04.2019 .
- ^ abcdef Sieber PR (декабрь 2007 г.). «Лечение заболеваний груди, вызванных бикалутамидом». Expert Rev Anticancer Ther . 7 (12): 1773– 9. doi :10.1586/14737140.7.12.1773. PMID 18062751. S2CID 40410461.
- ^ Bland KI, Copeland EM, Klimberg VS, Gradishar WJ (29 июня 2017 г.). Электронная книга о груди: комплексное лечение доброкачественных и злокачественных заболеваний. Elsevier Health Sciences. стр. 86–. ISBN 978-0-323-51187-2.
- ^ Tabbal M, Fuleihan GE (2010). «Будущие терапии». Остеопороз у мужчин . С. 713–732 . doi :10.1016/B978-0-12-374602-3.00057-2. ISBN 9780123746023.
- ^ Wirfs MJ (9 мая 2019 г.). Полное руководство APRN и PA по назначению лекарственной терапии 2020 г. Springer Publishing Company. стр. 60–. ISBN 978-0-8261-7934-0.
- ^ Casciato DA (2012). "Глава 4: Химиотерапевтические агенты для лечения рака". В Casciato DA, Territo MC (ред.). Руководство по клинической онкологии . Lippincott Williams & Wilkins. стр. 122–. ISBN 978-1-4511-1560-4.
- ^ ab Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (март 2006 г.). «Торемифен — перспективная терапия для профилактики рака простаты и осложнений андрогенной депривационной терапии». Expert Opin Investig Drugs . 15 (3): 293– 305. doi :10.1517/13543784.15.3.293. PMID 16503765. S2CID 29510508.
- ^ Workman P (6 декабря 2012 г.). Новые подходы в фармакологии рака: проектирование и разработка лекарств. Springer Science & Business Media. стр. 104–. ISBN 978-3-642-77874-2.
- ^ ab Каллио С, Кангас Л, Бланко Г, Йоханссон Р, Карьялайнен А, Перила М, Пиппо I, Сундквист Х, Сёдервалл М, Тойвола Р (1986). «Новое соединение трифенилэтилена, Fc-1157a. I. Гормональные эффекты». Химиотер Фармакол от рака . 17 (2): 103–8 . doi : 10.1007/BF00306736. PMID 2941176. S2CID 13238715.
- ^ Wittliff JL, Kerr II JL, Andres SA (2005). "Эстрогены IV: эстрогеноподобные фармацевтические препараты". В Wexler P (ред.). Энциклопедия токсикологии, 2-е издание . Т. Dib– L. Elsevier. стр. 254–258 . ISBN 9780080548005.
- ^ Blair RM, Fang H, Branham WS, Hass BS, Dial SL, Moland CL, Tong W, Shi L, Perkins R, Sheehan DM (март 2000 г.). «Относительное сродство связывания эстрогеновых рецепторов 188 природных и ксенохимических веществ: структурное разнообразие лигандов». Toxicol Sci . 54 (1): 138– 53. doi : 10.1093/toxsci/54.1.138 . PMID 10746941.
- ^ Fang H, Tong W, Shi LM, Blair R, Perkins R, Branham W, Hass BS, Xie Q, Dial SL, Moland CL, Sheehan DM (март 2001 г.). «Структурно-активностные связи для большого разнообразного набора природных, синтетических и экологических эстрогенов». Chem Res Toxicol . 14 (3): 280– 94. doi :10.1021/tx000208y. PMID 11258977.
- ^ Чандер СК, Сахота СС, Эванс ТР, Лукмани ЙА (декабрь 1993 г.). «Биологическая оценка новых антиэстрогенов для лечения рака груди». Crit Rev Oncol Hematol . 15 (3): 243–69 . doi :10.1016/1040-8428(93)90044-5. PMID 8142059.
- ^ Kavlock RJ, Daston GP (6 декабря 2012 г.). Токсичность лекарств в эмбриональном развитии II: Достижения в понимании механизмов врожденных дефектов: Понимание механизмов токсичных веществ, влияющих на развитие человека. Springer Science & Business Media. стр. 437–. ISBN 978-3-642-60447-8.
- ^ abcd Kangas L (1990). «Биохимические и фармакологические эффекты метаболитов торемифена». Cancer Chemother Pharmacol . 27 (1): 8– 12. doi :10.1007/BF00689269. PMID 2147128. S2CID 11502291.
- ^ abcde Robinson SP, Parker CJ, Jordan VC (август 1990 г.). «Доклинические исследования торемифена как противоопухолевого средства». Breast Cancer Res Treat . 16 (Suppl): S9–17. doi :10.1007/BF01807139. PMID 2149286. S2CID 19989845.
- ^ Osborne CK (6 декабря 2012 г.). Эндокринная терапия при раке груди и простаты. Springer Science & Business Media. стр. 104–. ISBN 978-1-4613-1731-9.
- ^ Vogel CL, Johnston MA, Capers C, Braccia D (февраль 2014 г.). «Торемифен при раке груди: обзор данных за 20 лет». Clin Breast Cancer . 14 (1): 1– 9. doi : 10.1016/j.clbc.2013.10.014 . PMID 24439786.
- ^ MacGregor JI, Jordan VC (июнь 1998). «Базовое руководство по механизмам действия антиэстрогенов». Pharmacol. Rev. 50 ( 2): 151–96 . PMID 9647865.
- ^ ab Ellmén J, Hakulinen P, Partanen A, Hayes DF (ноябрь 2003 г.). "Эстрогенные эффекты торемифена и тамоксифена у пациентов с раком груди в постменопаузе" (PDF) . Breast Cancer Res. Treat . 82 (2): 103– 11. doi :10.1023/B:BREA.0000003957.54851.11. hdl : 2027.42/44217 . PMID 14692654. S2CID 207694212.
- ^ Tsourdi E, Kourtis A, Farmakiotis D, Katsikis I, Salmas M, Panidis D (апрель 2009 г.). «Влияние введения селективного модулятора рецептора эстрогена на гипоталамо-гипофизарно-яичковую ось у мужчин с идиопатической олигозооспермией». Fertil. Steril . 91 (4 Suppl): 1427– 30. doi : 10.1016/j.fertnstert.2008.06.002 . PMID 18692782.
- ^ Roelfsema F, Yang RJ, Takahashi PY, Erickson D, Bowers CY, Veldhuis JD (февраль 2018 г.). «Влияние торемифена, селективного модулятора рецепторов эстрогена, на спонтанную и стимулированную секрецию ГР, IGF-I и IGF-связывающие белки у здоровых пожилых людей». Журнал эндокринного общества . 2 (2): 154– 165. doi :10.1210/js.2017-00457. PMC 5789038. PMID 29383334 .
- ^ Ariazi EA, Jordan VC (2006). «Эстроген-связанные рецепторы как новые мишени при раке и метаболических расстройствах». Curr Top Med Chem . 6 (3): 203–15 . doi :10.2174/1568026610606030203. PMID 16515477.
- ^ abc Gennari L, Merlotti D, Stolakis K, Nuti R (апрель 2012 г.). «Фармакокинетическая оценка торемифена и ее клинические последствия для лечения остеопороза». Expert Opin Drug Metab Toxicol . 8 (4): 505– 13. doi :10.1517/17425255.2012.665873. PMID 22356442. S2CID 19547631.
- ^ Анттила М., Валаваара Р., Кивинен С., Мяэнпяя Дж. (июнь 1990 г.). «Фармакокинетика торемифена». J Стероид Биохим . 36 (3): 249–52 . doi :10.1016/0022-4731(90)90019-о. ПМИД 2142247.
- ^ Brenner GM, Stevens C (28 сентября 2017 г.). Электронная книга по фармакологии Brenner and Stevens. Elsevier Health Sciences. стр. 394–. ISBN 978-0-323-39172-6.
- ^ Вебер ГФ (22 июля 2015 г.). Молекулярная терапия рака. Springer. стр. 304–. ISBN 978-3-319-13278-5.
- ^ Максимов PY, Макдэниел RE, Джордан VC (23 июля 2013 г.). Тамоксифен: новаторская медицина при раке груди. Springer Science & Business Media. стр. 170–. ISBN 978-3-0348-0664-0.
- ^ Elks J (14 ноября 2014 г.). Словарь лекарств: химические данные: химические данные, структуры и библиографии. Springer. стр. 1222–. ISBN 978-1-4757-2085-3.
- ^ abc Index Nominum 2000: Международный каталог лекарств. Тейлор и Фрэнсис. 2000. С. 1048–. ISBN 978-3-88763-075-1.
- ^ Morton IK, Hall JM (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы. Springer Science & Business Media. стр. 277–. ISBN 978-94-011-4439-1.
- ^ abc "Toremifene - Drugs.com". Drugs.com . Получено 2018-02-08 .
- ^ Прайс Н., Сартор О., Хатсон Т., Мариани С. (2005). «Роль ингибиторов 5a-редуктазы и селективных модуляторов эстрогеновых рецепторов как потенциальных химиопрофилактических агентов при раке простаты». Clin Prostate Cancer . 3 (4): 211– 4. doi :10.1016/s1540-0352(11)70089-0. PMID 15882476.
- ^ "Клиническая разработка III фазы препарата АКАПОДЕН компанией GTx продолжается после запланированного обзора безопасности" (пресс-релиз). GTx Inc. 2007-07-12 . Получено 2006-07-14 .
- ^ «GTx объявляет о том, что препарат Торемифен 80 мг NDA принят к рассмотрению FDA» (пресс-релиз).
- ^ «GTx и Ipsen прекращают сотрудничество в области рака простаты из-за расходов на исследование фазы III, запрошенное FDA». 2 марта 2011 г.
- ^ "Toremifene - AdisInsight". adisinsight.springer.com . Получено 2018-02-08 .
- ^ Томпсон-младший, И. М., и Лич, Р., Рак простаты и простатическая интраэпителиальная неоплазия: правда, правда и не связана? J Clin Oncol, 2013;31:515-6. https://ascopubs.org/doi/full/10.1200/JCO.2012.46.6151= [ постоянная мертвая ссылка ] Получено 31 июля 2019 г.
- ^ Taneja, SS, Morton, R., Barnette, G., Sieber, P., Hancock, ML и Steiner, M., Диагностика рака простаты среди мужчин с изолированной интраэпителиальной неоплазией высокой степени, включенных в трехлетнее проспективное клиническое исследование фазы III перорального торемифена J Clin Oncol, 2013;31:523-9. https://ascopubs.org/doi/abs/10.1200/JCO.2012.41.7634= [ постоянная мертвая ссылка ] Получено 31 июля 2019 г.
- ^ Raghow, S., Hooshdaran, MZ, Katiyar, S., и Steiner, MS, Toremifene предотвращает рак простаты в трансгенной аденокарциноме модели простаты у мышей. Cancer Research 2002;62:1370-6. http://cancerres.aacrjournals.org/content/62/5/1370= Получено 31 июля 2019 г.
Дальнейшее чтение
- Тарас Т.Л., Вурц Г.Т., Линарес Г.Р., ДеГрегорио М.В. (2000). «Клиническая фармакокинетика торемифена». Клин Фармакокинетика . 39 (5): 327–34 . doi : 10.2165/00003088-200039050-00002. PMID 11108432. S2CID 26647296.
- Harvey HA, Kimura M, Hajba A (2006). «Торемифен: оценка профиля его безопасности». Breast . 15 (2): 142–57 . doi :10.1016/j.breast.2005.09.007. PMID 16289904.
- Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (2006). «Торемифен — перспективная терапия для профилактики рака простаты и осложнений терапии андрогенной депривации». Expert Opin Investig Drugs . 15 (3): 293– 305. doi :10.1517/13543784.15.3.293. PMID 16503765. S2CID 29510508.
- Zhou WB, Ding Q, Chen L, Liu XA, Wang S (2011). «Торемифен — эффективная и безопасная альтернатива тамоксифену в адъювантной эндокринной терапии рака молочной железы: результаты четырех рандомизированных исследований». Breast Cancer Res. Treat . 128 (3): 625– 31. doi :10.1007/s10549-011-1556-5. PMID 21553116. S2CID 36985808.
- Дженнари Л., Мерлотти Д., Столакис К., Нути Р. (2012). «Фармакокинетическая оценка торемифена и ее клинические последствия для лечения остеопороза». Expert Opin Drug Metab Toxicol . 8 (4): 505– 13. doi :10.1517/17425255.2012.665873. PMID 22356442. S2CID 19547631.
- Mao C, Yang ZY, He BF, Liu S, Zhou JH, Luo RC, Chen Q, Tang JL (2012). «Торемифен против тамоксифена при прогрессирующем раке груди». Cochrane Database Syst Rev. 2021 ( 7): CD008926. doi :10.1002/14651858.CD008926.pub2. PMC 8407374. PMID 22786516 .
- Vogel CL, Johnston MA, Capers C, Braccia D (2014). «Торемифен при раке груди: обзор данных за 20 лет». Clin. Breast Cancer . 14 (1): 1– 9. doi : 10.1016/j.clbc.2013.10.014 . PMID 24439786.
- Мустонен М.В., Пирхёнен С., Келлокумпу-Лехтинен П.Л. (2014). «Торемифен в лечении рака молочной железы». Мировой Джей Клин Онкол . 5 (3): 393–405 . doi : 10.5306/wjco.v5.i3.393 . ПМК 4127610 . ПМИД 25114854.
Внешние ссылки
- Торемифен - AdisInsight
