Эстрадиол
 | |
 | |
| Имена | |
|---|---|
| Произношение | / ˌ ɛ s t r ə ˈ d aɪ oʊ l / ES -trə- DY -ohl [1][2] |
| Название ИЮПАК Эстра-1,3,5(10)-триен-3,17β-диол | |
| Систематическое название ИЮПАК (1 S ,3a S ,3b R ,9b S ,11a S )-11a-Метил-2,3,3a,3b,4,5,9b,10,11,11a-декагидро-1 H -циклопента[ a ]фенантрен-1,7-диол | |
| Другие имена Эстрадиол; E2; 17β-Эстрадиол; 17β-Эстрадиол | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Информационная карта ECHA | 100.000.022 |
| Номер ЕС |
|
| КЕГГ | |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| Характеристики | |
| С18Н24О2 | |
| Молярная масса | 272,38 г/моль |
| -186,6·10 −6 см 3 /моль | |
| Фармакология | |
| G03CA03 ( ВОЗ ) | |
| Данные лицензии |
|
| Перорально , сублингвально , интраназально , местно / трансдермально , вагинально , внутримышечно или подкожно (в виде эфира ), подкожный имплантат | |
| Фармакокинетика : | |
| Перорально: <5% [3] | |
| ~98%: [3] [4] • Альбумин : 60% • ГСПГ : 38% • Свободный: 2% | |
| Печень (через гидроксилирование , сульфатирование , глюкуронирование ) | |
| Перорально: 13–20 часов [3] Сублингвально: 8–18 часов [5] Местно (гель): 36,5 часов [6] | |
| Моча : 54% [3] Кал : 6% [3] | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Эстрадиол ( E2 ), также называемый эстрогеном , эстрадиолом , является эстрогеновым стероидным гормоном и основным женским половым гормоном . Он участвует в регуляции женских репродуктивных циклов, таких как эстральный и менструальный циклы . Эстрадиол отвечает за развитие женских вторичных половых признаков , таких как грудь , расширение бедер и женский тип распределения жира . Он также важен для развития и поддержания женских репродуктивных тканей, таких как молочные железы , матка и влагалище, в период полового созревания , взрослой жизни и беременности . [7] Он также оказывает важное влияние на многие другие ткани, включая кости , жир , кожу , печень и мозг .
Хотя уровень эстрадиола у мужчин намного ниже, чем у женщин, эстрадиол играет важную роль и у мужчин. Помимо людей и других млекопитающих , эстрадиол также обнаружен у большинства позвоночных и ракообразных , насекомых , рыб и других видов животных . [8] [9]
Эстрадиол вырабатывается в основном в фолликулах яичников , но также и в других тканях, включая яички , надпочечники , жир, печень , грудь и мозг. Эстрадиол вырабатывается в организме из холестерина через ряд реакций и промежуточных продуктов . [10] Основной путь включает образование андростендиона , который затем преобразуется ароматазой в эстрон и впоследствии преобразуется в эстрадиол. Альтернативно, андростендион может быть преобразован в тестостерон , который затем может быть преобразован в эстрадиол. После менопаузы у женщин выработка эстрогенов яичниками прекращается, и уровень эстрадиола снижается до очень низкого уровня.
Помимо своей роли естественного гормона, эстрадиол используется в качестве лекарственного средства , например, в менопаузальной гормональной терапии и феминизирующей гормональной терапии для трансгендерных женщин ; для получения информации об эстрадиоле как лекарственном средстве см. статью Эстрадиол (лекарство) .
Биологическая функция
Половое развитие
Развитие вторичных половых признаков у женщин обусловлено эстрогенами, а именно эстрадиолом. [11] [12] Эти изменения инициируются во время полового созревания , большинство из них усиливаются в репродуктивном возрасте и становятся менее выраженными с уменьшением поддержки эстрадиола после менопаузы . Таким образом, эстрадиол вызывает развитие груди и отвечает за изменения формы тела , влияя на кости, суставы и отложение жира . [11] [12] У женщин эстрадиол вызывает развитие груди, расширение бедер , женское распределение жира (с отложением жира, в частности, в груди, бедрах, бедрах и ягодицах), а также созревание влагалища и вульвы , тогда как он опосредует пубертатный скачок роста (косвенно через повышенную секрецию гормона роста ) [13] и эпифизарное закрытие (тем самым ограничивая окончательный рост ) у обоих полов. [11] [12]
Репродукция
Женская репродуктивная система
У женщин эстрадиол действует как гормон роста для тканей репродуктивных органов, поддерживая слизистую оболочку влагалища , цервикальные железы, эндометрий и слизистую оболочку маточных труб. Он усиливает рост миометрия . Эстрадиол, по-видимому, необходим для поддержания ооцитов в яичнике . Во время менструального цикла эстрадиол, вырабатываемый растущими фолликулами, запускает через систему положительной обратной связи гипоталамо-гипофизарные события, которые приводят к выбросу лютеинизирующего гормона , вызывая овуляцию. В лютеиновой фазе эстрадиол в сочетании с прогестероном подготавливает эндометрий к имплантации . Во время беременности эстрадиол увеличивается из-за продукции плаценты . Эффект эстрадиола вместе с эстроном и эстриолом во время беременности менее ясен. Они могут способствовать кровотоку в матке, росту миометрия, стимулировать рост груди и в срок, способствовать размягчению шейки матки и экспрессии миометриальных окситоциновых рецепторов. [ необходима цитата ] У бабуинов блокирование выработки эстрогена приводит к потере беременности, что предполагает, что эстрадиол играет роль в поддержании беременности. Исследования изучают роль эстрогенов в процессе инициации родов . Действия эстрадиола необходимы до воздействия прогестерона в лютеиновой фазе. [ необходима цитата ]
Мужская репродуктивная система
Влияние эстрадиола (и эстрогенов в целом) на мужскую репродуктивную функцию является сложным. Эстрадиол вырабатывается под действием ароматазы, в основном, в клетках Лейдига яичек млекопитающих , а также некоторыми зародышевыми клетками и клетками Сертоли неполовозрелых млекопитающих. [14] Он действует ( in vitro ), предотвращая апоптоз мужских сперматозоидов . [15] Хотя некоторые исследования в начале 1990-х годов утверждали о связи между глобальным снижением количества сперматозоидов и воздействием эстрогена в окружающей среде, [16] более поздние исследования не обнаружили такой связи или доказательств общего снижения количества сперматозоидов. [17] [18] Подавление выработки эстрадиола в субпопуляции субфертильных мужчин может улучшить анализ спермы . [19]
У мужчин с определенными генетическими заболеваниями половых хромосом , такими как синдром Клайнфельтера , будет более высокий уровень эстрадиола. [20]
Костная система
Эстрадиол оказывает сильное воздействие на кости. Люди без него (или других эстрогенов) станут высокими и евнухоидными , поскольку закрытие эпифизов задерживается или может не произойти. [21] Плотность костей также страдает, что приводит к ранней остеопении и остеопорозу . [22] Низкий уровень эстрадиола также может предсказывать переломы, причем женщины в постменопаузе имеют самую высокую частоту переломов костей . [23] Женщины после менопаузы испытывают ускоренную потерю костной массы из-за относительного дефицита эстрогена. [24]
Здоровье кожи
Рецептор эстрогена , а также рецептор прогестерона были обнаружены в коже , в том числе в кератиноцитах и фибробластах . [25] [26] В период менопаузы и после нее снижение уровня женских половых гормонов приводит к атрофии , истончению и увеличению морщинистости кожи, а также к снижению эластичности , упругости и прочности кожи. [25] [26] Эти изменения кожи представляют собой ускорение старения кожи и являются результатом снижения содержания коллагена , нарушений в морфологии эпидермальных клеток кожи , уменьшения основного вещества между волокнами кожи и уменьшения капилляров и кровотока . [25] [26] Кожа также становится более сухой во время менопаузы, что связано с уменьшением гидратации кожи и поверхностных липидов (выработки кожного сала). [25] Наряду с хронологическим старением и фотостарением, дефицит эстрогена в период менопаузы является одним из трех основных факторов, которые преимущественно влияют на старение кожи. [25]
Гормонозаместительная терапия, состоящая из системного лечения эстрогеном отдельно или в сочетании с прогестагеном, имеет хорошо документированные и значительные полезные эффекты на кожу женщин в постменопаузе. [25] [26] Эти преимущества включают увеличение содержания коллагена в коже, толщины и эластичности кожи, а также увлажнения кожи и поверхностных липидов. [25] [26] Было обнаружено, что местный эстроген оказывает аналогичное полезное воздействие на кожу. [25] Кроме того, исследование показало, что местный 2% прогестероновый крем значительно повышает эластичность и упругость кожи и заметно уменьшает морщины у женщин в пери- и постменопаузе. [26] С другой стороны, увлажнение кожи и поверхностные липиды существенно не изменились при местном применении прогестерона. [26] Эти результаты свидетельствуют о том, что прогестерон, как и эстроген, также оказывает полезное воздействие на кожу и может независимо защищать от старения кожи. [26]
Нервная система
Эстрогены могут вырабатываться в мозге из стероидных предшественников. Как антиоксиданты , они, как было обнаружено, обладают нейропротекторной функцией. [27]
Положительные и отрицательные обратные связи менструального цикла включают эстрадиол яичников как связующее звено с гипоталамо-гипофизарной системой для регуляции гонадотропинов . [28]
Эстроген, как полагают, играет важную роль в психическом здоровье женщин, и предполагается связь между уровнем гормонов, настроением и благополучием. Внезапные падения или колебания или длительные периоды устойчиво низких уровней эстрогена могут быть связаны со значительным снижением настроения. Было показано, что клиническое выздоровление от депрессии после родов, перименопаузы и постменопаузы эффективно после стабилизации и/или восстановления уровней эстрогена. [29] [30]
Было обнаружено, что объемы сексуально диморфных структур мозга у трансгендерных женщин изменяются и приближаются к типичным женским структурам мозга при воздействии эстрогена одновременно с лишением андрогенов в течение нескольких месяцев [31] , что позволяет предположить, что эстроген и/или андрогены играют важную роль в половой дифференциации мозга как в пренатальный период , так и на более поздних этапах жизни.
Также имеются данные, что программирование полового поведения взрослых самцов у многих позвоночных в значительной степени зависит от эстрадиола, вырабатываемого в пренатальном периоде и раннем младенчестве. [32] Пока неизвестно, играет ли этот процесс значительную роль в сексуальном поведении человека, хотя данные, полученные в ходе исследований других млекопитающих, указывают на наличие связи. [33]
Было обнаружено, что эстроген увеличивает секрецию окситоцина и увеличивает экспрессию его рецептора , рецептора окситоцина , в мозге . [34] Было обнаружено, что у женщин однократная доза эстрадиола достаточна для увеличения концентрации циркулирующего окситоцина. [35]
Гинекологические раковые заболевания
Эстрадиол был связан с развитием и прогрессированием таких видов рака, как рак груди, рак яичников и рак эндометрия. Эстрадиол влияет на целевые ткани в основном путем взаимодействия с двумя ядерными рецепторами, называемыми рецептором эстрогена α (ERα) и рецептором эстрогена β (ERβ). [36] [37] Одной из функций этих рецепторов эстрогена является модуляция экспрессии генов . После того, как эстрадиол связывается с ER, рецепторные комплексы затем связываются со специфическими последовательностями ДНК , что может привести к повреждению ДНК и увеличению деления клеток и репликации ДНК . Эукариотические клетки реагируют на поврежденную ДНК, стимулируя или нарушая фазы G1, S или G2 клеточного цикла, чтобы инициировать репарацию ДНК . В результате происходит клеточная трансформация и пролиферация раковых клеток. [38]
Сердечно-сосудистая система
Эстроген влияет на определенные кровеносные сосуды . Улучшение артериального кровотока было продемонстрировано в коронарных артериях . [39] 17-бета-эстрадиол (E2) считается самым мощным эстрогеном, обнаруженным у людей. E2 влияет на сосудистую функцию, апоптоз и повреждение во время сердечной ишемии и реперфузии. E2 может защитить сердце и отдельные сердечные миоциты от повреждений, связанных с ишемией. После сердечного приступа или длительных периодов гипертонии E2 подавляет неблагоприятные эффекты патологического ремоделирования сердца. [40]
Во время беременности высокий уровень эстрогенов, а именно эстрадиола, увеличивает коагуляцию и риск венозной тромбоэмболии .
| Абсолютная частота первой ВТЭ на 10 000 человеко-лет во время беременности и в послеродовом периоде | ||||||||
|---|---|---|---|---|---|---|---|---|
| Шведские данные A | Шведские данные B | Данные на английском языке | Датские данные | |||||
| Период времени | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) |
| Вне беременности | 1105 | 4,2 (4,0–4,4) | 1015 | 3.8 (?) | 1480 | 3,2 (3,0–3,3) | 2895 | 3,6 (3,4–3,7) |
| Дородовой | 995 | 20,5 (19,2–21,8) | 690 | 14,2 (13,2–15,3) | 156 | 9,9 (8,5–11,6) | 491 | 10,7 (9,7–11,6) |
| Триместр 1 | 207 | 13,6 (11,8–15,5) | 172 | 11,3 (9,7–13,1) | 23 | 4,6 (3,1–7,0) | 61 | 4.1 (3.2–5.2) |
| Триместр 2 | 275 | 17,4 (15,4–19,6) | 178 | 11,2 (9,7–13,0) | 30 | 5,8 (4,1–8,3) | 75 | 5,7 (4,6–7,2) |
| Триместр 3 | 513 | 29,2 (26,8–31,9) | 340 | 19,4 (17,4–21,6) | 103 | 18,2 (15,0–22,1) | 355 | 19,7 (17,7–21,9) |
| Около доставки | 115 | 154,6 (128,8–185,6) | 79 | 106,1 (85,1–132,3) | 34 | 142,8 (102,0–199,8) | – | |
| Послеродовой | 649 | 42,3 (39,2–45,7) | 509 | 33,1 (30,4–36,1) | 135 | 27,4 (23,1–32,4) | 218 | 17,5 (15,3–20,0) |
| Ранний послеродовой период | 584 | 75,4 (69,6–81,8) | 460 | 59,3 (54,1–65,0) | 177 | 46,8 (39,1–56,1) | 199 | 30,4 (26,4–35,0) |
| Поздний послеродовой период | 65 | 8,5 (7,0–10,9) | 49 | 6,4 (4,9–8,5) | 18 | 7,3 (4,6–11,6) | 319 | 3,2 (1,9–5,0) |
| Коэффициенты заболеваемости (IRR) первой ВТЭ во время беременности и в послеродовом периоде | ||||||||
| Шведские данные A | Шведские данные B | Данные на английском языке | Датские данные | |||||
| Период времени | ВНД* (95% ДИ) | ВНД* (95% ДИ) | ВСД (95% ДИ)† | ВСД (95% ДИ)† | ||||
| Вне беременности | Ссылка (т.е. 1.00) | |||||||
| Дородовой | 5,08 (4,66–5,54) | 3,80 (3,44–4,19) | 3,10 (2,63–3,66) | 2,95 (2,68–3,25) | ||||
| Триместр 1 | 3,42 (2,95–3,98) | 3,04 (2,58–3,56) | 1,46 (0,96–2,20) | 1,12 (0,86–1,45) | ||||
| Триместр 2 | 4,31 (3,78–4,93) | 3,01 (2,56–3,53) | 1,82 (1,27–2,62) | 1,58 (1,24–1,99) | ||||
| Триместр 3 | 7.14 (6.43–7.94) | 5.12 (4.53–5.80) | 5,69 (4,66–6,95) | 5,48 (4,89–6,12) | ||||
| Около доставки | 37,5 (30,9–44,45) | 27.97 (22.24–35.17) | 44,5 (31,68–62,54) | – | ||||
| Послеродовой | 10.21 (9.27–11.25) | 8,72 (7,83–9,70) | 8.54 (7.16–10.19) | 4,85 (4,21–5,57) | ||||
| Ранний послеродовой период | 19.27 (16.53–20.21) | 15.62 (14.00–17.45) | 14.61 (12.10–17.67) | 8.44 (7.27–9.75) | ||||
| Поздний послеродовой период | 2,06 (1,60–2,64) | 1,69 (1,26–2,25) | 2,29 (1,44–3,65) | 0,89 (0,53–1,39) | ||||
| Примечания: Шведские данные A = Использование любого кода для ВТЭ независимо от подтверждения. Шведские данные B = Использование только подтвержденного алгоритмом ВТЭ. Ранний послеродовой период = Первые 6 недель после родов. Поздний послеродовой период = Более 6 недель после родов. * = Скорректировано по возрасту и календарному году. † = Нескорректированное соотношение, рассчитанное на основе предоставленных данных. Источник: [41] | ||||||||
Другие функции
Эстрадиол оказывает комплексное воздействие на печень . Он влияет на выработку множества белков , включая липопротеины , связывающие белки и белки, отвечающие за свертываемость крови . [ необходима цитата ] В больших количествах эстрадиол может привести к холестазу , например, холестазу беременности .
Некоторые гинекологические состояния зависят от эстрогена, такие как эндометриоз , лейомиома матки и маточное кровотечение . [ необходима ссылка ]
Биологическая активность
Эстрадиол действует в первую очередь как агонист рецептора эстрогена ( ER), ядерного рецептора стероидных гормонов . Существует два подтипа ER, ERα и ERβ , и эстрадиол мощно связывается с обоими этими рецепторами и активирует их. Результатом активации ER является модуляция транскрипции и экспрессии генов в клетках , экспрессирующих ER , что является преобладающим механизмом, с помощью которого эстрадиол опосредует свои биологические эффекты в организме. Эстрадиол также действует как агонист мембранных рецепторов эстрогена (mER), таких как GPER (GPR30), недавно обнаруженный неядерный рецептор эстрадиола, через который он может опосредовать множество быстрых негеномных эффектов . [42] В отличие от случая ER, GPER, по-видимому, является селективным для эстрадиола и демонстрирует очень низкое сродство к другим эндогенным эстрогенам, таким как эстрон и эстриол . [43] Дополнительные mER помимо GPER включают ER-X , ERx и G q -mER . [44] [45]
ERα/ERβ находятся в неактивном состоянии, запертые в мультимолекулярных шаперонных комплексах, организованных вокруг белка теплового шока 90 (HSP90), содержащего белок p23 и иммунофилин, и расположенных в основном в цитоплазме и частично в ядре. В классическом пути E2 или классическом пути эстрогена эстрадиол попадает в цитоплазму , где взаимодействует с ER. После связывания с E2 ER диссоциируют от молекулярных шаперонных комплексов и становятся компетентными для димеризации, миграции в ядро и связывания со специфическими последовательностями ДНК ( элемент ответа эстрогена , ERE), что позволяет транскрипцию генов, которая может происходить в течение часов и дней.
Введенный мышам путем подкожной инъекции , эстрадиол примерно в 10 раз более эффективен, чем эстрон, и примерно в 100 раз более эффективен, чем эстриол. [46] [47] [48] Таким образом, эстрадиол является основным эстрогеном в организме, хотя роль эстрона и эстриола как эстрогенов, как говорят, не является незначительной. [48]
| Эстроген | ERПодсказка Рецептор эстрогена РБАПодсказка относительной привязки сродства(%) | Вес матки (%) | Утеротрофия | ЛГПодсказка Лютеинизирующий гормонуровни (%) | ГСПГПодсказка Глобулин, связывающий половые гормоны РБАПодсказка относительной привязки сродства(%) |
|---|---|---|---|---|---|
| Контроль | – | 100 | – | 100 | – |
| Эстрадиол (E2) | 100 | 506 ± 20 | +++ | 12–19 | 100 |
| Эстрон (E1) | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Эстриол (E3) | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Эстетрол (E4) | 0,5 ± 0,2 | ? | Неактивный | ? | 1 |
| 17α-Эстрадиол | 4,2 ± 0,8 | ? | ? | ? | ? |
| 2-гидроксиэстрадиол | 24 ± 7 | 285 ± 8 | + б | 31–61 | 28 |
| 2-метоксиэстрадиол | 0,05 ± 0,04 | 101 | Неактивный | ? | 130 |
| 4-гидроксиэстрадиол | 45 ± 12 | ? | ? | ? | ? |
| 4-метоксиэстрадиол | 1,3 ± 0,2 | 260 | ++ | ? | 9 |
| 4-Фторэстрадиол а | 180 ± 43 | ? | +++ | ? | ? |
| 2-гидроксиэстрон | 1,9 ± 0,8 | 130 ± 9 | Неактивный | 110–142 | 8 |
| 2-метоксиэстрон | 0,01 ± 0,00 | 103 ± 7 | Неактивный | 95–100 | 120 |
| 4-гидроксиэстрон | 11 ± 4 | 351 | ++ | 21–50 | 35 |
| 4-метоксиэстрон | 0,13 ± 0,04 | 338 | ++ | 65–92 | 12 |
| 16α-Гидроксиэстрон | 2,8 ± 1,0 | 552 ± 42 | +++ | 7–24 | <0,5 |
| 2-гидроксиэстриол | 0,9 ± 0,3 | 302 | + б | ? | ? |
| 2-метоксиэстриол | 0,01 ± 0,00 | ? | Неактивный | ? | 4 |
| Примечания: Значения представляют собой среднее значение ± SD или диапазон. ER RBA = Относительное сродство связывания с рецепторами эстрогена цитозоля матки крысы . Вес матки = Процентное изменение сырого веса матки овариэктомированных крыс через 72 часа непрерывного введения 1 мкг/час через подкожно имплантированные осмотические насосы . Уровни ЛГ = Уровни лютеинизирующего гормона относительно исходного уровня овариэктомированных крыс через 24–72 часа непрерывного введения через подкожный имплантат. Сноски: a = Синтетический (т. е. не эндогенный ). b = Атипичный утеротрофический эффект, который достигает плато в течение 48 часов (утеротрофия эстрадиола продолжается линейно до 72 часов). Источники: см. шаблон. | |||||
Биохимия

Биосинтез
Эстрадиол, как и другие стероидные гормоны , образуется из холестерина . После расщепления боковой цепи и использования Δ 5 или Δ 4 - пути, андростендион является ключевым посредником. Часть андростендиона преобразуется в тестостерон, который, в свою очередь, подвергается преобразованию в эстрадиол ароматазой. В альтернативном пути андростендион ароматизируется в эстрон , который впоследствии преобразуется в эстрадиол через 17β-гидроксистероиддегидрогеназу (17β-HSD). [50]
В репродуктивном возрасте большая часть эстрадиола у женщин вырабатывается гранулезными клетками яичников путем ароматизации андростендиона (вырабатываемого в клетках теки фолликули) в эстрон, с последующим преобразованием эстрона в эстрадиол 17β-HSD. Меньшие количества эстрадиола также вырабатываются корой надпочечников , а у мужчин — яичками. [ медицинская цитата необходима ]
Эстрадиол вырабатывается не только в половых железах ; в частности, жировые клетки вырабатывают активные предшественники эстрадиола и будут продолжать делать это даже после менопаузы. [51] Эстрадиол также вырабатывается в мозге и в стенках артерий .
У мужчин приблизительно от 15 до 25% циркулирующего эстрадиола вырабатывается в яичках . [52] [53] Остальная часть синтезируется путем периферической ароматизации тестостерона в эстрадиол и андростендиона в эстрон (который затем трансформируется в эстрадиол через периферический 17β-HSD). [52] [53] Эта периферическая ароматизация происходит преимущественно в жировой ткани , но также происходит и в других тканях, таких как кости , печень и мозг . [52] Примерно от 40 до 50 мкг эстрадиола вырабатывается в день у мужчин. [52]
Распределение
В плазме эстрадиол в основном связан с ГСПГ и альбумином . Только около 2,21% (± 0,04%) эстрадиола является свободным и биологически активным. Процент остается постоянным в течение менструального цикла . [54]
Метаболизм
Метаболические пути эстрадиола у человека Описание: Метаболические пути , участвующие в метаболизме эстрадиола и других природных эстрогенов (например, эстрона , эстриола ) у людей. В дополнение к метаболическим превращениям, показанным на схеме, конъюгация (например, сульфатирование и глюкуронирование ) происходит в случае эстрадиола и метаболитов эстрадиола, которые имеют одну или несколько доступных гидроксильных (–ОН) групп . Источники: см. страницу шаблона. |
Инактивация эстрадиола включает преобразование в менее активные эстрогены, такие как эстрон и эстриол. Эстриол является основным мочевым метаболитом . [ требуется цитата ] Эстрадиол конъюгируется в печени с образованием конъюгатов эстрогена , таких как эстрадиолсульфат , эстрадиолглюкуронид , и, как таковые, выводятся через почки . Некоторые из водорастворимых конъюгатов выводятся через желчные протоки и частично реабсорбируются после гидролиза из кишечного тракта . Эта энтерогепатическая циркуляция способствует поддержанию уровня эстрадиола.
Эстрадиол также метаболизируется посредством гидроксилирования в катехолэстрогены . В печени он неспецифически метаболизируется CYP1A2 , CYP3A4 и CYP2C9 посредством 2-гидроксилирования в 2-гидроксиэстрадиол , а также CYP2C9 , CYP2C19 и CYP2C8 посредством 17β-гидроксидегидрогенизации в эстрон , [55] с участием различных других ферментов цитохрома P450 (CYP) и метаболических преобразований . [56]
Эстрадиол дополнительно конъюгируется со сложным эфиром в липоидные формы эстрадиола, такие как эстрадиолпальмитат и эстрадиолстеарат в определенной степени; эти сложные эфиры хранятся в жировой ткани и могут действовать как очень долгосрочный резервуар эстрадиола. [57] [58]
Выделение
Эстрадиол выводится в виде глюкуронида и сульфатных эстрогеновых конъюгатов в мочу . После внутривенной инъекции меченого эстрадиола у женщин почти 90% выводится с мочой и калом в течение 4–5 дней. [59] [60] Энтерогепатическая рециркуляция вызывает задержку выведения эстрадиола. [59 ]
Уровни

Уровни эстрадиола у женщин в пременопаузе сильно варьируются в течение менструального цикла, и референтные диапазоны значительно различаются от источника к источнику. [62] Уровни эстрадиола минимальны и, по данным большинства лабораторий, колеблются от 20 до 80 пг/мл в течение ранней и средней фолликулярной фазы (или первой недели менструального цикла, также известной как менструация). [63] [64] Уровни эстрадиола постепенно увеличиваются в течение этого времени и в течение средней и поздней фолликулярной фазы (или второй недели менструального цикла) до преовуляторной фазы. [62] [63] Во время преовуляции (период примерно от 24 до 48 часов) уровни эстрадиола кратковременно повышаются и достигают самых высоких концентраций в любое другое время в течение менструального цикла. [62] Уровень циркулирующего эстрадиола обычно составляет от 130 до 200 пг/мл в это время, но у некоторых женщин он может достигать 300–400 пг/мл, а верхний предел референтного диапазона некоторых лабораторий даже выше (например, 750 пг/мл). [62] [63] [65] [66] [67] После овуляции (или середины цикла) и во второй половине менструального цикла или лютеиновой фазы уровни эстрадиола выходят на плато и колеблются между примерно 100 и 150 пг/мл в течение ранней и средней лютеиновой фазы, а во время поздней лютеиновой фазы или за несколько дней до менструации достигают минимума около 40 пг/мл. [62] [64] Средние интегрированные уровни эстрадиола в течение полного менструального цикла по-разному сообщались разными источниками как 80, 120 и 150 пг/мл. [64] [68] [69] Хотя существуют противоречивые сообщения, одно исследование обнаружило средние интегрированные уровни эстрадиола 150 пг/мл у молодых женщин, тогда как средние интегрированные уровни варьировались от 50 до 120 пг/мл у женщин старшего возраста. [69]
В репродуктивном возрасте у женщин уровень эстрадиола несколько выше, чем у эстрона, за исключением ранней фолликулярной фазы менструального цикла; таким образом, эстрадиол можно считать преобладающим эстрогеном в репродуктивном возрасте у женщин с точки зрения абсолютных уровней в сыворотке и эстрогенной активности. [ необходима цитата ] Во время беременности эстриол становится преобладающим циркулирующим эстрогеном, и это единственное время, когда в организме появляется эстерол, в то время как во время менопаузы преобладает эстрон (оба на основе уровней в сыворотке). [ необходима цитата ] Эстрадиол, вырабатываемый мужчинами из тестостерона, присутствует на уровнях в сыворотке, примерно сопоставимых с уровнями у женщин в постменопаузе (14–55 против <35 пг/мл соответственно). [ необходима цитата ] Также сообщалось, что если сравнить концентрацию эстрадиола у 70-летнего мужчины с концентрацией у 70-летней женщины, то у мужчины она будет примерно в 2–4 раза выше. [70]
| Группа | E2 ( производство ) | E2 (уровни) | E1 (уровни) | Соотношение |
|---|---|---|---|---|
| Девочки в пубертатном возрасте Стадия Таннера I (детство) Стадия Таннера II (возраст 8–12 лет) Стадия Таннера III (возраст 10–13 лет) Стадия Таннера IV (возраст 11–14 лет) Стадия Таннера V (возраст 12–15 лет) Фолликулярная (дни 1–14) Лютеиновая (дни 15–28) | ? ? ? ? ? ? | 9 (<9–20) пг/мл 15 (<9–30) пг/мл 27 (<9–60) пг/мл 55 (16–85) пг/мл 50 (30–100) пг/мл 130 ( 70–300) пг/мл | 13 (<9–23) пг/мл 18 (10–37) пг/мл 26 (17–58) пг/мл 36 (23–69) пг/мл 44 (30–89) пг/мл 75 (39– 160) пг/мл | ? ? ? ? ? ? |
| Мальчики препубертатного возраста | ? | 2–8 пг/мл | ? | ? |
| Женщины в пременопаузе Ранняя фолликулярная фаза (дни 1–4) Средняя фолликулярная фаза (дни 5–9) Поздняя фолликулярная фаза (дни 10–14) Лютеиновая фаза (дни 15–28) Оральные контрацептивы ( ановуляторные ) | 30–100 мкг/день 100–160 мкг/день 320–640 мкг/день 300 мкг/день ? | 40–60 пг/мл 60–100 пг/мл 200–400 пг/мл 190 пг/мл 12–50 пг/мл | 40–60 пг/мл ? 170–200 пг/мл 100–150 пг/мл ? | 0,5–1 ? 1–2 1,5 ? |
| Женщины в постменопаузе | 18 мкг/день | 5–20 пг/мл | 30–70 пг/мл | 0,3–0,8 |
| Беременные женщины Первый триместр (1–12 недели) Второй триместр (13–26 недели) Третий триместр (27–40 недели) | ? ? ? | 1 000–5 000 пг/мл 5 000–15 000 пг/мл 10 000–40 000 пг/мл | ? ? ? | ? ? ? |
| Мужчины а | 20–60 мкг/день | 27 (20–55) пг/мл | 20–90 пг/мл | 0,4–0,6 |
| Сноски: a = Формат "среднее значение (диапазон)" или просто "диапазон". Источники: [71] [72] [73] [74] [75] [61] [76] | ||||
Измерение
У женщин сывороточный эстрадиол измеряется в клинической лаборатории и отражает в первую очередь активность яичников. Анализ крови на эстрадиол измеряет количество эстрадиола в крови. [77] Он используется для проверки функции яичников, плаценты, надпочечников. [77] Это может определить базовый уровень эстрогена у женщин с аменореей или менструальной дисфункцией, а также выявить состояние гипоэстрогении и менопаузы. Кроме того, мониторинг эстрогена во время терапии бесплодия оценивает рост фолликулов и полезен для мониторинга лечения. Опухоли, продуцирующие эстроген, будут демонстрировать постоянно высокие уровни эстрадиола и других эстрогенов. При преждевременном половом созревании уровни эстрадиола ненадлежащим образом повышаются.
Диапазоны
Результаты отдельных лабораторных исследований всегда следует интерпретировать с использованием диапазонов, предоставленных лабораторией, выполнившей тест.
| Тип пациента | Нижний предел | Верхний предел | Единица |
|---|---|---|---|
| Взрослый самец | 50 [78] | 200 [78] | пмоль/л |
| 14 | 55 | пг/мл | |
| Взрослая самка ( фолликулярная фаза , день 5) | 70 [78] 95% ПИ (стандарт) | 500 [78] 95% ПИ | пмоль/л |
| 110 [79] 90% ПИ (используется в диаграмме ) | 220 [79] 90% ПИ | ||
| 19 (95% ПИ) | 140 (95% ПИ) | пг/мл | |
| 30 (90% ПИ) | 60 (90% ПИ) | ||
| Взрослая самка ( преовуляторный пик) | 400 [78] | 1500 [78] | пмоль/л |
| 110 | 410 | пг/мл | |
| Взрослая самка ( лютеиновая фаза ) | 70 [78] | 600 [78] | пмоль/л |
| 19 | 160 | пг/мл | |
| Взрослая самка – свободная (не связанная с белком) | 0.5 [80] [ оригинальное исследование? ] | 9 [80] [ оригинальное исследование? ] | пг/мл |
| 1.7 [80] [ оригинальное исследование? ] | 33 [80] [ оригинальное исследование? ] | пмоль/л | |
| Женщина в постменопаузе | Н/Д [78] | < 130 [78] | пмоль/л |
| Н/Д | < 35 | пг/мл |
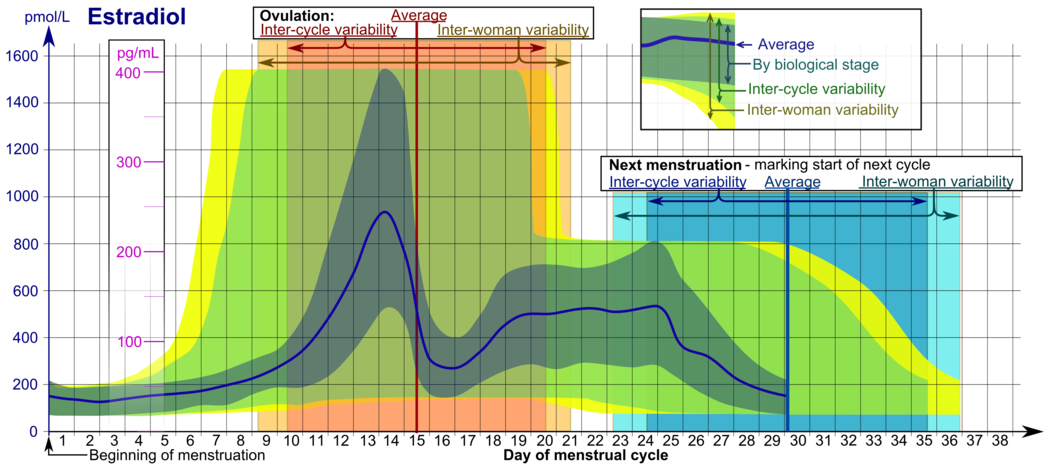
- Диапазоны, обозначенные как биологическая стадия, могут использоваться в тщательно контролируемых менструальных циклах в отношении других маркеров его биологического прогрессирования, при этом временная шкала сжимается или растягивается до того, насколько быстрее или медленнее, соответственно, развивается цикл по сравнению со средним циклом.
- Диапазоны, обозначенные как межцикловая изменчивость , более уместны для использования в неконтролируемых циклах, когда известно только начало менструации, но когда женщина точно знает среднюю продолжительность своего цикла и время овуляции, и что они в некоторой степени являются в среднем регулярными, при этом временная шкала сжимается или растягивается до того, насколько средняя продолжительность цикла женщины короче или длиннее, соответственно, чем в среднем по популяции.
- Диапазоны, обозначенные как межженская изменчивость, более уместны для использования, когда средняя продолжительность цикла и время овуляции неизвестны, но указано только начало менструации. [81]
В нормальном менструальном цикле уровень эстрадиола обычно составляет <50 пг/мл во время менструации, повышается с развитием фолликулов (пик: 200 пг/мл), кратковременно падает во время овуляции и снова повышается во время лютеиновой фазы для второго пика. В конце лютеиновой фазы уровень эстрадиола падает до менструального уровня, если только не наступает беременность.
Во время беременности уровень эстрогенов, включая эстрадиол, неуклонно растет к сроку. Источником этих эстрогенов является плацента , которая ароматизирует прогормоны, вырабатываемые в надпочечниках плода.
| секс | половой гормон | Репродуктивная фаза | Скорость выработки крови | Скорость секреции гонад | Скорость метаболического клиренса | Референтный диапазон (уровни в сыворотке) | |
|---|---|---|---|---|---|---|---|
| Единицы СИ | Единицы измерения, не входящие в систему СИ | ||||||
| Мужчины | Андростендион | – | 2,8 мг/день | 1,6 мг/день | 2200 л/сутки | 2,8–7,3 нмоль/л | 80–210 нг/дл |
| Тестостерон | – | 6,5 мг/день | 6,2 мг/день | 950 л/сутки | 6,9–34,7 нмоль/л | 200–1000 нг/дл | |
| Эстрон | – | 150 мкг/день | 110 мкг/день | 2050 л/сутки | 37–250 пмоль/л | 10–70 пг/мл | |
| Эстрадиол | – | 60 мкг/день | 50 мкг/день | 1600 л/сутки | <37–210 пмоль/л | 10–57 пг/мл | |
| Эстрон сульфат | – | 80 мкг/день | Незначительный | 167 л/день | 600–2500 пмоль/л | 200–900 пг/мл | |
| Женщины | Андростендион | – | 3,2 мг/день | 2,8 мг/день | 2000 л/день | 3,1–12,2 нмоль/л | 89–350 нг/дл |
| Тестостерон | – | 190 мкг/день | 60 мкг/день | 500 л/день | 0,7–2,8 нмоль/л | 20–81 нг/дл | |
| Эстрон | Фолликулярная фаза | 110 мкг/день | 80 мкг/день | 2200 л/сутки | 110–400 пмоль/л | 30–110 пг/мл | |
| Лютеиновая фаза | 260 мкг/день | 150 мкг/день | 2200 л/сутки | 310–660 пмоль/л | 80–180 пг/мл | ||
| Постменопауза | 40 мкг/день | Незначительный | 1610 л/сутки | 22–230 пмоль/л | 6–60 пг/мл | ||
| Эстрадиол | Фолликулярная фаза | 90 мкг/день | 80 мкг/день | 1200 л/сутки | <37–360 пмоль/л | 10–98 пг/мл | |
| Лютеиновая фаза | 250 мкг/день | 240 мкг/день | 1200 л/сутки | 699–1250 пмоль/л | 190–341 пг/мл | ||
| Постменопауза | 6 мкг/день | Незначительный | 910 л/сутки | <37–140 пмоль/л | 10–38 пг/мл | ||
| Эстрон сульфат | Фолликулярная фаза | 100 мкг/день | Незначительный | 146 л/день | 700–3600 пмоль/л | 250–1300 пг/мл | |
| Лютеиновая фаза | 180 мкг/день | Незначительный | 146 л/день | 1100–7300 пмоль/л | 400–2600 пг/мл | ||
| прогестерон | Фолликулярная фаза | 2 мг/день | 1,7 мг/день | 2100 л/сутки | 0,3–3 нмоль/л | 0,1–0,9 нг/мл | |
| Лютеиновая фаза | 25 мг/день | 24 мг/день | 2100 л/сутки | 19–45 нмоль/л | 6–14 нг/мл | ||
Примечания и источники Примечания: « Концентрация стероида в кровотоке определяется скоростью, с которой он секретируется железами, скоростью метаболизма предшественников или прегормонов в стероид и скоростью, с которой он извлекается тканями и метаболизируется. Скорость секреции стероида относится к общей секреции соединения из железы за единицу времени. Скорость секреции оценивалась путем отбора проб венозного оттока из железы с течением времени и вычитания артериальной и периферической венозной концентрации гормона. Скорость метаболического клиренса стероида определяется как объем крови, который был полностью очищен от гормона за единицу времени. Скорость продукции стероидного гормона относится к поступлению в кровь соединения из всех возможных источников, включая секрецию из желез и превращение прогормонов в интересующий стероид. В устойчивом состоянии количество гормона, поступающего в кровь из всех источников, будет равно скорости, с которой он очищается (скорость метаболического клиренса), умноженной на концентрацию в крови (скорость продукции = скорость метаболического клиренса × концентрация). Если вклад метаболизма прогормонов в циркулирующий пул стероидов невелик, то скорость продукции будет приблизительно равна скорости секреции». Источники: см. шаблон. | |||||||
Медицинское применение
Эстрадиол используется в качестве лекарственного средства, в основном в гормональной терапии симптомов менопаузы , а также в феминизирующей гормональной терапии для трансгендерных людей. [82]
Химия
Структуры основных эндогенных эстрогенов Обратите внимание на гидроксильные группы (–OH) : у эстрона (E1) их одна, у эстрадиола (E2) — две, у эстриола (E3) — три, а у эстетрола (E4) — четыре. |
Эстрадиол — это эстрановый стероид . [82] Он также известен как 17β-эстрадиол (чтобы отличить его от 17α-эстрадиола ) или как эстра-1,3,5(10)-триен-3,17β-диол. Он имеет две гидроксильные группы , одну в положении C3, а другую в положении 17β, а также три двойные связи в кольце A. Из-за двух гидроксильных групп эстрадиол часто сокращенно обозначается как E2. Структурно родственные эстрогены, эстрон (E1), эстриол (E3) и эстетрол (E4) имеют одну, три и четыре гидроксильные группы соответственно.
Нейропсихофармакология
В рандомизированном, двойном слепом, плацебо-контролируемом исследовании было показано, что эстрадиол оказывает гендерно-специфическое воздействие на чувствительность к справедливости. В целом, когда раздел определенной суммы денег был оформлен как справедливый или несправедливый в модифицированной версии игры в ультиматум , эстрадиол увеличивал процент принятия справедливо сформулированных предложений среди мужчин и уменьшал его среди женщин. Однако в группе плацебо «простая вера в получение лечения эстрадиолом значительно увеличивала принятие несправедливо сформулированных предложений у обоих полов», что указывает на то, что так называемые «средовые» факторы играли роль в организации ответов на эти презентации игры в ультиматум . [83]
История
Открытие эстрогена обычно приписывают американским ученым Эдгару Аллену и Эдварду А. Дойзи . [84] [85] В 1923 году они наблюдали, что инъекция жидкости из фолликулов свиных яичников вызывала изменения пубертатного и эстрального типа (включая изменения влагалища , матки и молочных желез , а также половую восприимчивость ) у неполовозрелых , овариэктомированных мышей и крыс. [84] [85] [86] Эти результаты продемонстрировали существование гормона , который вырабатывается яичниками и участвует в половом созревании и воспроизводстве . [84] [85] [86] Во время его открытия Аллен и Дойзи не дали гормону названия, а просто назвали его «гормоном яичников» или «фолликулярным гормоном»; [85] другие называли его по-разному: феминин , фолликулин , менформон , теликинин и эмменин . [87] [88] В 1926 году Паркс и Беллерби ввели термин эстрин для описания гормона на основе того, что он вызывает эструс у животных. [89] [87] Эстрон был выделен и очищен независимо Алленом и Дойзи и немецким ученым Адольфом Бутенандтом в 1929 году, а эстриол был выделен и очищен Маррианом в 1930 году; они были первыми идентифицированными эстрогенами. [85] [90] [91]
Эстрадиол, самый мощный из трех основных эстрогенов, был идентифицирован последним из трех. [85] [89] Он был открыт Швенком и Хильдебрантом в 1933 году, которые синтезировали его путем восстановления эстрона. [85] Эстрадиол был впоследствии выделен и очищен из яичников свиноматки Дойзи в 1935 году, при этом его химическая структура была определена одновременно, [92] и назывался по-разному: дигидротелин , дигидрофолликулин , дигидрофолликулярный гормон и дигидроксиэстрин . [85] [93] [94] В 1935 году название эстрадиол и термин эстроген были официально установлены Комитетом по половым гормонам Организации здравоохранения Лиги Наций ; это последовало за названиями эстрон (который изначально назывался телин, прогинон, фолликулин и кетогидроксиэстрин) и эстриол (первоначально называвшийся телол и тригидроксиэстрин), которые были установлены в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондоне . [89] [95] После его открытия частичный синтез эстрадиола из холестерина был разработан Инхоффеном и Хольвегом в 1940 году, а полный синтез был разработан Аннером и Мишером в 1948 году. [85]
Общество и культура
Этимология
Название эстрадиол происходит от estra- , греч. οἶστρος ( oistros , буквально означает «воодушевление или вдохновение»), [96] что относится к стероидной кольцевой системе эстрана , и -диол , химического термина и суффикса, указывающего на то, что соединение представляет собой тип спирта, содержащего две гидроксильные группы .
Ссылки
- ^ Ford SR, Roach SS (7 октября 2013 г.). Вводная клиническая фармакология Роуча. Lippincott Williams & Wilkins. стр. 525–. ISBN 978-1-4698-3214-2.
- ^ Hochadel M (1 апреля 2015 г.). Справочник по лекарственным препаратам для специалистов здравоохранения Мосби. Elsevier Health Sciences. стр. 602–. ISBN 978-0-323-31103-8.
- ^ abcde Stanczyk FZ, Archer DF, Bhavnani BR (июнь 2013 г.). «Этинилэстрадиол и 17β-эстрадиол в комбинированных оральных контрацептивах: фармакокинетика, фармакодинамика и оценка риска». Контрацепция . 87 (6): 706–27. doi :10.1016/j.contraception.2012.12.011. PMID 23375353.
- ^ Falcone T, Hurd WW (2007). Клиническая репродуктивная медицина и хирургия. Elsevier Health Sciences. стр. 22–. ISBN 978-0-323-03309-1. Архивировано из оригинала 10 января 2023 . Получено 22 октября 2016 .
- ^ Price TM, Blauer KL, Hansen M, Stanczyk F, Lobo R, Bates GW (март 1997). «Фармакокинетика однократного сублингвального и перорального введения микронизированного 17 бета-эстрадиола». Акушерство и гинекология . 89 (3): 340–5. doi :10.1016/S0029-7844(96)00513-3. PMID 9052581. S2CID 71641652.
- ^ Naunton M, Al Hadithy AF, Brouwers JR, Archer DF (2006). «Эстрадиоловый гель: обзор фармакологии, фармакокинетики, эффективности и безопасности у женщин в менопаузе». Менопауза . 13 (3): 517–27. doi :10.1097/01.gme.0000191881.52175.8c. PMID 16735950. S2CID 42748448.
- ^ Райан К.Дж. (август 1982 г.). «Биохимия ароматазы: значение для женской репродуктивной физиологии». Cancer Research . 42 (8 Suppl): 3342s–3344s. PMID 7083198.
- ^ Mechoulam R, Brueggemeier RW, Denlinger DL (сентябрь 1984 г.). «Эстрогены у насекомых». Cellular and Molecular Life Sciences . 40 (9): 942–944. doi :10.1007/BF01946450. S2CID 31950471.
- ^ Ozon R (1972). «Эстрогены у рыб, амфибий, рептилий и птиц». В Idler DR (ред.). Стероиды у позвоночных, не относящихся к млекопитающим . Oxford: Elsevier Science. стр. 390–414. ISBN 978-0323140980. Архивировано из оригинала 10 января 2023 . Получено 17 октября 2020 .
- ^ Салдана, Колин Дж., Люк Ремейдж-Хили и Барни А. Шлингер. «Синаптокринная сигнализация: синтез стероидов и действие в синапсе». Эндокринные обзоры 32.4 (2011): 532–549.
- ^ abc McMillan JA, Feigin RD, DeAngelis C, Jones MD (2006). Педиатрия Оски: принципы и практика. Lippincott Williams & Wilkins. стр. 550–. ISBN 978-0-7817-3894-1.
- ^ abc Craig CR, Stitzel RE (2004). Современная фармакология с клиническими приложениями. Lippincott Williams & Wilkins. стр. 706–. ISBN 978-0-7817-3762-3.
- ^ Preedy VR (2 декабря 2011 г.). Справочник по росту и мониторингу роста в области здоровья и болезней. Springer Science & Business Media. стр. 2661–. ISBN 978-1-4419-1794-2. Архивировано из оригинала 10 января 2023 . Получено 9 июня 2017 .
- ^ Carreau S, Lambard S, Delalande C, Denis-Galeraud I, Bilinska B, Bourguiba S (апрель 2003 г.). "Экспрессия ароматазы и роль эстрогенов в мужских гонадах: обзор". Reproductive Biology and Endocrinology . 1 : 35. doi : 10.1186/1477-7827-1-35 . PMC 155680. PMID 12747806 .
- ^ Пентикайнен В., Эрккиля К., Суомалайнен Л., Парвинен М., Дункель Л. (май 2000 г.). «Эстрадиол действует как фактор выживания зародышевых клеток в семенниках человека in vitro». Журнал клинической эндокринологии и метаболизма . 85 (5): 2057–67. дои : 10.1210/jcem.85.5.6600 . ПМИД 10843196.
- ^ Sharpe RM, Skakkebaek NE (май 1993). «Влияют ли эстрогены на снижение количества сперматозоидов и расстройства мужского репродуктивного тракта?». Lancet . 341 (8857): 1392–5. doi :10.1016/0140-6736(93)90953-E. PMID 8098802. S2CID 33135527.
- ^ Handelsman DJ (2001). «Эстрогены и падение количества сперматозоидов». Reproduction, Fertility, and Development . 13 (4): 317–24. doi :10.1071/rd00103. PMID 11800170.
- ^ Фиш Х, Голдстедин Р (2003). «Экологические эстрогены и количество сперматозоидов» (PDF) . Чистая и прикладная химия . 75 (11–12): 2181–2193. doi :10.1351/pac200375112181. S2CID 11068097. Архивировано из оригинала (PDF) 4 марта 2016 года . Получено 29 декабря 2015 года .
- ^ Raman JD, Schlegel PN (февраль 2002 г.). «Ингибиторы ароматазы при мужском бесплодии». Журнал урологии . 167 (2 Pt 1): 624–9. doi :10.1016/S0022-5347(01)69099-2. PMID 11792932.
- ^ Висотсак Дж., Грэм Дж. М. (октябрь 2006 г.). «Синдром Клайнфельтера и другие анеуплоидии половых хромосом». Orphanet Journal of Rare Diseases . 1 (42): 42. doi : 10.1186/1750-1172-1-42 . PMC 1634840. PMID 17062147 .
- ^ Вандершуерен Д., Лоран М.Р., Классенс Ф., Гилен Э., Лагерквист М.К., Ванденпут Л. и др. (декабрь 2014 г.). «Действие половых стероидов на мужские кости». Эндокринные обзоры . 35 (6): 906–60. дои : 10.1210/er.2014-1024. ПМЦ 4234776 . ПМИД 25202834.
- ^ Карани С., Цинь К., Симони М., Фаустини-Фустини М., Серпенте С., Бойд Дж. и др. (июль 1997 г.). «Влияние тестостерона и эстрадиола на мужчину с дефицитом ароматазы». Медицинский журнал Новой Англии . 337 (2): 91–5. дои : 10.1056/NEJM199707103370204 . ПМИД 9211678.
- ^ Берг К., Веннергрен Д., Мёллер М., Брисби Х. (21 декабря 2020 г.). «Частота переломов у взрослых в зависимости от возраста и пола: исследование 27 169 переломов в Шведском регистре переломов в четко определенной зоне охвата». PLOS ONE . 15 (12): e0244291. Bibcode : 2020PLoSO..1544291B. doi : 10.1371/journal.pone.0244291 . PMC 7751975. PMID 33347485 .
- ^ Albright F , Smith PH, Richardson AM (31 мая 1941 г.). «Постменопаузальный остеопороз: его клинические особенности». JAMA . 116 (22): 2465–2474. doi :10.1001/jama.1941.02820220007002.
- ^ abcdefgh Raine-Fenning NJ, Brincat MP, Muscat-Baron Y (2003). «Старение кожи и менопауза: последствия для лечения». Американский журнал клинической дерматологии . 4 (6): 371–8. doi :10.2165/00128071-200304060-00001. PMID 12762829. S2CID 20392538.
- ^ abcdefgh Holzer G, Riegler E, Hönigsmann H, Farokhnia S, Schmidt JB, Schmidt B (сентябрь 2005 г.). «Эффекты и побочные эффекты 2% прогестеронового крема на коже женщин в пери- и постменопаузе: результаты двойного слепого рандомизированного исследования с контролем за транспортным средством». The British Journal of Dermatology . 153 (3): 626–34. doi :10.1111/j.1365-2133.2005.06685.x. PMID 16120154. S2CID 6077829.
- ^ Behl C, Widmann M, Trapp T, Holsboer F (ноябрь 1995 г.). «17-бета-эстрадиол защищает нейроны от гибели клеток, вызванной окислительным стрессом in vitro». Biochemical and Biophysical Research Communications . 216 (2): 473–82. doi :10.1006/bbrc.1995.2647. PMID 7488136.
- ^ Meethal SV, Liu T, Chan HW, Ginsburg E, Wilson AC, Gray DN, Bowen RL, Vonderhaar BK, Atwood CS (август 2009 г.). «Идентификация регуляторной петли для синтеза нейростероидов: стероидогенный острый регуляторный белок-зависимый механизм с участием рецепторов гипоталамо-гипофизарно-гонадной оси». Журнал нейрохимии . 110 (3): 1014–27. doi :10.1111/j.1471-4159.2009.06192.x. PMC 2789665. PMID 19493163 .
- ^ Douma SL, Husband C, O'Donnell ME, Barwin BN, Woodend AK (2005). «Расстройства настроения, связанные с эстрогеном: факторы репродуктивного жизненного цикла». Advances in Nursing Science . 28 (4): 364–75. doi :10.1097/00012272-200510000-00008. PMID 16292022. S2CID 9172877.
- ^ Lasiuk GC, Hegadoren KM (октябрь 2007 г.). «Влияние эстрадиола на центральные серотонинергические системы и его связь с настроением у женщин». Biological Research for Nursing . 9 (2): 147–60. doi :10.1177/1099800407305600. PMID 17909167. S2CID 37965502.
- ^ Hulshoff HE, Cohen-Kettenis PT, Van Haren NE, Peper JS, Brans RG, Cahn W, Schnack HG, Gooren LJ, Kahn RS (июль 2006 г.). «Изменение пола меняет ваш мозг: влияние тестостерона и эстрогена на структуру мозга взрослого человека». European Journal of Endocrinology . 155 (suppl_1): 107–114. doi : 10.1530/eje.1.02248 .
- ^ Harding CF (июнь 2004 г.). «Гормональная модуляция пения: гормональная модуляция мозга певчей птицы и певческое поведение». Annals of the New York Academy of Sciences . 1016 (1): 524–39. Bibcode : 2004NYASA1016..524H. doi : 10.1196/annals.1298.030. PMID 15313793. S2CID 12457330. Архивировано из оригинала 27 сентября 2007 г.
- ^ Simerly RB (27 марта 2002 г.). «Wired for playback: organization and development of sexually dimorphic circuits in the infantilian forebrain» (PDF) . Annual Review of Neuroscience . 25 : 507–36. doi :10.1146/annurev.neuro.25.112701.142745. PMID 12052919. Архивировано из оригинала (PDF) 1 октября 2008 г. . Получено 7 марта 2007 г. .
- ^ Goldstein I, Meston CM, Davis S, Traish A (17 ноября 2005 г.). Женская сексуальная функция и дисфункция: исследование, диагностика и лечение. CRC Press. стр. 205–. ISBN 978-1-84214-263-9.
- ^ Асеведо-Родригес А., Мани С.К., Ханда Р.Дж. (2015). «Окситоцин и рецептор эстрогена β в мозге: обзор». Границы эндокринологии . 6 : 160. дои : 10.3389/fendo.2015.00160 . ПМК 4606117 . ПМИД 26528239.
- ^ Bulzomi P, Bolli A, Galluzzo P, Leone S, Acconcia F, Marino M (январь 2010 г.). «Совместное применение нарингенина и 17бета-эстрадиола предотвращает гормонально-индуцированный рост раковых клеток человека». IUBMB Life . 62 (1): 51–60. doi : 10.1002/iub.279 . PMID 19960539. S2CID 7903757.
- ^ Sreeja S, Santhosh Kumar TR, Lakshmi BS, Sreeja S (июль 2012 г.). «Экстракт граната демонстрирует селективный профиль модулятора рецептора эстрогена в линиях опухолевых клеток человека и моделях in vivo недостатка эстрогена». Журнал пищевой биохимии . 23 (7): 725–32. doi :10.1016/j.jnutbio.2011.03.015. PMID 21839626.
- ^ Thomas CG, Strom A, Lindberg K, Gustafsson JA (июнь 2011 г.). «Эстрогенный рецептор бета снижает выживаемость раковых клеток с дефектом p53 после повреждения ДНК, нарушая сигнализацию контрольной точки G₂/M». Breast Cancer Research and Treatment . 127 (2): 417–27. doi :10.1007/s10549-010-1011-z. PMID 20623183. S2CID 6752694.
- ^ Collins P, Rosano GM, Sarrel PM, Ulrich L, Adamopoulos S, Beale CM, McNeill JG, Poole-Wilson PA (июль 1995 г.). «17 бета-эстрадиол ослабляет вызванное ацетилхолином сужение коронарных артерий у женщин, но не у мужчин с ишемической болезнью сердца». Circulation . 92 (1): 24–30. doi :10.1161/01.CIR.92.1.24. PMID 7788912.
- ^ Knowlton, AA; Lee, AR (июль 2012 г.). «Эстроген и сердечно-сосудистая система». Pharmacology & Therapeutics . 135 (1): 54–70. doi :10.1016/j.pharmthera.2012.03.007. PMC 5688223. PMID 22484805 .
- ^ Абдул Султан А, Вест Дж, Стефанссон О, Грейндж МДж, Тата ЛДж, Флеминг КМ, Хьюмс Д, Людвигссон ДжФ (ноябрь 2015 г.). «Определение венозной тромбоэмболии и измерение ее заболеваемости с использованием шведских реестров здравоохранения: общенациональное когортное исследование беременности». BMJ Open . 5 (11): e008864. doi :10.1136/bmjopen-2015-008864. PMC 4654387. PMID 26560059.
- ^ Prossnitz ER, Barton M (май 2014). «Биология эстрогена: новые взгляды на функцию GPER и клинические возможности». Молекулярная и клеточная эндокринология . 389 (1–2): 71–83. doi :10.1016/j.mce.2014.02.002. PMC 4040308. PMID 24530924 .
- ^ Prossnitz ER, Arterburn JB, Sklar LA (2007). "GPR30: AG белок-связанный рецептор для эстрогена". Mol. Cell. Endocrinol . 265–266: 138–42. doi :10.1016/j.mce.2006.12.010. PMC 1847610. PMID 17222505 .
- ^ Soltysik K, Czekaj P (апрель 2013). «Мембранные рецепторы эстрогена — это альтернативный способ действия эстрогена?». Журнал физиологии и фармакологии . 64 (2): 129–42. PMID 23756388.
- ^ Micevych PE, Kelly MJ (2012). «Регуляция функции гипоталамуса мембранными эстрогеновыми рецепторами». Neuroendocrinology . 96 (2): 103–10. doi :10.1159/000338400. PMC 3496782 . PMID 22538318.
- ^ Labhart A (6 декабря 2012 г.). Клиническая эндокринология: теория и практика. Springer Science & Business Media. стр. 548–. ISBN 978-3-642-96158-8. Архивировано из оригинала 10 января 2023 . Получено 11 ноября 2018 .
- ^ Tucker SB (2007). Физиология матери, плода и новорожденного: клиническая перспектива. Elsevier Health Sciences. стр. 43–. ISBN 978-1-4160-2944-1. Архивировано из оригинала 10 января 2023 . Получено 7 июня 2017 .
- ^ ab Hall JE (31 мая 2015 г.). Электронная книга учебника медицинской физиологии Guyton and Hall. Elsevier Health Sciences. стр. 1043–. ISBN 978-0-323-38930-3.
- ^ Häggström M, Richfield D (2014). «Схема путей стероидогенеза человека». WikiJournal of Medicine . 1 (1). doi : 10.15347/wjm/2014.005 . ISSN 2002-4436.
- ^ Борон ВФ, Булпаеп ЭЛ (2003). Медицинская физиология: клеточный и молекулярный подход . Elsevier/Saunders. стр. 1300. ISBN 978-1-4160-2328-9.
- ^ Мучлер Э, Шефер-Кортинг М (2001). Arzneimittelwirkungen (на немецком языке) (8-е изд.). Штутгарт: Wissenschaftliche Verlagsgesellschaft. стр. 434, 444. ISBN. 978-3-8047-1763-3.
- ^ abcd Melmed S (1 января 2016 г.). Учебник эндокринологии Уильямса. Elsevier Health Sciences. стр. 710–. ISBN 978-0-323-29738-7. Архивировано из оригинала 10 января 2023 . Получено 21 марта 2018 .
- ^ ab Marcus R, Feldman D, Dempster DW, Luckey M, Cauley JA (13 июня 2013 г.). Остеопороз. Academic Press. стр. 331–. ISBN 978-0-12-398252-0.
- ^ Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Michael G (август 1976 г.). «Свободный и связанный с белком эстрадиол-17 бета плазмы во время менструального цикла». Журнал клинической эндокринологии и метаболизма . 43 (2): 436–45. doi :10.1210/jcem-43-2-436. PMID 950372.
- ^ Cheng ZN, Shu Y, Liu ZQ, Wang LS, Ou-Yang DS, Zhou HH (февраль 2001 г.). «Роль цитохрома P450 в метаболизме эстрадиола in vitro». Acta Pharmacologica Sinica . 22 (2): 148–54. PMID 11741520.
- ^ Lee AJ, Cai MX, Thomas PE, Conney AH, Zhu BT (август 2003 г.). «Характеристика окислительных метаболитов 17бета-эстрадиола и эстрона, образованных 15 селективно экспрессируемыми изоформами человеческого цитохрома p450». Эндокринология . 144 (8): 3382–98. doi : 10.1210/en.2003-0192 . PMID 12865317.
- ^ Oettel M, Schillinger E (6 декабря 2012 г.). Эстрогены и антиэстрогены I: Физиология и механизмы действия эстрогенов и антиэстрогенов. Springer Science & Business Media. стр. 235–237. ISBN 978-3-642-58616-3.
- ^ Oettel M, Schillinger E (6 декабря 2012 г.). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов. Springer Science & Business Media. стр. 268, 271. ISBN 978-3-642-60107-1.
- ^ Аб Дорфман, Ральф И. (1961). «Метаболизм стероидных гормонов». Радиоактивные изотопы в физиологической диагностике и терапии / Künstliche Radioaktive Isotope in Physiologie Diagnostik und Therapie . стр. 1223–1241. дои : 10.1007/978-3-642-49761-2_39. ISBN 978-3-642-49477-2.
- ^ Sandberg AA, Slaunwhite WR (август 1957 г.). «Исследования фенольных стероидов у людей. II. Метаболическая судьба и гепатобилиарно-энтеральная циркуляция C14-эстрона и C14-эстрадиола у женщин». J. Clin. Invest . 36 (8): 1266–78. doi :10.1172/JCI103524. PMC 1072719. PMID 13463090 .
- ^ ab "Эстрадиол" (PDF) . ilexmedical.com . Архивировано (PDF) из оригинала 4 февраля 2024 г. . Получено 4 июля 2024 г. .
- ^ abcde Becker JB, Berkley KJ, Geary N, Hampson E, Herman JP , Young E (4 декабря 2007 г.). Половые различия в мозге: от генов к поведению. Oxford University Press. стр. 64–. ISBN 978-0-19-804255-6.
Уровни эстрадиола минимальны в течение самых ранних дней фолликулярной фазы, но по мере созревания фолликула в общий кровоток выделяется все большее количество эстрадиола. Самые высокие уровни достигаются примерно за 24–48 часов до пика ЛГ. Фактически, предовуляторный пик эстрадиола представляет собой его самую высокую концентрацию в течение всего менструального цикла. Концентрации сыворотки в это время обычно составляют около 130–200 пг/мл, но у некоторых женщин могут быть достигнуты концентрации до 300–400 пг/мл. После временного падения, связанного с овуляцией, секреция эстрадиола восстанавливается за счет продукции желтым телом во время лютеиновой фазы. Уровни плато около 100–150 пг/мл (Abraham, 1978; Thorneycroft et al., 1971) чаще всего наблюдаются в период от −10 до −5 дней до начала менструации. С регрессией желтого тела уровни эстрадиола падают, постепенно у некоторых женщин и стремительно у других, в течение последних нескольких дней лютеиновой фазы. Это знаменует начало менструации, отторжение эндометрия. Эстрадиол в сыворотке во время менструации составляет приблизительно 30–50 пг/мл. (Источник.)
- ^ abc Strauss JR, Barbieri RL (2009). Репродуктивная эндокринология Йена и Джаффе: физиология, патофизиология и клиническое управление. Elsevier Health Sciences. стр. 807–. ISBN 978-1-4160-4907-4. Архивировано из оригинала 10 января 2023 г. . Получено 21 декабря 2016 г. .
В большинстве лабораторий уровень эстрадиола в сыворотке варьируется от 20 до 80 пг/мл в течение ранней и средней фолликулярной фазы менструального цикла и достигает пика в 200–500 пг/мл во время преовуляторного всплеска. В середине лютеиновой фазы уровень эстрадиола в сыворотке варьируется от 60 до 200 пг/мл.
- ^ abc Christian C, von Schoultz B (15 марта 1994 г.). Гормонозаместительная терапия: стандартизированные или индивидуально адаптированные дозы?. CRC Press. стр. 60–. ISBN 978-1-85070-545-1.
Уровень эстрадиола в плазме колеблется от 40 до 80 пг/мл в течение 1-й недели овариального цикла (ранняя фолликулярная фаза) и от 80 до 300 пг/мл в течение 2-й недели (средняя и поздняя фолликулярная фаза, включая периовуляторный пик). Затем в течение 3-й и 4-й недель эстрадиол колеблется от 100 до 150 пг/мл (ранняя и средняя лютеиновая фаза) до 40 пг/мл за несколько дней до менструации (поздняя лютеиновая фаза). Средний интегрированный уровень эстрадиола в течение полного 28-дневного нормального цикла составляет около 80 пг/мл.
- ^ Jameson JL, De Groot LJ (18 мая 2010 г.). Эндокринология: взрослая и детская. Elsevier Health Sciences. стр. 2812–. ISBN 978-1-4557-1126-0.
В середине цикла: 150-750 пг/мл
- ^ Hay ID, Wass JA (26 января 2009 г.). Клиническая эндокринная онкология. John Wiley & Sons. стр. 623–. ISBN 978-1-4443-0023-9.
Середина цикла: 110-330 пг/мл
- ↑ Донс РФ (12 июля 1994 г.). Руководство по эндокринному и метаболическому тестированию. CRC Press. стр. 8–. ISBN 978-0-8493-7657-3.
Овуляторный: 200-400 пг/мл
- ^ Notelovitz M, van Keep PA (6 декабря 2012 г.). Климактерический период в перспективе: Труды Четвертого международного конгресса по менопаузе, состоявшегося в Лейк-Буэна-Виста, Флорида, 28 октября – 2 ноября 1984 г. Springer Science & Business Media. стр. 397–. ISBN 978-94-009-4145-8. Архивировано из оригинала 10 января 2023 г. . Получено 22 октября 2016 г. .
[...] после менопаузы уровень циркулирующего эстрадиола снижается со среднего значения в пременопаузе 120 пг/мл до всего лишь 13 пг/мл.
- ^ ab Müller EE, MacLeod RM (6 декабря 2012 г.). Neuroendocrine Perspectives. Springer Science & Business Media. стр. 121–. ISBN 978-1-4612-3554-5. Архивировано из оригинала 10 января 2023 г. . Получено 22 октября 2016 г. .
[...] [пременопаузальная] средняя концентрация [эстрадиола] 150 пг/мл [...]
- ^ Sayed Y, Taxel P (декабрь 2003 г.). «Использование терапии эстрогенами у мужчин». Current Opinion in Pharmacology . 3 (6): 650–4. doi :10.1016/j.coph.2003.07.004. PMID 14644018.
- ^ Nichols KC, Schenkel L, Benson H (1984). "17 бета-эстрадиол для заместительной терапии эстрогенами в постменопаузе". Obstet Gynecol Surv . 39 (4): 230–45. doi :10.1097/00006254-198404000-00022. PMID 6717863.
- ^ Синтия С. Чернецки; Барбара Дж. Бергер (31 октября 2012 г.). Лабораторные тесты и диагностические процедуры – Электронная книга. Elsevier Health Sciences. стр. 488–. ISBN 978-1-4557-4502-9. Архивировано из оригинала 22 августа 2023 г. . Получено 22 августа 2023 г. .
- ^ Powers MS, Schenkel L, Darley PE, Good WR, Balestra JC, Place VA (август 1985 г.). «Фармакокинетика и фармакодинамика трансдермальных лекарственных форм 17 бета-эстрадиола: сравнение с обычными пероральными эстрогенами, используемыми для заместительной гормональной терапии». Am. J. Obstet. Gynecol . 152 (8): 1099–106. doi :10.1016/0002-9378(85)90569-1. PMID 2992279.
- ^ Кеннет Л. Беккер (2001). Принципы и практика эндокринологии и метаболизма. Lippincott Williams & Wilkins. стр. 889, 1059–1060, 2153. ISBN 978-0-7817-1750-2.
- ^ Лалит Баджадж; Стивен Берман (1 января 2011 г.). Педиатрическое принятие решений Берманом. Elsevier Health Sciences. стр. 160–. ISBN 978-0-323-05405-8. Архивировано из оригинала 11 января 2023 г. . Получено 22 августа 2023 г. .
- ^ Куль Х (2003). «Эстроген для Манна?» [Эстрогены для мужчины?]. Бликпункт дер Манн . 1 (3): 6–12. ISSN 1727-0669. Архивировано из оригинала 22 августа 2023 года . Проверено 22 августа 2023 г.
- ^ ab "Анализ крови на эстрадиол: Медицинская энциклопедия MedlinePlus". medlineplus.gov . Архивировано из оригинала 18 марта 2021 г. . Получено 6 мая 2019 г. .
- ^ abcdefghij GPNotebook — референтный диапазон (эстрадиол) Архивировано 9 июня 2012 г. на Wayback Machine Получено 27 сентября 2009 г.
- ^ ab Значения, взятые с 1-го дня после всплеска ЛГ в: Stricker R, Eberhart R, Chevailler MC, Quinn FA, Bischof P, Stricker R (2006). «Установление подробных референтных значений для лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола и прогестерона в различные фазы менструального цикла на анализаторе Abbott ARCHITECT». Клиническая химия и лабораторная медицина . 44 (7): 883–7. doi :10.1515/CCLM.2006.160. PMID 16776638. S2CID 524952.как PDF-файл
- ^ abcd Общая сумма, умноженная на 0,022 в соответствии с 2,2%, представленными в: Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Michael G (август 1976 г.). «Свободный и связанный с белком эстрадиол-17 бета в плазме во время менструального цикла». Журнал клинической эндокринологии и метаболизма . 43 (2): 436–45. doi :10.1210/jcem-43-2-436. PMID 950372.[ оригинальное исследование? ]
- ^ Häggström M (2014). «Референтные диапазоны для эстрадиола, прогестерона, лютеинизирующего гормона и фолликулостимулирующего гормона во время менструального цикла». WikiJournal of Medicine . 1 (1). doi : 10.15347/wjm/2014.001 . ISSN 2002-4436.
- ^ ab Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения». Climacteric . 8 (1 Suppl 1): 3–63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ Coenjaerts M, Pape F, Santoso V, Grau F, Stoffel-Wagner B, Philipsen A, Schultz J, Hurlemann R, Scheele D (сентябрь 2021 г.). «Различия между полами в принятии экономических решений: экзогенный эстрадиол оказывает противоположное влияние на формирование представлений о справедливости у женщин и мужчин». Eur. Neuropsychopharmacol . 50 (2): 46–54. doi : 10.1016/j.euroneuro.2021.04.006. hdl : 20.500.11811/11066 . ISSN 0924-977X. PMID 33957337. S2CID 233982738.
- ^ abc Лорио DL, Лорио L (14 марта 2016 г.). Биографическая история эндокринологии. Джон Уайли и сыновья. стр. 345–. ISBN 978-1-119-20246-2.
- ^ abcdefghi Lauritzen C, Studd JW (22 июня 2005 г.). Текущее управление менопаузой. CRC Press. стр. 44–. ISBN 978-0-203-48612-2.
- ^ ab Allen E, Doisy EA (1923). «Гормон яичников». Журнал Американской медицинской ассоциации . 81 (10): 819. doi :10.1001/jama.1923.02650100027012. ISSN 0002-9955.
- ^ ab Gruhn JG, Kazer RR (11 ноября 2013 г.). Гормональная регуляция менструального цикла: эволюция концепций. Springer Science & Business Media. стр. 69–73. ISBN 978-1-4899-3496-3.
- ^ Newerla GJ (1944). «История открытия и выделения женских половых гормонов». New England Journal of Medicine . 230 (20): 595–604. doi :10.1056/NEJM194405182302001. ISSN 0028-4793.
- ^ abc Fritz MA, Speroff L (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие. Lippincott Williams & Wilkins. стр. 750–. ISBN 978-1-4511-4847-3.
- ^ Parl FF (2000). Эстрогены, рецепторы эстрогена и рак молочной железы. IOS Press. стр. 4–. ISBN 978-0-9673355-4-4. Архивировано из оригинала 10 января 2023 . Получено 27 ноября 2016 .
- ^ Sartorelli AC, Johns DG (27 ноября 2013 г.). Противоопухолевые и иммунодепрессивные агенты. Springer Science & Business Media. стр. 104–. ISBN 978-3-642-65806-8.
- ^ Shoupe D, Haseltine FP (6 декабря 2012 г.). Контрацепция. Springer Science & Business Media. стр. 2–. ISBN 978-1-4612-2730-4.
- ^ MacCorquodale DW, Thayer SA, Doisy EA (1935). «Кристаллический фолликулярный гормон яичников». Experimental Biology and Medicine . 32 (7): 1182. doi :10.3181/00379727-32-8020P. ISSN 1535-3702. S2CID 83557813.
- ^ Химические вещества, обнаруженные в биологических средах человека: база данных. Отдел проектирования и разработки, Отдел исследований и анализа, Офис интеграции программ и информации, Офис пестицидов и токсичных веществ, Агентство по охране окружающей среды. 1981. С. 114–.
- ^ Fausto-Sterling A (2000). Определение пола тела: гендерная политика и конструирование сексуальности . Basic Books. стр. 189–. ISBN 978-0-465-07714-4.
- ^ "Инструмент изучения греческих слов: oistros". Perseus Digital Library . Архивировано из оригинала 17 марта 2012 года . Получено 28 декабря 2011 года .





