- Уровни нандролона после однократной внутримышечной инъекции 50, 100 или 150 мг нандролона деканоата в масляном растворе у мужчин. [38]
- Уровни нандролона после однократной внутримышечной инъекции 100 мг нандролона деканоата или нандролона фенилпропионата в 4 мл или 1 мл раствора арахисового масла в ягодичную или дельтовидную мышцу у мужчин. [39]
- Уровни нандролона при однократной внутримышечной инъекции 50 мг нандролона деканоата или нандролона гексилоксифенилпропионата в масляном растворе у мужчин. [40]
- Нормализованное по дозе воздействие нандролона (уровень в сыворотке, деленный на введенную дозу) с нандролоном деканоатом в масляном растворе путем внутримышечной или подкожной инъекции у мужчин. [41] [42]
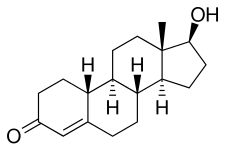
Нандролон
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / ˈ n æ n d r ə l oʊ n / [ 1] |
| Торговые наименования | • Дека-Дураболин (как NDПодсказка нандролон деканоат) • Дураболин (как НПППодсказка нандролон фенилпропионат) • Многие другие (см. здесь ) |
| Другие имена | • 19-нортестостерон [2] [3] • 10-нортестостерон • Эстр -4-ен-17β-ол-3-он • Эстренолон • Эстренолон • 19-норандрост-4-ен-17β-ол-3-он • Норандростенолон [2] • Нортестрионат [2] • Нортестонат [2] • Норандроон • SG-4341 [2] [3] |
Категория беременности |
|
| Пути введения | • Внутримышечная инъекция ( эфиры ) • Подкожная инъекция ( эфиры ) • Глазные капли ( NS)Подсказка нандролон сульфат) |
| Класс наркотиков | Андроген ; Анаболический стероид ; Прогестоген |
| код АТС | |
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | • Перорально : <3% (свиньи) [5] • Внутримышечно : высокая [6] |
| Метаболизм | Печень ( сокращение ) [7] [9] |
| Метаболиты | • 5α-дигидронандролон [7] [8] • 19-норандростерон [7] • 19-норэтиохоланолон [7] • Конъюгаты [9] |
| Период полувыведения | • Нандролон: <4,3 часов [7] • НОПодсказка Нандролон деканоат( ЯПодсказка Внутримышечная инъекция): 6–12 дней [7] [8] [10] • АЭСПодсказка Нандролон фенилпропионат: 2,7 дня [10] |
| Продолжительность действия | • ND ( IM ): 2–3 недели [8] [11] • NPP ( IM ): 5–7 дней [8] [10] |
| Выделение | Моча [7] |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| ИУФАР/БПС |
|
| DrugBank |
|
| ChemSpider | |
| УНИИ |
|
| ХЭБИ | |
| ChEMBL | |
| Панель инструментов CompTox ( EPA ) |
|
| Информационная карта ECHA | 100.006.457 |
| Химические и физические данные | |
| Формула | С18Н26О2 |
| Молярная масса | 274,404 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| (проверять) | |
Нандролон , также известный как 19-нортестостерон , является эндогенным андрогеном . Это также анаболический стероид (ААС), который в медицине используется в форме эфиров, таких как нандролон деканоат (торговая марка Deca-Durabolin ) и нандролон фенилпропионат (торговая марка Durabolin ). [2] [12] [8] [13] Эфиры нандролона используются при лечении анемии , кахексии ( синдрома мышечной атрофии), остеопороза , рака молочной железы и по другим показаниям. [8] В настоящее время они используются перорально или вместо этого вводятся путем инъекции в мышцы или жир . [8] [13] [14]
Побочные эффекты эфиров нандролона включают симптомы маскулинизации , такие как акне , усиленный рост волос и изменение голоса . [8] Они являются синтетическими андрогенами и анаболическими стероидами и, следовательно, являются агонистами андрогенового рецептора (АР), биологической мишени андрогенов, таких как тестостерон и дигидротестостерон (ДГТ). [8] [15] Нандролон обладает сильным анаболическим эффектом и слабым андрогенным эффектом, что придает им мягкий профиль побочных эффектов и делает их особенно подходящими для использования у женщин и детей. [8] [15] [16] Существуют метаболиты нандролона, которые действуют как длительно действующие пролекарства в организме, [8] такие как 5α-дигидронандролон .
Эфиры нандролона были впервые описаны и введены для медицинского применения в конце 1950-х годов. [8] Они являются одними из наиболее широко используемых анаболических стероидов во всем мире. [8] Помимо медицинского применения, эфиры нандролона используются для улучшения телосложения и производительности , и, как говорят, являются наиболее широко используемыми анаболическими стероидами для таких целей. [8] [17] Препараты являются контролируемыми веществами во многих странах, поэтому их немедицинское использование, как правило, незаконно. [8]
Медицинское применение
Эфиры нандролона используются в клинической практике, хотя и все реже, для людей в катаболических состояниях с серьезными ожогами, раком и СПИДом, а также была доступна офтальмологическая формула для поддержки заживления роговицы. [18] : 134
Положительные эффекты эфиров нандролона включают рост мышц, стимуляцию аппетита и увеличение выработки эритроцитов , [ необходима медицинская ссылка ] и плотности костей . [19] Клинические исследования показали, что они эффективны при лечении анемии , остеопороза и рака молочной железы .
Нандролон сульфат использовался в составе глазных капель в качестве офтальмологического препарата. [2] [12]
Немедицинское использование
Эфиры нандролона используются для улучшения телосложения и производительности спортсменами , бодибилдерами и пауэрлифтерами . [8 ]
Побочные эффекты
Побочные эффекты эфиров нандролона включают маскулинизацию среди прочих. [8] У женщин нандролон и эфиры нандролона , как сообщается, вызывают повышенное либидо , угри , рост волос на лице и теле , изменение голоса и увеличение клитора . [20] Однако, как сообщается, маскулинизирующие эффекты нандролона и его эфиров слабее, чем у тестостерона . [20] Также было обнаружено, что нандролон вызывает рост полового члена у мальчиков препубертатного возраста. [20] Аменорея и меноррагия были зарегистрированы как побочные эффекты нандролона ципионата . [20]
Нандролон теоретически может вызывать эректильную дисфункцию в качестве побочного эффекта, хотя в настоящее время нет клинических доказательств, подтверждающих это мнение. [21] [ неудачная проверка ] Побочные эффекты высоких доз нандролона могут включать сердечно-сосудистую токсичность , а также гипогонадизм и бесплодие . [ необходима ссылка ] Нандролон может не вызывать выпадение волос на голове , хотя это также теоретически. [21]
Фармакология
Фармакодинамика
| Медикамент | Коэффициент а |
|---|---|
| Тестостерон | ~1:1 |
| Андростанолон ( ДГТ ) | ~1:1 |
| Метилтестостерон | ~1:1 |
| Метандриол | ~1:1 |
| Флюоксиместерон | 1:1–1:15 |
| Метандиенон | 1:1–1:8 |
| Дростанолон | 1:3–1:4 |
| Метенолон | 1:2–1:30 |
| Оксиметолон | 1:2–1:9 |
| Оксандролон | 1:3–1:13 |
| Станозолол | 1:1–1:30 |
| Нандролон | 1:3–1:16 |
| Этилэстренол | 1:2–1:19 |
| Норэтандролон | 1:1–1:20 |
| Примечания: У грызунов. Сноски: a = Соотношение андрогенной и анаболической активности. Источники: См. шаблон. | |
Нандролон является агонистом АР, биологической мишени андрогенов , таких как тестостерон и ДГТ.Подсказка дигидротестостерон. В отличие от тестостерона и некоторых других анаболических стероидов, нандролон не потенцируется в андрогенных тканях, таких как кожа головы , кожа и простата , поэтому вредные эффекты в этих тканях уменьшаются. [22] Это связано с тем, что нандролон метаболизируется 5α-редуктазой в гораздо более слабый лиганд AR 5α-дигидронандролон (DHN), который имеет как сниженное сродство к андрогенному рецептору (AR) по сравнению с нандролоном in vitro , так и более слабую агонистическую активность AR in vivo . [22] Отсутствие алкилирования на 17α-углероде резко снижает гепатотоксический потенциал нандролона. [ необходима медицинская цитата ] Эффекты эстрогена , возникающие в результате реакции с ароматазой, также уменьшаются из-за уменьшения взаимодействия ферментов, [23] но такие эффекты, как гинекомастия и снижение либидо, все еще могут возникать при достаточно высоких дозах. [ необходима ссылка ]
В дополнение к своей агонистической активности AR, в отличие от многих других анаболических стероидов, нандролон также является мощным прогестагеном . [ 24] Он связывается с рецептором прогестерона примерно с 22% сродства прогестерона . [24] Прогестагенная активность нандролона служит для усиления его антигонадотропных эффектов, [25] [8] поскольку антигонадотропное действие является известным свойством прогестагенов. [26] [27]
| Сложный | PRПодсказка Рецептор прогестерона | АРПодсказка Андрогенный рецептор | ERПодсказка Рецептор эстрогена | ГРПодсказка Глюкокортикоидный рецептор | МИСТЕРПодсказка Минералокортикоидный рецептор | ГСПГПодсказка Глобулин, связывающий половые гормоны | КБГПодсказка Глобулин, связывающий кортикостероиды |
|---|---|---|---|---|---|---|---|
| Нандролон | 20 | 154–155 | <0,1 | 0,5 | 1.6 | 1–16 | 0.1 |
| Тестостерон | 1,0–1,2 | 100 | <0,1 | 0,17 | 0.9 | 19–82 | 3–8 |
| Эстрадиол | 2.6 | 7.9 | 100 | 0,6 | 0,13 | 8.7–12 | <0,1 |
| Примечания: Значения указаны в процентах (%). Контрольными лигандами (100%) для PR были прогестерон .Подсказка рецептор прогестерона, тестостерон для АРПодсказка андрогенный рецептор, эстрадиол для ERПодсказка эстрогеновый рецептор, дексаметазон для ГРПодсказка глюкокортикоидный рецептор, альдостерон для МРПодсказка минералокортикоидный рецептор, дигидротестостерон для SHBGПодсказка глобулин, связывающий половые гормоны, и кортизол для CBGПодсказка кортикостероид-связывающий глобулин. Источники: см. шаблон. | |||||||
Анаболическая и андрогенная активность
Нандролон имеет очень высокое соотношение анаболической и андрогенной активности. [15] Фактически, многие нандролон-подобные анаболические стероиды и даже сам нандролон, как говорят, имеют одно из самых высоких соотношений анаболического и андрогенного эффекта среди всех анаболических стероидов. [25] Это объясняется тем фактом, что в то время как тестостерон потенцируется путем преобразования в дигидротестостерон (ДГТ) в андрогенных тканях, противоположное справедливо для нандролона и подобных анаболических стероидов (т. е. других производных 19-нортестостерона). [15] Таким образом, нандролон-подобные анаболические стероиды, а именно эфиры нандролона, являются наиболее часто используемыми анаболическими стероидами в клинических условиях, в которых желательны анаболические эффекты; например, при лечении кахексии , связанной со СПИДом , тяжелых ожогов и хронической обструктивной болезни легких . [25] Однако анаболические стероиды с очень высоким соотношением анаболического и андрогенного действия, такие как нандролон, все еще оказывают значительное андрогенное действие и могут вызывать симптомы маскулинизации, такие как гирсутизм и огрубение голоса у женщин и детей при длительном использовании. [15]
| Сложный | рАР (%) | хАР (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Тестостерон | 38 | 38 | ||||||
| 5α-дигидротестостерон | 77 | 100 | ||||||
| Нандролон | 75 | 92 | ||||||
| 5α-дигидронандролон | 35 | 50 | ||||||
| Этилэстренол | НД | 2 | ||||||
| Норэтандролон | НД | 22 | ||||||
| 5α-дигидроноретандролон | НД | 14 | ||||||
| Метриболон | 100 | 110 | ||||||
| Источники: см. шаблон. | ||||||||
Фармакокинетика
Была изучена пероральная активность нандролона. [ 28] [29] [30] [31] [5] [ 32] При пероральном введении нандролона грызунам его эффективность составляла около одной десятой от подкожной инъекции нандролона. [28] [33] [20]
Нандролон имеет очень низкое сродство к глобулину, связывающему половые гормоны (ГСПГ) в сыворотке человека , около 5% от такового тестостерона и 1% от такового ДГТ. [34] Он метаболизируется ферментом 5α-редуктазой , среди прочих. [35] [ необходимы дополнительные ссылки ] Нандролон менее восприимчив к метаболизму 5α-редуктазой и 17β-гидроксистероиддегидрогеназой, чем тестостерон . [35] Это приводит к тому, что он меньше трансформируется в так называемых «андрогенных» тканях , таких как кожа , волосяные фолликулы и предстательная железа , а также в почках , соответственно. [35] Метаболиты нандролона включают 5α-дигидронандролон , 19-норандростерон и 19-норэтиохоланолон , и эти метаболиты могут быть обнаружены в моче . [36]
Было обнаружено, что однократные внутримышечные инъекции 100 мг нандролона фенилпропионата или нандролона деканоата вызывают анаболический эффект в течение 10–14 дней и 20–25 дней соответственно. [37] Напротив, неэтерифицированный нандролон использовался путем внутримышечной инъекции один раз в день. [20] [33]
Химия

Нандролон, также известный как 19-нортестостерон (19-NT) или как эстренолон, а также эстра-4-ен-17β-ол-3-он или 19-норандрост-4-ен-17β-ол-3-он, [43] является естественным эстрановым (19-норандростан) стероидом и производным тестостерона (андрост-4-ен-17β-ол-3-он). [2] [12] Это, в частности, C19- деметилированный ( nor ) аналог тестостерона . [2] [12] Нандролон является эндогенным промежуточным продуктом в производстве эстрадиола из тестостерона через ароматазу у млекопитающих, включая людей, и присутствует в организме естественным образом в следовых количествах. [44] Его можно обнаружить во время беременности у женщин. [45] Эфиры нандролона имеют эфир, такой как деканоат или фенилпропионат, присоединенный в положении C17β. [2] [12]
Производные
Эстеры
Различные эфиры нандролона продавались и использовались в медицине. [2] [12] Наиболее часто используемые эфиры - это нандролон деканоат и в меньшей степени нандролон фенилпропионат . Примеры других эфиров нандролона, которые продавались и использовались в медицине, включают нандролон циклогексилпропионат , нандролон ципионат , нандролон гексилоксифенилпропионат , нандролон лаурат , нандролон сульфат и нандролон ундеканоат . [2] [12] [8]
Анаболические стероиды
Нандролон является исходным соединением большой группы анаболических стероидов. Известные примеры включают не-17α-алкилированный тренболон и 17α-алкилированный этилэстренол (этилнандрол) и метриболон (R-1881), а также 17α-алкилированные дизайнерские стероиды норболетон и тетрагидрогестринон (THG). Ниже приведен список производных нандролона, которые были разработаны как анаболические стероиды: [8]
|
|
Прогестины
Нандролон, вместе с этистероном (17α-этинилтестостероном), также является родительским соединением большой группы прогестинов , производных норэтистерона (17α-этинил-19-нортестостерона). [46] [47] Это семейство подразделяется на две группы: эстраны и гонаны . [46] Эстраны включают норэтистерон (норэтиндрон), норэтистерона ацетат , норэтистерона энантат , линестренол , этинодиолдиацетат и норэтинодрел , в то время как гонаны включают норгестрел , левоноргестрел , дезогестрел , этоногестрел , гестоден , норгестимат , диеногест (фактически производное 17α-цианометил-19-нортестостерона) и норелгестромин . [46]
Синтез
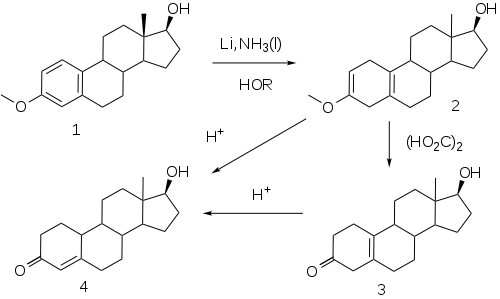
Разработка А. Дж. Бирчем метода восстановления ароматических колец до соответствующих дигидробензолов в контролируемых условиях открыла удобный путь к соединениям, родственным предполагаемому 19-норпрогестерону .
Эта реакция, теперь известная как восстановление по Берчу , [51] типична для обработки монометилового эфира эстрадиола ( 1 ) раствором металлического лития в жидком аммиаке в присутствии спирта в качестве источника протонов. Первоначальные компоненты реакции 1,4-диметаллирования наиболее электронодефицитных положений ароматического кольца — в случае эстрогена, положений 1 и 4. Rxn промежуточного соединения с источником протонов приводит к дигидробензолу; особым достоинством этой последовательности в стероидах является тот факт, что двойная связь в положении 2 фактически становится фрагментом енольного эфира. Обработка этого продукта ( 2 ) слабой кислотой, например, щавелевой , приводит к гидролизу енольного эфира, в результате чего образуется β,γ-неконъюгированный кетон 3 . Гидролиз в более жестких условиях ( минеральные кислоты ) приводит к миграции/конъюгации олефина с образованием нандролона ( 4 ).
Эстеры
- Обработка 4 декановым ангидридом и пиридином дает нандролона деканоат . [52]
- Ацилирование 4 фенилпропионилхлоридом дает нандролон фенпропионат . [53]
Обнаружение в жидкостях организма
Использование нандролона можно напрямую обнаружить в волосах или косвенно обнаружить в моче путем тестирования на наличие 19-норандростерона , метаболита . Международный олимпийский комитет установил предел в 2,0 мкг/л 19-норандростерона в моче в качестве верхнего предела, [54] за пределами которого спортсмен подозревается в употреблении допинга . В крупнейшем исследовании нандролона, проведенном на 621 спортсмене на Олимпийских играх 1998 года в Нагано , ни один спортсмен не показал более 0,4 мкг/л. 19-норандростерон был идентифицирован как следовая примесь в коммерческих препаратах андростендиона , который до 2004 года был доступен без рецепта в качестве пищевой добавки в США [55] [56] [57] [58]
В 1999 году произошло несколько случаев употребления нандролона в легкой атлетике , в том числе у таких известных спортсменов, как Мерлин Отти , Дитер Бауманн и Линфорд Кристи . [59] Однако в следующем году было доказано, что метод обнаружения нандролона в то время был неисправен. Марк Ричардсон , британский олимпийский бегун-эстафетист, у которого был положительный результат на это вещество, сдал значительное количество образцов мочи в контролируемой среде и показал положительный результат на препарат, продемонстрировав, что возможны ложные положительные результаты, что привело к пересмотру его запрета на участие в соревнованиях. [60]
Интенсивное потребление незаменимой аминокислоты лизина (как указано в лечении герпеса) предположительно показало ложные положительные результаты у некоторых и было упомянуто американским толкателем ядра С. Дж. Хантером в качестве причины его положительного теста, хотя в 2004 году он признался федеральному большому жюри , что он вводил себе нандролон. [61] Возможной причиной неверных результатов анализа мочи является присутствие метаболитов других анаболических стероидов, хотя современный анализ мочи обычно может определить точный используемый анаболический стероид, анализируя соотношение двух оставшихся метаболитов нандролона. В результате многочисленных отмененных вердиктов процедура тестирования была пересмотрена UK Sport . В октябре 2007 года трехкратная олимпийская чемпионка по легкой атлетике Мэрион Джонс призналась в употреблении препарата и была приговорена к шести месяцам тюремного заключения за ложь федеральному большому жюри в 2000 году. [62]
Масс-спектрометрия также используется для обнаружения небольших количеств нандролона в образцах мочи. [63]
История

Нандролон был впервые синтезирован в 1950 году. [2] [43] [18] : 130 [64] Впервые он был представлен как нандролон фенилпропионат в 1959 году, а затем как нандролон деканоат в 1962 году, за которым последовали дополнительные эфиры. [65]
Общество и культура
Общие названия
Нандролон — это общее название препарата и его МНН.Подсказка Международное непатентованное название, БАНПодсказка: одобренное британцами имя, ДКФПодсказка: Наименование: Французская коммунаи DCITПодсказка: Denominazione Comune Italiana. [2] [12] [3] [66] Официальные дженерики эфиров нандролона включают нандролон циклогексилпропионат ( BANMПодсказка: одобренное британцами имя), нандролона циклотат ( СШАПодсказка Соединенные Штаты Принятое название), нандролона деканоат ( USANПодсказка USAN, USPПодсказка Фармакопея США, БАНМПодсказка: одобренное британцами имя, ЯНВАРЬПодсказка Японское принятое имя), нандролона лаурат ( BANMПодсказка: одобренное британцами имя), нандролон фенпропионат ( USPПодсказка Фармакопея США) и нандролон фенилпропионат ( BANMПодсказка: одобренное британцами имя, ЯНВАРЬПодсказка Японское принятое имя). [2] [12] [3] [66]
Допинг в спорте
Нандролон, вероятно, был одним из первых анаболических стероидов, использовавшихся в качестве допингового агента в спорте в 1960-х годах. [ необходима ссылка ] Он был запрещён на Олимпийских играх с 1974 года. [18] : 128 Известно много случаев использования допинга в спорте с использованием эфиров нандролона профессиональными спортсменами .
Исследовать
Эфиры нандролона изучались по нескольким показаниям. Они интенсивно изучались на предмет остеопороза , а также увеличения усвоения кальция и снижения потери костной массы, но вызывали вирилизацию примерно у половины женщин, которые их принимали, и в основном были оставлены для этого использования, когда стали доступны лучшие препараты, такие как бисфосфонаты . [21] Они также изучались в клинических испытаниях на предмет хронической почечной недостаточности , апластической анемии и в качестве мужских контрацептивов . [18] : 134
Ссылки
- ^ «Значение нандролона в Кембриджском словаре английского языка».
- ^ abcdefghijklmno Elks J, Ganellin CR, ред. (2014). Словарь лекарств: химические данные: химические данные, структуры и библиографии . Нью-Йорк: Springer. стр. 660–. ISBN 978-1-4757-2085-3. OCLC 1079003025.
- ^ abcd Morton IK, Hall JM (6 декабря 2012 г.). Краткий словарь фармакологических средств: свойства и синонимы. Springer Science & Business Media. ISBN 978-94-011-4439-1.
- ^ Анвиса (31 марта 2023 г.). «RDC № 784 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial» [Постановление Коллегиального совета № 784 - Списки наркотических, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем] (на бразильском португальском языке). Diário Oficial da União (опубликовано 4 апреля 2023 г.). Архивировано из оригинала 3 августа 2023 г. Проверено 15 августа 2023 г.
- ^ ab McEvoy JD, McVeigh CE, McCaughey WJ (декабрь 1998 г.). «Остатки эфиров нортестостерона в местах инъекций. Часть 1. Оральная биодоступность». The Analyst . 123 (12): 2475– 8. doi :10.1039/a804919j. PMID 10435281.
- ^ Беккер К. Л. (2001). Принципы и практика эндокринологии и метаболизма. Lippincott Williams & Wilkins. стр. 1185–. ISBN 978-0-7817-1750-2.
- ^ abcdefg "Deca-Durabolin" (PDF) . Schering-Plough . Архивировано из оригинала (PDF) 18 декабря 2010 г.
- ^ abcdefghijklmnopqrst Llewellyn W (2011). Анаболики. Molecular Nutrition Llc. стр. 402– 412, 460– 467, 193– 194. ISBN 978-0-9828280-1-4.
- ^ ab Thomas JA (6 декабря 2012 г.). Лекарства, спортсмены и физическая работоспособность. Springer Science & Business Media. стр. 27–29 . ISBN 978-1-4684-5499-4.
- ^ abc Minto CF, Howe C, Wishart S, Conway AJ, Handelsman DJ (апрель 1997 г.). «Фармакокинетика и фармакодинамика эфиров нандролона в масляном растворителе: эффекты эфира, места инъекции и объема инъекции». Журнал фармакологии и экспериментальной терапии . 281 (1): 93–102 . PMID 9103484.
- ^ "Дека-Дураболин" (PDF) . Merck Sharp & Dohme (Австралия) .
- ^ abcdefghi Index Nominum 2000: Международный каталог лекарств. Тейлор и Фрэнсис. Январь 2000 г., стр. 716–. ISBN 978-3-88763-075-1.
- ^ ab Sneader W (23 июня 2005 г.). Drug Discovery: A History. John Wiley & Sons. стр. 206–. ISBN 978-0-471-89979-2.
- ^ Singh GK, Turner L, Desai R, Jimenez M, Handelsman DJ (июль 2014 г.). «Фармакокинетическое-фармакодинамическое исследование подкожной инъекции депо нандролона деканоата с использованием отбора проб сухих пятен крови в сочетании с тандемными масс-спектрометрическими анализами под давлением». Журнал клинической эндокринологии и метаболизма . 99 (7): 2592– 8. doi : 10.1210/jc.2014-1243 . PMID 24684468.
- ^ abcde Kicman AT (июнь 2008). «Фармакология анаболических стероидов». British Journal of Pharmacology . 154 (3): 502– 21. doi :10.1038/bjp.2008.165. PMC 2439524. PMID 18500378 .
- ^ Kochakian CD (6 декабря 2012 г.). Анаболические-андрогенные стероиды. Springer Science & Business Media. стр. 401–. ISBN 978-3-642-66353-6.
- ^ Jameson JL, De Groot LJ (25 февраля 2015 г.). Эндокринология: электронная книга для взрослых и детей. Elsevier Health Sciences. стр. 2388–. ISBN 978-0-323-32195-2.
- ^ abcd Hemmersbach P, Große J (2009). «Нандролон: многогранный допинг». В Тиме Д., Хеммерсбах П. (ред.). Допинг в спорте . Берлин: Шпрингер. стр. 127–154 . ISBN. 978-3-540-79088-4.
- ^ Handelsman DJ (2013). "Андрогенная физиология, фармакология и злоупотребление". В De Groot LJ (ред.). Endotext . MDText.com. 4.1.2 Фармакологическая андрогенная терапия. PMID 25905160 – через NCBI Bookshelf.
И тестостерон, и его неароматизируемое производное нандролон вызывают повышение плотности костной ткани у мужчин с остеопорозом, вызванным глюкокортикоидами, с минимальными краткосрочными побочными эффектами....
- ^ abcdef Камерино Б, Сала Г (1960). «Анаболические стероиды». Fortschritte der Arzneimittelforschung / Прогресс в исследованиях лекарств / Progrès des recherches pharmaceutiques . Том. 2. С. 71–134 . doi :10.1007/978-3-0348-7038-2_2. ISBN 978-3-0348-7040-5. PMID 14448579.
{{cite book}}:|journal=проигнорировано ( помощь ) - ^ abc Pan MM, Kovac JR (апрель 2016 г.). «За пределами тестостерона ципионата: доказательства использования нандролона в мужском здоровье и благополучии». Трансляционная андрология и урология . 5 (2): 213– 9. doi : 10.21037 / tau.2016.03.03 . PMC 4837307. PMID 27141449.
- ^ ab Bergink EW, Janssen PS, Turpijn EW, van der Vies J (июнь 1985). «Сравнение свойств связывания рецепторов нандролона и тестостерона в условиях in vitro и in vivo». Journal of Steroid Biochemistry . 22 (6): 831– 6. doi :10.1016/0022-4731(85)90293-6. PMID 4021486.
- ^ Brueggemeier RW (16 сентября 2006 г.). "Половые гормоны (мужские): аналоги и антагонисты". В Meyers RA (ред.). Энциклопедия молекулярной клеточной биологии и молекулярной медицины (аннотация). John Wiley & Sons . doi :10.1002/3527600906.mcb.200500066. ISBN 978-3527600908.
- ^ ab Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения». Climacteric . 8 (Suppl 1): 3– 63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ abc de Souza GL, Hallak J (декабрь 2011 г.). «Анаболические стероиды и мужское бесплодие: всесторонний обзор». BJU International . 108 (11): 1860– 5. doi : 10.1111/j.1464-410X.2011.10131.x . PMID 21682835. S2CID 29035729.
- ^ Couzinet B, Young J, Brailly S, Chanson P, Thomas JL, Schaison G (декабрь 1996 г.). «Антигонадотропная активность прогестинов (19-нортестостерона и производных 19-норпрогестерона) не опосредована андрогеновым рецептором». Журнал клинической эндокринологии и метаболизма . 81 (12): 4218– 23. doi : 10.1210/jcem.81.12.8954018 . PMID 8954018.
- ^ Мове-Джарвис, П. «Прогестерон и прогестины: общий обзор». (1983): 1-16.
- ^ ab Camerino B, Sciaky R (1975). «Структура и эффекты анаболических стероидов». Pharmacology & Therapeutics B . 1 (2): 233– 75. doi :10.1016/0306-039X(75)90007-0. PMID 817322.
- ^ Holtkamp DE, Heming AE, Mansor LF (1955). «Сравнение перорального и подкожного введения анаболической и андрогенной эффективности 19-нортестостерона и тестостерона». Журнал клинической эндокринологии и метаболизма . 15 (7): 848. doi : 10.1210/jcem-15-7-834 . ISSN 0021-972X.
- ^ Furman RH, Howard RP, Smith CW, Norcia LN (январь 1956). «Сравнение эффектов перорального метилтестостерона, 19-нортестостерона и 17-метил-19-нортестостерона на сывороточные липиды и липопротеины». Журнал лабораторной и клинической медицины . 48 (5): 808–809 .
- ^ Furman RH, Howard RP, Norcia LN, Keaty EC (январь 1958). «Влияние андрогенов, эстрогенов и родственных стероидов на липиды сыворотки и липопротеины». The American Journal of Medicine . 24 (1): 80–97 . doi :10.1016/0002-9343(58)90364-4. PMID 13498038.
- ^ Арнольд А., Поттс ГО (январь 1964 г.). «Пероральные анаболические и андрогенные эффекты 19-нортестостерона и 17α-метил-19-нортестостерона». Труды Федерации . 23 (2): 412.
- ^ ab Baker WH, Henneman PH, Baggett B, Engel LL, Tibbetts D, Brown M (январь 1955 г.). «Метаболический эффект 19-нортестостерона». Журнал клинической эндокринологии и метаболизма . 15 (7): 848– 849. doi : 10.1210/jcem-15-7-834 . ISSN 0021-972X.
- ^ Saartok T, Dahlberg E, Gustafsson JA (июнь 1984). «Относительная связывающая способность анаболических андрогенных стероидов: сравнение связывания с рецепторами андрогенов в скелетных мышцах и простате, а также с глобулином, связывающим половые гормоны». Эндокринология . 114 (6): 2100– 6. doi :10.1210/endo-114-6-2100. PMID 6539197.
- ^ abc Бергинк Э.В., Гилен Дж.А., Турпейн Э.В. (1985). «Метаболизм и связывание рецепторов нандролона и тестостерона в условиях in vitro и in vivo». Акта Эндокринологика. Дополнение . 271 (3_Suppla): 31–7 . doi :10.1530/acta.0.109S0031. ПМИД 3865479.
- ^ Mottram DR (12 ноября 2010). Наркотики в спорте. Routledge. стр. 63–. ISBN 978-1-135-25825-2.
- ^ Дорфман RI (5 декабря 2016 г.). Стероидная активность у экспериментальных животных и человека. Elsevier Science. стр. 68–. ISBN 978-1-4832-7300-6.
- ^ Багчус В.М., Смитс Дж.М., Верхеул Х.А., Де Ягер-Ван Дер Вин С.М., Порт А, Гертс ТБ (2005). «Фармакокинетическая оценка трех различных внутримышечных доз деканоата нандролона: анализ образцов сыворотки и мочи у здоровых мужчин». Дж. Клин. Эндокринол. Метаб . 90 (5): 2624–30 . doi :10.1210/jc.2004–1526. ПМИД 15713722.
- ^ Minto CF, Howe C, Wishart S, Conway AJ, Handelsman DJ (1997). «Фармакокинетика и фармакодинамика эфиров нандролона в масляном растворителе: эффекты эфира, места инъекции и объема инъекции». J. Pharmacol. Exp. Ther . 281 (1): 93–102 . PMID 9103484.
- ^ Белкин Л., Шюрмейер Т., Хано Р., Гуннарссон П.О., Нишлаг Э. (май 1985 г.). «Фармакокинетика эфиров 19-нортестостерона у нормальных мужчин». Дж. Стероидная биохимия . 22 (5): 623–9 . doi :10.1016/0022-4731(85)90215-8. ПМИД 4010287.
- ^ Kalicharan RW, Schot P, Vromans H (февраль 2016 г.). «Фундаментальное понимание абсорбции лекарств из парентерального масляного депо». Eur J Pharm Sci . 83 : 19–27 . doi :10.1016/j.ejps.2015.12.011. PMID 26690043.
- ^ Каличаран, Равин Викеш (2017). Новые знания о всасывании лекарств из нефтяных складов (PhD). Утрехтский университет.
- ^ ab Schnitzer R (1 января 1967 г.). Экспериментальная химиотерапия. Elsevier Science. стр. 165–. ISBN 978-0-323-14611-1.
- ^ Bricout V, Wright F (июнь 2004 г.). «Обновление по нандролону и норстероидам: насколько эндогенными или ксенобиотическими являются эти вещества?». European Journal of Applied Physiology . 92 ( 1–2 ): 1–12 . doi :10.1007/s00421-004-1051-3. PMID 15042372. S2CID 6472015.
- ^ Lippi G, Franchini M, Banfi G (май 2011). «Биохимия и физиология допинга анаболических андрогенных стероидов». Mini Reviews in Medicinal Chemistry . 11 (5): 362–73 . doi :10.2174/138955711795445952. PMID 21443514. S2CID 3862299.
- ^ abc Шиндлер А.Е., Кампаньоли С., Друкманн Р., Хубер Дж., Паскуалини Дж.Р., Швеппе К.В., Тийссен Дж.Х. (декабрь 2003 г.). «Классификация и фармакология прогестинов». Матуритас . 46 (Приложение 1): S7 – S16 . doi :10.1016/j.maturitas.2003.09.014. ПМИД 14670641.
- ^ Meikle AW (24 апреля 2003 г.). Эндокринная заместительная терапия в клинической практике. Springer Science & Business Media. стр. 489–. ISBN 978-1-59259-375-0.
Эстраны. Эстрановые и гонановые прогестагены получены из 19-нортестостерона, исходного прогестагенного соединения, используемого в оральных контрацептивах в Соединенных Штатах. Эстраны характеризуются наличием этинильной группы в положении 17 и отсутствием метильной группы между кольцами A и B (см. рис. 10). Эстрановые прогестагены, структурно связанные с норэтиндроном (норэтинодрел, линестренол, норэтиндрона ацетат, этинодиол диацетат), преобразуются в это исходное соединение. Норэтиндрон является вторым наиболее часто используемым прогестагеном в Соединенных Штатах для ЗГТ. Гонаны. Гонаны разделяют структурные модификации, обнаруженные в эстранах, а также обладают этинильной группой в положении 13 и кетогруппой в положении 3 (см. рис. 11). Норгестрел был синтезирован в 1963 году и представляет собой рацемическую смесь правовращающей и левовращающей форм. Левовращающая форма, левоноргестрел, обеспечивает биологическую активность. Гонаны третьего поколения (дезогестрел, гестоден и норгестимат) были разработаны для снижения нежелательных побочных эффектов прогестагенов, [...]
- ^ Wilds AL, Nelson NA (1953). «Простой синтез 19-нортестостерона и 19-норандростендиона из эстрона». Журнал Американского химического общества . 75 (21): 5366– 5369. doi :10.1021/ja01117a065.
- ^ Убервассер Х, Хейслер К, Кальвода Дж, Мейстре Ч, Виланд П, Аннер Г, Веттштейн А (1963). «19-Норстероид II. Ein einfaches Herstellungsverfahren für 19-Norandrostan-Derivate. Убер-стероид, 193. Mitteilung». Helvetica Chimica Acta . 46 : 344–352 . doi : 10.1002/hlca.19630460135.
- ^ Shimizu I, Naito Y, Tsuji J (1980). «Синтез оптически активного (+)-19-нортестостерона с помощью асимметричной реакции бис-аннуляции». Tetrahedron Letters . 21 (5): 487– 490. doi :10.1016/S0040-4039(00)71440-7.
- ^ Birch AJ (1950). «Восстановление органических соединений металл-аммиачными растворами». Quarterly Reviews, Chemical Society . 4 : 69. doi :10.1039/QR9500400069.
- ^ US 2998423, DeWytt ED, Overbeek O, Overbeek GA, выдан в 1961 году, передан Organon .
- ^ CH 206119, выдан в 1939 году, передан Gesellschaft für Chemische Industrie Basel.
- ^ "Разъяснение о тестировании нандролона". Всемирное антидопинговое агентство. 2005-05-30. Архивировано из оригинала 2012-09-15 . Получено 2012-01-31 .
- ^ Bresson M, Cirimele V, Villain M, Kintz P (май 2006 г.). «Допинг-контроль метандиенона с использованием анализа волос методом газовой хроматографии-тандемной масс-спектрометрии». Журнал хроматографии. B, Аналитические технологии в биомедицинских и биологических науках . 836 ( 1– 2): 124– 8. doi :10.1016/j.jchromb.2006.03.040. PMID 16597518.
- ^ Ueki M, Ikekita A, Takao Y (2000). «[Метаболит нандролона в моче спортсмена-олимпийца Нагано]». Jap. J. For. Tox. (на японском языке). 18 : 198– 199.
- ^ Catlin DH, Leder BZ, Ahrens B, Starcevic B, Hatton CK, Green GA, Finkelstein JS (2000). «Следовое загрязнение безрецептурного андростендиона и положительные результаты анализа мочи на метаболит нандролона». JAMA . 284 (20): 2618– 21. doi : 10.1001/jama.284.20.2618 . PMID 11086369.
- ^ Базелт RC (2008). Распределение токсичных лекарств и химикатов в организме человека (8-е изд.). Фостер-Сити, Калифорния: Биомедицинские публикации. стр. 1078–1080 . ISBN 978-0-9626523-7-0. Архивировано из оригинала 2020-12-04 . Получено 2010-08-19 .
- ^ Baron P (19 сентября 2000 г.). «Проблема наркотиков: Бауманн будет бороться до конца» . The Telegraph . Получено 13 ноября 2010 г.
- ^ Ричардсон М. (2004-02-19). «Легкая атлетика: Марк Ричардсон объясняет, что он чувствовал на дисциплинарном слушании». The Guardian . Получено 2010-11-13 .
- ^ "Звезда легкой атлетики Мэрион Джонс призналась в употреблении стероидов". National Public Radio. 2007-10-05 . Получено 2009-11-09 .
- ^ Спортивное антидопинговое управление Великобритании (январь 2000 г.). Обзор нандролона (PDF) (Отчет). UK Sport . Архивировано из оригинала (PDF) 2005-04-04 . Получено 2013-02-02 .
- ^ Buiarelli F, Giannetti L, Jasionowska R, Cruciani C, Neri B (июль 2010 г.). «Определение метаболитов нандролона в моче человека: сравнение жидкостной хроматографии/тандемной масс-спектрометрии и газовой хроматографии/масс-спектрометрии». Rapid Communications in Mass Spectrometry . 24 (13): 1881– 1894. Bibcode :2010RCMS...24.1881B. doi : 10.1002/rcm.4583 . PMID 20533318.
- ^ Birch AJ (1950). "80. Гидроароматические стероидные гормоны. Часть I. 10-нортестостерон". Журнал химического общества (возобновлено) : 367. doi :10.1039/jr9500000367. ISSN 0368-1769.
- ^ Сводный список продуктов, потребление и/или продажа которых запрещены, изъяты, строго ограничены или не одобрены правительствами. Издания Организации Объединенных Наций. 1983. С. 154–. ISBN 978-92-1-130230-1.[ постоянная мертвая ссылка ]
- ^ ab "Нандролон".
Дальнейшее чтение
- Geusens P (сентябрь 1995 г.). «Нандролона деканоат: фармакологические свойства и терапевтическое применение при остеопорозе». Клиническая ревматология . 14 (Приложение 3): 32– 9. doi :10.1007/bf02210686. PMID 8846659. S2CID 24365057.
- Kicman AT (июнь 2008 г.). «Фармакология анаболических стероидов». British Journal of Pharmacology . 154 (3): 502– 21. doi :10.1038/bjp.2008.165. PMC 2439524. PMID 18500378 .
- Хеммерсбах П., Гроссе Дж. (2010). «Нандролон: многогранный допинговый агент». Допинг в спорте . Справочник экспериментальной фармакологии. Том 195. С. 127–54 . doi :10.1007/978-3-540-79088-4_6. ISBN 978-3-540-79087-7. PMID 20020363.
- Velema MS, Kwa BH, de Ronde W (март 2012 г.). «Следует ли рассматривать андрогенные анаболические стероиды в режиме лечения отдельных пациентов с хронической обструктивной болезнью легких?». Current Opinion in Pulmonary Medicine . 18 (2): 118– 24. doi :10.1097/MCP.0b013e32834e9001. PMID 22189453. S2CID 6155275.
- Busardò FP, Frati P, Sanzo MD, Napoletano S, Pinchi E, Zaami S, Fineschi V (январь 2015 г.). «Влияние нандролона деканоата на центральную нервную систему». Current Neuropharmacology . 13 (1): 122– 31. doi :10.2174/1570159X13666141210225822. PMC 4462037. PMID 26074747 .
- Wu C, Kovac JR (октябрь 2016 г.). «Новые способы применения анаболических андрогенных стероидов нандролона и оксандролона в лечении мужского здоровья». Current Urology Reports . 17 (10): 72. doi :10.1007/s11934-016-0629-8. PMID 27535042. S2CID 43199715.
- Pan MM, Kovac JR (апрель 2016 г.). «За пределами тестостерона ципионата: доказательства использования нандролона в мужском здоровье и благополучии». Трансляционная андрология и урология . 5 (2): 213– 9. doi : 10.21037/tau.2016.03.03 . PMC 4837307. PMID 27141449 .

![Уровень нандролона после однократной внутримышечной инъекции 50, 100 или 150 мг нандролона деканоата в масляном растворе у мужчин.[38]](http://upload.wikimedia.org/wikipedia/commons/thumb/0/03/Nandrolone_levels_after_a_single_intramuscular_injection_of_different_doses_of_nandrolone_decanoate.png/298px-Nandrolone_levels_after_a_single_intramuscular_injection_of_different_doses_of_nandrolone_decanoate.png)
![Уровни нандролона после однократной внутримышечной инъекции 100 мг нандролона деканоата или нандролона фенилпропионата в 4 мл или 1 мл раствора арахисового масла в ягодичную или дельтовидную мышцу у мужчин.[39]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/da/Nandrolone_levels_after_a_single_100_mg_intramuscular_injection_of_nandrolone_esters.png/300px-Nandrolone_levels_after_a_single_100_mg_intramuscular_injection_of_nandrolone_esters.png)
![Уровни нандролона при однократной внутримышечной инъекции 50 мг нандролона деканоата или нандролона гексилоксифенилпропионата в масляном растворе у мужчин.[40]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/e8/Nandrolone_levels_with_a_single_dose_of_nandrolone_decanoate_or_nandrolone_hexyloxyphenylpropionate_by_intramuscular_injection_in_men.png/300px-Nandrolone_levels_with_a_single_dose_of_nandrolone_decanoate_or_nandrolone_hexyloxyphenylpropionate_by_intramuscular_injection_in_men.png)
![Нормализованное по дозе воздействие нандролона (уровень в сыворотке, деленный на введенную дозу) при внутримышечной или подкожной инъекции нандролона деканоата в масляном растворе у мужчин.[41][42]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/50/Dose-normalized_nandrolone_exposure_with_nandrolone_decanoate_by_intramuscular_or_subcutaneous_injection_in_men.png/300px-Dose-normalized_nandrolone_exposure_with_nandrolone_decanoate_by_intramuscular_or_subcutaneous_injection_in_men.png)