Антраниловая кислота
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 2-Аминобензойная кислота [1] | |||
| Систематическое название ИЮПАК 2-Аминобензолкарбоновая кислота | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 3DMet |
| ||
| 471803 | |||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Информационная карта ECHA | 100.003.898 | ||
| Номер ЕС |
| ||
| 3397 | |||
| КЕГГ | |||
CID PubChem |
| ||
| Номер RTECS |
| ||
| УНИИ |
| ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С7Н7НО2 | |||
| Молярная масса | 137,138 г·моль −1 | ||
| Появление | белое или желтое твердое вещество | ||
| Запах | без запаха | ||
| Плотность | 1,412 г/см 3 | ||
| Температура плавления | 146–148 °C (295–298 °F; 419–421 K) [3] | ||
| Точка кипения | 200 °C (392 °F; 473 K) (возгоняется) | ||
| 0,572 г/100 мл (25 °C) | |||
| Растворимость | очень хорошо растворим в хлороформе , пиридине, растворим в этаноле , эфире , этиловом эфире , слабо растворим в трифторуксусной кислоте , бензоле | ||
| лог P | 1.21 | ||
| Давление пара | 0,1 Па (52,6 °С) | ||
| Кислотность ( pK a ) |
| ||
| -77,18·10 −6 см 3 /моль | |||
Показатель преломления ( nD ) | 1,578 (144 °С) | ||
| Термохимия | |||
Стандартная энтальпия образования (Δ f H ⦵ 298 ) | -380,4 КДж/моль | ||
| Опасности | |||
| Маркировка СГС : | |||
  | |||
| Опасность | |||
| Н318 , Н319 | |||
| П264 , П280 , П305+П351+П338 , П310 , П337+П313 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | > 150 °C (302 °F; 423 К) | ||
| > 530 °C (986 °F; 803 К) | |||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD 50 ( средняя доза ) | 1400 мг/кг (перорально, крыса) | ||
| Паспорт безопасности (SDS) | Внешний ПБС | ||
| Правовой статус |
| ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Антраниловая кислота — ароматическая кислота с формулой C 6 H 4 (NH 2 )(CO 2 H) и имеет сладковатый вкус. [5] [6] [7] Молекула состоит из бензольного кольца, орто -замещенного карбоновой кислотой и амином . В результате содержания как кислотных, так и основных функциональных групп соединение является амфотерным . Антраниловая кислота представляет собой белое твердое вещество в чистом виде, хотя коммерческие образцы могут выглядеть желтыми. Анион [C 6 H 4 (NH 2 )(CO 2 )] − , полученный путем депротонирования антраниловой кислоты, называется антранилатом . Антраниловая кислота когда-то считалась витамином и упоминалась как витамин L 1 в этом контексте, но теперь известно, что она не является существенной в питании человека. [8]
Структура
Хотя обычно ее так не называют, это аминокислота . Твердая антраниловая кислота обычно состоит из аминокарбоновой кислоты и цвиттерионного аммонийкарбоксилата и имеет моноклинную кристаллическую структуру с пространственной группой P2 1 . [9] Она триболюминесцентна . [10] Выше 81 °C (178 °F; 354 K) она превращается в орторомбическую форму с пространственной группой Pbca, которая не является триболюминесцентной; также известна нетриболюминесцентная моноклинная фаза с похожей структурой. [10]
Производство
Описано много путей получения антраниловой кислоты. В промышленности ее получают из фталевого ангидрида , начиная с аминирования:
- C 6 H 4 (CO) 2 O + NH 3 + NaOH → C 6 H 4 (C(O)NH 2 )CO 2 Na + H 2 O
Полученная натриевая соль фталамовой кислоты декарбонилируется посредством перегруппировки Гофмана амидной группы, вызванной гипохлоритом : [11]
- C 6 H 4 (C(O)NH 2 )CO 2 Na + HOCl → C 6 H 4 NH 2 CO 2 H + NaCl + CO 2
Схожий метод включает обработку фталимида гипобромитом натрия в водном растворе гидроксида натрия с последующей нейтрализацией. [12] В эпоху, когда краситель индиго получали из растений, его разлагали с образованием антраниловой кислоты.
Антраниловая кислота была впервые получена путем щелочной деградации индиго. [13]
Биосинтез
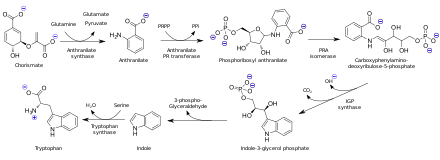
Антраниловая кислота биосинтезируется из хоризмовой кислоты под действием антранилатсинтазы . В организмах, способных к синтезу триптофана, антранилат является предшественником аминокислоты триптофана посредством присоединения фосфорибозилпирофосфата к аминогруппе . После этого происходит циклизация с образованием индола .
Использует
В промышленности антраниловая кислота является промежуточным продуктом в производстве азокрасителей и сахарина . Она и ее эфиры используются в изготовлении духов, имитирующих жасмин и апельсин , фармацевтических препаратов ( петлевые диуретики , такие как фуросемид ) и УФ-поглотителей, а также ингибиторов коррозии металлов и ингибиторов плесени в соевом соусе .
В качестве замены ДЭТА были предложены репелленты на основе антранилата .
Фенамовая кислота является производным антраниловой кислоты, [14] : 235 которая в свою очередь является азотным изостером салициловой кислоты , которая является активным метаболитом аспирина . [14] : 235 Несколько нестероидных противовоспалительных препаратов , включая мефенамовую кислоту , толфенамовую кислоту , флуфенамовую кислоту и меклофенамовую кислоту , являются производными фенамовой кислоты или антраниловой кислоты и называются «производными антраниловой кислоты» или «фенаматами». [15] : 17
Реакции
Антраниловая кислота может быть диазотирована с образованием катиона диазония [C 6 H 4 (CO 2 H)(N 2 )] + . Этот катион может быть использован для получения бензина [16] , димеризован с образованием дифеновой кислоты [ 17] или подвергнут реакциям сочетания диазония, например, при синтезе метилового красного [18] .
Он реагирует с фосгеном, образуя изатовый ангидрид , универсальный реагент. [19]
Хлорирование антраниловой кислоты дает 2,4-дихлорпроизводное, которое может подвергаться восстановительной реакции с образованием биарильного соединения. [20]
Безопасность и регулирование
Он также входит в список I химических веществ Управления по борьбе с наркотиками из-за его использования в производстве ныне повсеместно запрещенного эйфорического седативного препарата метаквалон (Кваалюд, Мандракс). [21]
Смотрите также
Ссылки
- ^ "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 748. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Хейнс, Уильям М., ред. (2016). CRC Handbook of Chemistry and Physics (97-е изд.). CRC Press . стр. 5–89. ISBN 978-1498754286.
- ^ МПХБ
- ^ Анвиса (31 марта 2023 г.). «RDC № 784 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial» [Постановление Коллегиального совета № 784 - Списки наркотических, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем] (на бразильском португальском языке). Diário Oficial da União (опубликовано 4 апреля 2023 г.). Архивировано из оригинала 3 августа 2023 г. Проверено 15 августа 2023 г.
- ^ Актон, К. Эштон (2013). Аминобензойные кислоты — достижения в исследованиях и применении (ред. 2013 г.). Атланта: ScholarlyEditions. стр. 23. ISBN 9781481684842– через Google Книги.
- ^ Харди, Марк Р. (1997). «Маркировка гликанов с помощью флуорофоров 2-аминобензамида и антраниловой кислоты». В Таунсенд, Р. Рейд; Хотчкисс, Арланд Т. младший (ред.). Методы в гликобиологии. Marcel Dekker, Inc. стр. 360. ISBN 9780824798222– через Google Книги.
- ↑ The Merck Index, 10-е изд. (1983), стр. 62., Rahway: Merck & Co.
- ^ Дэвидсон, Майкл У. (2004). "Антраниловая кислота (витамин L)]". Университет штата Флорида . Получено 20 ноября 2019 г.
- ^ Браун, CJ (1968). «Кристаллическая структура антраниловой кислоты». Труды Лондонского королевского общества. Серия A. Математические и физические науки . 302 (1469): 185–199. Bibcode : 1968RSPSA.302..185B. doi : 10.1098/rspa.1968.0003. S2CID 93221347.
- ^ ab Hardy, Gordon E.; Kaska, William C.; Chandra, BP; Zink, Jeffrey I. (март 1981 г.). «Связь триболюминесценции и структуры в полиморфах гексафенилкарбодифосфорана и антраниловой кислоты, молекулярных кристаллах и солях». Журнал Американского химического общества . 103 (5): 1074–1079. doi :10.1021/ja00395a014.
- ^ Маки, Такао; Такеда, Казуо (2000). «Бензойная кислота и ее производные». Энциклопедия промышленной химии Ульмана . doi :10.1002/14356007.a03_555. ISBN 3527306730..
- ^ Учебник практической органической химии Фогеля, 4-е изд. , (ред. Б. С. Фернисс и др.) (1978), стр. 666, Лондон: Longman.
- ^ Sheibley, Fred E. (1943). "Карл Юлиус Фрицше и открытие антраниловой кислоты, 1841". Журнал химического образования . 20 (3): 115. Bibcode : 1943JChEd..20..115S. doi : 10.1021/ed020p115.
- ^ ab Sriram D, Yogeeswari P. Лечебная химия, 2-е издание. Pearson Education India, 2010. ISBN 9788131731444
- ^ Материал курса Университета Оберн. Джек ДеРуйтер, Принципы действия лекарств 2, осень 2002 г. 1: Нестероидные противовоспалительные препараты (НПВП)
- ^ Логулло, FM; Seitz, AH; Friedman, L. (1968). "Бензендиазоний-2-карбокси- и бифенилен". Органические синтезы . 48 : 12.
- ^ Аткинсон, Э. Р.; Лоулер, Х. Дж. (1927). «Дифеновая кислота». Органические синтезы . 7 : 30. doi :10.15227/orgsyn.007.0030.
- ^ Кларк, HT; Кирнер, WR (1922). "Метиловый красный". Органические синтезы . 2 : 47.
- ^ Вагнер, EC; Фегли, Мэрион Ф. (1947). «Изатоовый ангидрид». Орг. Синтез . 27 : 45. дои : 10.15227/orgsyn.027.0045.
- ^ Аткинсон, Эдвард Р.; Мерфи, Дональд М.; Лафкин, Джеймс Э. (1951). "dl-4,4',6,6'-Тетрахлордифеновая кислота". Органические синтезы . 31 : 96.
- ^ Angelos SA, Meyers JA (1985). «Выделение и идентификация прекурсоров и продуктов реакции при подпольном производстве метаквалона и меклоквалона». Журнал судебной экспертизы . 30 (4): 1022–1047. doi :10.1520/JFS11044J. PMID 3840834.