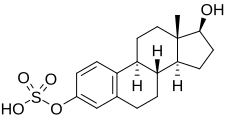
Эстрадиол сульфат
 | |
| Имена | |
|---|---|
| Название ИЮПАК 17β-Гидроксиэстра-1,3,5(10)-триен-3-ил гидросульфат | |
| Систематическое название ИЮПАК (1 S ,3a S ,3b R ,9b S ,11a S )-1-гидрокси-11a-метил-2,3,3a,3b,4,5,9b,10,11,11a-декагидро-1 H -циклопента[ a ]фенантрен-7-ил гидросульфат | |
| Другие имена Эстра-1,3,5(10)-триен-3,17β-диол 3-сульфат | |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| ЧЭБИ |
|
| ChEMBL |
|
| ChemSpider |
|
CID PubChem |
|
| УНИИ |
|
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С18Н24О5С | |
| Молярная масса | 352,445 г/моль |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Эстрадиолсульфат ( E2S ), или 17β-эстрадиол 3-сульфат , [1] является естественным эндогенным стероидом и эфиром эстрогена . [2] Сам по себе E2S биологически неактивен, [3] но он может быть преобразован стероидсульфатазой (также называемой эстрогенсульфатазой) в эстрадиол , который является мощным эстрогеном . [2] [4] [5] Одновременно эстрогенсульфотрансферазы преобразуют эстрадиол в E2S, что приводит к равновесию между двумя стероидами в различных тканях. [2] [5] Эстрон и E2S являются двумя непосредственными метаболическими источниками эстрадиола. [6] E2S также может метаболизироваться в эстронсульфат (E1S), который, в свою очередь, может быть преобразован в эстрон и эстрадиол. [7] Циркулирующие концентрации E2S намного ниже, чем концентрации E1S. [1] Высокие концентрации E2S присутствуют в тканях молочной железы , и E2S участвует в биологии рака молочной железы , выступая в качестве активного резервуара эстрадиола. [2] [4]
Как натриевая соль сульфата эстрадиола натрия , E2S присутствует в качестве второстепенного компонента (0,9%) конъюгированных конских эстрогенов (КЭЭ) или премарина . [8] Он эффективно функционирует как пролекарство эстрадиола в этом препарате, аналогично E1S. E2S также образуется как метаболит эстрадиола, а также эстрона и E1S. [9] [10] Помимо своего присутствия в КЭЭ, E2S недоступен в качестве коммерческого фармацевтического препарата . [11]
E2S демонстрирует примерно в 10 000 раз более низкую эффективность в активации рецепторов эстрогена по сравнению с эстрадиолом in vitro . [12] Он в 10 раз менее эффективен , чем пероральный сульфат эстрона с точки зрения утеротрофического эффекта in vivo у крыс. [13] Эстрогенные сульфаты, такие как сульфат эстрадиола или сульфат эстрона, примерно в два раза эффективнее соответствующих свободных эстрогенов с точки зрения эстрогенного эффекта при пероральном введении грызунам. [14] Это отчасти привело к появлению в 1941 году конъюгированных эстрогенов (Премарин), которые в основном представляют собой сульфат эстрона. [14]
Хотя E2S неактивен в отношении рецепторов стероидных гормонов , было обнаружено, что он действует как мощный ингибитор глутатион- S-трансферазы [15] , фермента , который способствует инактивации эстрадиола путем его превращения в конъюгат эстрадиол- глутатион . [16] Таким образом, E2S может косвенно служить положительным эффектором сигнализации эстрогена. [15]
Уровни эстрадиола примерно в 1,5-4 раза выше, чем уровни E2S у женщин. Это контрастирует с E1S, уровни которого примерно в 10-15 раз выше, чем у эстрона. [17]
E2S при пероральном приеме в дозе 5 мг/день у женщин приводил к подавлению овуляции в 89% циклов (47 из 53). [18]
| Эстроген | Другие имена | РБАПодсказка Относительная сродство связывания(%) а | РЕП (%) б | |||
|---|---|---|---|---|---|---|
| ER | ЭРα | ЭРβ | ||||
| Эстрадиол | Е2 | 100 | 100 | 100 | ||
| Эстрадиол 3-сульфат | Е2С; Е2-3С | ? | 0,02 | 0,04 | ||
| Эстрадиол 3-глюкуронид | Е2-3Г | ? | 0,02 | 0,09 | ||
| Эстрадиол 17β-глюкуронид | Е2-17Г | ? | 0,002 | 0,0002 | ||
| Эстрадиол бензоат | ЭБ; Эстрадиол 3-бензоат | 10 | 1.1 | 0,52 | ||
| Эстрадиол 17β-ацетат | Е2-17А | 31–45 | 24 | ? | ||
| Эстрадиол диацетат | ЭДА; Эстрадиол 3,17β-диацетат | ? | 0,79 | ? | ||
| Эстрадиол пропионат | ЭП; Эстрадиол 17β-пропионат | 19–26 | 2.6 | ? | ||
| Эстрадиол валерат | EV; Эстрадиол 17β-валерат | 2–11 | 0,04–21 | ? | ||
| Эстрадиол ципионат | EC; Эстрадиол 17β-ципионат | ? с | 4.0 | ? | ||
| Эстрадиол пальмитат | Эстрадиол 17β-пальмитат | 0 | ? | ? | ||
| Эстрадиола стеарат | Эстрадиол 17β-стеарат | 0 | ? | ? | ||
| Эстрон | E1; 17-кетоэстрадиол | 11 | 5.3–38 | 14 | ||
| Эстрон сульфат | E1S; Эстрон 3-сульфат | 2 | 0,004 | 0,002 | ||
| Глюкуронид эстрона | E1G; эстрон 3-глюкуронид | ? | <0,001 | 0,0006 | ||
| Этинилэстрадиол | ЭЭ; 17α-Этинилэстрадиол | 100 | 17–150 | 129 | ||
| Местранол | ЭЭ 3-метиловый эфир | 1 | 1.3–8.2 | 0,16 | ||
| Квинестрол | ЭЭ 3-циклопентиловый эфир | ? | 0,37 | ? | ||
| Сноски: a = Относительные сродства связывания (RBA) определялись посредством in vitro вытеснения меченого эстрадиола из эстрогеновых рецепторов (ER), как правило, цитозоля матки грызунов . Эфиры эстрогена в этих системах гидролизуются в эстрогены по-разному (более короткая длина эфирной цепи -> более высокая скорость гидролиза), а RBA ER эфиров сильно снижаются, когда гидролиз предотвращается. b = Относительные эстрогенные активности (REP) рассчитывались из полумаксимальных эффективных концентраций (EC50 ) , которые определялись посредством in vitro анализов продукции β-галактозидазы (β-gal) и зеленого флуоресцентного белка (GFP) в дрожжах, экспрессирующих человеческий ERα и человеческий ERβ . Как клетки млекопитающих , так и дрожжи обладают способностью гидролизовать эстрогеновые эфиры. c = Сродство эстрадиола ципионата к ER аналогично сродству эстрадиола валерата и эстрадиола бензоата ( рисунок ). Источники: см. страницу шаблона. | ||||||
| Эстроген | Структура | Эстер(ы) | Относительная мол. масса | Относительное содержание E2 b | лог P c | ||||
|---|---|---|---|---|---|---|---|---|---|
| Позиция(и) | Мойет(ы) | Тип | Длина а | ||||||
| Эстрадиол | 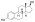 | – | – | – | – | 1.00 | 1.00 | 4.0 | |
| Эстрадиол ацетат | 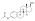 | С3 | Этановая кислота | Жирная кислота с прямой цепью | 2 | 1.15 | 0,87 | 4.2 | |
| Эстрадиол бензоат |  | С3 | бензойная кислота | Ароматические жирные кислоты | – (~4–5) | 1.38 | 0,72 | 4.7 | |
| Эстрадиол дипропионат | 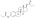 | С3, С17β | Пропионовая кислота (×2) | Жирная кислота с прямой цепью | 3 (×2) | 1.41 | 0,71 | 4.9 | |
| Эстрадиол валерат |  | С17β | Пентановая кислота | Жирная кислота с прямой цепью | 5 | 1.31 | 0,76 | 5.6–6.3 | |
| Эстрадиол бензоат бутират |  | С3, С17β | Бензойная кислота , масляная кислота | Смешанные жирные кислоты | – (~6, 2) | 1.64 | 0,61 | 6.3 | |
| Эстрадиол ципионат | 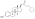 | С17β | Циклопентилпропановая кислота | Циклическая жирная кислота | – (~6) | 1.46 | 0,69 | 6.9 | |
| Эстрадиол энантат |  | С17β | Гептановая кислота | Жирная кислота с прямой цепью | 7 | 1.41 | 0,71 | 6.7–7.3 | |
| Эстрадиол диенантат | 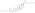 | С3, С17β | Гептановая кислота (×2) | Жирная кислота с прямой цепью | 7 (×2) | 1.82 | 0,55 | 8.1–10.4 | |
| Эстрадиол ундецилат |  | С17β | Ундекановая кислота | Жирная кислота с прямой цепью | 11 | 1.62 | 0,62 | 9.2–9.8 | |
| Эстрадиола стеарат |  | С17β | Октадекановая кислота | Жирная кислота с прямой цепью | 18 | 1.98 | 0,51 | 12.2–12.4 | |
| Эстрадиол дистеарат |  | С3, С17β | Октадекановая кислота (×2) | Жирная кислота с прямой цепью | 18 (×2) | 2.96 | 0,34 | 20.2 | |
| Эстрадиол сульфат |  | С3 | Серная кислота | Водорастворимый конъюгат | – | 1.29 | 0,77 | 0,3–3,8 | |
| Эстрадиол глюкуронид |  | С17β | глюкуроновая кислота | Водорастворимый конъюгат | – | 1.65 | 0,61 | 2.1–2.7 | |
| Эстрамустин фосфат d |  | С3, С17β | Нормустин , фосфорная кислота | Водорастворимый конъюгат | – | 1.91 | 0,52 | 2,9–5,0 | |
| Полиэстрадиолфосфат е |  | С3–С17β | Фосфорная кислота | Водорастворимый конъюгат | – | 1.23 ф | 0,81 ф | 2,9 г | |
| Сноски: a = Длина эфира в атомах углерода для жирных кислот с прямой цепью или приблизительная длина эфира в атомах углерода для ароматических или циклических жирных кислот. b = Относительное содержание эстрадиола по весу (т. е. относительное эстрогенное воздействие). c = Экспериментальный или предсказанный коэффициент распределения октанол/вода (т. е. липофильность / гидрофобность ). Получено из PubChem , ChemSpider и DrugBank . d = Также известен как эстрадиолнормустинфосфат . e = Полимер эстрадиолфосфата (~13 повторяющихся единиц ). f = Относительная молекулярная масса или содержание эстрадиола на повторяющуюся единицу. g = log P повторяющейся единицы (т. е. эстрадиолфосфата). Источники: см . отдельные статьи. | |||||||||
Смотрите также
- Катехол эстроген
- ДГЭА сульфат
- Эстрадиол глюкуронид
- Эстриол сульфат
- Эстрогенный конъюгат
- Липоидный эстрадиол
- Прегненолона сульфат
- Список эфиров эстрогена § Эстеры эстрадиола
Ссылки
- ^ ab FA Kincl; JR Pasqualini (22 октября 2013 г.). Гормоны и плод: Том 1: Производство, концентрация и метаболизм во время беременности. Elsevier Science. стр. 39–. ISBN 978-1-4832-8538-2.
- ^ abcd Питер Дж. О'Брайен; Уильям Роберт Брюс (2 декабря 2009 г.). Эндогенные токсины: мишени для лечения и профилактики заболеваний, 2 тома. John Wiley & Sons. стр. 869–. ISBN 978-3-527-32363-0.
- ^ Ван, Ли-Куан; Джеймс, Маргарет О. (2005). «Сульфотрансфераза 2А1 образует эстрадиол-17-сульфат, а целекоксиб переключает доминирующий продукт с эстрадиол-3-сульфата на эстрадиол-17-сульфат». Журнал стероидной биохимии и молекулярной биологии . 96 (5): 367– 374. doi :10.1016/j.jsbmb.2005.05.002. ISSN 0960-0760. PMID 16011896. S2CID 24671971.
- ^ ab Хорхе Р. Паскуалини (17 июля 2002 г.). Рак молочной железы: прогноз, лечение и профилактика. CRC Press. стр. 195–. ISBN 978-0-203-90924-9.
- ^ ab IARC Working Group on the Evaluation of Cancerogenic Risks to Humans; Всемирная организация здравоохранения; Международное агентство по изучению рака (2007). Комбинированные эстроген-прогестагенные контрацептивы и комбинированная эстроген-прогестагенная менопаузальная терапия. Всемирная организация здравоохранения. стр. 279–. ISBN 978-92-832-1291-1.
- ^ G. Leclercq; S. Toma; R. Paridaens; JC Heuson (6 декабря 2012 г.). Клинический интерес рецепторов стероидных гормонов при раке молочной железы. Springer Science & Business Media. стр. 2105–. ISBN 978-3-642-82188-2.
- ^ AT Gregoire (13 марта 2013 г.). Контрацептивные стероиды: фармакология и безопасность. Springer Science & Business Media. стр. 109–. ISBN 978-1-4613-2241-2.
- ^ Марк А. Фриц; Леон Сперофф (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие. Lippincott Williams & Wilkins. стр. 751–. ISBN 978-1-4511-4847-3.
- ^ Кристиан Лауритцен; Джон WW Стадд (22 июня 2005 г.). Текущее управление менопаузой. CRC Press. стр. 364–. ISBN 978-0-203-48612-2.
- ^ Райан Дж. Хакстейбл (11 ноября 2013 г.). Биохимия серы. Springer Science & Business Media. стр. 312–. ISBN 978-1-4757-9438-0.
- ^ Кинг, Роберта; Гош, Анасуя; Ву, Цзиньфан (2006). «Ингибирование сульфотрансферазы фенола и эстрогена человека некоторыми нестероидными противовоспалительными средствами». Current Drug Metabolism . 7 (7): 745– 753. doi :10.2174/138920006778520615. ISSN 1389-2002. PMC 2105742. PMID 17073578 .
- ^ Coldham NG, Dave M, Sivapathasundaram S, McDonnell DP, Connor C, Sauer MJ (июль 1997 г.). «Оценка скринингового анализа рекомбинантных дрожжевых клеток на эстроген». Environ . Health Perspect . 105 (7): 734– 42. doi :10.1289/ehp.97105734. PMC 1470103. PMID 9294720.
- ^ Bhavnani BR (ноябрь 1988). «Сага о ненасыщенных конских эстрогенах кольца B». Endocr. Rev. 9 ( 4): 396– 416. doi :10.1210/edrv-9-4-396. PMID 3065072.
- ^ ab Herr, F.; Revesz, C.; Manson, AJ; Jewell, JB (1970). «Биологические свойства сульфатов эстрогена». Химические и биологические аспекты конъюгации стероидов . стр. 368–408 . doi :10.1007/978-3-642-95177-0_8 (неактивен 2024-11-02). ISBN 978-3-642-95179-4.
{{cite book}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка ) - ^ ab Runge-Morris MA (1997). "Регуляция экспрессии цитозольных сульфотрансфераз грызунов". FASEB J . 11 (2): 109– 17. doi : 10.1096/fasebj.11.2.9039952 . PMID 9039952. S2CID 22112485.
- ^ Сингх Д., Пандей РС (1996). «Глутатион-S-трансфераза в яичниках крыс: ее изменения во время эстрального цикла и увеличение ее активности эстрадиолом-17 бета». Indian J. Exp. Biol . 34 (11): 1158– 60. PMID 9055636.
- ^ Коуи, Альфред Т.; Форсайт, Изабель А.; Харт, Ян К. (1980). «Рост и развитие молочной железы». Гормональный контроль лактации . Монографии по эндокринологии. Т. 15. С. 58–145 . doi :10.1007/978-3-642-81389-4_3. ISBN 978-3-642-81391-7. ISSN 0077-1015. PMID 6250026.
- ^ Gual C, Becerra C, Rice-Wray E, Goldzieher JW (февраль 1967). «Подавление овуляции эстрогенами». Am J Obstet Gynecol . 97 (4): 443– 7. doi :10.1016/0002-9378(67)90555-8. PMID 4163201.