Салициловый альдегид
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 2-Гидроксибензальдегид [1] | |||
| Другие имена Салициловый альдегид Салициловый альдегид o -Гидроксибензальдегид | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 471388 | |||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.001.783 | ||
| Номер ЕС |
| ||
| 3273 | |||
| КЕГГ |
| ||
CID PubChem |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С7Н6О2 | |||
| Молярная масса | 122,123 г·моль −1 | ||
| Плотность | 1,146 г/см 3 | ||
| Температура плавления | −7 °C (19 °F; 266 K) | ||
| Точка кипения | 196–197 °C (385–387 °F; 469–470 K) | ||
| -64,4·10 −6 см 3 /моль | |||
| Опасности [2] | |||
| Маркировка СГС : | |||
  | |||
| Предупреждение | |||
| Х302 , Х315 , Х317 , Х319 , Х335 , Х411 | |||
| П280 , П305+П351+П338 | |||
| Паспорт безопасности (SDS) | [2] | ||
| Родственные соединения | |||
Родственные соединения | Салициловая кислота Бензальдегид Салицилальдоксим | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Салициловый альдегид (2-гидроксибензальдегид) — органическое соединение с формулой C6H4OH (CHO) . [ 3] [ 4] Наряду с 3-гидроксибензальдегидом и 4-гидроксибензальдегидом, это один из трех изомеров гидроксибензальдегида . Эта бесцветная маслянистая жидкость имеет горьковатый миндальный запах при более высокой концентрации. Салициловый альдегид является предшественником кумарина и различных хелатирующих агентов .
Производство
Салициловый альдегид получают путем конденсации фенола с формальдегидом с образованием гидроксибензилового спирта, который окисляется до альдегида. [4] Салициловые альдегиды в целом получают путем ортоселективных реакций формилирования из соответствующего фенола, например, с помощью реакции Даффа , реакции Реймера-Тимана или путем обработки параформальдегидом в присутствии хлорида магния и основания. [5] [6]
Природные явления
Салициловый альдегид является характерным компонентом аромата гречихи . [7] Салициловый альдегид также встречается в защитных выделениях личинок нескольких видов листоедов , которые относятся к подтрибе Chrysomelina. [8] Примером вида листоедов, который вырабатывает салициловый альдегид, является красный тополевой листоед Chrysomela populi .
Реакции и приложения
Салициловый альдегид в основном используется в коммерческих целях как предшественник кумарина . Превращение влечет за собой конденсацию с уксусным ангидридом (« синтез Перкина »). [4]
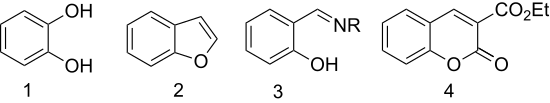
- Окисление перекисью водорода дает катехол (1,2-дигидроксибензол) ( реакция Дейкина ). [9]
- Этерификация с хлоруксусной кислотой с последующей циклизацией дает гетероцикл бензофуран (кумарон). [10] Первый шаг в этой реакции замещенного бензофурана называется конденсацией Рапа-Штермера в честь Э. Рапа (1895) и Р. Штермера (1900). [11] [12]
- Салицилальдегид преобразуется в хелатирующие лиганды путем конденсации с аминами. С этилендиамином он конденсируется с образованием лиганда сален . Гидроксиламин дает салицилальдоксим .
- Конденсация с диэтилмалонатом дает 3-карбэтоксикумарин (производное кумарина ) путем альдольной конденсации . [13]
Окисление персульфатом Эльбса дает гентисальдегид (2,5-дигидроксибензальдегид). [14] [15]
Внутренняя водородная связь
Из-за орто- расположения гидрокси- и альдегидных групп между группами образуется внутренняя водородная связь . Гидроксигруппа здесь служит донором водородной связи, а альдегид — акцептором водородной связи. Этот внутренний водород не встречается в других изомерах гидроксибензальдегида . Когда альдегид реагирует с амином с образованием имина, внутренняя водородная связь становится еще сильнее. [16] Кроме того, таутомеризация еще больше увеличивает стабильность соединения. [17] Внутренняя водородная связь также гарантирует, что альдегид (или соответствующий имин) удерживается в одной плоскости, делая всю молекулу по существу плоской. [18]
Ссылки
- ^ "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 652. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ ab Sigma-Aldrich Co. , Салициловый альдегид. Получено 24.05.2018.
- ^ Merck Index , 11-е издание, 8295
- ^ abc Maliverney, Christian; Mulhauser, Michel (2000). "Гидроксибензальдегиды". Энциклопедия химической технологии Кирка-Отмера . doi :10.1002/0471238961.0825041813011209.a01. ISBN 978-0-471-48494-3.
- ^ Тронд Видар Хансен; Ларс Скаттебёль (2005). «Ортоформилирование фенолов; Получение 3-бромсалицилового альдегида». Органические синтезы . 82:64 . дои :10.15227/orgsyn.089.0220.
- ^ Брюне, Ф.; Райт, Э. «Бензальдегид». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. doi :10.1002/14356007.a03_463.pub2. ISBN 978-3-527-30673-2.
{{cite encyclopedia}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Янеш, Д.; Крефт, С. (2008). «Салициловый альдегид является характерным компонентом аромата гречневой крупы». Пищевая химия . 109 (2): 293– 298. doi :10.1016/j.foodchem.2007.12.032. PMID 26003350.
- ^ Pauls, G., Becker, T., et al. (2016). Две защитные линии у молодых листоедов; Эфиры 3-нитропропионовой кислоты в гемолимфе и апосематическое предупреждение. Журнал химической экологии 42 (3) 240-248.
- ^ Dakin, HD (1923). "Катехин". Органические синтезы . 3 : 28. doi :10.15227/orgsyn.003.0028; Собрание томов , т. 1, стр. 149.
- ^ Бургшталер, AW; Уорден, Л.Р. (1966). «Кумарон». Органические синтезы . 46:28 . дои :10.15227/orgsyn.046.0028
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ). - ^ Рэп, Э. (ноябрь 1895 г.). «Сулл α-бензоилкумарон» [Об α-бензоилкумароне]. Газетта Химика Итальяна . 2 (4): 285–290 .
- ^ Стермер, Р. (1900). «Synthesen und Abbaureactionen in der Cumaronreihe». «Анналы химии» Либиха . 312 (3): 237–336 . doi :10.1002/jlac.19003120302.
- ^ Хорнинг, EC; Хорнинг, MG; Диммиг, DA (1948). "3-Карбетоксикумарин". Органические синтезы . 28 : 24. doi :10.15227/orgsyn.028.0024
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ). - ^ Sethna, Suresh M. (1951-08-01). «Окисление персульфата Элбса». Chemical Reviews . 49 (1): 91– 101. doi :10.1021/cr60152a002. ISSN 0009-2665.
- ^ Дания, Скотт Э., ред. (2004-04-30). Органические реакции (1-е изд.). Wiley. doi :10.1002/0471264180.or035.02. ISBN 978-0-471-26418-7.
- ^ Шустра, SK; Асади, V.; Цуйлхоф, H.; Смалдерс, MMJ (2023). «Внутреннее водородное связывание иминов для контроля и улучшения динамических механических свойств ковалентных адаптивных сетей». European Polymer Journal . 195 : 112209. doi : 10.1016/j.eurpolymj.2023.112209 .
- ^ Мецлер, CM; Кахилл, A.; Мецлер, DE (1980). «Равновесия и спектры поглощения оснований Шиффа». J. Am. Chem. Soc. 102 (19): 6075– 6082. doi :10.1021/ja00539a017.
- ^ Kandambeth, S.; Shinde, DB; Panda, MK; Lukose, B.; Heine, T.; Banerjee, R. (2013). «Повышение химической стабильности и кристалличности в ковалентных органических каркасах, содержащих порфирин, с помощью внутримолекулярных водородных связей». Angew. Chem. Int. Ed. 52 (49): 13052– 13056. doi : 10.1002/anie.201306775 .





