реакция Даффа
Реакция Даффа или гексаминовое ароматическое формилирование — это реакция формилирования, используемая в органической химии для синтеза бензальдегидов с гексамином в качестве источника формильного углерода. Метод, как правило, неэффективен. [1] Реакция названа в честь Джеймса Купера Даффа. [2]
Реакция требует сильных электронодонорных заместителей на ароматическом кольце, таких как в феноле . Формилирование происходит преимущественно в орто-положении к электронодонорному заместителю, если только орто -положения не заблокированы, в этом случае формилирование происходит в пара -положении. [3]
Примеры
Модифицированный салициловый альдегид 3,5-ди- трет -бутилсалициловый альдегид получают по реакции Даффа: [4]
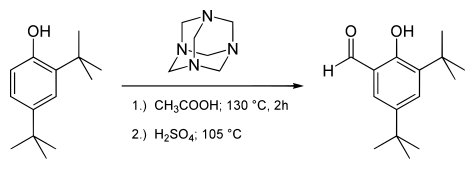
Натуральный продукт сиреневый альдегид также может быть получен реакцией Даффа. В этом примере формилирование происходит в пара-положении к фенольному ОН. [5]

В отличие от других реакций формилирования реакция Даффа способна присоединять несколько альдегидных групп. Если обе орто- позиции вакантны, то возможно диформилирование, как при образовании диформилкрезола из п- крезола . [6] Также сообщалось о превращении фенола в соответствующий 1,3,5-триальдегид [7]
Механизм реакции
Механизм реакции связан с механизмом реакции Реймера-Тимана , в которой в качестве формилирующего агента используется хлороформ. [1] Протонированное гексаминовое кольцо раскрывается, обнажая иминиевую группу. Присоединение к ароматическому кольцу приводит к образованию промежуточного продукта в степени окисления бензиламина. Затем следует внутримолекулярная окислительно-восстановительная реакция, повышающая бензильный углерод до степени окисления альдегида. Атом кислорода обеспечивается водой при кислотном гидролизе на заключительном этапе.

Исторические справки
Дафф был химиком в Технологическом колледже Бирмингема примерно в 1920–1950 годах. [2] который
- Дафф, Дж. К.; Биллс, Э. Дж. (1934). "282. Реакции между гексаметилентетрамином и фенольными соединениями. Часть II. Образование фенольных альдегидов. Отличительное поведение п -нитрофенола". J. Chem. Soc. : 1305. doi :10.1039/jr9340001305.
- Дафф, Дж. К.; Биллс, Э. Дж. (1941). "96. Новый общий метод получения о- гидроксиальдегидов из фенолов и гексаметилентетрамина". J. Chem. Soc. : 547. doi :10.1039/jr9410000547.
- Дафф, Дж. К.; Биллс, Э. Дж. (1945). "71. Новый метод получения п -диалкиламинобензальдегидов". J. Chem. Soc. : 276. doi :10.1039/jr9450000276.
- Ллойд Ноэль Фергюсон (1946). «Синтез ароматических альдегидов». Chem. Rev. 38 (2): 227–254. doi :10.1021/cr60120a002. PMID 21024865.
- Огата, Ю.; Сугиура, Ф. (1968). «Кинетика и механизм реакции Даффа». Тетраэдр . 24 (14): 5001. doi :10.1016/S0040-4020(01)88408-8.
Смотрите также
- Синтез альдегида Буво
- Синтез альдегида Бодру-Чичибабина
- Реакция Раймера-Тимана
- реакция Соммелета
- Реакция Вильсмейера-Хаака
Ссылки
- ^ ab March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 3-е издание, Нью-Йорк: Wiley, стр. 727, ISBN 9780471854722, OCLC 642506595
- ^ ab Duff, JC; Bills, EJ (1932). "273. Реакции между гексаметилентетрамином и фенольными соединениями. Часть I. Новый метод получения 3- и 5-альдегидосалициловых кислот". J. Chem. Soc. : 1987. doi :10.1039/jr9320001987.
- ^ Манди, Брэдфорд П.; Эллерд, Майкл Г.; Фавалоро, Фрэнк Г. (2005). Назовите реакции и реагенты в органическом синтезе , 2-е издание, John Wiley & Sons, стр. 222–223.
- ^ Ларроу, Джей Ф.; Якобсен, Эрик Н. (1998). "(R,R)-N,N'-Бис(3,5-ди-трет-бутилсалицилальдегид)-1,2-циклогександиамино марганец(III) хлорид, высокоэнантиоселективный катализатор эпоксидирования". Органические синтезы . 75 : 1. doi :10.15227/orgsyn.075.0001; Собрание томов , т. 10, стр. 96.
- ^ Аллен, CFH; Лейбнер, Герхард В. (1951). "Сиринговый альдегид". Органические синтезы . 31 : 92. doi :10.15227/orgsyn.031.0092; Собрание томов , т. 4, стр. 866.
- ^ Линдой, Леонард Ф. (июль 1998 г.). «Моно- и диформилирование 4-замещенных фенолов: новое применение реакции Даффа». Синтез . 1998 (7): 1029–1032. doi :10.1055/s-1998-2110.
- ^ Андерсон, Эндрю А.; Гетцен, Томас; Шакелфорд, Скотт А.; Цанк, Стелла (сентябрь 2000 г.). «Удобный одношаговый синтез 2-гидрокси-1,3,5-бензолтрикарбальдегида». Synthetic Communications . 30 (17): 3227–3232. doi :10.1080/00397910008086933.