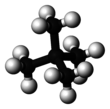
Неопентан
 | |||
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 2,2-Диметилпропан [2] | |||
| Другие имена Неопентан Тетраметилметан [1] | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 1730722 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.006.677 | ||
| Номер ЕС |
| ||
| 1850 | |||
| МеШ | неопентан | ||
CID PubChem |
| ||
| УНИИ | |||
| Номер ООН | 2044 | ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| Характеристики | |||
| С 5 Н 12 | |||
| Молярная масса | 72,151 г·моль −1 | ||
| Появление | Бесцветный газ. | ||
| Запах | Без запаха | ||
| Плотность | 3,255 кг/м 3 (газ, 9,5 °C) 601,172 кг/м 3 (жидкость, 9,5 °C) | ||
| Температура плавления | −16,5 °C (2,3 °F; 256,6 К) | ||
| Точка кипения | 9,5 °C (49,1 °F; 282,6 К) | ||
| Давление пара | 146 кПа (при 20 °C) [3] | ||
Константа закона Генри ( k H ) | 4,7 нмоль Па −1 кг −1 | ||
| Термохимия | |||
Теплоемкость ( С ) | 121,07–120,57 ДжК -1 моль -1 | ||
Стандартная молярная энтропия ( S ⦵ 298 ) | 217 ДжК −1 моль −1 | ||
Стандартная энтальпия образования (Δ f H ⦵ 298 ) | −168,5–−167,3 кДж моль −1 | ||
Стандартная энтальпия сгорания (Δ c H ⦵ 298 ) | −3,51506–−3,51314 МДж моль −1 | ||
| Опасности | |||
| Маркировка СГС : | |||
  | |||
| Опасность | |||
| Н220 , Н411 | |||
| П210 , П273 , П377 , П381 , П391 , П403 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Родственные алканы | |||
Родственные соединения | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
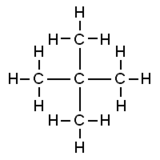
Неопентан , также называемый 2,2-диметилпропаном , представляет собой алкан с двойной разветвленной цепью и пятью атомами углерода . Неопентан — это горючий газ при комнатной температуре и давлении , который может конденсироваться в высоколетучую жидкость в холодный день, в ледяной бане или при сжатии до более высокого давления.
Неопентан — простейший алкан с четвертичным углеродом , имеющий ахиральную тетраэдрическую симметрию . Это один из трех структурных изомеров с молекулярной формулой C5H12 ( пентаны ), два других — н -пентан и изопентан . Из этих трех он единственный, кто является газом при стандартных условиях; остальные — жидкости .
Впервые он был синтезирован русским химиком Михаилом Львовым в 1870 году. [4]
Номенклатура
Традиционное название неопентан, придуманное Уильямом Одлингом в 1876 году [5] , все еще сохранялось в рекомендациях ИЮПАК 1993 года [6] [7] , но больше не рекомендуется согласно рекомендациям 2013 года. [2] Предпочтительным названием ИЮПАК является систематическое название 2,2-диметилпропан, но номера заместителей излишни, поскольку это единственный возможный «диметилпропан».

Неопентильный заместитель , часто обозначаемый как "Np", имеет структуру Me 3 C–CH 2 – например, неопентиловый спирт (Me 3 CCH 2 OH или NpOH). Поскольку Np также символизирует элемент нептуний (атомный номер 93), следует использовать эту аббревиатуру с осторожностью.
Также используется устаревшее название тетраметилметан, особенно в старых источниках. [8] [9]
Физические свойства
Температуры кипения и плавления
Температура кипения неопентана составляет всего 9,5 °C, что значительно ниже, чем у изопентана (27,7 °C) и нормального пентана (36,0 °C). Поэтому неопентан является газом при комнатной температуре и атмосферном давлении, в то время как два других изомера являются (едва ли) жидкостями.
Температура плавления неопентана (−16,6 °C), с другой стороны, на 140 градусов выше, чем у изопентана (−159,9 °C) и на 110 градусов выше, чем у н -пентана (−129,8 °C). Эта аномалия была приписана лучшей твердотельной упаковке, которая, как предполагалось, возможна с тетраэдрической молекулой неопентана; но это объяснение было оспорено из-за того, что она имеет более низкую плотность, чем два других изомера. Более того, его энтальпия плавления ниже, чем энтальпии плавления как н -пентана, так и изопентана, что указывает на то, что его высокая температура плавления обусловлена энтропийным эффектом, возникающим в результате более высокой молекулярной симметрии. Действительно, энтропия плавления неопентана примерно в четыре раза ниже, чем у н -пентана и изопентана. [10]
1Спектр ЯМР 1H
Из-за полной тетраэдрической симметрии неопентана все протоны химически эквивалентны, что приводит к единственному химическому сдвигу ЯМР δ = 0,902 при растворении в четыреххлористом углероде . [11] В этом отношении неопентан похож на свой силановый аналог, тетраметилсилан , единственный химический сдвиг которого по соглашению равен нулю.
Симметрия молекулы неопентана может быть нарушена, если некоторые атомы водорода заменить атомами дейтерия . В частности, если каждая метильная группа имеет разное количество замещенных атомов (0, 1, 2 и 3), то получается хиральная молекула. Хиральность в этом случае возникает исключительно за счет распределения масс ее ядер, тогда как распределение электронов по-прежнему остается по существу ахиральным. [12]
Производные
Спирт пентаэритрит можно описать как результат замены одного водорода в каждой из четырех метильных групп на гидроксильную ( –ОН) группу.
Линейный полимер с чередующимися неопентановыми и ортокарбонатными группами, который можно описать как сложный эфир ( ортокарбонат пентаэритрита ) с формулой [(−CH 2 ) 2 C(CH 2 −) 2 (−O) 2 C(O−) 2 ] n , был синтезирован в 2002 году. [13]
Ссылки
- ^ Aston, JG; Messerly, GH, Теплоемкости и энтропии органических соединений II. Данные о тепловом и паровом давлении тетраметилметана от 13,22 К до точки кипения. Энтропия из его Рамановского спектра, J. Am. Chem. Soc., 1936, 58, 2354.
- ^ ab "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 652. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ «Неопентан | C5H12 - PubChem».
- ^ Zeitschrift für Chemie (на немецком языке). Квандт и Гендель. 1870.
- ↑ Философский журнал. Тейлор и Фрэнсис. 1876.
- ^ Таблица 19(а) Ациклические и моноциклические углеводороды. Исходные углеводороды
- ^ Panico, R. & Powell, WH, ред. (1994). Руководство по номенклатуре органических соединений ИЮПАК 1993. Оксфорд: Blackwell Science. ISBN 978-0-632-03488-8.
- ^ Уитмор, Фрэнк К.; Флеминг, Гео. Х. (1934-09-01). «Получение тетраметилметана (неопентана) и определение его физических констант1». Журнал Американского химического общества . 55 (9): 3803– 3806. doi :10.1021/ja01336a058. ISSN 0002-7863.
- ^ ЛаКост, Люсьен Дж. Б. (1934-10-15). «Уравнение вращательной волны тетраметилметана для нулевого потенциала и обобщение». Physical Review . 46 (8): 718– 724. Bibcode : 1934PhRv...46..718L. doi : 10.1103/PhysRev.46.718.
- ^ Вэй, Джеймс (1999). «Молекулярная симметрия, вращательная энтропия и повышенные точки плавления». Ind. Eng. Chem. Res. 38 (12): 5019– 5027. doi :10.1021/ie990588m.
- ^ База данных спектров органических соединений , Протонный ЯМР-спектр неопентана, доступ 4 июня 2018 г.
- ^ Haesler, Jacques; Schindelholz, Ivan; Riguet, Emmanuel; Bochet, Christian G.; Hug, Werner (2007). "Абсолютная конфигурация хирально дейтерированного неопентана" (PDF) . Nature . 446 (7135): 526– 529. Bibcode :2007Natur.446..526H. doi :10.1038/nature05653. PMID 17392783. S2CID 4423560.
- ^ Водак, Дэвид Т.; Браун, Мэтью; Иорданидис, Ликургос; Плевер, Жак; Стивенс, Майкл; Бек, Ларри; Спенс, Джон CH; О'Киф, Майкл; Яги, Омар М. (2002). «Одношаговый синтез и структура олиго(спиро-ортокарбоната)». Журнал Американского химического общества . 124 (18): 4942– 4943. doi :10.1021/ja017683i. PMID 11982342.
Внешние ссылки
- Линстром, Питер Дж.; Маллард, Уильям Г. (ред.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69 , Национальный институт стандартов и технологий, Гейтерсберг (Мэриленд)
- Номенклатура ИЮПАК по органической химии (электронная версия « Синей книги »)