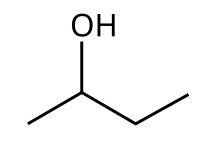
2-бутанол
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Бутан-2-ол [2] | |
| Другие имена сек -Бутанол [1] сек -Бутиловый спирт 2-Бутанол 2-Бутиловый спирт | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| 773649 1718764 ( Р ) | |
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Информационная карта ECHA | 100.001.053 |
| Номер ЕС |
|
| 1686 396584 ( Р ) | |
| МеШ | 2-бутанол |
CID PubChem |
|
| Номер RTECS |
|
| УНИИ | |
| Номер ООН | 1120 |
Панель инструментов CompTox ( EPA ) |
|
| |
| Характеристики | |
| С4Н10О | |
| Молярная масса | 74,123 г·моль −1 |
| Плотность | 0,808 г см −3 |
| Температура плавления | −115 °C; −175 °F; 158 К |
| Точка кипения | от 98 до 100 °C; от 208 до 212 °F; от 371 до 373 K |
| 390 г/л [3] | |
| лог P | 0,683 |
| Давление пара | 1,67 кПа (при 20 °C) |
| Кислотность ( pK a ) | 17.6 [4] |
| −5,7683 × 10 −5 см 3 моль −1 | |
Показатель преломления ( nD ) | 1,3978 (при 20 °С) |
| Термохимия | |
Теплоемкость ( С ) | 197,1 Дж К −1 моль −1 |
Стандартная молярная энтропия ( S ⦵ 298 ) | 213,1 Дж К −1 моль −1 |
Стандартная энтальпия образования (Δ f H ⦵ 298 ) | −343,3 до −342,1 кДж моль −1 |
Стандартная энтальпия сгорания (Δ c H ⦵ 298 ) | −2,6611 до −2,6601 МДж моль −1 |
| Опасности | |
| Маркировка СГС : | |
  | |
| Предупреждение | |
| Н226 , Н319 , Н335 , Н336 | |
| П261 , П305+П351+П338 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | от 22 до 27 °C (от 72 до 81 °F; от 295 до 300 K) |
| 405 °C (761 °F; 678 К) | |
| Пределы взрывоопасности | 1,7–9,8% |
| Смертельная доза или концентрация (ЛД, ЛК): | |
LC Lo ( самый низкий опубликованный ) | 16 000 ppm (крыса, 4 часа) 10 670 ppm (мышь, 3,75 часа) 16 000 ppm (мышь, 2,67 часа) [5] |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (допустимый) | TWA 150 частей на миллион (450 мг/м 3 ) [5] |
РЕЛ (рекомендуется) | TWA 100 ppm (305 мг/м 3 ) ST 150 ppm (455 мг/м 3 ) [5] |
IDLH (Непосредственная опасность) | 2000 частей на миллион [5] |
| Паспорт безопасности (SDS) | inchem.org |
| Родственные соединения | |
Родственные бутанолы | н -Бутанол Изобутанол трет -Бутанол |
Родственные соединения | Бутанон |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Бутан-2-ол , или втор -бутанол , представляет собой органическое соединение с формулой C H 3 CH( O H)CH 2 CH 3 . Его структурными изомерами являются 1-бутанол , изобутанол и трет -бутанол . 2-Бутанол хиральный и, таким образом, может быть получен в виде одного из двух стереоизомеров, обозначенных как ( R )-(−)-бутан-2-ол и ( S )-(+)-бутан-2-ол. Обычно он встречается в виде смеси 1:1 двух стереоизомеров — рацемической смеси.
Этот вторичный спирт представляет собой негорючую бесцветную жидкость, растворимую в трех частях воды и полностью смешивающуюся с органическими растворителями. Он производится в больших масштабах, в первую очередь как прекурсор промышленного растворителя метилэтилкетона .
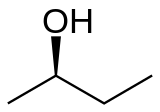 |  |
 |  |
| ( R )-(−)-2-бутанол | ( S )-(+)-2-бутанол |
Производство и применение
Бутан-2-ол производится в промышленности путем гидратации 1-бутена или 2 -бутена :
В качестве катализатора этого превращения используется серная кислота . [6]
В лаборатории его можно получить с помощью реакции Гриньяра путем взаимодействия этилмагнийбромида с ацетальдегидом в сухом диэтиловом эфире или тетрагидрофуране .
Хотя некоторое количество бутан-2-ола используется в качестве растворенного вещества, в основном он преобразуется в бутанон (метилэтилкетон, МЭК), важный промышленный растворитель, который содержится во многих бытовых чистящих средствах и средствах для удаления краски. Хотя большинство средств для удаления краски перестали использовать МЭК в своих продуктах из-за проблем со здоровьем и новых законов. Летучие эфиры бутан-2-ола имеют приятный аромат и используются в небольших количествах в качестве духов или в искусственных ароматизаторах. [6]
Растворимость
Указанная растворимость бутан-2-ола часто неверна, [3] включая некоторые из самых известных источников, таких как Merck Index , CRC Handbook of Chemistry and Physics и Lange's Handbook of Chemistry . Даже Международная программа по химической безопасности указывает неправильную растворимость. Эта распространенная ошибка возникла из-за Handbuch der Organischen Chemie ( Справочник по органической химии ) Бейльштейна. В этой работе приводится ложная растворимость 12,5 г/100 г воды. Многие другие источники использовали эту растворимость, которая превратилась в распространенную ошибку в промышленном мире. Правильные данные (35,0 г/100 г при 20 °C, 29 г/100 г при 25 °C и 22 г/100 г при 30 °C) были впервые опубликованы в 1886 году Алексеевым, а затем аналогичные данные были представлены другими учеными, включая Долголенко и Драйера, в 1907 и 1913 годах соответственно. [3]
Меры предосторожности
Как и другие бутанолы, бутан-2-ол имеет низкую острую токсичность. LD 50 составляет 4400 мг/кг (крыса, перорально). [6]
Сообщалось о нескольких взрывах [7] [8] [9] во время обычной перегонки 2-бутанола, по-видимому, из-за накопления пероксидов с температурой кипения выше, чем у чистого спирта (и, следовательно, концентрирующихся в кубе во время перегонки). Поскольку спирты, в отличие от эфиров, не являются широко известными как способные образовывать примеси пероксидов, опасность, скорее всего, будет упущена из виду. 2-бутанол относится к классу B пероксидообразующих химикатов [10]
Ссылки
- ^ "Alcohols Rule C-201.1". Nomenclature of Organic Chemistry (The IUPAC 'Blue Book'), Sections A, B, C, D, E, F, and H . Oxford: Pergamon Press. 1979.
Такие обозначения, как изопропанол, втор-бутанол и трет-бутанол, неверны, поскольку не существует углеводородов изопропан, втор-бутан и трет-бутан, к которым можно добавить суффикс "-ол"; такие названия следует исключить. Однако изопропиловый спирт, втор-бутиловый спирт и трет-бутиловый спирт допустимы (см. Правило C-201.3), поскольку радикалы изопропил, втор-бутил и трет-бутил существуют
- ^ "2-бутанол - Сводка по соединению". PubChem Compound . США: Национальный центр биотехнологической информации. 26 марта 2005 г. Идентификация и связанные с ней записи . Получено 12 октября 2011 г.
- ^ abc Alger, Donald B. (ноябрь 1991 г.). «Растворимость бутан-2-ола в воде: широко распространенная ошибка». Journal of Chemical Education . 68 (11): 939. Bibcode : 1991JChEd..68..939A. doi : 10.1021/ed068p939.1.
- ^ Serjeant, EP, Dempsey B.; Константы ионизации органических кислот в водных растворах. Международный союз теоретической и прикладной химии (ИЮПАК). Серия химических данных ИЮПАК № 23, 1979. Нью-Йорк, Нью-Йорк: Pergamon Press, Inc., стр. 989
- ^ abcd Карманный справочник NIOSH по химическим опасностям. "#0077". Национальный институт охраны труда и здоровья (NIOSH).
- ^ abc Хан, Хайнц-Дитер; Дамбкес, Георг; Руприх, Норберт (2005). «Бутанолы». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. ISBN 978-3-527-30673-2..
- ^ Дойл, Р. Р. (1986). «Предупреждение о безопасности 2-бутанола». Журнал химического образования . 63 (2): 186. Bibcode : 1986JChEd..63..186D. doi : 10.1021/ed063p186.2 .
- ^ Петерсон, Дональд (11 мая 1981 г.). «Письма: Взрыв 2-бутанола». Chemical & Engineering News . 59 (19): 3. doi : 10.1021/cen-v059n019.p002 .
- ^ Уоткинс, Кеннет В. (май 1984 г.). «Опасность демонстрации». Журнал химического образования . 61 (5): 476. Bibcode : 1984JChEd..61..476W. doi : 10.1021/ed061p476.3 .
- ^ «Классификация химических веществ, образующих пероксиды». ehs.ucsc.edu .
Внешние ссылки
- Международная карта химической безопасности 0112
- Карманный справочник NIOSH по химическим опасностям. "#0077". Национальный институт охраны труда и техники безопасности (NIOSH).
- Критерии здоровья окружающей среды IPCS 65: Бутанолы: четыре изомера
- Руководство IPCS по охране труда и технике безопасности 4: 2-бутанол




