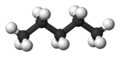Пентан
 | |||
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Пентан [2] | |||
| Другие имена Кинтан; [1] Хладагент-4-13-0 | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 969132 | |||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Информационная карта ECHA | 100.003.358 | ||
| Номер ЕС |
| ||
| 1766 | |||
| МеШ | пентан | ||
CID PubChem |
| ||
| Номер RTECS |
| ||
| УНИИ | |||
| Номер ООН | 1265 | ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| Свойства [4] | |||
| С 5 Н 12 | |||
| Молярная масса | 72,151 г·моль −1 | ||
| Появление | Бесцветная жидкость. | ||
| Запах | Похож на бензин [3] | ||
| Плотность | 0,626 г/мл; 0,6262 г/мл (20 °С) | ||
| Температура плавления | от −130,5 до −129,1 °C; от −202,8 до −200,3 °F; от 142,7 до 144,1 K | ||
| Точка кипения | 35,9–36,3 °C; 96,5–97,3 °F; 309,0–309,4 K | ||
| 40 мг/л (20 °C) | |||
| лог P | 3.255 | ||
| Давление пара | 57,90 кПа (20,0 °С) | ||
Константа закона Генри ( k H ) | 7,8 нмоль Па −1 кг −1 | ||
| Кислотность ( pK a ) | ~45 | ||
| Основность (p K b ) | ~59 | ||
| УФ-видимый (λ макс ) | 200 нм | ||
| -63,05·10 −6 см 3 /моль | |||
Показатель преломления ( nD ) | 1.358 | ||
| Вязкость | 0,240 мПа·с (при 20 °C) | ||
| Термохимия | |||
Теплоемкость ( С ) | 167,19 ДжК −1 моль −1 | ||
Стандартная молярная энтропия ( S ⦵ 298 ) | 263,47 ДжК −1 моль −1 | ||
Стандартная энтальпия образования (Δ f H ⦵ 298 ) | −174,1–−172,9 кДж моль −1 | ||
Стандартная энтальпия сгорания (Δ c H ⦵ 298 ) | −3,5095–−3,5085 МДж моль −1 | ||
| Опасности | |||
| Маркировка СГС : | |||
    | |||
| Опасность | |||
| Н225 , Н304 , Н336 , Н411 | |||
| П210 , П261 , П273 , П301+П310 , П331 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −49,0 °C (−56,2 °F; 224,2 К) | ||
| 260,0 °C (500,0 °F; 533,1 К) | |||
| Пределы взрывоопасности | 1,5–7,8% [3] | ||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD 50 ( средняя доза ) |
| ||
LC 50 ( средняя концентрация ) | 130 000 мг/м 3 (мышь, 30 мин) 128 200 частей на миллион (мышь, 37 мин) 325 000 мг/м 3 (мышь, 2 ч) [5] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (допустимый) | TWA 1000 частей на миллион (2950 мг/м 3 ) [3] | ||
РЕЛ (рекомендуется) | TWA 120 ppm (350 мг/м 3 ) C 610 ppm (1800 мг/м 3 ) [15 минут] [3] | ||
IDLH (Непосредственная опасность) | 1500 частей на миллион [3] | ||
| Родственные соединения | |||
Родственные алканы | |||
| Страница дополнительных данных | |||
| Пентан (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Пентан — органическое соединение с формулой C5H12 , то есть алкан с пятью атомами углерода . Термин может относиться к любому из трех структурных изомеров или к их смеси: однако в номенклатуре ИЮПАК пентан означает исключительно изомер н -пентана , в этом случае пентаны относятся к их смеси; два других называются изопентаном (метилбутаном) и неопентаном (диметилпропаном). Циклопентан не является изомером пентана, поскольку он имеет только 10 атомов водорода , тогда как у пентана их 12.
Пентаны являются компонентами некоторых видов топлива и используются в качестве специальных растворителей в лабораторных условиях . Их свойства очень похожи на свойства бутанов и гексанов .
Изомеры
| Общее название | нормальный пентан неразветвленный пентан н -пентан | изопентан | неопентан |
| Название ИЮПАК | пентан | 2-метилбутан | 2,2-диметилпропан |
| Молекулярная диаграмма |  |  | 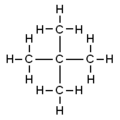 |
| Скелетная диаграмма | 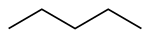 | 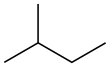 |  |
| Температура плавления (°С) [6] | −129,8 | −159,9 | −16,6 |
| Температура кипения (°С) [6] | 36.0 | 27.7 | 9.5 |
| Плотность (0 °C, кг/м 3 ) [6] | 621 | 616 | 586 |
Промышленное использование
Пентаны являются одними из основных вспенивающих агентов, используемых в производстве пенополистирола и других пен. Обычно для этой цели используется смесь н-, и- и все чаще циклопентана.
Кислотно-катализируемая изомеризация дает изопентан, который используется в производстве высокооктанового топлива. [7]
Благодаря низким температурам кипения , низкой стоимости и относительной безопасности пентаны используются в качестве рабочего тела на геотермальных электростанциях и органических циклах Ренкина . Он также используется в некоторых смешанных хладагентах .
Пентаны являются растворителями во многих обычных продуктах, например, в некоторых пестицидах . [8]
Лабораторное использование
Пентаны относительно недороги и являются наиболее летучими жидкими алканами при комнатной температуре, поэтому их часто используют в лаборатории в качестве растворителей , которые можно легко и быстро испарять. Однако из-за их неполярности и отсутствия функциональности они растворяют только неполярные и алкил-богатые соединения. Пентаны смешиваются с большинством распространенных неполярных растворителей, таких как хлоруглероды , ароматические соединения и эфиры .
Их часто используют в жидкостной хроматографии .
Физические свойства
Температуры кипения изомеров пентана колеблются от 9 до 36 °C. Как и в случае с другими алканами, более густо разветвленные изомеры, как правило, имеют более низкие температуры кипения.
То же самое справедливо и для температур плавления изомеров алканов, а температура плавления изопентана на 30 °C ниже, чем у н -пентана. Однако температура плавления неопентана , наиболее разветвленного из трех, на 100 °C выше , чем у изопентана. Аномально высокая температура плавления неопентана была приписана тетраэдрическим молекулам, более плотно упакованным в твердой форме; это объяснение противоречит тому факту, что неопентан имеет более низкую плотность, чем два других изомера, [9] и высокая температура плавления на самом деле вызвана значительно более низкой энтропией плавления неопентана .
Разветвленные изомеры более стабильны (имеют более низкую теплоту образования и теплоту сгорания ), чем н-пентан. Разница составляет 1,8 ккал / моль для изопентана и 5 ккал/моль для неопентана. [10] [11]
Вращение вокруг двух центральных одинарных связей CC н -пентана дает четыре различные конформации . [12]
Реакции
Как и другие алканы , пентаны в значительной степени инертны при стандартной комнатной температуре и условиях, однако при наличии достаточной энергии активации (например, открытого пламени) они легко окисляются с образованием диоксида углерода и воды:
- C 5 H 12 + 8 O 2 → 5 CO 2 + 6 H 2 O + тепло/энергия
Как и другие алканы , пентаны подвергаются свободнорадикальному хлорированию :
- С5Н12 + Cl2 → С5Н11Cl + HCl
Без цеолитных катализаторов такие реакции неселективны, поэтому с н -пентаном получается смесь 1-, 2- и 3-хлорпентанов, а также более высокохлорированных производных. Могут также происходить и другие радикальные галогенирования .
Производство и возникновение
Пентан получают путем фракционной перегонки нефти и очищают путем ректификации (последовательных перегонок). [13]
Он встречается в алкогольных напитках и в хмелевом масле . [13] Он является компонентом выдыхаемого воздуха для некоторых людей. Продукт распада ненасыщенных жирных кислот, его присутствие связано с некоторыми заболеваниями и раком. [14]
Ссылки
- ↑ Хофманн, Август Вильгельм фон (1 января 1867 г.). «I. О действии трихлорида фосфора на соли ароматических моноаминов». Труды Лондонского королевского общества . 15 : 54–62. doi :10.1098/rspl.1866.0018. S2CID 98496840.
- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013. Королевское химическое общество . стр. 59. doi :10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ abcde Карманный справочник NIOSH по химическим опасностям. "#0486". Национальный институт охраны труда и здоровья (NIOSH).
- ↑ Запись о н-пентане в базе данных веществ GESTIS Института охраны труда и техники безопасности , доступ 19 апреля 2011 г.
- ^ "н-пентан". Концентрации, представляющие немедленную опасность для жизни или здоровья (IDLH) . Национальный институт охраны труда (NIOSH).
- ^ abc Wei, James (1999). «Молекулярная симметрия, вращательная энтропия и повышенные точки плавления». Industrial & Engineering Chemistry Research . 38 (12): 5019–5027. doi :10.1021/ie990588m.
- ^ Карл Грисбаум; Арно Бер; Дитер Биденкапп; Хайнц-Вернер Фогес; Доротея Гарбе; Кристиан Паец; Герд Коллин; Дитер Майер; Хартмут Хёке (2002). «Углеводороды». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a13_227. ISBN 978-3-527-30673-2.
- ^ Milne, GWA, ред. (2005). Коммерчески важные химические вещества Гарднера: синонимы, торговые наименования и свойства . Хобокен, Нью-Джерси: John Wiley & Sons, Inc. стр. 477. ISBN 978-0-471-73518-2.
- ^ Вэй, Джеймс (1999). «Молекулярная симметрия, вращательная энтропия и повышенные точки плавления». Industrial & Engineering Chemistry Research . 38 (12). Американское химическое общество (ACS): 5019–5027. doi :10.1021/ie990588m. ISSN 0888-5885.
- ^ Из значений, указанных в разделе Стандартное изменение энтальпии образования (таблица данных) .
- ^ Good, WD (1970). «Энтальпии сгорания и образования изомерных пентанов». Журнал химической термодинамики . 2 (2). Elsevier BV: 237–244. doi :10.1016/0021-9614(70)90088-1. ISSN 0021-9614.
- ^ Роман М. Балабин (2009). «Разница энтальпии между конформациями нормальных алканов: исследование н-пентана и н-бутана методом рамановской спектроскопии». J. Phys. Chem. A. 113 ( 6): 1012–9. Bibcode : 2009JPCA..113.1012B. doi : 10.1021/jp809639s. PMID 19152252.
- ^ ab "Pentane". PubChem . Получено 29-06-2023 .
- ^ Филлипс, Майкл; Эррера, Иоланта; Кришнан, Сунити; Зайн, Муена; Гринберг, Джоэл; Катанео, Рене Н. (1999). «Изменение летучих органических соединений в дыхании нормальных людей». Журнал хроматографии B: Биомедицинские науки и приложения . 729 (1–2): 75–88. doi :10.1016/S0378-4347(99)00127-9. PMID 10410929.
Внешние ссылки
- Международная карта химической безопасности 0534 на ILO.org
- Карманный справочник NIOSH по химическим опасностям на CDC.gov
- Фитохимические данные по пентану на Ars-grin.gov