Молекула не-Кекюле

Молекула , не относящаяся к структуре Кекуле, представляет собой сопряженный углеводород , которому нельзя приписать классическую структуру Кекуле [ требуется определение ] .
Поскольку не-Кекюле молекулы имеют два или более формальных заряда или радикальных центров, их спин-спиновые взаимодействия могут вызывать электропроводность или ферромагнетизм ( магниты на основе молекул ), и ожидается применение в функциональных материалах. Однако, поскольку эти молекулы довольно реактивны и большинство из них легко разлагаются или полимеризуются при комнатной температуре, для их практического использования необходимы стратегии стабилизации. Синтез и наблюдение за этими реактивными молекулами обычно осуществляются методами матричной изоляции .
Бирадикалы
Простейшие не-Кекюле молекулы — бирадикалы. Бирадикал — это четное электронное химическое соединение с двумя центрами свободных радикалов , которые действуют независимо друг от друга. Их не следует путать с более общим классом бирадикалов . [1]
Один из первых бирадикалов был синтезирован Вильгельмом Шленком в 1915 году по той же методологии, что и трифенилметильный радикал Моисея Гомберга . Так называемые углеводороды Шленка-Браунса : [2]

Юджин Мюллер с помощью весов Гуи впервые установил, что эти соединения являются парамагнитными с триплетным основным состоянием .
Другой классический бирадикал был синтезирован Алексеем Чичибабиным в 1907 году. [3] [4] Другими классическими примерами являются бирадикалы, описанные Янгом в 1960 году [5] и Коппингером в 1962 году. [6] [7] [8]
 | 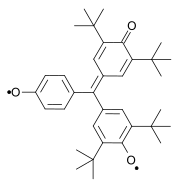 | 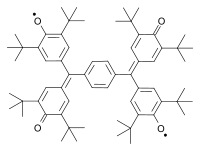 | ||
| Чичибабин бирадикал (1907) | Ян бирадикал (1960) | Коппингер бирадикал 1962 |
Триметиленметан
Хорошо изученным бирадикалом является триметиленметан (ТММ), C
4ЧАС
6. В 1966 году Пол Дауд определил с помощью электронного спинового резонанса , что это соединение также имеет триплетное состояние . В кристаллическом хозяине 6 атомов водорода в ТММ идентичны.
Хинодиметаны и ПАУ
Другими примерами не-Кекюле-молекул являются бирадикалоидные хинодиметаны , имеющие шестичленное кольцо с метиленовыми заместителями.
Не-Кекюле полинуклеарные ароматические углеводороды состоят из нескольких конденсированных шестичленных колец. Простейшим представителем этого класса является триангулен . После неудачных попыток Эриха Клара в 1953 году, триокситриангулен был синтезирован Ричардом Дж. Бушби в 1995 году, а кинетически стабилизированный триангулен — Казухиро Накасудзи в 2001 году. Однако в 2017 году проект под руководством Дэвида Фокса и Аниша Мистри из Уорикского университета в сотрудничестве с IBM синтезировал и визуализировал триангулен . [9] В 2019 году были синтезированы более крупные гомологи триангулена, состоящие из десяти ([4]триангулен) [10] и пятнадцати конденсированных шестичленных колец ([5]триангулен) [11]. В 2021 году был достигнут синтез до сих пор крупнейшего гомолога триангулена, состоящего из двадцати восьми конденсированных шестичленных колец ([7]триангулен) [12] . Эксперименты с использованием сканирующей туннельной микроскопии на спиновых цепях триангуленов выявили самое четкое на сегодняшний день доказательство существования щели Холдейна и дробных краевых состояний, предсказанных для цепи Гейзенберга со спином 1. [13] [14] Родственный класс бирадикалов — пара-бензины .
Другие изученные бирадикалы основаны на плеядене, [15] расширенных виологенах , [16] [17] кораннуленах , [18] нитронил-нитроксиде, [19] бис(феналенилах) [20] и терантенах. [21] [22]
 | 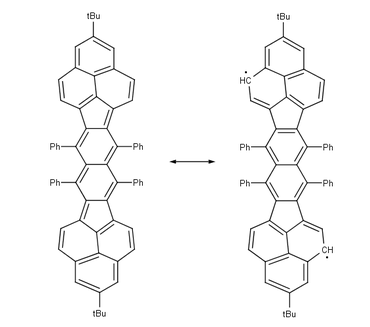 | |
| Терантен бирадикальный синглет. макс. 3 стабилизирующих секстета Clar , стабильный rt, воздух. 50% бирадикальный, молекулярный разрез графена | Бисфеналениловый бирадикальный синглет. макс. 6 стабилизирующих секстетов Clar, стабильный rt, воздух. 42% бирадикальный |
Плеяден был синтезирован из аценафтилена и антраниловой кислоты / амилнитрита :
 |
| Генерация и димеризация плеяден |
Оксиаллил
Оксиаллильный дирадикал (OXA) представляет собой молекулу триметиленметана с одной метиленовой группой , замещенной кислородом . Предполагается, что этот реакционноспособный промежуточный продукт возникает при раскрытии кольца циклопропанонов , оксидов аллена и в перегруппировке Фаворского . Промежуточный продукт был получен в результате реакции радикальных анионов кислорода с ацетоном и изучен методом фотоэлектронной спектроскопии . [23] Экспериментальное сродство к электрону OXA составляет 1,94 эВ.
Классификация

Молекулы не-Кекюле с двумя формальными радикальными центрами (дирадикалы не-Кекюле) можно классифицировать на непересекающиеся и непересекающиеся по форме их двух несвязывающих молекулярных орбиталей (НММО).
Оба NBMO молекул с неразъединяющимися характеристиками, такими как триметиленметан, имеют электронную плотность на одном и том же атоме . Согласно правилу Хунда , каждая орбиталь заполнена одним электроном с параллельным спином, избегая кулоновского отталкивания путем заполнения одной орбитали двумя электронами. Поэтому ожидается, что такие молекулы с неразъединяющимися NBMO будут предпочитать триплетное основное состояние .
Напротив, NBMO молекул с непересекающимися характеристиками, такими как тетраметиленэтан, могут быть описаны без электронной плотности на том же атоме. С такими МО фактор дестабилизации кулоновским отталкиванием становится намного меньше, чем с молекулами непересекающегося типа, и поэтому относительная устойчивость синглетного основного состояния к триплетному основному состоянию будет почти одинаковой или даже обратной из-за обменного взаимодействия .
Ссылки
- ^ Определения бирадикалов и бирадикалов в Золотой книге ИЮПАК
- ^ Роберт А. Мосс ред. (2004), "Реактивная промежуточная химия" (книга) Wiley-Interscience. ISBN 0-471-23324-2
- ^ Чичибабин, А.Э. (1907). «Über einige phenilierte Derivate des p, p-дитолилов». Berichte der Deutschen Chemischen Gesellschaft . 40 (2): 1810–1819 . doi :10.1002/cber.19070400282.
- ^ Монтгомери, Лоуренс К.; Хаффман, Джон К.; Юрчак, Эдвард А.; Грендзе-младший, Мартин П. (1986). «Молекулярные структуры углеводородов Тиле и Чичибабина». Журнал Американского химического общества . 108 (19): 6004– 6011. doi :10.1021/ja00279a056. PMID 22175364.
- ^ Yang, NC; Castro, AJ (1960). "Синтез стабильного бирадикала" n P. Grendze Jr. (1986), "Молекулярные структуры углеводородов Тиле и Чичибабина". Журнал Американского химического общества . 82 (23): 6208. doi :10.1021/ja01508a067.
- ^ Коппингер, GM (1962). «Стабильный феноксирадикал, инертный к кислороду». Тетраэдр . 18 (1): 61– 65. doi :10.1016/0040-4020(62)80024-6.
- ^ Коппингер, GM (1964). «Реакции ингибирования затрудненных фенолов». Журнал Американского химического общества . 86 (20): 4385– 4388. doi :10.1021/ja01074a032.
- ^ М. Баумгартен (2003/2004), «Высокоспиновые молекулы, направленные к молекулярным магнитам», глава 12 в «ЭПР свободных радикалов в твердых телах, тенденции в методах и применении», А. Лунд, М. Шиотани (редакторы), Kluwer, страницы 491-528
- ^ Павличек, Нико; Мистри, Аниш; Майзик, Жолт; Молл, Николай; Мейер, Герхард; Фокс, Дэвид Дж.; Гросс, Лео (2017-02-13). "Синтез и характеристика триангулена" (PDF) . Nature Nanotechnology . advanced online publication (4): 308–311 . Bibcode : 2017NatNa..12..308P. doi : 10.1038/nnano.2016.305. ISSN 1748-3395. PMID 28192389.
- ^ Мишра, Шантану; Бейер, Дорин; Эймре, Кристьян; Лю, Цзюньчжи; Бергер, Рейнхард; Грёнинг, Оливер; Пиньедоли, Карло А.; Мюллен, Клаус; Фазель, Роман; Фэн, Синьлян; Руффье, Паскаль (10 июля 2019 г.). «Синтез и характеристика π-расширенного триангулена». Журнал Американского химического общества . 141 (27): 10621–10625 . doi :10.1021/jacs.9b05319. ISSN 0002-7863. PMID 31241927. S2CID 195696890.
- ^ Су, Цзе; Теличко, Николай; Ху, Пан; Макам, Женевьева; Мутомбо, Пинго; Чжан, Хэцзянь; Бао, Ян; Ченг, Фанг; Хуан, Чжи-Цюань; Цю, Чжижан; Тан, Шерман-младший (01 июля 2019 г.). «Атомно точный восходящий синтез π-расширенного [5] триангулена». Достижения науки . 5 (7): eaav7717. дои : 10.1126/sciadv.aav7717 . ISSN 2375-2548. ПМК 6660211 . ПМИД 31360763.
- ^ Мишра, Шантану; Сюй, Кун; Эймре, Кристьян; Комбер, Хартмут; Ма, Джи; Пиньедоли, Карло; Фазель, Роман; Фэн, Синьлян; Руффье, Паскаль (07 января 2021 г.). «Синтез и характеристика [7] триангулена». Наномасштаб . Принятая рукопись (3): 1624–1628 гг. doi : 10.1039/D0NR08181G. PMID 33443270. S2CID 231605335.
- ^ Mishra, Shantanu; Beyer, Doreen; Eimre, Kristjan; Ortiz, Ricardo; Fernández-Rossier, Joaquín; Berger, Reinhard; Gröning, Oliver; Pignedoli, Carlo A.; Fasel, Roman; Feng, Xinliang; Ruffieux, Pascal (13 июля 2020 г.). "Коллективный полностью углеродный магнетизм в димерах триангуленов". Angewandte Chemie International Edition . 59 (29): 12041– 12047. arXiv : 2003.00753 . doi : 10.1002/anie.202002687. PMC 7383983. PMID 32301570 .
- ^ Мишра, Шантану; Катарина, Гонсалу; Ву, Фупенг; Ортис, Рикардо; Джейкоб, Дэвид; Эймре, Кристьян; Ма, Джи; Пиньедоли, Карло А.; Фэн, Синьлян; Руффье, Паскаль; Фернандес-Россье, Хоакин; Фазель, Роман (13 октября 2021 г.). «Наблюдение дробных краевых возбуждений в спиновых цепочках нанографена». Природа . 598 (7880): 287–292 . arXiv : 2105.09102 . Бибкод : 2021Natur.598..287M. дои : 10.1038/s41586-021-03842-3. PMID 34645998. S2CID 234777902.
- ^ Колц, Ярослав; Михл, Йозеф (1973). «π,π-Бирадикалоидные углеводороды. Семейство плеяденов. I. Фотохимическое получение из предшественников циклобутенов». Журнал Американского химического общества . 95 (22): 7391– 7401. doi :10.1021/ja00803a030.
- ^ Уильям, В. Портер III; Вайд, Томас П.; Рейнгольд, Арнольд Л. (2005). «Синтез и характеристика высоковосстанавливающего нейтрального «расширенного виологена» и изоструктурного углеводорода 4,4''''-ди-н-октил-п-кватерфенила». Журнал Американского химического общества . 127 (47): 16559– 16566. doi :10.1021/ja053084q. PMID 16305245.
- ^ Casado, J.; Patchkovskii, S.; Zgierski, M.; Hermosilla, L.; Sieiro, C.; Oliva, M. Moreno; Navarrete, J. López (2008). "Raman Detection of "ambiguous" conjugated biradicals: Rapid thermal singlet-to-triplet intersystem crossing in an extended viologen". Angewandte Chemie International Edition . 47 (8): 1443– 1446. doi :10.1002/anie.200704398. PMID 18200638.
- ^ Ueda, A.; Nishida, S.; Fukui, K.; Ise, T.; Shiomi, D.; Sato, K.; Takui, T.; Nakasuji, K.; Morita, Y. (2010). "Трехмерное внутримолекулярное обменное взаимодействие в изогнутой и неальтернантной π-сопряженной системе: кораннулен с двумя феноксильными радикалами". Angewandte Chemie International Edition . 49 (9): 1678– 1682. doi :10.1002/anie.200906666. PMID 20108294.
- ^ Ziessel Christophe Stroh, Raymond; Heise, Henrike; Köhler, Frank H.; Turek, Philippe; Claiser, Nicolas; Souhassou, Mohamed; Lecomte, Claude (2004). «Сильные обменные взаимодействия между двумя радикалами, прикрепленными к неароматическим спейсерам, выведенные из измерений магнитной, ЭПР, ЯМР и электронной плотности». J. Am. Chem. Soc . 126 (39): 12604– 12613. doi :10.1021/ja0305959. PMID 15453793.
- ^ Кубо, Такаши; Симидзу, Акихиро; Уруичи, Микио; Якуши, Кюя; Накано, Масаеши; Сиоми, Дайсуке; Сато, Казунобу; Такуи, Такеджи; Морита, Ясуши; Накасудзи, Казухиро (2007). «Синглетный бирадикальный характер углеводорода кекуле на основе феналенила с нафтохиноидной структурой». Орг. Летт . 9 (1): 81–84 . doi :10.1021/ol062604z. ПМИД 17192090.
- ^ Кониси, Акихито; Хирао, Ясуказу; Накано, Масаеши; Симидзу, Акихиро; Ботек, Эдит; Шампанское, Бено; Сиоми, Дайсуке; Сато, Казунобу; Такуи, Такеджи; Мацумото, Кодзо; Курата, Хироюки; Кубо, Такаши (2010). «Синтез и характеристика терантена: синглетный бирадикальный полициклический ароматический углеводород, имеющий структуры Кекуле». Журнал Американского химического общества . 132 (32): 11021–11023 . doi :10.1021/ja1049737. ПМИД 20698663.
- ^ Ламберт, С (2011). «К полициклическим ароматическим углеводородам с синглетным открытым основным состоянием оболочки». Angewandte Chemie International Edition . 50 (8): 1756– 1758. doi :10.1002/anie.201006705. PMID 21284072.
- ^ Ичино, Такатоши; Виллано, Стефани М.; Джианола, Адам Дж.; Гебберт, Даниэль Дж.; Веларде, Луис; Санов, Андрей; Бланксби, Стивен Дж.; Чжоу, Синь; Хроват, Дэвид А.; Тэтчер Борден, Уэстон; Линебергер, В. Карл (2009). "Низшие синглетные и триплетные состояния оксиаллильного дирадикала" (PDF) . Angewandte Chemie International Edition . 48 (45): 8509– 8511. doi :10.1002/anie.200904417. PMID 19739188.