Виниленкарбонат
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 2 H -1,3-Диоксол-2-он | |
| Другие имена 1,3-Диоксолен-2-он Винилкарбонат | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.011.659 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С3Н2О3 | |
| Молярная масса | 86,05 г· моль −1 |
| Появление | бесцветная жидкость [1] |
| Плотность | 1.35 |
| Температура плавления | 22 °C (72 °F; 295 К) |
| Точка кипения | 178 °C (352 °F; 451 К) [2] |
| Опасности | |
| Маркировка СГС : | |
     | |
| Опасность | |
| Н302 , Н311 , Н315 , Н317 , Н318 , Н373 , Н411 | |
| P260 , P261 , P264 , P270 , P272 , P273 , P280 , P301+P312 , P302+P352 , P305+P351+P338 , P310 , P312 , P314 , P321 , P322 , P330 , П332+П313 , П333+П313 , П361 , П362 , П363 , П391 , П405 , П501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Виниленкарбонат ( VC ) или 1,3-диоксол-2-он — простейший ненасыщенный циклический эфир угольной кислоты . Виниленкарбонат также можно рассматривать как циклический карбонат гипотетического ( Z )-этен-1,2-диола. Активированная двойная связь в этом пятичленном кислородсодержащем гетероцикле делает молекулу реакционноспособным мономером для гомополимеризации и сополимеризации и диенофилом в реакциях Дильса-Альдера . Ниже комнатной температуры виниленкарбонат представляет собой бесцветное стабильное твердое вещество.
Подготовка
С момента своего первого описания в 1953 году [3] этиленкарбонат обычно использовался в качестве исходного материала для виниленкарбоната. На первом этапе монохлорэтиленкарбонат производится в УФ-инициированной реакции фотохлорирования с хлором или сульфурилхлоридом при 60-70 °C в массе. На втором этапе монохлорэтиленкарбонат подвергается дегидрохлорированию с основанием, таким как триэтиламин . [4] [5] [6]
Вместо жидкой фазы дегидрохлорирование может также проводиться в газовой фазе на пропитанном хлоридом цинка катализаторе в реакторе с псевдоожиженным слоем при температуре 350-500 °C. [7] Кажущаяся простой реакция дает только 70-80% нечистого конечного продукта из-за множества побочных реакций. Например, при хлорировании этиленкарбоната в веществе или растворе, помимо прочего, образуются 2-хлорацетальдегид , полихлорированный этиленкарбонат и хлорированные продукты раскрытия цикла. Отделение побочных продуктов от конечного продукта путем перегонки с помощью тонкопленочного испарителя [4] , фракционной перекристаллизации [8] или зонной плавки [9] является очень дорогим. Содержание побочных продуктов можно уменьшить путем перемешивания с борогидридом натрия [10] или мочевиной [11] при повышенной температуре. Однако очистка осложняется выраженной термолабильностью виниленкарбоната, поскольку он разлагается при температурах выше 80 °C в течение нескольких минут. [4] Высокочистый виниленкарбонат может быть получен с выходом более 70% путем оптимизации условий хлорирования для подавления образования побочных продуктов [6] и комбинации нескольких щадящих процессов очистки. [12] Тенденция жидкого виниленкарбоната к полимеризации подавляется добавлением ингибиторов, таких как бутилгидрокситолуол (БГТ).
Характеристики
Промышленно производимый виниленкарбонат обычно представляет собой жидкость от желтого до коричневого цвета. При соответствующем контроле процесса и этапах очистки можно получить твердый продукт с температурой плавления 20-22 °C и содержанием хлора ниже 10 ppm. Жидкий виниленкарбонат быстро становится желтым даже при отсутствии света и должен быть стабилизирован путем добавления поглотителей радикалов. В твердой форме высокочистое вещество является долгосрочно стабильным при хранении ниже 10 °C. [13] Виниленкарбонат растворяется в различных растворителях, таких как этанол , тетрагидрофуран, этиленкарбонат, пропиленкарбонат и другие диполярные апротонные электролитные растворители, используемые для литий-ионных аккумуляторных батарей, таких как диметилкарбонат, диэтилкарбонат и тому подобное.
Использовать
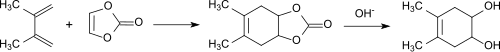
Первая публикация о виниленкарбонате описывала его реакцию Дильса-Альдера на примере реакции присоединения с 2,3-диметилбутадиеном к бициклическому карбонату и последующего гидролиза до цис-4,5-дигидрокси-1,2-циклогексена: [3]
При использовании в качестве диена циклопентадиена после гидролиза образуется вицинальный норборнендиол бицикло[2.2.1]гепт-5-ен-2,3-диол. Окисление по Сверну до 1,2-кетона бицикло[2.2.1]гепт-5-ен-2,3 - диона протекает (в варианте с трифторуксусным ангидридом вместо оксалилхлорида ) с выходом 73%. [14]
Под действием УФ -излучения кетоны реагируют с виниленкарбонатом с образованием бициклических экзооксетанов :
С фосфором(V)сульфидом виниленкарбонат реагирует с соответствующим винилентионокарбонатом (2-тионо-1,3-диоксол-4-ен), [15] который дает кетен с количественным выходом при УФ-облучении. Реакция является хорошей альтернативой разложению α -диазокетонов. [16]
Виниленкарбонат широко используется в качестве электролитной добавки для литий-ионных аккумуляторов , где он способствует образованию нерастворимой пленки между электролитом и отрицательным электродом: SEI (твердо-электролитный интерфейс). [17] Эта полимерная пленка допускает ионную проводимость, но предотвращает восстановление электролита на отрицательном (графитовом) электроде и вносит значительный вклад в долгосрочную стабильность литий-ионных аккумуляторов. [18] [19] В публикации 2013 года предполагается, что циклический сультон 3-фтор-1,3-пропансультон (FPS) превосходит виниленкарбонат в образовании SEI. [20]
Поскольку 1,3-пропансультон (на основе которого создан FPS) классифицируется как особо опасное канцерогенное вещество, следует предположить, что FPS также представляет значительную потенциальную опасность.
Полимеры
Уже первая работа по виниленкарбонату описывает его полимеризацию в массе бесцветного полимера, который гидролизуется до водорастворимого продукта. [3] Последующие публикации предполагают, что первые авторы производили только низкомолекулярные олигомеры. [21] [22] Получение полимеров с более высокой молекулярной массой с полезными свойствами критически зависит от чистоты мономера виниленкарбоната. [23] Виниленкарбонат может быть гомополимеризован в массе , в растворе , в суспензии и в дисперсии с использованием радикальных инициаторов, таких как азобис(изобутиронитрил) (AIBN) или перекись бензоила . Он также может быть сополимеризован с другими виниловыми мономерами, такими как винилпирролидон или винилпропионат . [24]
Поливиниленкарбонат легко растворяется в ацетоне и диметилформамиде . Однако полученные растворы имеют тенденцию разлагаться уже при комнатной температуре. [25] В патентной литературе описано использование поливинилкарбоната для прочных волокон, прозрачных, бесцветных и механически прочных пленок, [21] [10] мембран для обратного осмоса [26] и в качестве носителя во время аффинной хроматографии . [27]
Помимо нестабильности в растворах, поливинилкарбонат имеет тенденцию к гидролизу в слабощелочной среде. При этом образуется полигидроксиметилен (ПГМ) путем расщепления циклического углеродного кольца с повторяющимся звеном –(CHOH)–. Его поведение гораздо больше похоже на целлюлозу, чем на структурно родственный поливиниловый спирт с повторяющимся звеном –(CH 2 –CHOH)–.
Например, полигидроксиметиленовые пленки, полученные щелочным гидролизом поливиниленкарбонатных пленок с помощью метоксида натрия в метаноле, являются кристаллическими и демонстрируют высокую прочность на разрыв . [10] Аналогично целлюлозе, полигидроксиметилен может быть растворен в горячем растворе гидроксида натрия и преобразован путем сшивания в высоконабухающий полимер, который может впитывать до 10 000 раз больше своего веса в воде. [28] Полигидроксиметилен растворим в безводном гидразине [29] и может быть преобразован в целлюлозоподобные волокна путем прядения в воде. Подобно целлюлозе, полигидроксиметилен реагирует с сероуглеродом в щелочном состоянии с образованием ксантогената , из которого нерастворимый в воде полигидроксиметилен снова получается осаждением в разбавленной серной кислоте . [30]
Безопасность
Виниленкарбонат требует особой осторожности при обращении из-за его проблемного токсикологического и экотоксикологического профиля. [1]
Ссылки
- ^ ab Sigma-Aldrich Co. , номер продукта {{{id}}}.
- ^ Haynes, WM, ред. (2016). CRC Handbook of Chemistry and Physics (96-е изд.). Бока-Ратон, Флорида : CRC Press / Taylor & Francis . стр. 3-228. ISBN 978-1482260960.
- ^ abc М. С. Ньюман, Р. В. Аддор (1953), «Виниленкарбонат», Журнал Американского химического общества , том. 75, нет. 5, стр. 1263–1264 , doi :10.1021/ja01101a526
- ^ abc US 6395908, B. Seifert et al., "Process for the preparation of vinylenecarbon, and the use Their", выдан 2002-05-28, передан Merck Patentgesellschaft
- ^ EP 1881972, Райнхард Лангер, Анке Бекманн, Пауль Вагнер, Генрих Грзиния, Марилуиза Шнайдер, Ульрих Нотейс, Ларс Родефельд, Николаус Мюллер, «Процесс производства виниленкарбоната», выдано 28 августа 2013 г., передано Saltigo GmbH
- ^ ab US 8022231, M. Lerm et al., "Процесс приготовления монохлорэтиленкарбоната и последующего преобразования в виниленкарбонат", выданный 2011-09-20, переданный Evonik Degussa GmbH
- ^ EP 1881973, R. Langer et al., "ПРОЦЕСС ПОЛУЧЕНИЯ ВИНИЛЕНКАРБОНАТА", выпущенный 2008-01-30
- ^ GB 899205, Nesbitt BF & Goodman I, "Очистка и полимеризация виниленкарбоната", выдан 20 июня 1962 г., передан ICI Ltd.
- ^ Zief, Morris; Ruch, Hollister; Schramm, Charles H (1963). "Аппарат для низкотемпературной зоны очистки". Журнал химического образования (на немецком языке). 40 (7): 351. Bibcode : 1963JChEd..40..351Z. doi : 10.1021/ed040p351.
- ^ abc ND Field, JR Schaefgen (1962), "Высокомолекулярный поливиниленкарбонат и его производные", Journal of Polymer Science A: Polymer Chemistry (на немецком языке), т. 58, № 166, стр. 533–543 , Bibcode : 1962JPoSc..58..533F, doi : 10.1002/pol.1962.1205816630
- ^ PCT-Anmeldung WO 2006/119910, Verfahren zur Reinigung von Vinylencarbonat , изобретение 1: Р. Лангер и др., правопреемство 1: Lanxess Deutschland GmbH, veröffentlicht am 16 ноября 2006 г.
- ^ EP 1881971, Рейнхард Лангер, Пауль Вагнер, Генрих Грзиниа, «Высокочистый виниленкарбонат и метод очистки виниленкарбоната», выдан 30.01.2008, передан Saltigo GmbH
- ^ WO 2006119908, Р. Лангер, «СПОСОБ ХРАНЕНИЯ И ТРАНСПОРТИРОВКИ ВИНИЛЕНКАРБОНАТА», выдан 16.11.2006, передан Lanxess Deutschland GmbH
- ^ T. Kobayashi, S. Kobayashi (2000), «Окисление по Сверну бицикло[2.2.1]гепт-5-ен-2,3-диола и его производных, конденсированных с пиразином: улучшенный синтез бицикло[2.2.1]гепт-5-ен-2,3-диона и неожиданная реакция раскрытия кольца», Molecules (на немецком языке), т. 5, № 9, стр. 1062–1067 , doi : 10.3390/50901062
- ^ Ханс-Майкл Фишлер, Вилли Хартманн (1972), «Notiz über die Darstellung von Vinylenthioncarbonat und einigen алкил-сови арилзамещенные производные», Chemische Berichte (на немецком языке), vol. 105, нет. 8, стр. 2769–2771 , doi :10.1002/cber.19721050838.
- ^ Справочник по реагентам для органических синтезов, Серосодержащие реагенты , ред. LA Paquette, Wiley-VCH, 2010, ISBN 978-0-470-74872-5 , стр. 535.
- ^ Ли, Сян-Хван; Ван, Юн-Юнь; Ван, Чи-Чао; Ян, Мо-Хуа; Дэн-Цвэнь Ши, Хун-Чун Ву (2005). «Функция виниленкарбоната как термической добавки к электролиту в литиевых батареях». Журнал прикладной электрохимии (на немецком языке). 35 (6): 615– 623. doi :10.1007/s10800-005-2700-x. S2CID 97739869.
- ^ М. Бруссели и др., Основные механизмы старения литий-ионных аккумуляторов , J. Power Sources, 146 (1), 90–96 (2005), doi:10.1016/j.jpowsour.2005.03.172.
- ^ DE 102004018929, В. Хенниге и др., "Elektrolytzusammensetzung sowie deren Verwendung als Elektrolytmaterial für elektrochemische Energiespeichersysteme", выдан 17 ноября 2005 г., передано правопреемнику1 Degussa AG.
- ^ HM Jung et al., Фторпропановый сультон как добавка, образующая SEI, которая превосходит виниленкарбонат , J. Mater. Chem. A, 1, 11975–11981 (2013), doi:10.1039/C3TA12580G.
- ^ ab US 2993030, GE Ham, M. Zief, "Process for polymerizing vinylene carbonate", выдан 1961-07-16, передан JT Baker Chemical Co.
- ^ М. Кребс, К. Шнайдер, Виниленкарбонат – исследование его полимеризационного и сополимеризационного поведения , Adv. Chem., 142 (9), 92–98 (1975), doi:10.1021/ba-1975-0142.ch009.
- ^ GB 899205, Бренда Фрэнсис Несбитт, Айзек Гудман, «Очистка и полимеризация виниленкарбоната», выдан 20 июня 1962 г., передан Imperial Chemical Industries Ltd.
- ^ US 4098771, H. Huemer, K. Burg, "Process for the preparation of polymers of vinylenecarbon", выдан 1978-07-04, передан Hoechst AG
- ^ J. Huang et al., Исследования виниленкарбоната I. Получение и свойства поли-(виниленкарбоната) , Chinese J. Polym. Sci., 8 (3), 197–203 (1990).
- ^ US 3332894, PA Cantor, RE Kesting, «Опреснительная мембрана из поливинилкарбоната и способ ее получения», выдан 25 июля 1967 г.
- ^ US 4788278, O. Mauz, «Поливиниленкарбонат и полигидроксиметилен, процессы их получения и использования», выдан 29 ноября 1988 г., передан Hoechst AG
- ^ US 4061692, A. Holst, M. Kostrzewa, «Процесс производства набухающих, абсорбирующих полимеров полигидроксиметилена», выдан 1977-12-06
- ^ US 4076680, MK Akkapeddi, HK Reimschuessel, "Поли(гидроксиметилен) растворы", выдан 28.02.1978
- ^ US 3331800, H. Schübel et al., «Приготовление растворов полигидроксиметиленсодержащих полимеров», выдан 1967-07-18