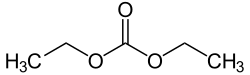
Диэтилкарбонат
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Диэтилкарбонат | |
| Другие имена Углекислый эфир; Этилкарбонат, ди-; Эуфин [1] | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChEMBL |
|
| ChemSpider | |
| Информационная карта ECHA | 100.003.011 |
| Номер ЕС |
|
CID PubChem |
|
| Номер RTECS |
|
| УНИИ | |
| Номер ООН | 2366 |
Панель инструментов CompTox ( EPA ) |
|
| |
| Характеристики | |
| С5Н10О3 | |
| Молярная масса | 118,132 г·моль −1 |
| Появление | Бесцветная жидкость. |
| Плотность | 0,975 г/см 3 |
| Температура плавления | −74,3 °C (−101,7 °F; 198,8 К) [3] |
| Точка кипения | 125,9 °C (258,6 °F; 399,0 К) [2] |
| Нерастворимый | |
| Опасности | |
| Маркировка СГС : | |
  | |
| Предупреждение | |
| Н226 , Н315 , Н319 , Н335 | |
| Р210 , Р233 , Р240 , Р241 , Р242 , Р243 , Р261 , Р264 , Р271 , Р280 , Р302+Р352 , Р303+Р361+Р353 , Р304+Р340 , Р305+Р351+Р338 , Р312 , Р321 , Р332+Р313 , Р337+Р313 , Р362 , Р370+Р378 , Р403+Р233 , Р403+Р235 , Р405 , Р501 | |
| точка возгорания | 33 °C (91 °F; 306 К) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Диэтилкарбонат (иногда сокращенно ДЭК ) представляет собой эфир угольной кислоты и этанола с формулой OC(OCH2CH3 ) 2 . При комнатной температуре (25 ° C) диэтилкарбонат представляет собой бесцветную жидкость с низкой температурой вспышки .
Диэтилкарбонат используется в качестве растворителя , например, при внутримышечных инъекциях эритромицина . [4] [5] [6] Его можно использовать в качестве компонента электролитов в литиевых батареях . Он был предложен в качестве топливной добавки для поддержки более чистого сгорания дизельного топлива, поскольку его высокая температура кипения может снизить летучесть смешанного топлива, минимизируя накопление паров в теплую погоду, которые могут засорять топливные магистрали. [7] В качестве топливной добавки он может снизить выбросы, такие как летучие органические соединения, CO2 и твердые частицы. [8]
Производство
Его можно получить путем реакции фосгена с этанолом, производя хлористый водород в качестве побочного продукта. Поскольку хлороформ может реагировать с кислородом с образованием фосгена, хлороформ можно стабилизировать для хранения, добавив 1 часть (по массе) этанола к 100 частям (по массе) хлороформа, так что любой образующийся фосген преобразуется в диэтилкарбонат.
- 2 СН 3 СН 2 ОН + COCl 2 → CO 3 (СН 2 СН 3 ) 2 + 2 HCl
Его также можно получить путем алкоголиза мочевины с этанолом. Эта реакция требует гетерогенного катализа, который может действовать как кислота Льюиса и основание, например, различные оксиды металлов. Реакция протекает через образование промежуточного этилкарбамата . [8]
- 2 CH 3 CH 2 OH + CO(NH 2 ) 2 → CO 3 (CH 2 CH 3 ) 2 + 2 NH 3
Его также можно синтезировать напрямую из диоксида углерода и этанола, используя различные методы, а также посредством окислительного карбонилирования с помощью оксида углерода . Другой метод — переэтерификация из диметилкарбоната . Еще один метод — из реакции этилнитрита и оксида углерода, где этилнитрит может быть получен из оксида азота и этанола. Этот метод требует катализатора, такого как палладий . [8]
Использование в биологических исследованиях
0,01% об./об. растворы ДЭК можно использовать в качестве относительно мягкого холодного стерилизующего реагента для смол для лабораторной хроматографии . [9]
Смотрите также
Ссылки
- ^ "ДИЭТИЛ КАРБОНАТ" . Получено 2010-02-01 .
- ^ Уильям М. Хейнс, ред. (2016). CRC Handbook of Chemistry and Physics (97-е изд.). CRC Press . стр. 15-15. ISBN 978-1498754293.
- ^ Дин, Майкл С.; Сюй, Кан; Джоу, Т. Ричард (2001). «Диаграммы жидкая/твердая фаза бинарных карбонатов для литиевых батарей». Журнал электрохимического общества . 148 (5): A299–A304. doi :10.1149/1.1393419 – через ECS.
- ^ Андерсон, Роберт С.; Харрис, Пол Н.; Чен, КК (1955). «Дальнейшие токсикологические исследования с илотицином® (эритромицин, Lilly)». Журнал Американской фармацевтической ассоциации . 44 (4): 199–204. doi :10.1002/jps.3030440404. ISSN 1930-2304. PMID 14367139.
- ↑ US 4382086, Sciavolino, Frank C. & Hauske, James R., «9-дигидро-11,12-кетальные производные эритромицина А и эпи-эритромицина А», опубликовано 03.05.1983, выдано 01.03.1982, передано Pfizer Inc.
- ^ US 4363803, Хауске, Джеймс Р., «3»,4»-Оксиаллиленэритромицин и олеандомицин, состав и способ применения», опубликовано 14 декабря 1982 г., выдано 1 марта 1982 г., передано Pfizer Inc.
- ^ Уолтер, К. Ученые открыли метод получения более чистого ископаемого топлива. Журнал MR&D. 18.09.2017 - 15:16
- ^ abc Шукла, Картикея; Шривастава, Вимал Чандра (2016). «Диэтилкарбонат: критический обзор путей синтеза, используемых катализаторов и инженерных аспектов». RSC Advances . 6 (39): 32624–32645. Bibcode : 2016RSCAd...632624S. doi : 10.1039/c6ra02518h . Получено 3 августа 2021 г.
- ^ Rad, Bio-. "Bio-Gel A Gels - Instruction Manual" (PDF) . Получено 12 апреля 2023 г. .


