Тетродотоксин
Эта научная статья нуждается в дополнительных ссылках на вторичные или третичные источники . ( Февраль 2016 ) |
 | |
 | |
| Имена | |
|---|---|
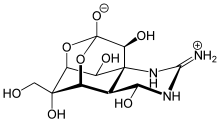
| Название ИЮПАК (4 R ,4a R ,5 R ,6 S ,7 S ,8 S ,8a R ,10 S ,12 S )-2-азаниелиден-4,6,8,12-тетрагидрокси-6-(гидроксиметил)-2,3,4,4a,5,6,7,8-октагидро-1 H -8a,10-метано-5,7-(эпоксиметаноокси)хиназолин-10-олат | |
| Другие имена ангидротетродотоксин, 4-эпитетродотоксин, тетродоновая кислота, ТТХ | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| Информационная карта ECHA | 100.022.236 |
| |
| КЕГГ | |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С11Н17Н3О8 | |
| Молярная масса | 319,270 г·моль −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Тетродотоксин ( TTX ) — мощный нейротоксин . Его название происходит от Tetraodontiformes , отряда , в который входят рыбы-собаки , рыбы-ежики , океанические солнечные рыбы и рыбы-спинороги ; некоторые из этих видов несут этот токсин. Хотя тетродотоксин был обнаружен у этих рыб, он обнаружен и у некоторых других животных (например, у сине-кольчатых осьминогов , тритонов с грубой кожей и лунных улиток ). Он также вырабатывается некоторыми инфекционными или симбиотическими бактериями , такими как Pseudoalteromonas , Pseudomonas и Vibrio , а также другими видами, находящимися в симбиотических отношениях с животными и растениями. [1] [2]
Хотя он ежегодно вызывает тысячи случаев отравления и несколько смертей [3] , он продемонстрировал эффективность в лечении боли, связанной с раком, в клинических испытаниях II и III фазы. [4]
Тетродотоксин — блокатор натриевых каналов . Он подавляет активацию потенциалов действия в нейронах, связываясь с потенциалзависимыми натриевыми каналами в мембранах нервных клеток и блокируя прохождение ионов натрия (ответственных за восходящую фазу потенциала действия) в нейрон. Это не позволяет нервной системе передавать сообщения и, таким образом, мышцам сокращаться в ответ на нервную стимуляцию. [5]
Механизм его действия – селективная блокировка натриевых каналов – был окончательно продемонстрирован в 1964 году Тошио Нарахаши и Джоном У. Муром в Университете Дьюка с использованием метода фиксации потенциала в зазоре сахарозы . [6]
Источники в природе
Помимо бактериальных видов, которые, скорее всего, изначально являются биосинтетическими (см. ниже), тетродотоксин был выделен из самых разных видов животных, включая: [1]
- все осьминоги и каракатицы в небольших количествах, но особенно несколько видов синекольчатых осьминогов , [1] [2] [5] включая Hapalochlaena maculosa (где он был назван «макулотоксином»), [2]
- различные виды рыб-собак , [1] [2] [5]
- некоторые рыбы-ангелы , [7]
- виды брюхоногих моллюсков Nassarius , [1] [2] [5]
- вид Naticidae (лунные улитки), [1] [8]
- несколько морских звезд , включая виды Astropecten , [1] [2] [5]
- несколько видов крабов-ксантидов . [1] [2]
- виды Chaetognatha (черви-стрелки), [1] [5]
- виды Nemertea (ленточные черви), [1] [5]
- многослойный плоский червь , [1]
- наземные планарии рода Bipalium , [9]
- жабы рода Atelopus , [1]
- жабы рода Brachycephalus , [10]
- восточный тритон ( Notophthalmus viridescens ) [11]
- западные или грубокожие тритоны ( Taricha ; первоначально он назывался «тарихатоксин»), [1]
В 1964 году Мошер и др. [12] [13] показали, что тарихатоксин идентичен ТТХ, а в 1978 году в журнале Science было сообщено об идентичности макулотоксина и ТТХ , [14] а синонимичность этих двух токсинов подтверждается в современных отчетах (например, в Pubchem [15] и в современных учебниках по токсикологии [16] ), хотя исторические монографии, подвергающие это сомнению, продолжают переиздаваться. [17]
Токсин по-разному используется животными в качестве защитного биотоксина для отражения хищников или как защитный и хищный яд (например, у осьминогов, щетинкочелюстных и ленточных червей ). [18] Несмотря на то, что токсин действует как защитный механизм, некоторые хищники, такие как обыкновенная подвязочная змея , выработали нечувствительность к ТТХ, что позволяет им охотиться на ядовитых тритонов . [19]
Связь TTX с потребляемыми, инфицирующими или симбиотическими бактериальными популяциями в пределах вида животных, из которых он выделен, относительно ясна; [1] присутствие бактерий, продуцирующих TTX, в микробиоме животного определяется методами культивирования, наличие токсина — химическим анализом, а связь бактерий с продукцией TTX — анализом токсичности сред, в которых выращиваются предполагаемые бактерии. [2] Как отмечают Лаго и др., «есть веские доказательства того, что поглощение бактерий, продуцирующих TTX, является важным элементом токсичности TTX у морских животных, которые представляют этот токсин». [2] Бактерии, продуцирующие TTX, включают виды Actinomyces , Aeromonas , Alteromonas , Bacillus , Pseudomonas и Vibrio ; [2] у следующих животных были обнаружены определенные виды бактерий: [a]
| Животное | Бактерии | Ссылка |
|---|---|---|
| Takifugu obscurus , малоизвестная рыба-фугу |
| [2] [5] |
| Nassarius semiplicatus , брюхоногий моллюск |
| [1] |
| Hapalochlaena maculosa , южный синекольчатый осьминог |
| [1] [2] [5] [20] |
| Astropecten polyacanthus , морская звезда | Вибрион альгинолитический | [2] [5] |
| Takifugu vermicularis , рыба-собака |
| [1] [2] [5] [21] |
| Четыре вида щетинкочелюстных (червей-стрелок) |
| [22] |
| Виды немертин (ленточных червей) | Вибрионы рода Вибрион | [1] [23] |
Связь видов бактерий с продукцией токсина не вызывает сомнений – Лаго и его коллеги утверждают, что «[эндоцеллюлярные] симбиотические бактерии были предложены в качестве возможного источника эукариотического ТТХ посредством экзогенного пути» [2] , а Чау и его коллеги отмечают, что «широко распространенное распространение ТТХ в филогенетически различных организмах... убедительно свидетельствует о том, что симбиотические бактерии играют роль в биосинтезе ТТХ» [1] – хотя эта корреляция была распространена на большинство, но не на всех животных, у которых был идентифицирован токсин. [1] [2] [5] Напротив, в одном случае, с тритонами ( Taricha granulosa ), не удалось обнаружить бактерии, продуцирующие ТТХ, в тканях с самыми высокими уровнями токсина ( кожа , яичники , мышцы ) с использованием методов ПЦР [24], хотя были высказаны технические опасения по поводу этого подхода. [1] Критически важным для общего аргумента является то, что иглобрюхи Takifugu rubripes, пойманные и выращенные в лабораторных условиях на контролируемых диетах без ТТХ, «теряют токсичность со временем», в то время как культивируемые иглобрюхи Takifugu niphobles, не содержащие ТТХ и питающиеся диетами, содержащими ТТХ, показали, что ТТХ в печени рыб увеличивается до токсичных уровней. [1] Следовательно, поскольку виды бактерий, которые производят ТТХ, широко представлены в водных отложениях, есть веские основания для приема внутрь ТТХ и/или бактерий, продуцирующих ТТХ, с накоплением и возможной последующей колонизацией и производством. [1] Тем не менее, без четких путей биосинтеза (еще не обнаруженных у животных, но показанных для бактерий), [25] остается неясным, накапливает ли каждое животное ТТХ просто через бактерии; остается вопрос, можно ли в достаточной степени объяснить эти количества приемом внутрь, приемом внутрь плюс колонизацией или каким-то другим механизмом. [1] [2] [5]
Биохимия
Тетродотоксин связывается с тем, что известно как сайт 1 быстрого потенциалзависимого натриевого канала . [26] Сайт 1 расположен в отверстии внеклеточной поры ионного канала. Любая молекула, связанная с этим сайтом, будет блокировать ионы натрия от проникновения в нервную клетку через этот канал (что в конечном итоге необходимо для нервной проводимости). Сакситоксин , неосакситоксин и несколько конотоксинов также связываются с тем же сайтом. [27]
Использование этого токсина в качестве биохимического зонда выявило два различных типа потенциалзависимых натриевых каналов (VGSC), присутствующих у млекопитающих: тетродотоксин-чувствительные потенциалзависимые натриевые каналы (TTX-s Na + каналы) и тетродотоксин-резистентные потенциалзависимые натриевые каналы (TTX-r Na + каналы). Тетродотоксин ингибирует TTX-s Na + каналы в концентрациях около 1–10 нМ, [28] тогда как для ингибирования TTX-r Na + каналов требуются микромолярные концентрации тетродотоксина . [29] Нервные клетки, содержащие TTX-r Na + каналы, расположены в основном в сердечной ткани, в то время как нервные клетки, содержащие TTX-s Na + каналы, доминируют в остальной части тела.
TTX и его аналоги исторически были важными агентами для использования в качестве химических инструментальных соединений, для использования в характеристике каналов и в фундаментальных исследованиях функций каналов. [30] [31] Распространенность Na + -каналов TTX в центральной нервной системе делает тетродотоксин ценным агентом для подавления нейронной активности в клеточной культуре .
Биосинтез
Биосинтетический путь к TTX изучен лишь частично. Давно известно, что молекула связана с сакситоксином , и по состоянию на 2011 год считается, что существуют отдельные пути для водного (бактериального) и наземного (тритона) TTX. [32] В 2020 году новые промежуточные продукты, обнаруженные у тритонов, предполагают, что синтез начинается с геранилгуанидина у амфибий; эти промежуточные продукты не были обнаружены у водных животных, содержащих TTX, что подтверждает теорию раздельного пути. [33] В 2021 году был получен первый геном бактерии, продуцирующей TTX. Эта « Bacillus sp. 1839» была идентифицирована как Cytobacillus gottheilii с использованием ее последовательности рРНК. Исследователь, ответственный за это исследование, еще не определил последовательный путь, но надеется сделать это в будущем. [34]
Сопротивление
Животные, которые накапливают TTX в качестве защитного механизма, а также их хищники должны эволюционировать, чтобы стать устойчивыми к воздействию TTX. Мутации в генах VGSC, особенно генах Na v 1.4 (скелетно-мышечный VGSC, «TTX-s» [35] ), обнаружены у многих таких животных. [36] Эти мутации возникали независимо несколько раз, даже многократно в разных популяциях одного и того же вида, как это было отмечено у подвязочной змеи. Они состоят из различных аминокислотных замен в схожих позициях, что является слабым примером конвергентной эволюции, вызванной тем, как TTX связывается с немутировавшим VGSC. [36]
Другой путь к устойчивости к TTX — это токсин-связывающие белки, которые достаточно крепко удерживают TTX, чтобы не допустить его попадания в уязвимые VGSC. Различные белки, связывающие TTX, были обнаружены у рыбы-собаки, крабов и брюхоногих моллюсков. Существуют также белки, связывающие сакситоксин (STX), токсин с похожим механизмом действия. [36]
Химический синтез
В 1964 году группа ученых под руководством Роберта Б. Вудворда выяснила структуру тетродотоксина. [37] Структура была подтверждена рентгеновской кристаллографией в 1970 году. [38] Йошито Киши и его коллеги сообщили о первом полном синтезе рацемического тетродотоксина в 1972 году. [39] [40] М. Изобэ и его коллеги [41] [42] [43] и Дж. Дюбуа сообщили об асимметричном полном синтезе тетродотоксина в 2003 году. [44] Два синтеза 2003 года использовали совершенно разные стратегии: путь Изобэ был основан на подходе Дильса-Альдера , а работа Дюбуа использовала активацию связи C–H . С тех пор методы быстро совершенствовались, и было разработано несколько новых стратегий синтеза тетродотоксина. [45] [46]
Отравление
Токсичность
TTX чрезвычайно токсичен. В паспорте безопасности материала для TTX указана пероральная средняя летальная доза ( LD 50 ) для мышей, равная 334 мкг на кг. [47] Для сравнения, пероральная LD 50 цианида калия для мышей составляет 8500 мкг на кг, [48] демонстрируя, что даже перорально TTX более ядовит, чем цианид . TTX еще более опасен, если вводится внутривенно; количество, необходимое для достижения летальной дозы путем инъекции, составляет 8 мкг на кг для мышей. [49]
Токсин может попасть в организм жертвы через рот , инъекцию, вдыхание или через поврежденную кожу. [50]
Отравление , возникающее в результате потребления рыбы отряда Tetraodontiformes, является чрезвычайно серьезным. Органы (например, печень) рыбы-собаки могут содержать уровни тетродотоксина, достаточные для того, чтобы вызвать описанный паралич диафрагмы и соответствующую смерть из-за дыхательной недостаточности . [51] Токсичность варьируется между видами, в зависимости от сезона и географического положения, а мясо многих рыб-собаки может быть не опасно токсичным. [5]
Механизм токсичности заключается в блокировке быстрых потенциалзависимых натриевых каналов, которые необходимы для нормальной передачи сигналов между телом и мозгом. [52] В результате ТТХ вызывает потерю чувствительности и паралич произвольных мышц, включая диафрагму и межреберные мышцы, останавливая дыхание. [53]
История

Терапевтическое использование яиц рыбы-собаки ( тетраодона ) упоминается в первой китайской фармакопее Pen-T'so Ching (Книга трав, предположительно 2838–2698 гг. до н. э. Шэньнуна ; но более поздняя дата более вероятна ), где они были классифицированы как имеющие «среднюю» токсичность, но могут оказывать тонизирующее действие при использовании в правильной дозе. Основное применение было «для остановки судорожных заболеваний». [30] В Pen-T'so Kang Mu (Указатель трав или Великий травник Ли Ши-Чена, 1596) некоторые виды рыб Хо-Тун (современное китайское название тетраодона ) также были признаны как токсичные, но при правильной дозе полезные как часть тонизирующего средства. Повышенная токсичность Хо-Туна была отмечена у рыбы, пойманной в море (а не в реке) после марта. Было признано, что наиболее ядовитыми частями являются печень и яйца, но токсичность можно снизить, замочив яйца. [30] (Тетродотоксин малорастворим в воде и растворим в концентрации 1 мг/мл в слабокислых растворах.) [54]
Немецкий врач Энгельберт Кемпфер в своей «Истории Японии» (переведенной и опубликованной на английском языке в 1727 году) описал, насколько хорошо были известны токсические эффекты рыбы, вплоть до того, что ее использовали для самоубийства, и что император специально постановил, что солдатам не разрешалось есть ее. [55] Существуют также свидетельства из других источников, что знания о такой токсичности были широко распространены по всей Юго-Восточной Азии и Индии. [30]
Первые зарегистрированные случаи отравления ТТХ у западных людей были зафиксированы в судовых журналах капитана Джеймса Кука от 7 сентября 1774 года. [51] В тот день Кук записал, что его команда съела немного местной тропической рыбы (рыбы-собаки), а затем скормила остатки свиньям, содержавшимся на борту. Экипаж испытал онемение и одышку, а свиньи были найдены мертвыми на следующее утро. Оглядываясь назад, становится ясно, что команда пережила слабую дозу тетродотоксина, в то время как свиньи съели части тела рыбы-собаки, содержащие большую часть токсина, таким образом, получив смертельное отравление.
Токсин был впервые выделен и назван в 1909 году японским ученым доктором Ёсидзуми Тахарой. [2] [56] [51] Это был один из агентов, изученных японским подразделением 731 , которое оценивало биологическое оружие на людях в 1930-х годах. [57]
Симптомы и лечение
Диагноз отравления рыбой фугу ставится на основании наблюдаемых симптомов и недавнего анамнеза питания. [58]
Симптомы обычно развиваются в течение 30 минут после приема внутрь, но могут быть отсрочены до четырех часов; однако, если доза смертельная, симптомы обычно проявляются в течение 17 минут после приема. [51] За покалыванием губ и языка следует его развитие в конечностях, гиперсаливация , потливость , головная боль, слабость, летаргия, нарушение координации , тремор , паралич, синюшная кожа , потеря голоса , затрудненное глотание и судороги . Желудочно-кишечные симптомы часто бывают серьезными и включают тошноту , рвоту , диарею и боли в животе ; смерть обычно наступает из-за дыхательной недостаточности . [53] [58] Увеличивается респираторный дистресс , нарушается речь, и у жертвы обычно наблюдается одышка , чрезмерное расширение зрачков и аномально низкое кровяное давление . Паралич усиливается, могут возникнуть судороги , умственные нарушения и нерегулярное сердцебиение . Жертва, хотя и полностью парализованная, может быть в сознании и в некоторых случаях полностью понятна до самой смерти, которая обычно наступает в течение 4-6 часов (диапазон ~20 минут до ~8 часов). Однако некоторые жертвы впадают в кому . [ 53] [59]
Если пациент выживает в течение 24 часов, выздоровление без каких-либо последствий обычно происходит в течение нескольких дней. [58]
Терапия поддерживающая и основана на симптомах, с агрессивным ранним контролем дыхательных путей. [51] В случае употребления лечение может состоять из опорожнения желудка, кормления жертвы активированным углем для связывания токсина и принятия стандартных мер жизнеобеспечения, чтобы поддерживать жизнь жертвы до тех пор, пока не прекратится действие яда. [51] Альфа-адренергические агонисты рекомендуются в дополнение к внутривенным жидкостям для повышения артериального давления; антихолинэстеразные агенты «были предложены в качестве варианта лечения, но не были должным образом протестированы». [59]
Антидот не был разработан и одобрен для использования человеком, но первичный отчет об исследовании (предварительный результат) показывает, что USAMRIID разрабатывает моноклональное антитело, специфичное к тетродотоксину , которое было эффективно в одном исследовании для снижения летальности токсина в тестах на мышах. [60]
Распространение токсичности по всему миру
Отравления тетродотоксином были почти исключительно связаны с потреблением рыбы-собаки из вод Индо-Тихоокеанского региона, в первую очередь потому, что столь же токсичные рыбы-собаки из других регионов употребляются в пищу гораздо реже. Несколько зарегистрированных случаев отравлений, включая смертельные случаи, тем не менее, были связаны с рыбой-собакой из Атлантического океана, Мексиканского залива и Калифорнийского залива . Не было подтвержденных случаев тетродотоксичности от атлантической рыбы-собаки, Spheroides maculatus , но три исследования обнаружили, что экстракты из рыбы этого вида высокотоксичны для мышей. Несколько недавних отравлений этими рыбами во Флориде были вызваны сакситоксином , который вызывает паралитическое отравление моллюсками с очень похожими симптомами и признаками. Раковина-трубач Charonia sauliae была замешана в пищевых отравлениях, и данные свидетельствуют о том, что она содержит производное тетродотоксина. Было зарегистрировано несколько случаев отравления неправильно маркированной рыбой-собакой, и по крайней мере один случай со смертельным исходом в Орегоне, когда человек на спор проглотил тритона Taricha granulosa с грубой кожей. [61]
В 2009 году в регионе Окленд в Новой Зеландии началась серьезная паника после того, как несколько собак погибли, съев Pleurobranchaea maculata (серого морского слизняка) на пляжах. [62] Детей и владельцев домашних животных попросили избегать пляжей, а любительская рыбалка также была прервана на некоторое время. После исчерпывающего анализа было обнаружено, что морские слизни, должно быть, проглотили тетродотоксин. [63]
Статистические факторы
Статистика Токийского бюро социального обеспечения и общественного здравоохранения показывает, что в период с 1996 по 2006 год по всей стране ежегодно регистрировалось 20–44 случая отравления фугу , что приводило к 34–64 госпитализациям и 0–6 смертельным случаям в год, при этом средний уровень смертности составил 6,8%. [64] Из 23 инцидентов, зарегистрированных в Токио в период с 1993 по 2006 год, только один произошел в ресторане, а все остальные были связаны с рыбаками, поедавшими свой улов. [64] С 2006 по 2009 год в Японии произошло 119 инцидентов с участием 183 человек, но погибло всего семь человек. [65]
Только несколько случаев были зарегистрированы в Соединенных Штатах, а вспышки в странах за пределами Индо-Тихоокеанского региона редки. На Гаити считалось, что тетродотоксин использовался в препаратах вуду , в так называемых зомби -ядах. Однако последующий тщательный анализ неоднократно ставил под сомнение ранние исследования по техническим причинам и не смог идентифицировать токсин ни в одном препарате. [66] [67] [68] Поэтому обсуждение этого вопроса практически исчезло из первичной литературы с начала 1990-х годов. Као и Ясумото пришли к выводу в первой из своих статей в 1986 году, что «широко распространенное в светской прессе утверждение о том, что тетродотоксин является причинным агентом в первоначальном процессе зомбирования, не имеет под собой фактических оснований». [66] : 748
Генетический фон не является фактором восприимчивости к отравлению тетродотоксином. Этого токсикоза можно избежать, не употребляя в пищу виды животных, которые, как известно, содержат тетродотоксин, в основном, рыбу-собаку; другие тетродотоксичные виды обычно не употребляются в пищу людьми.
Фугу как еда
Отравление тетродотоксином вызывает особую озабоченность общественного здравоохранения в Японии, где фугу является традиционным деликатесом. Его готовят и продают в специальных ресторанах, где обученные и лицензированные повара аккуратно удаляют внутренности , чтобы снизить опасность отравления. [69] Существует вероятность неправильной идентификации и маркировки, особенно приготовленных, замороженных рыбных продуктов.
Анализ пищевых продуктов
Биопроба на мышах, разработанная для паралитического отравления моллюсками (PSP), может использоваться для мониторинга тетродотоксина у рыбы-собаки и является текущим методом выбора. Метод ВЭЖХ с постколоночной реакцией со щелочью и флуоресценцией был разработан для определения тетродотоксина и связанных с ним токсинов. Продукты щелочной деградации могут быть подтверждены как их триметилсилильные производные с помощью газовой хроматографии/масс-спектрометрии. [ необходима цитата ]
Обнаружение в жидкостях организма
Тетродотоксин может быть количественно определен в сыворотке, цельной крови или моче для подтверждения диагноза отравления у госпитализированных пациентов или для оказания помощи в судебно-медицинском расследовании случая смертельной передозировки. Большинство аналитических методов включают масс-спектрометрическое обнаружение после газового или жидкостного хроматографического разделения. [70]
Современные терапевтические исследования
Тетродотоксин исследовался как возможное средство от боли, связанной с раком. Ранние клинические испытания демонстрируют значительное облегчение боли у некоторых пациентов. [71] [72]
Он также изучался в связи с мигренью . Мутации в одном конкретном TTX-чувствительном Na + канале связаны с некоторыми мигренями , [73] хотя неясно, имеет ли это какое-либо терапевтическое значение для большинства людей с мигренью. [74]
Тетродотоксин использовался в клинической практике для облегчения негативных последствий, связанных с отменой героина . [75]
Регулирование
The examples and perspective in this article deal primarily with the United States and do not represent a worldwide view of the subject. (February 2017) |
В США тетродотоксин фигурирует в списке избранных агентов Департамента здравоохранения и социальных служб , [76] и ученые должны зарегистрироваться в HHS, чтобы использовать тетродотоксин в своих исследованиях. Однако исследователи, имеющие менее 500 мг, освобождаются от регулирования. [77]
Массовая культура
Тетродотоксин служит сюжетным приемом для персонажей, чтобы подделать смерть, как в фильмах Hello Again (1987), The Serpent and the Rainbow (1988), The A-Team (2010), Captain America: The Winter Soldier (2014) и War (2019), а также в эпизодах « Jane the Virgin », Miami Vice (1985), [78] Nikita , MacGyver (сезон 7, эпизод 6, где противоядием является лист дурмана ), CSI: NY (сезон 4, эпизод 9, «Boo») и Chuck . В Law Abiding Citizen (2009) и Alex Cross (2012) его паралич представлен как метод содействия пыткам. Токсин также упоминался в «синтетической форме» в сезоне 1, эпизоде 2 сериала « FBI ». Токсин используется как оружие во втором сезоне «Арчера» , в «Тайных делах» и в эпизоде Inside No. 9 « Загадка Сфинкса ». [79] [80] В «Коломбо » , эпизоде 2 сезона 7, фугу используется для убийства жертвы антагониста. В ранобэ «Дневники аптекаря» , а также в соответствующих манга- [81] [82] и аниме- [83] [84] адаптациях токсин фугу встречается в нескольких таинственных арках.
Основываясь на предположении, что тетродотоксин не всегда смертелен, но в дозах, близких к смертельным, может сделать человека крайне нездоровым, при этом человек остается в сознании, [58] тетродотоксин, как утверждается, приводит к зомбизму и был предложен в качестве ингредиента в гаитянских препаратах вуду . [85] Эта идея впервые появилась в 1938 году в научно-популярной книге Tell My Horse Зоры Нил Херстон, в которой было несколько рассказов о предполагаемом отравлении тетродотоксином на Гаити колдуном вуду, называемым Бокор . [86] Эти истории позже были популяризированы этноботаником , получившим образование в Гарварде, Уэйдом Дэвисом [85] в его книге 1985 года и фильме Уэса Крейвена 1988 года, оба под названием «Змея и радуга» . Джеймс Эллрой включает «токсин рыбы-иглы» в качестве ингредиента в гаитянские препараты Вуду для создания зомбирования и отравления смертей в своем темном, тревожном, жестоком романе Blood's a Rover . Но эта теория была подвергнута сомнению научным сообществом с 1990-х годов на основе аналитических химических испытаний многочисленных препаратов и обзора более ранних отчетов (см. выше). [66] [67] [68]
Смотрите также
- Клэрвиус Нарцисс , гаитянин, предположительно похороненный заживо под воздействием ТТХ
- Тетродокаин , северокорейская медицинская инъекция, полученная из тетродотоксина
- 4-аминопиридин
- Бреветоксин
- Сигуатоксин
- Конотоксин
- Домоевая кислота
- Неосакситоксин
- Нейротоксин
- Окадаиковая кислота
- Сакситоксин
- Тектин
Ссылки
- ^ Более полный список видов бактерий, продуцирующих ТТХ, связанных с животными, у которых был выделен токсин или наблюдалась токсичность, а также подробное обсуждение исследовательской литературы относительно происхождения бактерий (и оставшихся противоположных точек зрения, например, у тритонов), а также подробное спекулятивное обсуждение относительно биосинтеза см. в [1]
- ^ abcdefghijklmnopqrstu vwxy Chau R, Kalaitzis JA, Neilan BA (июль 2011 г.). "О происхождении и биосинтезе тетродотоксина" (PDF) . Aquatic Toxicology . 104 ( 1– 2): 61– 72. Bibcode :2011AqTox.104...61C. doi :10.1016/j.aquatox.2011.04.001. PMID 21543051. Архивировано из оригинала (PDF) 2016-03-05 . Получено 2016-02-29 .
- ^ abcdefghijklmnopqr Lago J, Rodríguez LP, Blanco L, Vieites JM, Cabado AG (2015). «Тетродотоксин, чрезвычайно мощный морской нейротоксин: распространение, токсичность, происхождение и терапевтическое использование». Marine Drugs . 13 (10): 6384– 406. doi : 10.3390/md13106384 . PMC 4626696. PMID 26492253 .
- ^ Guardone L, Maneschi A, Meucci V, Gasperetti L, Nucera D, Armani A (2020-10-02). «Глобальное ретроспективное исследование случаев отравления людей тетродотоксином (TTX) после употребления морепродуктов». Food Reviews International . 36 (7): 645– 667. doi : 10.1080/87559129.2019.1669162. hdl : 11568/1013333 . ISSN 8755-9129. S2CID 204144112.
- ^ Huerta MÁ, de la Nava J, Artacho-Cordón A, Nieto FR (май 2023 г.). «Эффективность и безопасность тетродотоксина при лечении боли, связанной с раком: систематический обзор и метаанализ». Marine Drugs . 21 (5): 316. doi : 10.3390/md21050316 . ISSN 1660-3397. PMC 10221257 . PMID 37233510.
- ^ abcdefghijklmn Bane V, Lehane M, Dikshit M, O'Riordan A, Furey A (февраль 2014 г.). «Тетродотоксин: химия, токсичность, источник, распространение и обнаружение». Токсины . 6 (2): 693–755 . doi : 10.3390/toxins6020693 . PMC 3942760. PMID 24566728 .
- ^ Нарахаши Т, Мур Дж. В., Скотт В. Р. (май 1964 г.). «Блокирование тетродотоксином увеличения натриевой проводимости в гигантских аксонах лобстера». Журнал общей физиологии . 47 (5): 965–974 . doi :10.1085/jgp.47.5.965. PMC 2195365. PMID 14155438 .
- ^ Тетродотоксин Sigma-Aldrich (T8024) – Информационный лист продукта.
- ^ Hwang DF, Tai KP, Chueh CH, Lin LC, Jeng SS (1991). «Тетродотоксин и его производные у нескольких видов брюхоногих моллюсков Naticidae». Toxicon . 29 (8): 1019– 24. Bibcode : 1991Txcn...29.1019H. doi : 10.1016/0041-0101(91)90084-5. PMID 1949060.
- ^ Stokes AN, Ducey PK, Neuman-Lee L, Hanifin CT, French SS, Pfrender ME, Brodie ED, Brodie ED (2014). «Подтверждение и распределение тетродотоксина впервые у наземных беспозвоночных: два вида наземных плоских червей (Bipalium adventitium и Bipalium kewense)». PLOS ONE . 9 (6): e100718. Bibcode : 2014PLoSO...9j0718S. doi : 10.1371/journal.pone.0100718 . PMC 4070999. PMID 24963791 .
- ^ Pires, OR Jr., A. Sebben, EF Schwartz, RAV Morales, C. Bloch Jr., CA Schwartz (2005). «Дальнейший отчет о появлении тетродотоксина и новых аналогов в семействе бесхвостых амфибий Brachycephalidae». Toxicon . 45 (1): 73– 79. Bibcode : 2005Txcn...45...73P. doi : 10.1016/j.toxicon.2004.09.016. PMID 15581685.
- ^ Marion Z, Hay M (2011). «Химическая защита восточного тритона (Notophthalmus viridescens): вариации эффективности против разных потребителей и в разных средах обитания». PLOS ONE . 6 (12): e27581. Bibcode : 2011PLoSO...627581M. doi : 10.1371/journal.pone.0027581 . PMC 3229496. PMID 22164212 .
- ^ Scheuer PJ (1970). "Токсины из рыб и других морских организмов". Advances in Food Research . 18 : 141– 61. doi :10.1016/S0065-2628(08)60369-9. ISBN 9780120164189. PMID 4929140.
- ^ Mosher HS, Fuhrman FA, Buchwald HD, Fischer HG (май 1964). «Тарихатоксин – тетродотоксин: мощный нейротоксин». Science . 144 (3622): 1100– 10. Bibcode :1964Sci...144.1100M. doi :10.1126/science.144.3622.1100. PMID 14148429.
- ^ Sheumack DD, Howden ME, Spence I, Quinn RJ (январь 1978). «Макулотоксин: нейротоксин из ядовитых желез осьминога Hapalochlaena maculosa, идентифицированный как тетродотоксин». Science . 199 (4325): 188– 89. Bibcode :1978Sci...199..188S. doi :10.1126/science.619451. PMID 619451.
Макулотоксин, мощный нейротоксин, выделенный из задних слюнных желез синекольчатого осьминога. Hapalochlaena maculosa теперь идентифицирована как тетродотоксин. Это первый зарегистрированный случай, когда тетродотоксин был обнаружен в яде.
- ^ "Тетродотоксин". PubChem . Национальный центр биотехнологической информации (NCBI).
- ^ Stine KE, Brown TM (2015). Принципы токсикологии (3-е изд.). Boca Raton, FL: CRC Press. стр. 196, 390. ISBN 978-1466503434.
- ^ Gage PW, Dulhunty AF (2012) [1973]. «Эффекты токсина сине-кольчатого осьминога ( Hapalochlaena maculosa ) [Глава III]». В Martin D, Padilla G (ред.). Морская фармакогнозия: действие морских биотоксинов на клеточном уровне. Филадельфия, Пенсильвания [Нью-Йорк, Нью-Йорк]: Elsevier [Academic Press]. стр. 85–106 . ISBN 978-0323155601.
- ^ Spafford J, Spencer AN, Gallin WJ (27 марта 1998 г.). «Предполагаемая субъединица α-потенциал-зависимого натриевого канала (PpSCN1) из гидроидной медузы Polyorchis penicillatus: структурные сравнения и эволюционные соображения». Biochemical and Biophysical Research Communications . 244 (3): 772– 80. doi :10.1006/bbrc.1998.8332. PMID 9535741.
- ^ Броди Э.Д., Броди Э.Д.-младший (май 1990 г.). «Устойчивость к тетродотоксину у подвязочных змей: эволюционный ответ хищников на опасную добычу». Эволюция . 44 (3): 651– 659. doi :10.2307/2409442. JSTOR 2409442. PMID 28567972.
- ^ Hwang DF, Arakawa O, Saito T, Noguchi T, Simidu U, Tsukamoto K, Shida Y, Hashimoto K (1988). «Бактерии, продуцирующие тетродотоксин, из сине-кольчатого осьминога Octopus maculosus [так в оригинале]». Marine Biology . 100 (3): 327–32 . doi :10.1007/BF00391147. S2CID 84188968.
- ^ Ногучи Т., Хванг Д., Аракава О., Сугита Х., Дегучи Й., Шида Й., Хашимото К. (1987). «Vibrio alginolyticus, бактерия, продуцирующая тетродотоксин, в кишечнике рыбы Fugu vermicularis vermicularis». Морская биология . 94 (4): 625–30 . Bibcode : 1987MarBi..94..625N. doi : 10.1007/BF00431409. S2CID 84437298.
- ^ Туесен Э.В., Когуре К. (1989). «Бактериальное производство тетродотоксина у четырех видов щетинкочелюстных» (PDF) . Биологический бюллетень . 176 (2): 191– 94. doi :10.2307/1541587. JSTOR 1541587.
- ^ Кэрролл С., МакЭвой Э., Гибсон Р. (2003). «Производство тетродотоксиноподобных веществ немертинскими червями в сочетании с бактериями». Журнал экспериментальной морской биологии и экологии . 288 (1): 51– 63. Bibcode : 2003JEMBE.288...51C. doi : 10.1016/S0022-0981(02)00595-6.
- ^ Lehman EM, Brodie ED, Brodie ED (1 сентября 2004 г.). «Нет доказательств эндосимбиотического бактериального происхождения тетродотоксина у тритона Taricha granulosa». Toxicon . 44 (3): 243– 49. Bibcode :2004Txcn...44..243L. doi :10.1016/j.toxicon.2004.05.019. PMID 15302530.
- ^ Как отмечают Чау и др., цит. выше, «Несмотря на его долгую историю и доскональное знание его токсичности и фармакологии, ни путь к ТТХ, ни даже биогенное происхождение ТТХ не известны. Дискуссия о том, происходит ли ТТХ от бактерий или является эндогенным для животных-хозяев, продолжается, и единственное опубликованное исследование субстратов биосинтеза ТТХ оказалось неубедительным».
- ^ Moczydlowski EG (март 2013). «Молекулярная мистика тетродотоксина». Toxicon . 63 : 165– 83. Bibcode : 2013Txcn...63..165M. doi : 10.1016/j.toxicon.2012.11.026. PMID 23261990.
- ^ Shen H, Li Z, Jiang Y, Pan X, Wu J, Cristofori-Armstrong B, Smith JJ, Chin Y, Lei J, Zhou Q, King GF, Yan N (19 октября 2018 г.). "Структурная основа модуляции потенциалзависимых натриевых каналов токсинами животных". Science . 362 (6412). doi : 10.1126/science.aau2596 . PMID 30049784.
- ^ "Тетродотоксин | Страница лигандов | Руководство по фармакологии IUPHAR/BPS". Руководство по фармакологии . Международный союз фармакологов.
- ^ Нарахаси Т (2008). «Тетродотоксин: краткая история». Proc Jpn Acad Ser B Phys Biol Sci . 84 (5): 147– 54. doi :10.2183/pjab.84.147. PMC 2858367. PMID 18941294 .
- ^ abcd Kao CY (июнь 1966). «Тетродотоксин, сакситоксин и их значение в изучении явлений возбуждения». Pharmacological Reviews . 18 (2): 997–1049 . PMID 5328391.
- ^ Бланкеншип, Дж. Э. (1976). «Тетродотоксин: от яда к мощному инструменту». Перспективы в биологии и медицине . 19 (4, лето): 509–26 . doi :10.1353/pbm.1976.0071. PMID 785373. S2CID 6117457.
- ^ Чау Р., Калаитзис JA, Нейлан BA (июль 2011 г.). «О происхождении и биосинтезе тетродотоксина». Aquatic Toxicology (Амстердам, Нидерланды) . 104 ( 1–2 ): 61–72 . Bibcode : 2011AqTox.104...61C. doi : 10.1016/j.aquatox.2011.04.001. PMID 21543051.
- ^ Kudo Y, Hanifin CT, Kotaki Y, Yotsu-Yamashita M (25 сентября 2020 г.). «Структуры аналогов тетродотоксина N-гидрокси-типа и бициклических соединений гуанидиния, обнаруженных у токсичных тритонов». Журнал натуральных продуктов . 83 (9): 2706– 17. doi : 10.1021/acs.jnatprod.0c00623 . PMID 32896120.
- ^ Мельникова ДИ, Нийланд Р, Магарламов ТЮ (9 июня 2021 г.). «Первые данные о полном геноме бактерии, продуцирующей тетродотоксин». Токсины . 13 (6): 410. doi : 10.3390/toxins13060410 . PMC 8228330 . PMID 34207879.
- ^ Марута С., Ямаока К., Йоцу-Ямашита М. (март 2008 г.). «Два критических остатка в областях p-петли Na+-каналов рыбы-собаки на чувствительность к TTX». Toxicon . 51 (3): 381– 387. doi :10.1016/j.toxicon.2007.10.014. PMID 18067939.
- ^ abc van Thiel J, Khan MA, Wouters RM, Harris RJ, Casewell NR, Fry BG, Kini RM, Mackessy SP, Vonk FJ, Wüster W, Richardson MK (октябрь 2022 г.). «Конвергентная эволюция устойчивости к токсинам у животных». Biological Reviews of the Cambridge Philosophical Society . 97 (5): 1823– 1843. doi :10.1111/brv.12865. PMC 9543476. PMID 35580905 .
- ^ Woodward RB (1964). "Структура тетродотоксина" (PDF) . Pure Appl. Chem . 9 (1): 49– 75. doi :10.1351/pac196409010049. S2CID 98806870. Архивировано из оригинала (PDF) 2016-03-04 . Получено 2013-11-11 .
- ^ Furusaki A, Tomiie Y, Nitta I (1970). «Кристаллическая и молекулярная структура гидробромида тетродотоксина». Бюллетень химического общества Японии . 43 (11): 3332– 41. doi :10.1246/bcsj.43.3332.
- ^ Kishi Y, Aratani M, Fukuyama T, Nakatsubo F, Goto T (декабрь 1972 г.). «Синтетические исследования тетродотоксина и родственных соединений. 3. Стереоспецифический синтез эквивалента ацетилированного тетродамина». Журнал Американского химического общества . 94 (26): 9217– 19. Bibcode : 1972JAChS..94.9217K. doi : 10.1021/ja00781a038. PMID 4642370.
- ^ Kishi Y, Fukuyama T, Aratani M, Nakatsubo F, Goto T (декабрь 1972 г.). «Синтетические исследования тетродотоксина и родственных соединений. IV. Стереоспецифические полные синтезы DL -тетродотоксина». Журнал Американского химического общества . 94 (26): 9219– 21. doi :10.1021/ja00781a039. PMID 4642371.
- ^ Табер Д. (2005-05-02). "Синтез (-)-тетродотоксина". Портал органической химии . organic-chemistry.org.
- ^ Ohyabu N, Nishikawa T, Isobe M (июль 2003 г.). «Первый асимметричный полный синтез тетродотоксина». Журнал Американского химического общества . 125 (29): 8798– 805. Bibcode : 2003JAChS.125.8798O. doi : 10.1021/ja0342998. PMID 12862474.
- ^ Nishikawa T, Urabe D, Isobe M (сентябрь 2004 г.). «Эффективный полный синтез оптически активного тетродотоксина». Angewandte Chemie . 43 (36): 4782– 85. doi :10.1002/anie.200460293. PMID 15366086.
- ^ Хинман А., Дюбуа Дж. (сентябрь 2003 г.). «Стереоселективный синтез (–)-тетродотоксина». Журнал Американского химического общества . 125 (38): 11510– 11. doi :10.1021/ja0368305. ПМИД 13129349.
- ^ Чау Дж., Чиуфолини МА (2011). «Химический синтез тетродоксин: продолжающийся поиск». Marine Drugs . 9 (10): 2046–74 . doi : 10.3390/md9102046 . PMC 3210618. PMID 22073009 .
- ^ Sato K, Akai S, Yoshimura J (июль 2013 г.). «Стереоконтролируемый полный синтез тетродотоксина из мио-инозитола и D-глюкозы тремя путями: аспекты построения сложных многофункциональных циклитолов с разветвленными цепями». Natural Product Communications . 8 (7): 987– 98. doi : 10.1177/1934578X1300800726 . PMID 23980434. S2CID 23840469.
- ^ "Паспорт безопасности материала Тетродотоксин ACC# 01139". Acros Organics NV Архивировано из оригинала 2016-03-03 . Получено 2008-03-01 .
- ^ "Цианиды (как CN)". Концентрации, представляющие немедленную опасность для жизни или здоровья (IDLH) . Национальный институт охраны труда (NIOSH).
- ^ Gilman AG, Goodman LS, Gilman AZ (1980). Goodman & Gilman's The pharmacological Basis of Therapeutics . Нью-Йорк: McGraw-Hill. стр. 310. ISBN 0-07-146891-9.
- ^ Patockaa J, Stredab L (23 апреля 2002 г.). Price R (ред.). «Краткий обзор природных небелковых нейротоксинов». ASA Newsletter . 02– 2 (89). Applied Science and Analysis inc.: 16– 23. ISSN 1057-9419 . Получено 26 мая 2012 г.
- ^ abcdef Clark RF, Williams SR, Nordt SP, Manoguerra AS (1999). «Обзор отдельных отравлений морепродуктами». Undersea & Hyperbaric Medicine . 26 (3): 175–84 . PMID 10485519. Архивировано из оригинала 7 октября 2008 г.
- ^ Ранг Х., Риттер Дж., Флауэр Р., Хендерсон Г. (2015). Фармакология Ранга и Дейла (8-е изд.). Черчилль Ливингстон. ISBN 9780702053627.
- ^ abc "CDC – База данных по безопасности и охране здоровья при чрезвычайных ситуациях: Биотоксин: Тетродотоксин – NIOSH". www.cdc.gov . Получено 03.01.2016 .
- ^ "T8024 Sigma Tetrodotoxin". Каталог . Sigma-Aldrich . Получено 23 августа 2015 .
- ^ Kaempfer E, Scheuchzer Johannes Caspar, перевод (1727). История Японии… Historia imperii Japonici. Т. 1. Лондон, Англия: JC Scheuchzer (ред.). С. 134–135 .
{{cite book}}: CS1 maint: multiple names: authors list (link) - ^ Suehiro M (1994). "[Исторический обзор химических и медицинских исследований токсина рыбы-шара до Второй мировой войны]". Yakushigaku Zasshi . 29 (3): 428–34 . PMID 11613509.
- ^ Эрик Кродди, Джеймс Дж. Виртц, ред. (2005). Оружие массового поражения: химическое и биологическое оружие. ABC-CLIO. ISBN 9781851094905.
- ^ abcd Butterton J, Calderwell S (1998). «Острая инфекционная диарея и бактериальное пищевое отравление». В Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL, Hauser SL, Longo DL (ред.). Принципы внутренней медицины Харрисона (14-е изд.). Нью-Йорк: McGraw-Hill, Health Professions Division. стр. 796–601. ISBN 0070202915.
- ^ ab Benzer T. "Токсичность тетродотоксина". Medscape . Получено 23 августа 2015 г.
- ^ Rivera VR, Poli MA, Bignami GS (сентябрь 1995 г.). «Профилактика и лечение отравления мышей тетродотоксином с помощью моноклональных антител». Toxicon . 33 (9): 1231– 37. Bibcode :1995Txcn...33.1231R. doi :10.1016/0041-0101(95)00060-Y. PMID 8585093.

- ^ Брэдли СГ, Клика ЛДж (июль 1981 г.). «Смертельное отравление тритоном орегонской грубой кожи (Taricha granulosa)». JAMA . 246 (3): 247. doi :10.1001/jama.1981.03320030039026. PMID 7241765.

- ^ McNabb P, Mackenzie L, Selwood A, Rhodes L, Taylor D, Cornelison C (2009). "Обзор тетродотоксинов в морских слизняках Pleurobranchaea maculata и совпадение случаев гибели собак вдоль пляжей Окленда" (PDF) . Технический отчет регионального совета Окленда 2009/108 . Институт Коутрона для регионального совета Окленда. Архивировано из оригинала (PDF) 23-09-2015 . Получено 23-02-2010 .
- ^ Gibson E (15 августа 2009 г.). «Токсин рыбы фугу стал причиной смерти двух собак». The New Zealand Herald . Получено 19 ноября 2011 г.
- ^ ab 危険がいっぱい ふぐの素人料理 [Опасность в любительской кухне фугу] (на японском языке). Токийское бюро социального обеспечения и общественного здравоохранения. Архивировано из оригинала 28 января 2010 года.
- ^ 自然毒のリスクプロファイル:魚類:フグ毒 [Рыба: профиль риска естественного яда фугу] (на японском языке). 厚生労働省 (Министерство здравоохранения, труда и социального обеспечения (Япония)). Архивировано из оригинала 27 сентября 2011 года.
- ^ abc Ясумото Т, Као CY (1986). «Тетродотоксин и гаитянский зомби». Toxicon . 24 (8): 747– 49. Bibcode : 1986Txcn...24..747Y. doi : 10.1016/0041-0101(86)90098-x. PMID 3775790.
- ^ ab Kao CY, Yasumoto T (1990). "Тетродоксин в "зомби-порошке"". Toxicon . 28 (2): 129– 32. Bibcode :1990Txcn...28..129K. doi :10.1016/0041-0101(90)90330-a. PMID 2339427.
- ^ ab Hines T (май–июнь 2008 г.). «Зомби и тетродотоксин». Skeptical Inquirer . 32 (3): 60– 62. Архивировано из оригинала 2016-07-09 . Получено 2015-08-23 .
- ^ Варин Р.Х., Стивентон ГБ, Митчелл СК (2007). Молекулы смерти. Издательство Имперского колледжа. п. 390. ИСБН 978-1-86094-814-5.
- ^ Базелт РК (2008). Распределение токсичных лекарств и химикатов в организме человека (8-е изд.). Фостер-Сити, Калифорния: Биомедицинские публикации. С. 1521–22 . ISBN 978-0-9626523-7-0.
- ^ Hagen NA, Lapointe B, Ong-Lam M, Dubuc B, Walde D, Gagnon B, Love R, Goel R, Hawley P, Ngoc AH, du Souich P (июнь 2011 г.). «Многоцентровое открытое исследование безопасности и эффективности тетродотоксина при раковой боли». Current Oncology . 18 (3): e109–16. doi :10.3747/co.v18i3.732. PMC 3108870 . PMID 21655148.
- ^ Hagen NA, du Souich P, Lapointe B, Ong-Lam M, Dubuc B, Walde D, Love R, Ngoc AH (апрель 2008 г.). «Тетродотоксин при умеренной и сильной боли у больных раком: рандомизированное, двойное слепое, параллельное многоцентровое исследование». Журнал лечения боли и симптомов . 35 (4): 420–49 . doi : 10.1016/j.jpainsymman.2007.05.011 . PMID 18243639.
- ^ Ньето Ф.Р., Кобос Э.Дж., Техада Ма, Санчес-Фернандес С., Гонсалес-Кано Р., Сендан СМ (февраль 2012 г.). «Тетродотоксин (ТТХ) как терапевтическое средство от боли». Морские наркотики . 10 (2): 281–305 . doi : 10.3390/md10020281 . ПМК 3296997 . ПМИД 22412801.
- ^ Stimmel B (2002). "12: Героиновая зависимость". Алкоголизм, наркомания и путь к выздоровлению: жизнь на грани . Нью-Йорк: Haworth Medical Press. ISBN 0-7890-0553-0.
Тетродотоксин блокирует натриевые токи и, как полагают, обладает потенциалом как сильнодействующий анальгетик и как эффективное средство для детоксикации при героиновой зависимости без симптомов отмены и без вызывания физической зависимости.
- ^ Song H, Li J, Lu CL, Kang L, Xie L, Zhang YY, Zhou XB, Zhong S (август 2011 г.). «Тетродотоксин облегчает острый синдром отмены героина: многоцентровое, рандомизированное, двойное слепое, плацебо-контролируемое исследование». Clinical and Experimental Pharmacology & Physiology . 38 (8): 510– 14. doi :10.1111/j.1440-1681.2011.05539.x. PMID 21575032. S2CID 11221499.
- ^ "HHS и USDA Select Agents and Toxins 7 CFR Part 331, 9 CFR Part 121 и 42 CFR Part 73" (PDF) . Архивировано из оригинала (PDF) 17 января 2009 года . Получено 17 марта 2013 года .
- ^ "Допустимые количества токсинов". Федеральная программа избранных агентов . Центры США по контролю и профилактике заболеваний . Получено 20 февраля 2017 г.
- ↑ Полиция Майами (1984–1990) История о козле. IMDb
- ^ Miranda K (26 ноября 2014 г.). "Covert Affairs Recap: Starlings of the Slipstream". Movie News Guide . Архивировано из оригинала 6 августа 2018 г. Получено 25 июля 2015 г.
- ^ "Тайные операции: Скворцы Слипстрима (сезон 5, эпизод 12, первоначальная дата выхода в эфир 13 ноября 2014 г.)". USA Network . USA Networks. 2015 . Получено 25 июля 2015 г. .
- ^ "The Apothecary Diaries, Vol. 5, Chapter 25". Square Enix . Архивировано из оригинала 16 июня 2023 г. . Получено 13 июля 2022 г. .
- ^ "The Apothecary Diaries, Vol. 7, Chapter 33". Square Enix . Архивировано из оригинала 2 февраля 2023 г. Получено 19 ноября 2022 г.
- ↑ Silverman R (21 января 2024 г.). "The Apothecary Diaries Episode 15". Anime News Network . Архивировано из оригинала 21 января 2024 г. Получено 27 февраля 2024 г.
- ↑ Silverman R (25 февраля 2024 г.). "The Apothecary Diaries Episode 20". Anime News Network . Архивировано из оригинала 25 февраля 2024 г. Получено 27 февраля 2024 г.
- ^ ab Дэвис В. (1985).«Змея и радуга» (1-е издание Touchstone). Нью-Йорк: Simon and Schuster. ISBN 978-0671502478.
- ^ Hurston ZN (2009). Reed I, Louis H (ред.). Tell my horse: Voodoo and life in Haiti and Jamaica (1-е изд. Harper Perennial Modern Classics). Нью-Йорк: Harper Perennial. стр. 336. ISBN 978-0061695131.
Дальнейшее чтение
- Бэйн В., Лихейн М., Дикшит М., О'Риордан А., Фьюри А. (2014). «Тетродотоксин: химия, токсичность, источник, распространение и обнаружение». Токсины . 6 (2): 693–755 . doi : 10.3390/toxins6020693 . PMC 3942760. PMID 24566728 .
- Lago J, Rodríguez LP, Blanco L, Vieites JM, Cabado AG (2015). «Тетродотоксин, чрезвычайно мощный морской нейротоксин: распространение, токсичность, происхождение и терапевтическое использование». Marine Drugs . 13 (10): 6384– 406. doi : 10.3390/md13106384 . PMC 4626696. PMID 26492253 .
- Moczydlowski EG (2013). «Молекулярная мистика тетродотоксина». Toxicon . 63 : 165– 83. Bibcode : 2013Txcn...63..165M. doi : 10.1016/j.toxicon.2012.11.026. PMID 23261990.
- Lange WR (1990). «Отравление рыбой фугу». American Family Physician . 42 (4): 1029–33 . PMID 2220511.
- Нагасима Ю, Мацумото Т, Кадояма К, Ишизаки С, Танияма С, Такатани Т, Аракава О, Тераяма М (2012). «Отравление тетродотоксином, вызванное гладкоспинной иглобрюхой рыбой, Lagocephalus inermis и токсичностью L. inermis, пойманной у побережья Кюсю, Япония». Сёкухин Эйсейгаку Засси. Журнал Общества пищевой гигиены Японии . 53 (2): 85–90 . дои : 10.3358/шокуэйши.53.85 . ПМИД 22688023.
- Padera RF, Tse JY, Bellas E, Kohane DS (2006). «Тетродотоксин для пролонгированной местной анестезии с минимальной миотоксичностью». Muscle & Nerve . 34 (6): 747– 53. doi :10.1002/mus.20618. PMID 16897761. S2CID 22726109.
- Центры по контролю и профилактике заболеваний (CDC) (1996). «Отравление тетродотоксином, связанное с употреблением в пищу рыбы фугу, привезенной из Японии – Калифорния, 1996». Еженедельный отчет о заболеваемости и смертности . 45 (19): 389–91 . PMID 8609880.
- Cole JB, Heegaard WG, Deeds JR, McGrath SC, Handy SM (2015). «Вспышка отравления тетродотоксином из-за импортированной сушеной рыбы-собаки – Миннеаполис, Миннесота, 2014». Еженедельный отчет о заболеваемости и смертности . 63 (51): 1222–25 . PMID 25551594.
- Лю Ш, Ценг ЦЮ, Линь ЦК (2015). «Эффективен ли неостигмин при тяжелом отравлении тетродотоксином, связанным с рыбой-собакой?». Клиническая токсикология . 53 (1): 13– 21. doi :10.3109/15563650.2014.980581. PMID 25410493. S2CID 23055817.
- Rivera VR, Poli MA, Bignami GS (1995). «Профилактика и лечение отравления тетродотоксином у мышей моноклональными антителами». Toxicon . 33 (9): 1231– 37. Bibcode :1995Txcn...33.1231R. doi :10.1016/0041-0101(95)00060-y. PMID 8585093.
- Chang FC, Spriggs DL, Benton BJ, Keller SA, Capacio BR (1997). "4-аминопиридин устраняет кардиореспираторную депрессию, вызванную сакситоксином (STX) и тетродотоксином (TTX), у хронически инструментированных морских свинок". Fundamental and Applied Toxicology . 38 (1): 75– 88. doi :10.1006/faat.1997.2328. PMID 9268607. S2CID 17185707.
- Ахасан Х.А., Мамун А.А., Карим С.Р., Бакар М.А., Гази Э.А., Бала К.С. (2004). «Паралитические осложнения отравления рыбой фугу (тетродотоксином). Сингапурский медицинский журнал . 45 (2): 73–74 . PMID 14985845.
- How CK, Chern CH, Huang YC, Wang LM, Lee CH (2003). «Отравление тетродотоксином». Американский журнал неотложной медицины . 21 (1): 51– 54. doi :10.1053/ajem.2003.50008. PMID 12563582.
Внешние ссылки
- Тетродотоксин в рубриках медицинских предметов Национальной медицинской библиотеки США (MeSH)
- Тетродотоксин: основные данные (1999)
- Тетродотоксин из книги «Плохие микробы» на сайте Управления по контролю за продуктами и лекарствами США
- New York Times, «Все, что не убивает некоторых животных, может сделать их смертельно опасными»
- Национальная медицинская библиотека США: Банк данных опасных веществ – Тетродотоксин





