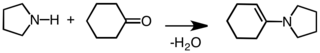Пирролидин
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Пирролидин [1] | |||
| Другие имена Азолидин Азациклопентан Тетрагидропиррол Проламин Азолан | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 102395 | |||
| ХЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.004.227 | ||
| Номер ЕС |
| ||
| 1704 | |||
CID PubChem |
| ||
| Номер RTECS |
| ||
| УНИИ | |||
| Номер ООН | 1922 | ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С 4 Н 9 Н | |||
| Молярная масса | 71,123 г·моль −1 | ||
| Появление | Прозрачная бесцветная жидкость | ||
| Плотность | 0,866 г/см 3 | ||
| Температура плавления | −63 °C (−81 °F; 210 K) | ||
| Точка кипения | 87 °C (189 °F; 360 К) | ||
| Смешивающийся | |||
| Кислотность ( pK a ) | 11,27 (p K a сопряженной кислоты в воде), [2] 19,56 (p K a сопряженной кислоты в ацетонитриле) [3] | ||
| -54,8·10 −6 см 3 /моль | |||
Показатель преломления ( nD ) | 1,4402 при 28°С | ||
| Опасности | |||
| Охрана труда и техника безопасности (OHS/OSH): | |||
Основные опасности | легковоспламеняющийся, вредный, едкий, возможный мутагенный | ||
| Маркировка СГС : | |||
   | |||
| Опасность | |||
| Н225 , Н302 , Н314 , Н332 | |||
| Р210 , Р233 , Р240 , Р241 , Р242 , Р243 , Р260 , Р261 , Р264 , Р270 , Р271 , Р280 , Р301+Р312 , Р301+Р330+Р331 , Р303+Р361+Р353 , Р304+Р312 , Р304+Р340 , Р305+Р351+Р338 , Р310 , Р312 , Р321 , Р330 , Р363 , Р370+Р378 , Р403+Р235 , Р405 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 3 °C (37 °F; 276 К) | ||
| 345 °C (653 °F; 618 К) | |||
| Паспорт безопасности (SDS) | ПБМ | ||
| Родственные соединения | |||
Родственные азотсодержащие гетероциклические соединения | Пиррол (ароматический с двумя двойными связями) Пирролин (одна двойная связь) Пирролизидин (два пентагональных кольца) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
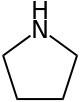
Пирролидин , также известный как тетрагидропиррол , является органическим соединением с молекулярной формулой (CH 2 ) 4 NH. Это циклический вторичный амин , также классифицируемый как насыщенный гетероцикл . Это бесцветная жидкость, которая смешивается с водой и большинством органических растворителей. Он имеет характерный запах, который был описан как «аммиачный, рыбный, моллюсковый». [4] Помимо самого пирролидина, известно много замещенных пирролидинов.
Производство и синтез
Промышленное производство
Пирролидин получают в промышленности реакцией 1,4-бутандиола и аммиака при температуре 165–200 °C и давлении 17–21 МПа в присутствии катализатора на основе оксида кобальта и никеля , нанесенного на оксид алюминия . [5]
Реакция осуществляется в жидкой фазе в непрерывном трубчатом или трубчатом реакторе, который работает по методу циркуляционного газа. Катализатор расположен в виде неподвижного слоя, а конверсия осуществляется в режиме нисходящего потока. Продукт получается после многоступенчатой очистки и разделения путем экстрактивной и азеотропной дистилляции . [5]
Лабораторный синтез
В лабораторных условиях пирролидин обычно синтезировали путем обработки 4-хлорбутан-1-амина сильным основанием:
Кроме того, 5-членное N -гетероциклическое кольцо производных пирролидина может быть синтезировано посредством каскадных реакций . [6]
Происшествие
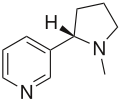
Многие модификации пирролидина обнаружены в природных и синтетических препаратах и кандидатах на роль лекарств. [6] Структура пирролидинового кольца присутствует во многих природных алкалоидах, в том числе никотине и гигрине . Она обнаружена во многих препаратах, таких как проциклидин и бепридил . Она также является основой для соединений рацетама ( например, пирацетама , анирацетама ). Аминокислоты пролин и гидроксипролин являются, в структурном смысле, производными пирролидина.
Реакции
Пирролидин является основанием. Его основность типична для других диалкиламинов. [7] По сравнению со многими вторичными аминами пирролидин отличается своей компактностью, которая является следствием его циклической структуры.
Пирролидин используется как строительный блок в синтезе более сложных органических соединений. Он используется для активации кетонов и альдегидов в направлении нуклеофильного присоединения путем образования енаминов (например, используется в алкилировании енаминов по Сторку ): [8]
Ссылки
- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013. Королевское химическое общество . стр. 142. doi :10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ Холл, ХК (1957). «Корреляция основных сил аминов». Журнал Американского химического общества . 79 (20): 5441–5444. doi :10.1021/ja01577a030.
- ^ Кальюранд, И.; Кютт, А.; Соовяли, Л.; Родима, Т.; Мяэметс, В.; Лейто, И.; Коппель, И.А. (2005). «Расширение самосогласованной спектрофотометрической шкалы основности в ацетонитриле до полного диапазона 28 единиц pKa: объединение различных шкал основности». Журнал органической химии . 70 (3): 1019–1028. doi :10.1021/jo048252w. PMID 15675863.
- ^ Пирролидин Архивировано 21.11.2017 в Wayback Machine , The Good Scents Company
- ^ ab Bou Chedid, Roland; Melder, Johann-Peter; Dostalek, Roman; Pastre, Jörg; Tan, Aik Meam. "Process for the preparation of pyrrolidine". Google Patents . BASF SE. Архивировано из оригинала 5 июля 2019 г. . Получено 5 июля 2019 г. .
- ^ ab Ловицки, Даниэль; Пржибыльский, Петр (2022). «Тандемное построение биологически значимых алифатических 5-членных N-гетероциклов». Европейский журнал медицинской химии . 235 : 114303. doi : 10.1016/j.ejmech.2022.114303. PMID 35344904. S2CID 247580048.
- ^ HK Hall Jr. (1957). «Корреляция основных сил аминов». J. Am. Chem. Soc . 79 (20): 5441. doi :10.1021/ja01577a030.
- ^ Р.Б. Вудворд , И.Дж. Пахтер и М.Л. Шейнбаум (1974). «2,2-(Триметилендитио)циклогексанон». Органические синтезы . 54 : 39
{{cite journal}}: CS1 maint: multiple names: authors list (link); Собрание томов , т. 6, стр. 1014.