Литий-серная батарея
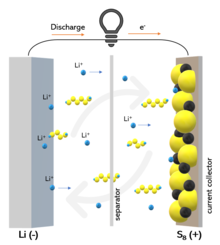 Принцип работы литий-серного аккумулятора и эффект «челнока» | |
| Удельная энергия | 450 Вт·ч/кг [1] |
|---|---|
| Плотность энергии | 550 Вт·ч/л [1] |
| Эффективность заряда/разряда | C/5 номинальный |
| Прочность цикла | Под вопросом |
| Номинальное напряжение ячейки | Напряжение элемента изменяется нелинейно в диапазоне 2,5–1,7 В во время разряда; аккумуляторы часто выпускаются на 3 В |
Литий -серная батарея (Li–S - батарея) — это тип перезаряжаемой батареи . Она отличается высокой удельной энергией . [2] Низкий атомный вес лития и умеренный атомный вес серы означают, что Li–S-батареи относительно легкие (плотностью примерно с воду). Они использовались в самом продолжительном и самом высоком полете беспилотного самолета на солнечных батареях (на тот момент) Zephyr 6 в августе 2008 года. [3]
Литий-серные батареи могут вытеснить литий-ионные элементы из-за их более высокой плотности энергии и сниженной стоимости. Это связано с двумя факторами. Во-первых, использование серы вместо менее плотных и более дорогих веществ, таких как соединения кобальта и/или железа, которые содержатся в литий-ионных батареях . [2] [4] Во-вторых, использование металлического лития вместо интеркалированных ионов лития позволяет добиться гораздо более высокой плотности энергии, поскольку для удержания «лития» требуется меньше веществ, а литий напрямую окисляется. [2] [4] [1] Литий-серные батареи предлагают удельную энергию порядка 550 Вт·ч / кг , [1] в то время как литий-ионные батареи находятся в диапазоне 150–260 Вт·ч/кг. [5]
В 2017 году были продемонстрированы Li–S-аккумуляторы с циклами заряда и разряда до 1500 [6], но испытания на циклическую долговечность в коммерческих масштабах и с обедненным электролитом не были завершены. По состоянию на начало 2021 года ни один из них не был коммерчески доступен.
Проблемы, которые замедлили принятие, включают эффект полисульфидного «челнока», который отвечает за прогрессирующую утечку активного материала из катода, что приводит к слишком малому количеству циклов перезарядки. [7] Кроме того, серные катоды имеют низкую проводимость, требуя дополнительной массы для проводящего агента, чтобы использовать вклад активной массы в емкость. [8] Объемное расширение серного катода во время преобразования S в Li 2 S и большое количество необходимого электролита также являются проблемами. Однако в начале 2000-х годов ученые начали добиваться прогресса в создании высокостабильных сульфидированных углеродных катодов [9] , и к 2020 году ученые из Университета Райса продемонстрировали батареи на основе сульфидированных углеродных катодов, которые сохраняли >70% своей емкости после 1000 циклов. [10] К 2023 году Zeta Energy, стартап из Техаса, объявил, что несколько национальных лабораторий независимо подтвердили, что его литий-серные батареи на основе сульфидированных углеродных катодов не содержат полисульфидного челнока. [11]
Конкурентные преимущества сернисто-углеродных катодов (например, сернистого полиакрилонитрила, также известного как SPAN) были подчеркнуты количественным анализом, проведенным исследователями из Университета Мэриленда, Колледж-Парка и Тихоокеанской северо-западной национальной лаборатории в 2024 году. [12] Их особенность полисульфидного челнока обеспечивает правильную работу в условиях обедненного электролита (< 3 г·(А·ч) −1 ), что, как было доказано, имеет чрезвычайно важное значение для достижения полного потенциала аккумуляторов Li-S. Исследователи предложили и проанализировали нетрадиционные перспективы дальнейшего улучшения как плотности энергии, так и срока службы, подчеркнув важность надлежащего электролита (т. е. стабильного, легкого и высокопроводящего Li + ). [12]
История
Аккумуляторы Li–S были изобретены в 1960-х годах, когда Герберт и Улам запатентовали первичную батарею, использующую литий или литиевые сплавы в качестве анодного материала, серу в качестве катодного материала и электролит, состоящий из алифатических насыщенных аминов . [13] [14] Несколько лет спустя технология была улучшена за счет введения органических растворителей, таких как ПК , ДМСО и ДМФ, что дало батарею 2,35–2,5 В. [15] К концу 1980-х годов была продемонстрирована перезаряжаемая батарея Li–S, использующая эфиры, в частности DOL , в качестве растворителя электролита. [16] [17]
В 2020 году компания Manthiram определила критические параметры, необходимые для достижения коммерческого признания. [18] [19] В частности, батареи Li–S должны достигать содержания серы >5 мг·см −2 , содержания углерода <5%, соотношения электролита к сере <5 мкл·мг −1 , соотношения электролита к емкости <5 мкл·(мА·ч) −1 и соотношения отрицательной и положительной емкости <5 в ячейках пакетного типа. [18]
В 2021 году исследователи объявили об использовании анодной добавки на основе сахара, которая предотвращала высвобождение полисульфидных цепей из катодов, загрязняющих анод. Прототип ячейки продемонстрировал 1000 циклов зарядки с емкостью 700 мАч/г. [20]
В 2022 году был представлен промежуточный слой, который, как утверждалось, уменьшает движение полисульфида (защищая анод) и облегчает перенос ионов лития для сокращения времени зарядки/разрядки. [21] Также в том же году исследователи использовали арамидные нановолокна (наноразмерные кевларовые волокна), сформированные в клеточные мембраноподобные сети. Это предотвратило образование дендритов. Он решал проблему перемещения полисульфида, используя ионную селективность, интегрируя крошечные каналы в сеть и добавляя электрический заряд. [22]
Также в 2022 году исследователи из Университета Дрекселя создали прототип литий-серной батареи, которая не деградировала более 4000 циклов зарядки. Анализ показал, что батарея содержала моноклинную гамма-фазу серы, которая считалась нестабильной при температуре ниже 95 градусов Цельсия, и только несколько исследований показали, что этот тип серы стабилен дольше 20–30 минут. [23]
В 2024 году исследователи из Калифорнийского университета в Сан-Диего объявили об открытии нового серно-йодного кристаллического материала, который может радикально увеличить электропроводность катода литий-серной батареи на 11 порядков, сделав его в 100 миллиардов раз более проводящим, чем кристаллы, сделанные только из серы. Более того, новый материал обладает свойствами самовосстановления, что позволяет восстанавливать повреждения, вызванные циклами перезарядки, путем нагревания нового материала. [24]
Химия
Химические процессы в ячейке Li–S включают растворение лития с поверхности анода (и включение в полисульфидные соли щелочных металлов ) во время разряда и обратное осаждение лития на аноде во время зарядки. [25]
Анод
На анодной поверхности происходит растворение металлического лития с образованием электронов и ионов лития во время разряда и электроосаждением во время заряда. Полуреакция выражается как: [26]
По аналогии с литиевыми батареями, реакция растворения/электроосаждения со временем вызывает проблемы нестабильного роста твердоэлектролитного интерфейса (SEI), создавая активные центры для зародышеобразования и дендритного роста лития. Дендритный рост является причиной внутреннего короткого замыкания в литиевых батареях и приводит к выходу из строя самой батареи. [27]
Катод
В батареях Li–S энергия хранится в серном катоде (S 8 ). Во время разряда ионы лития в электролите мигрируют к катоду, где сера восстанавливается до сульфида лития (Li 2 S) . Сера повторно окисляется до S 8 во время фазы перезарядки. Таким образом, полуреакция выражается как:
- (E° ≈ 2,15 В относительно Li/Li + )
На самом деле реакция восстановления серы до сульфида лития гораздо сложнее и включает образование полисульфидов лития (Li 2 S x , 2 ≤ x ≤ 8) при уменьшении длины цепи согласно: [28]
Общий:
И последний шаг:
Конечный продукт на самом деле представляет собой смесь Li 2 S 2 и Li 2 S, а не чистый Li 2 S, из-за медленной кинетики восстановления в Li 2 S. [29] Это контрастирует с обычными литий-ионными ячейками, где ионы лития интеркалированы в аноде и катодах. Каждый атом серы может содержать два иона лития. Обычно литий-ионные батареи содержат только 0,5–0,7 ионов лития на атом-хозяин. [30] Следовательно, Li–S обеспечивает гораздо более высокую плотность хранения лития. Полисульфиды восстанавливаются на поверхности катода последовательно, пока ячейка разряжается:
- С
8→ Ли
2С
8→ Ли
2С
6→ Ли
2С
4→ Ли
2С
3
По мере зарядки ячейки на катоде через пористый диффузионный сепаратор образуются полимеры серы:
- Ли
2С → Ли
2С
2→ Ли
2С
3→ Ли
2С
4→ Ли
2С
6→ Ли
2С
8→ С
8
Эти реакции аналогичны реакциям в натрий-серной батарее .
Главной проблемой аккумуляторов Li–S является низкая проводимость серы и ее значительное изменение объема при разрядке, а поиск подходящего катода является первым шагом для коммерциализации аккумуляторов Li–S. [31] Поэтому большинство исследователей используют углеродно-серный катод и литиевый анод. [ 32] Сера очень дешева, но практически не имеет электропроводности , 5 × 10−30 См ⋅см −1 при 25 °C. [33] Углеродное покрытие обеспечивает недостающую электропроводность. Углеродные нановолокна обеспечивают эффективный путь электронной проводимости и структурную целостность, но в ущерб более высокой стоимости. [34] В 2024 году исследователи объявили об открытии серно-йодного материала, который может значительно увеличить электропроводность катода литий-серного аккумулятора на 11 порядков, делая его в 100 миллиардов раз более проводящим, чем кристаллы, сделанные только из серы. [24]
Одна из проблем конструкции литий-сера заключается в том, что когда сера в катоде поглощает литий, происходит расширение объема композиций Li x S, а прогнозируемое расширение объема Li 2 S составляет почти 80% от объема исходной серы. [35] Это вызывает большие механические напряжения на катоде, что является основной причиной быстрой деградации. Этот процесс уменьшает контакт между углеродом и серой и предотвращает поток ионов лития к поверхности углерода. [36]
Механические свойства литиированных соединений серы в значительной степени зависят от содержания лития, и с увеличением содержания лития прочность литиированных соединений серы улучшается, хотя это увеличение не является линейным с литированием. [37]
Одним из основных недостатков большинства ячеек Li–S являются нежелательные реакции с электролитами. В то время как S и Li
2S относительно нерастворимы в большинстве электролитов, многие промежуточные полисульфиды не растворяются. Растворение Li
2С
нв электролиты вызывает необратимую потерю активной серы. [38] Использование высокореактивного лития в качестве отрицательного электрода вызывает диссоциацию большинства обычно используемых других типов электролитов. Использование защитного слоя на поверхности анода было изучено для повышения безопасности элемента, т. е. использование тефлонового покрытия показало улучшение стабильности электролита, [39] LIPON, Li 3 N также продемонстрировал многообещающие характеристики.
Полисульфидный «челнок»
Исторически, эффект «челнока» является основной причиной деградации в Li–S-батарее. [40] Полисульфид лития Li 2 S x (6≤x≤8) хорошо растворяется [41] в обычных электролитах, используемых для Li–S-батарей. Они образуются и вытекают из катода, а затем диффундируют к аноду, где восстанавливаются до полисульфидов с короткой цепью и диффундируют обратно к катоду, где снова образуются полисульфиды с длинной цепью. Этот процесс приводит к непрерывной утечке активного материала с катода, коррозии лития, низкой кулоновской эффективности и низкому сроку службы батареи. [42] Более того, эффект «челнока» отвечает за характерный саморазряд Li–S-батарей из-за медленного растворения полисульфида, которое происходит также в состоянии покоя. [40] Эффект «челнока» в Li–S-аккумуляторе можно количественно оценить с помощью фактора f c (0 < f c < 1), оцененного по расширению плато напряжения заряда. Фактор f c определяется выражением: [43]
где k s , q up , [S tot ] и I c — соответственно кинетическая константа, удельная емкость, вносящая вклад в анодное плато, общая концентрация серы и ток заряда.
В 2022 году [44] исследователи сообщили об использовании катода, изготовленного из углеродных нановолокон . Элементарная сера была осаждена на углеродную подложку (ср. физическое осаждение из паровой фазы ), что образовало редкий и обычно метастабильный моноклинный аллотроп γ-серы . Этот аллотроп обратимо реагирует с Li
2S без образования промежуточных полисульфидов Li
2С
х. Поэтому карбонатные электролиты, которые обычно реагируют с этими полисульфидами, можно использовать вместо довольно опасных электролитов на основе эфира (низкие температуры вспышки и кипения). [45]
Его начальная емкость составляла 800 Ач/кг (классические батареи LiCoO 2 /графит имеют емкость ячейки 100 Ач/кг). Он разлагался очень медленно, в среднем на 0,04% за каждый цикл, и сохранял 658 Ач/кг после 4000 циклов (82%). [44]
Электролит
Традиционно, Li–S батареи используют жидкий органический электролит, содержащийся в порах сепаратора PP. [40] Электролит играет ключевую роль в Li–S батареях, действуя как на эффект «челнока» путем растворения полисульфида, так и на стабилизацию SEI на поверхности анода. Было показано, что электролиты на основе органических карбонатов, обычно используемые в Li-ion батареях (то есть PC, EC , DEC и их смеси), несовместимы с химией Li–S батарей. [46] Длинноцепочечные полисульфиды подвергаются нуклеофильной атаке на электрофильные участки карбонатов, что приводит к необратимому образованию побочных продуктов, таких как этанол , метанол , этиленгликоль и тиокарбонаты . В Li–S батареях традиционно используются циклические эфиры (как DOL ) или короткоцепочечные эфиры (как DME ), а также семейство гликолевых эфиров, включая DEGDME и TEGDME . [47] Одним из распространенных электролитов является 1M LiTFSI в DOL:DME 1:1 по объему с 1% по весу LiNO 3 в качестве добавки для пассивации литиевой поверхности. [47]
Безопасность
Из-за высокой плотности потенциальной энергии и нелинейной реакции разряда и зарядки элемента иногда используются микроконтроллер и другие схемы безопасности вместе с регуляторами напряжения для управления работой элемента и предотвращения быстрого разряда . [48]
Продолжительность жизни
Литий-серные (Li-S) батареи имеют более короткий срок службы по сравнению с традиционными литий-ионными батареями . [49] Недавние достижения в области материалов и формул электролита показали потенциал для продления срока службы до более чем 1000 циклов. [10] Одним из основных факторов, ограничивающих срок службы Li-S батарей, является растворение полисульфидов в электролите , что приводит к эффекту челнока и потере емкости с течением времени. [50] Рабочая температура и скорость циклирования также играют важную роль в определении срока службы Li-S батарей. [51]
Исследовать
| Анод | Катод | Дата | Источник | Удельная емкость после цикла | Примечания |
|---|---|---|---|---|---|
| Литий металлический | Мезопористый углерод с покрытием из полиэтиленгликоля | 17 мая 2009 г. | Университет Ватерлоо [52] | 1110 мА⋅ч/г после 20 циклов при токе 168 мА⋅г −1 [52] | Минимальная деградация во время зарядного цикла. Для удержания полисульфидов в катоде поверхность была функционализирована для отталкивания (гидрофобных) полисульфидов. В тесте с использованием растворителя глима традиционный серный катод потерял 96% своей серы за 30 циклов , тогда как экспериментальный катод потерял только 25%. |
| Литий металлический | Покрытые серой, неупорядоченные углеродные полые нановолокна | 2011 | Стэнфордский университет [53] [54] | 730 мА⋅ч/г после 150 циклов (при 0,5 С) | Добавка электролита повысила эффективность Фарадея с 85% до более чем 99%. |
| Кремниевая нанопроволока/углерод | Покрытые серой, неупорядоченные углеродные нанотрубки, изготовленные из углеводов | 2013 | РСК [55] [56] | 1300 мА⋅ч/г после 400 циклов (при 1 С) | Микроволновая обработка материалов и лазерная печать электродов. |
| Кремний углерод | Сера | 2013 | Институт Фраунгофера по материаловедению и лучевым технологиям IWS [57] | ? после 1400 циклов | |
| Сополимеризованная сера | 2013 | Университет Аризоны [58] [59] | 823 мА⋅ч/г при 100 циклах | Использует «обратную вулканизацию » в основном на сере с небольшим количеством добавки 1,3-диизопропенилбензола (ДИБ) | |
| Пористый TiO 2-инкапсулированные наночастицы серы | 2013 | Стэнфордский университет [60] [61] | 721 мА⋅ч/г при 1000 циклах (0,5 С) | Оболочка защищает серно-литиевый промежуточный продукт от электролитного растворителя. Каждая катодная частица имеет диаметр 800 нанометров. Эффективность Фарадея 98,4%. | |
| Сера | Июнь 2013 г. | Национальная лаборатория Оук-Ридж | 1200 мА·ч/г при 300 циклах при 60 °C (0,1 C) 800 мА·ч/г при 300 циклах при 60 °C (1 C) [62] | Твердый литий-полисульфидофосфатный электролит. Половина напряжения типичных LIB. Оставшиеся проблемы включают низкую ионную проводимость электролита и хрупкость керамической структуры. [63] [64] | |
| Литий | Нанокомпозит оксида серы и графена со связующим на основе сополимера стирола, бутадиена и карбоксиметилцеллюлозы | 2013 | Национальная лаборатория Лоуренса в Беркли [65] | 700 мА·ч/г при 1500 циклах ( разряд 0,05 С) 400 мА·ч/г при 1500 циклах (0,5 С заряд/1 С разряд) | Напряжение между 1,7 и 2,5 вольтами в зависимости от состояния заряда. Литий бис(трифторметансульфонил)имид), растворенный в смеси н-метил-(н-бутил)пирролидиний бис(трифторметансульфонил)имида (PYR14TFSI), 1,3-диоксолана (DOL), диметоксиэтана (DME) с 1 моль лития бис-(трифторметилсульфонил)имида (LiTFSI) и нитрата лития ( LiNO 3). Сепаратор из полипропилена высокой пористости. Удельная энергия 500 Вт⋅ч/кг (исходная) и 250 Вт⋅ч/кг при 1500 циклах (C=1,0) |
| Литированный графит | Сера | Февраль 2014 г. | Тихоокеанская северо-западная национальная лаборатория | 400 циклов | Покрытие предотвращает разрушение анода полисульфидами. [66] |
| Литированный графен | Пассивирующий слой серы/литий-сульфида | 2014 | OXIS Энергия [67] [68] | 240 мА·ч/г (1000 циклов) 25 А·ч/элемент | Пассивирующий слой предотвращает потерю серы |
| Литированный твердый углерод | Сополимер серы (поли(S-co-DVB)) | 2019 | Национальный университет Чунгнам | 400 мАч/г на 500 циклов при 3С | SEI твердого углерода предотвращает отложение полисульфидов на аноде и обеспечивает высокую производительность. [69] |
| Литий-серные батареи | Углеродная нанотрубка/Сера | 2014 | Университет Цинхуа [70] | 15,1 мА·ч⋅см −2 при содержании серы 17,3 мг S⋅см − 2 | Был изготовлен отдельно стоящий бумажный электрод CNT–S с высокой поверхностной загрузкой серы, в котором короткие многостенные углеродные нанотрубки служили в качестве короткодействующей электропроводящей сети, а сверхдлинные углеродные нанотрубки действовали как длиннодействующая электропроводящая сеть и перекрестные связующие. |
| Покрытая стеклом сера со слегка восстановленным оксидом графена для структурной поддержки | 2015 | Калифорнийский университет, Риверсайд [71] | 700 мА⋅ч⋅г −1 (50 циклов) [72] | Стеклянное покрытие предотвращает постоянную миграцию полисульфидов лития на электрод | |
| Литий | Сера | 2016 | ЛЕЙТАТ | 500 Вт⋅ч/кг | Проект ALISE H2020 разрабатывает Li–S-аккумулятор для автомобилей с новыми компонентами и оптимизированными анодами, катодами, электролитом и сепаратором. |
| Литий металлический | Сульфированный графен | 2021 | КАТРИН, Университет Палацкого [1] | 644 мА⋅ч⋅г −1 (250 циклов) | Эффективный и простой подход к изготовлению ковалентно сульфурированного графенового катода для Li–S-аккумуляторов с высоким содержанием серы и высокой стабильностью при циклировании. [73] |
| Углеродные нанотрубки, содержащие серу | 2022 | Корейский научно-исследовательский институт электротехнологий [74] | 850 мА⋅ч⋅г −1 (100 циклов) | Использует разделительный слой из активированного угля, легированного фосфором, для минимизации эффекта полисульфидного челнока, создавая при этом складную батарею. | |
| Литий металлический | Литий тиофосфатный католит | 2023 | Дартмутский колледж , | 1271 мА⋅ч⋅г −1 (200 циклов) | Добавление пентасульфида фосфора к католиту Li–S приводит к образованию комплексов, которые связывают продукт разряда (Li 2 S) и обеспечивают высокую циклируемость и эффективность при низких температурах. |
Коммерциализация
По состоянию на 2021 год лишь немногие компании смогли коммерциализировать технологию в промышленных масштабах. Такие компании, как Sion Power, сотрудничают с Airbus Defence and Space для тестирования своей технологии литий-серных батарей. Airbus Defense and Space успешно запустила свой прототип самолета High Altitude Pseudo-Satellite (HAPS), работающего от солнечной энергии днем и от литий-серных батарей ночью в реальных условиях в течение 11-дневного полета. Батареи, используемые в испытательном полете, использовали элементы Li–S компании Sion Power, которые обеспечивают 350 Вт⋅ч/кг. [76] Первоначально Sion заявляла, что находится в процессе массового производства с доступностью к концу 2017 года; однако в последнее время можно увидеть, что они прекратили работу над своей литий-серной батареей в пользу литий-металлической батареи. [77] [78]
Британская фирма OXIS Energy разработала прототип литий-серных батарей. [79] [80] Совместно с Имперским колледжем Лондона и Университетом Крэнфилда они опубликовали модели эквивалентной цепи-сети для своих ячеек. [81] Совместно с Lithium Balance of Denmark они построили прототип системы аккумуляторов для скутеров, в первую очередь для китайского рынка, которая имела емкость 1,2 кВт·ч с использованием ячеек Long Life емкостью 10 А·ч и весила на 60% меньше свинцово-кислотных батарей со значительным увеличением диапазона. [82] Они также построили 3U, 3000 Вт·ч стоечную батарею, которая весила всего 25 кг и, как говорили, была полностью масштабируемой. [83] Они утверждали, что их литий-серные батареи будут стоить около 200 долларов США/кВт·ч при массовом производстве. [84] Однако в мае 2021 года фирма вступила в статус банкротства (несостоятельности). [85]
Sony , которая также выпустила на рынок первую литий-ионную батарею, планировала вывести на рынок литий-серные батареи в 2020 году, но не предоставила никаких обновлений с момента первоначального объявления в 2015 году. [86]
Факультет машиностроения и аэрокосмической техники Университета Монаша в Мельбурне, Австралия, разработал сверхмощную батарею Li–S, которая была изготовлена партнерами в Институте материалов и лучевых технологий Фраунгофера в Германии. Утверждается, что батарея может обеспечить питание смартфона в течение пяти дней. [87]
В 2022 году немецкая компания Theion заявила, что представит литий-серные батареи для мобильных устройств в 2023 году, а для транспортных средств — к 2024 году. [88]
В январе 2023 года компания Zeta Energy из Хьюстона, штат Техас, получила грант в размере 4 миллионов долларов от программы ARPA-E Министерства энергетики США на разработку литий-серных батарей на основе катода из сульфированного углерода и вертикально выровненного анода из углеродных нанотрубок. [89]
В июне 2023 года компания Lyten из Сан-Хосе, штат Калифорния, запустила пилотную производственную линию, производящую около 100 батарей в день. [90] В 2024 году Lyten объявила о планах строительства гигафабрики стоимостью в миллиард долларов в Рино, штат Невада, по производству до 10 гигаватт-часов литий-серных батарей в год. [91]
Смотрите также
Ссылки
- ^ abcd "OXIS ENERGY ГОТОВИТСЯ СДЕЛАТЬ ТЕХНОЛОГИЮ ТВЕРДОТЕЛЬНЫХ ЛИТИЙ-СЕРНЫХ ЭЛЕМЕНТОВ РЕАЛЬНОСТЬЮ" (pdf). 20 апреля 2021 г. Получено 7 июня 2021 г.
- ^ abc Zhang, Sheng S (2013). «Жидкоэлектролитная литий-серная батарея: фундаментальная химия, проблемы и решения». Journal of Power Sources . 231 : 153–162. doi : 10.1016/j.jpowsour.2012.12.102.
- ^ Амос, Дж. (24 августа 2008 г.) «Солнечный самолет совершает рекордный полет» BBC News
- ^ ab Manthiram, Arumugam; Fu, Yongzhu; Su, Yu-Sheng (2013). «Проблемы и перспективы литий-серных батарей» (PDF) . Acc. Chem. Res . 46 (5): 1125–1134. doi :10.1021/ar300179v. PMID 23095063. Архивировано из оригинала (PDF) 2020-01-03.
- ^ Автомобильные литий-ионные аккумуляторы: текущее состояние и будущие перспективы (отчет). Министерство энергетики США. 2019-01-01. стр. 26. Получено 15 марта 2021 г.
- ^ "Технология литий-серных аккумуляторов OXIS Energy". Архивировано из оригинала 28 июня 2017 г.В 2017 году: «можно циклировать около 1500 раз... В течение следующих 2 лет мы ожидаем, что это число достигнет 2500 циклов». В 2021 году: «В течение следующих двух лет мы намерены удвоить текущий циклический ресурс, чтобы достичь более 500 циклов».
- ^ Дяо, Янь; Се, Кай; Сюн, Шижао; Хун, Сяобинь (август 2013 г.). «Явление челнока – необратимый механизм окисления активного материала серы в аккумуляторе Li–S». Журнал источников питания . 235 : 181–186. doi :10.1016/j.jpowsour.2013.01.132.
- ^ Эфтехари, Али (2017). «Подъем литий-селеновых батарей». Sustainable Energy & Fuels . 1 : 14–29. doi :10.1039/C6SE00094K.
- ^ Ван, Дж.; Ян, Дж.; Се, Дж.; Сюй, Н. (2002). «Новый проводящий полимерно-серный композитный катодный материал для перезаряжаемых литиевых батарей». Advanced Materials . 14 (13–14): 963–965. doi :10.1002/1521-4095(20020705)14:13/14<963::AID-ADMA963>3.0.CO;2-P.
- ^ ab Salvatierra, Rodrigo V; James, Dustin K; Tour, James M (2022). Gupta, Ram K (ред.). Литий-серные батареи: материалы, проблемы и применение . Амстердам: Elsevier. стр. 241–270. ISBN 978-0-323-91934-0.
- ^ «Zeta Energy получает стороннее подтверждение того, что ее литий-серная батарея не содержит полисульфида». PR Newswire. 1 мая 2023 г. Получено 3 сентября 2023 г.
- ^ ab Phan, An L.; Le, Phung ML; Wang, Chunsheng (май 2024 г.). «Создание высокоэнергетических и долговечных батарей Li/SPAN». Joule . 8 (6): 1601–1618. doi :10.1016/j.joule.2024.04.003. ISSN 2542-4351.
- ↑ Патент США 3043896, Данута, Герберт и Юлиуш, Улам, «Электрические сухие элементы и аккумуляторные батареи», выдан 10 июля 1962 г., передан Electric Tech Corp.
- ^ Патент США 3532543, Ноул, Доминик А. и Мосс, Владимир, «Батарея, использующая литий-серные электроды с неводным электролитом», выдан 1970-10-06, передан Aerojet Rocketdyne Inc.
- ↑ Патент США 3413154, Mlarur, Rao & Bhaskara, Lakshmanar, «Органические электролитные элементы», выдан 26 ноября 1968 г., передан Duracell Inc USA
- ^ Пелед, Э.; Горенштейн, А.; Сегал, М.; Стернберг, Ю. (май 1989). «Перезаряжаемая литий-серная батарея (расширенный реферат)». Журнал источников питания . 26 (3–4): 269–271. Bibcode : 1989JPS....26..269P. doi : 10.1016/0378-7753(89)80133-8.
- ^ Пелед, Э. (1989). «Литий-серная батарея: оценка электролитов на основе диоксолана». Журнал электрохимического общества . 136 (6): 1621–1625. Bibcode : 1989JElS..136.1621P. doi : 10.1149/1.2096981.
- ^ ab Bhargav, Amruth; Jiarui, He (2020). «Литий-серные батареи: достижение критических показателей». Joule . 4 (2): 285–291. doi : 10.1016/j.joule.2020.01.001 .
- ^ Мантирам, Арумугам; Фу, Юнчжу; Чунг, Шэн-Хенг; Цзу, Чэньси; Су, Юй-Шэн (2014). «Перезаряжаемые литий-серные батареи». Химические обзоры . 114 (23): 11751–11787. дои : 10.1021/cr500062v. ПМИД 25026475.
- ^ Лаварс, Ник (2021-09-13). «Литий-серная батарея с добавлением сахара обещает увеличить емкость до 5 раз». Новый Атлас . Получено 20-09-2021 .
- ^ Лаварс, Ник (28.02.2022). «Пористый слой аккумулятора приближает зарядку электромобиля раз в неделю на шаг». Новый Атлас . Получено 01.03.2022 .
- ^ Лаварс, Ник (2022-01-17). "Кевларовые волокна укрепляют литий-серный аккумулятор с 5-кратной емкостью литий-ионного". Новый Атлас . Получено 2022-04-07 .
- ^ Пай, Рахул (2022-02-10). "Стабилизация гамма-серы при комнатной температуре для возможности использования карбонатного электролита в батареях Li-S". Химия коммуникаций . 5 (1): 17. doi : 10.1038/s42004-022-00626-2 . PMC 9814344. PMID 36697747. S2CID 246704531 .
- ^ ab "Healable Cathode Could Unlock Potential of Solid-state Lithium-Sulfur Batteries". US San Diego Today . 6 марта 2024 г. Получено 20 апреля 2024 г.
- ^ Tudron, FB, Akridge, JR, и Puglisi, VJ (2004) «Литий-серные аккумуляторные батареи: характеристики, состояние разработки и применимость для питания портативной электроники» (Тусон, Аризона: Sion Power)
- ^ Кумар, Рудра; Лю, Цзе; Хванг, Джанг-Ён (2018). «Последние тенденции исследований в области батарей Li–S». Journal of Materials Chemistry A . 6 (25): 11582–11605. doi :10.1039/C8TA01483C . Получено 04.07.2019 .
- ^ Ульд Эли, Тейеб; Камзабек, Дана; Чакраборти, Дхритиман (2018-05-29). «Литий-серные батареи: современное состояние и будущие направления». ACS Applied Energy Materials . 1 (5): 1783–1814. doi :10.1021/acsaem.7b00153.
- ^ Линь, Чжань; Лян, Чэнду (2015). «Литий-серные батареи: от жидких до твердых ячеек». Журнал химии материалов A . 3 (3): 18. doi :10.1039/C4TA04727C. OSTI 1185628 . Получено 04.07.2019 .
- ^ Song, Min-Kyu; Cairns, Elton J.; Zhang, Yuegang (2013). «Литий-серные батареи с высокой удельной энергией: старые проблемы и новые возможности». Nanoscale . 5 (6): 2186–204. Bibcode :2013Nanos...5.2186S. doi :10.1039/c2nr33044j. PMID 23397572 . Получено 04.07.2019 .
- ^ Буллис, Кевин (22 мая 2009 г.). «Возвращаясь к литий-серным батареям». Обзор технологий . Архивировано из оригинала 15 апреля 2012 г. Получено 12 августа 2016 г.
- ^ Эфтехари, А. (2017). «Катодные материалы для литий-серных батарей: практическая перспектива». Журнал химии материалов A. 5 ( 34): 17734–17776. doi :10.1039/C7TA00799J.
- ^ Чой, YJ; Ким, KW (2008). «Улучшение циклических свойств серного электрода для литий/серной батареи». Журнал сплавов и соединений . 449 (1–2): 313–316. doi :10.1016/j.jallcom.2006.02.098.
- ^ JA Dean, ред. (1985). Lange's Handbook of Chemistry (третье изд.). Нью-Йорк: McGraw-Hill. стр. 3–5. ISBN 978-0-07-016192-4.
- ^ Choi, YJ; Chung, YD; Baek, CY; Kim, KW; Ahn, JH (4 марта 2008 г.). «Влияние углеродного покрытия на электрохимические свойства серного катода для литий/серных ячеек». J. Power Sources . 184 (2): 548–552. Bibcode : 2008JPS...184..548C. doi : 10.1016/j.jpowsour.2008.02.053.
- ^ Ислам, Мд Махбубул; Остадхоссейн, Алиреза; Бородин, Олег; Йейтс, А. Тодд; Типтон, Уильям У.; Хенниг, Ричард Г.; Кумар, Нитин; Дуин, Адри CT van (2015-01-21). "Моделирование молекулярной динамики ReaxFF на катодных материалах из литиированной серы". Phys. Chem. Chem. Phys . 17 (5): 3383–3393. Bibcode :2015PCCP...17.3383I. doi :10.1039/c4cp04532g. PMID 25529209.
- ^ Брайан Додсон, «Новая литий-серная батарея удваивает плотность энергии литий-ионной», NewAtlas, 1 декабря 2013 г.
- ^ Ислам и др. (2015). «Моделирование молекулярной динамики ReaxFF на катодных материалах из литиированной серы». Phys. Chem. Chem. Phys . 17 (5): 3383–3393. Bibcode :2015PCCP...17.3383I. doi :10.1039/C4CP04532G. PMID 25529209.
- ^ Jeong, SS; Lim, Y.; Choi, YT; Kim, KW; Ahn, HJ; Cho, KK (2006). «Электрохимические свойства литий-серных ячеек с использованием полимерных электролитов PEO, приготовленных при трех различных условиях смешивания». J. Power Sources . 174 (2): 745–750. Bibcode : 2007JPS...174..745J. doi : 10.1016/j.jpowsour.2007.06.108.
- ^ Ислам, Мд Махбубул; Брянцев, Вячеслав С.; ван Дуин, Адри КТ (2014). "Моделирование реактивного силового поля ReaxFF о влиянии тефлона на разложение электролита во время разряда анода Li/SWCNT в литий-серных батареях" (PDF) . Журнал электрохимического общества . 161 (8): E3009–E3014. doi :10.1149/2.005408jes. S2CID 52235837. Архивировано из оригинала (PDF) 21.02.2019.
- ^ abc Мантирам, Арумугам; Фу, Юнчжу; Чунг, Шэн-Хенг; Цзу, Чэньси; Су, Юй-Шэн (10 декабря 2014 г.). «Перезаряжаемые литий-серные батареи». Химические обзоры . 114 (23): 11751–11787. дои : 10.1021/cr500062v. ISSN 0009-2665. ПМИД 25026475.
- ^ Чжан, Кинтао (2018). Химически полученный графен: функционализация, свойства и применение (иллюстрированное издание). Королевское химическое общество. стр. 224. ISBN 978-1-78801-080-1.Выдержка из страницы 224
- ^ Song, Min-Kyu; Cairns, Elton J.; Zhang, Yuegang (2013). «Литий-серные батареи с высокой удельной энергией: старые проблемы и новые возможности». Nanoscale . 5 (6): 2186–204. Bibcode : 2013Nanos...5.2186S. doi : 10.1039/c2nr33044j. ISSN 2040-3364. PMID 23397572.
- ^ Михайлик, Юрий В.; Акридж, Джеймс Р. (2004). «Исследование полисульфидного челнока в системе аккумуляторов Li/S». Журнал электрохимического общества . 151 (11): A1969. Bibcode : 2004JElS..151A1969M. doi : 10.1149/1.1806394 .
- ^ ab Pai, Rahul; Singh, Arvinder; Tang, Maureen H.; Kalra, Vibha (10 февраля 2022 г.). «Стабилизация гамма-серы при комнатной температуре для возможности использования карбонатного электролита в батареях Li-S». Communications Chemistry . 5 (1): 17. doi : 10.1038/s42004-022-00626-2 . ISSN 2399-3669. PMC 9814344. PMID 36697747. S2CID 246704531 .
- ^ Тао, Синьюн; Лю, Яюань; Лю, Вэй; Чжоу, Гуанминь; Чжао, Цзе; Линь, Динчан; Цзу, Чэньси; Шэн, Оувэй; Чжан, Вэнькуй; Ли, Хён Ук; Цуй, И (10 мая 2017 г.). «Твердотельные литий-серные батареи, работающие при 37 °C, с композитами наноструктурированного Li 7 La 3 Zr 2 O 12 /углеродной пены и полимера». Нано-буквы . 17 (5): 2967–2972. Бибкод : 2017NanoL..17.2967T. doi : 10.1021/acs.nanolett.7b00221. ISSN 1530-6984. PMID 28388080.
- ^ Йим, Тэын; Парк, Мин-Сик; Ю, Джи-Сан; Ким, Ки Джэ; Я, Гын Юнг; Ким, Джэ Хун; Чон, Гуджин; Джо, Ён Нам; Ву, Санг-Гиль (сентябрь 2013 г.). «Влияние химической активности полисульфида по отношению к электролиту на основе карбоната на электрохимические характеристики Li-S аккумуляторов». Электрохимика Акта . 107 : 454–460. doi :10.1016/j.electacta.2013.06.039.
- ^ ab Scheers, Johan; Fantini, Sébastien; Johansson, Patrik (июнь 2014 г.). «Обзор электролитов для литий-серных батарей». Journal of Power Sources . 255 : 204–218. Bibcode : 2014JPS...255..204S. doi : 10.1016/j.jpowsour.2014.01.023.
- ^ Akridge, JR (октябрь 2001 г.) «Безопасность литий-серных аккумуляторных батарей» Battery Power Products & Technology
- ^ Тренто, Чин (27 декабря 2023 г.). «Литий-серные батареи против литий-ионных батарей: сравнительный анализ». Stanford Advanced Materials . Получено 11 июля 2024 г.
- ^ Ю, Линхуэй; Онг, Сэмюэл ( 2021). «Важность растворения полисульфидов в литий-серных батареях и перспективы высокоэнергетического электролита/катода». Electrochimica Acta . 392. doi :10.1016/j.electacta.2021.139013. hdl : 10356/155660 .
- ^ Лю, Y; Ван, T (2023). «Проблемы и решения для низкотемпературных литий-серных батарей: обзор». Материалы . 16 (12): 4359. doi : 10.3390/ma16124359 . PMC 10302741. PMID 37374546 .
- ^ ab Xiulei Ji, Kyu Tae Lee и Linda F. Nazar. (17 мая 2009 г.) «Высокоупорядоченный наноструктурированный углеродно-серный катод для литий-серных аккумуляторов». Nature Materials
- ^ Гуанъюань, Чжэн; Юань Ян; Джуди Дж. Ча ; Сын Сэ Хонг; И Цуй (14 сентября 2011 г.). «Полые углеродные нановолоконные серные катоды для литиевых аккумуляторов высокой удельной емкости» (PDF) . Nano Letters . 11 (10): 4462–4467. Bibcode : 2011NanoL..11.4462Z. doi : 10.1021/nl2027684. PMID 21916442.
- ^ Келлер, Сара Джейн (4 октября 2011 г.). «Сера в полых нановолокнах преодолевает трудности проектирования литий-ионных аккумуляторов». Stanford News . Stanford University . Получено 18 февраля 2012 г.
- ^ Розенберг, Сара; Хинтеннах (1 апреля 2014 г.). «Лазерно-печатные литий-серные микроэлектроды для батарей Li/S». Российский журнал электрохимии . 50 (4): 327–335. doi :10.1134/S1023193514040065. S2CID 97154966.
- ^ Ванденберг, Аврелий; Хинтеннах (1 апреля 2014 г.). «Новый подход к проектированию литий-серных аккумуляторов». Российский журнал электрохимии . 50 (4): 317–326. doi :10.1134/S102319351306013X. S2CID 96826100.
- ^ "Исследователи увеличивают срок службы литий-серных батарей". Gizmag.com. 4 апреля 2013 г. Получено 04.12.2013 .
- ^ Chung, WJ; Griebel, JJ; Kim, ET; Yoon, H.; Simmonds, AG; Ji, HJ; Dirlam, PT; Glass, RS; Wie, JJ; Nguyen, NA; Guralnick, BW; Park, J.; Somogyi, Á. D.; Theato, P.; MacKay, ME; Sung, YE; Char, K.; Pyun, J. (2013). «Использование элементарной серы в качестве альтернативного сырья для полимерных материалов». Nature Chemistry . 5 (6): 518–524. Bibcode :2013NatCh...5..518C. doi :10.1038/nchem.1624. PMID 23695634.
- ^ Кэрил Ричардс (16.04.2013). «Радикальный подход к превращению серы в полимеры».
- ^ Национальная ускорительная лаборатория SLAC (6 сообщений) (2013-01-08). "Мировой рекорд производительности батареи достигнут с помощью яйцевидных наноструктур". CleanTechnica . Получено 2013-06-11 .
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Wei Seh, Z.; Li, W.; Cha, JJ; Zheng, G.; Yang, Y.; McDowell, MT; Hsu, PC; Cui, Y. (2013). "Наноархитектура желток–оболочка серы–TiO2 с внутренним пустотным пространством для литий-серных батарей с длительным циклом". Nature Communications . 4 : 1331. Bibcode : 2013NatCo...4.1331W. doi : 10.1038/ncomms2327 . PMID 23299881.
- ^ Lin, Z; Liu, Z; Fu, W; Dudney, NJ ; Liang, C (2013). «Lithium Polysulfidophosphates: A Family of Lithium-Conducting Sulfur-Rich Compounds for Lithium–Sulfur Batteries» (PDF) . Angewandte Chemie International Edition . 52 (29): 7460–7463. doi :10.1002/anie.201300680. PMID 23737078. S2CID 37368147. Архивировано из оригинала (PDF) 2016-09-10.
- ^ Lin, Z.; Liu, Z.; Fu, W.; Dudney, NJ ; Liang, C. (2013). «Lithium Polysulfidophosphates: A Family of Lithium-Conducting Sulfur-Rich Compounds for Lithium-Sulfur Batteries» (PDF) . Angewandte Chemie International Edition . 52 (29): 7460–7463. doi :10.1002/anie.201300680. PMID 23737078. S2CID 37368147. Архивировано из оригинала (PDF) 2016-09-10.
- ^ "Полностью литий-серная батарея хранит в четыре раза больше энергии, чем литий-ионная". NewAtlas.com. 7 июня 2013 г. Получено 13 июня 2013 г.
- ^ "Новая литий-серная батарея удваивает плотность энергии литий-ионной". NewAtlas.com. 2 декабря 2013 г. Получено 04.12.2013 .
- ^ Лаварс, Ник (20 февраля 2014 г.). «Гибридный анод увеличивает срок службы литий-серных аккумуляторов в четыре раза» . Получено 22 августа 2016 г.
- ^ "Запах серы". Economist . 3 января 2015 г. Получено 22 августа 2016 г.
- ^ "Компания OXIS Energy, производящая Li–S-аккумуляторы, сообщает о 300 Вт·ч/кг и 25 А·ч элементах, прогнозируя 33 А·ч к середине 2015 года, 500 Вт·ч/кг к концу 2018 года". Green Car Congress. 12 ноября 2014 г. Получено 22 августа 2016 г.
- ^ Нгуен, Д.-Т.; Хёфлинг, А.; Йи, М.; Нгуен, THG; Теато, П.; Ли, ЙДж; Сонг, С.-В. (2019). «Возможность создания высокоскоростной и безопасной литий-ионно-серной батареи за счет эффективного сочетания серно-сополимерного катода и твердого углеродного анода». ChemSusChem . 12 (2): 480–486. doi :10.1002/cssc.201802430. PMID 30479038. S2CID 53771189.
- ^ Юань, Чжэ; Пэн, Хун-Цзе; Хуан, Цзя-Ци; Лю, Синь-Янь; Ван, Дай-Вэй; Чэн, Синь-Бин; Чжан, Цян (2014-10-01). "Иерархические свободностоящие бумажные электроды из углеродных нанотрубок со сверхвысоким содержанием серы для литий-серных батарей" (PDF) . Advanced Functional Materials . 24 (39): 6105–6112. doi :10.1002/adfm.201401501. ISSN 1616-3028. S2CID 97124341. Архивировано из оригинала (PDF) 2020-01-03.
- ^ Нилон, Шон (2015-03-03). "Стеклянное покрытие для улучшения производительности батареи". R&D . Архивировано из оригинала 2015-03-07 . Получено 22 августа 2016 г.
- ^ Нилон, Шон (2 марта 2015 г.). «Стеклянное покрытие улучшает производительность батареи». phys.org . Получено 22 августа 2016 г. .
- ^ Тантис, Иосиф; Бакандритсос, Аристид; Заоралова, Дагмар; Медведь, Мирослав; Якубец, Петр; Гавлакова, Яна; Зборжил, Радек; Отепка, Михал (2021). «Ковалентно связанные листы графена с серными цепочками позволяют создавать превосходные катоды литий-серных батарей на уровне полной массы». Передовые функциональные материалы . 31 (30): 2101326. doi : 10.1002/adfm.202101326 . ISSN 1616-3028. S2CID 234870475.
- ^ Джо, Сон-Чан; Хонг, Чон-Вон; Чхве, Ик-Хён; Ким, Мин-Джу; Ким, Бён Гон; Ли, Ю-Джин; Чхве, Хе Ён; Ким, Духун; Ким, Тэ Ён; Бэг, Кан-Джун; Пак, Джун-У (май 2022 г.). «Мультимодальное улавливание полисульфидов углеродными композитами, легированными фосфором, для гибких литий-серных батарей высокой плотности». Small . 18 (21): 2200326. doi :10.1002/smll.202200326. ISSN 1613-6810. PMID 35285157. S2CID 247437352.
- ^ Ван, Пейю; Катерис, Николаос; Ли, Байхэн; Чжан, Ивэнь; Ло, Цзяньминь; Ван, Чуанлун; Чжан, Юэ; Джаяраман, Амитеш С.; Ху, Сяофэй; Ван, Хай; Ли, Вэйян (17 августа 2023 г.). «Высокопроизводительные литий-серные батареи посредством молекулярного комплексообразования». Журнал Американского химического общества . 145 (34): 18865–18876. doi : 10.1021/jacs.3c05209. ISSN 0002-7863. ПМИД 37589666.
- ^ Копера, Дж. (сентябрь 2014 г.) «Литий-серные батареи компании Sion Power обеспечивают электроэнергией псевдоспутниковый полет на большой высоте» Пресс-релиз компании Sion Power
- ^ "Sion Power обеспечивает производительность аккумуляторов нового поколения с помощью запатентованной технологии Licerion®". 2016-10-03 . Получено 4 октября 2016 г.
- ^ "Sion Power объявляет о запуске своей новаторской перезаряжаемой литиевой батареи Licerion, Sion Power". sionpower.com .
- ^ "Anesco и OXIS выпустят литий-серные аккумуляторные батареи к 2016 году" (пресс-релиз). OXIS Energy. 14 июля 2015 г. Получено 22 августа 2016 г.
- ^ "Аккумулятор OXIS питает беспилотный автомобиль для программы правительства Великобритании Smart City Gateway" (пресс-релиз). OXIS Energy. 22 февраля 2015 г. Архивировано из оригинала 29-04-2016 . Получено 22 августа 2016 г.
- ^ Пропп, К.; Маринеску, М.; Оже, DJ; и др. (12 августа 2016 г.). «Многотемпературная модель эквивалентной цепи разряда, зависящая от состояния, для литий-серных батарей». J. Power Sources . 328 : 289–299. Bibcode : 2016JPS...328..289P. doi : 10.1016/j.jpowsour.2016.07.090 . hdl : 10044/1/39221 .
- ^ "Литий-серные батареи впервые будут коммерциализированы к 2018 году в электровелосипедах, где плотность энергии будет улучшена для последующего использования в электромобилях". nextbigfuture.com . 2016-06-10 . Получено 2017-02-02 .
- ^ "OXIS Rack-Mounted Battery" (PDF) . OXIS Energy. Архивировано из оригинала (PDF) 26 августа 2018 г. . Получено 20 мая 2017 г. .
- ^ "Презентация технологии литий-серных аккумуляторов OXIS Energy". OXIS Energy. 2016-11-03 . Получено 20 мая 2017 г.
- ^ Скотт, Алекс (2021-06-26). "Oxis Energy подает заявление о банкротстве". Новости химии и машиностроения . Получено 2022-08-15 .
- ^ "Аккумулятор Sony продлит срок службы телефона на 40%". Nikkei Asian Review . 17 декабря 2015 г. Получено 22 августа 2016 г.
- ^ ««Самая эффективная в мире литий-серная батарея» готовится к запуску». The Engineer . 6 января 2020 г. . Получено 9 января 2020 г. .
- ^ Моррис, Джеймс. «Технология серных батарей может увеличить дальность полета электромобилей в три раза к 2024 году». Forbes . Получено 28 августа 2022 г.
- ^ «Zeta Energy: Обеспечение быстрой зарядки аккумуляторов с литий-металлической 3D-архитектурой и сульфированными углеродными катодами». Министерство энергетики США. 13 января 2023 г. Получено 28 сентября 2023 г.
- ^ Авалос, Джордж (14.06.2023). «Lyten запускает в Сан-Хосе опытное производство передовых аккумуляторов – Компания надеется, что литий-серные аккумуляторы могут произвести революцию в секторе». San Jose Mercury News .
- ^ "Американский стартап Lyten инвестирует более $1 млрд в завод литий-серных аккумуляторов в Неваде". Reuters. 15 октября 2024 г. Получено 16 октября 2024 г.
Внешние ссылки
- "PolyPlus Lithium Sulfur". Polyplus.com. Архивировано из оригинала 20.04.2013 . Получено 06.04.2013 .
- "Sion Power". Sion Power . Получено 2013-04-06 .
- "Winston Battery Limited". En.winston-battery.com. Архивировано из оригинала 2014-03-25 . Получено 2013-04-06 .
- "EEMB Battery". EEMB Battery. Получено 2018-04-13.







![{\displaystyle fc={\frac {k_{\text{s}}q_{\text{up}}[S_{\text{tot}}]}{I_{c}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/92767aff703c9811fcd59e4023389b4a8bdf304f)
