Диоксолан
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 1,3-Диоксолан [3] | |||
| Систематическое название ИЮПАК 1,3-Диоксациклопентан | |||
| Другие имена Диоксолан 5-Краун-2 Формальный гликоль [2] | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| ЧЭБИ | |||
| ChEMBL |
| ||
| ChemSpider | |||
| Информационная карта ECHA | 100.010.422 | ||
| Номер ЕС |
| ||
CID PubChem |
| ||
| УНИИ | |||
| Номер ООН | 1166 | ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С3Н6О2 | |||
| Молярная масса | 74,08 г/моль | ||
| Плотность | 1,06 г/см 3 | ||
| Температура плавления | −95 °C (−139 °F; 178 K) | ||
| Точка кипения | 75 °C (167 °F; 348 К) | ||
| Опасности | |||
| Маркировка СГС : [4] | |||
 | |||
| Опасность | |||
| H225 | |||
| Р210 , Р233 , Р240 , Р241 , Р242 , Р243 , Р280 , Р303+Р361+Р353 , Р370+Р378 , Р403+Р235 , Р501 | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Диоксолан представляет собой гетероциклический ацеталь с химической формулой (CH 2 ) 2 O 2 CH 2 . Он связан с тетрагидрофураном (ТГФ) заменой метиленовой группы (CH 2 ) в положении 2 на атом кислорода. Соответствующие насыщенные 6-членные кольца C 4 O 2 называются диоксанами . Изомерный 1,2-диоксолан (в котором два кислородных центра расположены рядом) является пероксидом . 1,3-диоксолан используется в качестве растворителя и сомономера в полиацеталях .
Как класс соединений
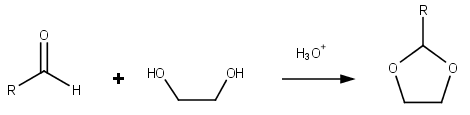
Диоксоланы — это группа органических соединений , содержащих диоксолановое кольцо. Диоксоланы могут быть получены ацетализацией альдегидов и кетализацией кетонов с этиленгликолем . [5]
(+)- цис -Диоксолан — это тривиальное название для L -(+)- цис -2-метил-4-триметиламмонийметил-1,3-диоксолана иодида, который является агонистом мускариновых ацетилхолиновых рецепторов .
Защита групп
Органические соединения, содержащие карбонильные группы, иногда нуждаются в защите , чтобы они не подвергались реакциям во время превращений других функциональных групп , которые могут присутствовать. Известны различные подходы к защите и снятию защиты карбонилов [6], включая диоксоланы [7] . Например, рассмотрим соединение метилциклогексанон-4-карбоксилат, где восстановление литийалюминийгидридом даст 4-гидроксиметилциклогексанол. Функциональная группа эфира может быть восстановлена без воздействия на кетон путем защиты кетона как кеталя . Кеталь получается в результате реакции с этиленгликолем , катализируемой кислотой , реакции восстановления, и защитной группы, удаленной гидролизом, с получением 4-гидроксиметилциклогексанона.

NaBArF 4 также можно использовать для снятия защиты с ацетальных или кеталь-защищенных карбонильных соединений. [6] [7] Например, снятие защиты с 2-фенил-1,3-диоксолана до бензальдегида можно осуществить в воде за пять минут при 30 °C. [8]
Натуральные продукты
Неоспорол — это натуральный продукт , включающий 1,3-диоксолановую группу , и является изомером спорола, имеющего 1,3-диоксановое кольцо. [9] Сообщалось о полном синтезе обоих соединений, и каждый из них включает этап, на котором диоксолановая система образуется с использованием трифторперуксусной кислоты (TFPAA), полученной методом перекиси водорода — мочевины . [10] [11] Этот метод не требует использования воды, поэтому он дает полностью безводную перкислоту, [12] необходимую в этом случае, поскольку присутствие воды приведет к нежелательным побочным реакциям . [10]
- CF
3COOCOCF
3 + Н
2О
2•CO(NH
2)
2 → CF
3СООН + CF
3СООН + СО(NH
2)
2
В случае неоспорола реакция Прилежаева [13] с трифторперуксусной кислотой используется для преобразования подходящего предшественника аллилового спирта в эпоксид , который затем подвергается реакции расширения кольца с ближайшей карбонильной функциональной группой с образованием диоксоланового кольца. [10] [11]

Аналогичный подход используется в общем синтезе спорола, при этом диоксолановое кольцо впоследствии расширяется до диоксановой системы. [9]
Смотрите также
Ссылки
- ^ 1,3-Диоксолан в Sigma-Aldrich
- ^ формальный гликоль - PubChem Public Chemical Database
- ^ "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 145. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ "1,3-Диоксолан". pubchem.ncbi.nlm.nih.gov .
- ^ RA Daignault, EL Eliel (1973). "2-Циклогексилоксиэтанол (включает ацетализацию циклогексанона)". Органические синтезы; Собрание томов , т. 5, стр. 303.
- ^ ab Greene, Theodora W.; Wuts, Peter GM (1999). "Диметилацетали". Greene's Protective Groups in Organic Synthesis (3-е изд.). Wiley-Interscience . стр. 297–304 , 724–727 . ISBN 9780471160199. Архивировано из оригинала 3 декабря 2016 г. . Получено 20 июня 2017 г. .
- ^ ab Greene, Theodora W.; Wuts, Peter GM (1999). "1,3-Диоксаны, 1,3-Диоксоланы". Защитные группы Грина в органическом синтезе (3-е изд.). Wiley-Interscience . стр. 308–322 , 724–727 . ISBN 9780471160199. Архивировано из оригинала 7 декабря 2016 г. . Получено 20 июня 2017 г. .
- ^ Чанг, Чи-Чин; Ляо, Бэй-Сих; Лю, Шиу-Цунг (2007). «Снятие защиты с ацеталей и кеталей в коллоидной суспензии, полученной с помощью тетракис(3,5-трифторметилфенил)бората натрия в воде». Synlett . 2007 (2): 283– 287. doi :10.1055/s-2007-968009.
- ^ ab Pirrung, Michael C.; Morehead, Andrew T.; Young, Bruce G., ред. (2000). "10. Neosporol, Sporol". Часть B: Бициклические и трициклические сесквитерпены . Полный синтез натуральных продуктов. Том 11. John Wiley & Sons . стр. 222–224 . ISBN 9780470129630.
- ^ abc Циглер, Фредрик Э.; Меткалф, Честер А.; Нангиа, Эшвини; Шульте, Гейл (1993). «Структура и общий синтез спорола и неоспорола». J. Am. Chem. Soc. 115 (7): 2581– 2589. doi :10.1021/ja00060a006.
- ^ ab Кастер, Кеннет С.; Рао, А. Сомасекар; Мохан, Х. Рама; МакГрат, Николас А.; Брихачек, Мэтью (2012). "Трифторперуксусная кислота". Энциклопедия реагентов для органического синтеза e-EROS . doi :10.1002/047084289X.rt254.pub2. ISBN 978-0471936237.
- ^ Купер, Марк С.; Хини, Гарри ; Ньюболд, Аманда Дж.; Сандерсон, Уильям Р. (1990). «Окислительные реакции с использованием мочевины–перекиси водорода; безопасная альтернатива безводной перекиси водорода». Synlett . 1990 (9): 533– 535. doi :10.1055/s-1990-21156.
- ^ Хаген, Тимоти Дж. (2007). «Реакция Прилежаева». В Ли, Джи Джек; Кори, Э. Дж. (ред.). Реакции именования преобразований функциональных групп . John Wiley & Sons . стр. 274–281 . ISBN 9780470176504.
Внешние ссылки
- экологические и токсикологические данные





![{\displaystyle {\ce {->[{\ce {NaBAr4}}][{\text{30 °C / 5 мин}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3fb42849d6133fe653a7fe5dd019b12e0f6184b5)