2,5-Диметокси-4-йодоамфетамин
 | |
 | |
| Имена | |
|---|---|
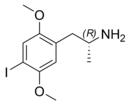
| Предпочтительное название ИЮПАК 1-(4-Иод-2,5-диметоксифенил)пропан-2-амин | |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| ChEMBL | |
| ChemSpider | |
| |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С 11 Н 16 ИНО 2 | |
| Молярная масса | 321,1558 г/моль |
| Температура плавления | 201,5 °C (394,7 °F; 474,6 K) ( гидрохлорид ) |
| 10 мг/мл [1] | |
| Фармакология | |
| Правовой статус |
|
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
2,5-Диметокси-4-йодоамфетамин ( DOI ) — психоделический препарат семейства амфетаминов и 4-замещенных-2,5-диметоксиамфетаминов (DOx). [3] [4]
DOI действует как мощный агонист серотониновых 5-HT 2 рецепторов . [3] [4] DOI имеет стереоцентр , а R -(−)-DOI является более активным стереоизомером . В нейробиологических исследованиях [ 125 I] - R -(−)-DOI используется как радиолиганд и индикатор наличия серотониновых 5-HT 2A рецепторов . [3]
Эффекты DOI сравнивали с LSD , хотя есть различия, которые могут заметить опытные пользователи. Помимо большей продолжительности, трип, как правило, более энергичный, чем трип с LSD, с большей нагрузкой на тело и другим субъективным визуальным опытом. Последствия включают остаточную стимуляцию и трудности со сном, которые, в зависимости от дозы, могут сохраняться в течение нескольких дней. [5] Хотя это случается редко, его иногда продают как заменитель LSD или даже ложно как LSD, что может быть опасно, поскольку DOI не имеет такого же установленного профиля безопасности, как LSD. [6]
DOI был впервые синтезирован в 1973 году Куттсом и Малики. [3]
Фармакология
Фармакодинамика
Действия
DOI является агонистом рецепторов серотонина 5-HT 2A , 5-HT 2B и 5-HT 2C . [4] Говорят, что он приблизительно в 5-12 раз селективнее для рецептора серотонина 5-HT 2A по сравнению с рецептором серотонина 5-HT 2C . [7]
Препарат не является моноаминовым высвобождающим агентом серотонина или дофамина . [8]
DOI является агонистом рецептора 1, ассоциированного со следовыми аминами крысы (TAAR1). [9]
| Рецептор | K i (рацемический DOI) [10] [ проверка не удалась ] | K i ( R -DOI) [10] [ проверка не пройдена ] | K i ( S -DOI) [10] [ проверка не пройдена ] | Внутренняя активность [4] |
|---|---|---|---|---|
| 5-НТ 1А | 2355 нМ | 3843 нМ | НД | НД |
| 5-HT 1B | 1261 нМ | НД | НД | НД |
| 5-HT 1D | 1241,3 нМ | НД | НД | НД |
| 5-HT 1E | 2970 нМ | НД | НД | НД |
| 5-HT 1F | 2125,44 нМ | НД | НД | НД |
| 5-НТ 2А | 0,68 нМ | 0,65 нМ | 0,65 нМ | Частичный агонист. |
| 5-НТ 2Б | 20,03 нМ | 53,70318 нМ | 28,183829 нМ | Частичный агонист/полный агонист |
| 5-НТ 2С | 2,38 нМ | 5,370318 нМ | 8,317638 нМ | Полный агонист при соединении с фосфолипазой А. Частичный агонист (внутренняя эффективность = 53%) при соединении с фосфолипазой С. |
| 5-НТ 5А | 1000 нМ | НД | НД | НД |
| 5- HT6 | >10000 нМ | НД | НД | НД |
Эффекты
Было обнаружено, что ( R )-DOI и несколько других серотонинергических психоделиков , включая TCB-2 , LSD и LA-SS-Az , демонстрируют мощное ингибирование воспаления , вызванного фактором некроза опухоли альфа (TNFα) . [11] [12] [13] ( R )-DOI был самым активным из оцениваемых препаратов и показал чрезвычайно высокую активность, которая находилась в пикомолярном диапазоне и была на порядок сильнее, чем его действие в качестве галлюциногена . TNFα может играть посредническую роль в патофизиологии дегенеративных воспалительных состояний, таких как ревматоидный артрит и болезнь Альцгеймера . Также было обнаружено, что ( R )-DOI блокирует воспаление легких, гиперпродукцию слизи, гиперреактивность дыхательных путей и отключает ключевые гены в иммунном ответе легких, эффекты, которые блокируют развитие аллергической астмы в моделях животных . [14] Эти результаты могут сделать DOI и другие агонисты серотониновых 5-HT 2A новыми методами лечения воспалительных состояний. [15]
Было показано, что DOI вызывает быстрый рост и реорганизацию дендритных шипиков и синаптических связей с другими нейронами , процессы, которые, как известно, лежат в основе нейропластичности , и, следовательно, являются психопластогеном . [16]
Химия
DOI, также известный как 2,5-диметокси-4-иодоамфетамин или как 2,5-диметокси-4-иодо-α-метилфенэтиламин, является замещенным производным фенэтиламина и амфетамина и членом семейства наркотиков DOx . Он структурно связан с встречающимся в природе психоделическим препаратом мескалином фенэтиламином (3,4,5-триметоксифенэтиламин). Другие тесно связанные наркотики DOx включают DOM , DOB , DOC и DOF , среди многих других.
История
DOI был впервые синтезирован Александром Шульгиным . [5] Форма DOI на основе радиоактивного йода-125 для ПЭТ-визуализации была впервые разработана в лаборатории Дэвида Э. Николса .
В январе 2007 года британская полиция сообщила, что трое молодых людей заболели, как сообщается, после того, как приняли DOI на рейве в Бигглсуэйде , недалеко от Милтон-Кинса , и предупредила других, кто принял его, обратиться за медицинской помощью. Это, по-видимому, первый признак того, что DOI нашел более широкое применение в качестве рекреационного наркотика в Великобритании. [17]
Южноавстралиец Коди Эдвардс, который жестоко убил Синамина Белла, спорно признал себя виновным в меньшем наказании за непредумышленное убийство , заявив, что препарат DOI вызвал у него паранойю , и что впоследствии он действовал в « самообороне », когда избил мать троих детей до смерти гантелью, в результате чего она получила более пятидесяти ранений. [18]
Общество и культура
Правовой статус
Австралия
Стандарт унифицированного перечня лекарственных средств и ядов (SUSMP) Австралии не включает DOI в список запрещенных веществ. [19]
Канада
Включен в Список 1 [20], поскольку является аналогом амфетамина. [21] CDSA был обновлен в результате принятия Закона о безопасности улиц и сообществ , изменив амфетамины из Списка 3 в Список 1. [ 22]
Дания
Незаконно с 8 апреля 2007 года . [23]
Финляндия
DOI классифицируется как психоактивное вещество, запрещенное на потребительском рынке Финляндии. [24]
Швеция
Sveriges riksdag добавил DOI в список I ( «вещества, растительные материалы и грибы, которые обычно не имеют медицинского применения» ) в качестве наркотиков в Швеции с 30 августа 2007 года, опубликованный Агентством по медицинским продуктам в своем постановлении LVFS 2007:10, указанный как DOI, 4-йод-2,5-диметокси-амфетамин. [25]
Соединенные Штаты
По состоянию на 2023 год DOI не включен в список в Соединенных Штатах, [26] но вполне вероятно, что DOI будет считаться аналогом ( DOB ), и в этом случае продажа или хранение могут преследоваться в соответствии с Федеральным законом об аналогах . В декабре 2023 года Управление по борьбе с наркотиками США опубликовало уведомление о предлагаемом нормотворчестве , которое классифицировало бы как 2,5-диметокси-4-йодоамфетамин, так и 2,5-диметокси-4-хлорамфетамин как контролируемые вещества списка I. [27]
DOI регулярно используется в исследованиях на животных и in vitro. [28] Планирование DOI может вызвать проблемы для медицинских исследователей. [27]
DOI — контролируемое вещество, включенное в Список I в штате Флорида. [29]
Ссылки
- ^ "D101 DOI гидрохлорид ≥98% (ВЭЖХ), твердый" . Получено 13 апреля 2008 г. .
- ^ Анвиса (24 июля 2023 г.). «RDC № 804 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial» [Постановление Коллегиального совета № 804 - Списки наркотических, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем] (на бразильском португальском языке). Diário Oficial da União (опубликовано 25 июля 2023 г.). Архивировано из оригинала 27 августа 2023 г. Проверено 27 августа 2023 г.
- ^ abcd Glennon RA, Dukat M (июнь 2024 г.). «1-(2,5-диметокси-4-иодфенил)-2-аминопропан (DOI): от неизвестного до основного члена семейства серотонинергических психоделических агентов DOX — обзор». ACS Pharmacol Transl Sci . 7 (6): 1722– 1745. doi : 10.1021/acsptsci.4c00157 . PMID 38898956.
- ^ abcd Canal, CE; Morgan, D (июль 2012 г.). «Реакция подергивания головы у грызунов, вызванная галлюциногеном 2,5-диметокси-4-иодоамфетамином: всеобъемлющая история, переоценка механизмов и ее полезность в качестве модели». Drug Testing and Analysis . 4 ( 7– 8): 556– 576. doi :10.1002/dta.1333. PMC 3722587. PMID 22517680 .
- ^ аб Шульгин, А; Шульгин, А (1990). «#67 ДОИ». PiHKAL: Химическая история любви . Трансформация Пресс. ISBN 978-0963009609. Архивировано из оригинала 2014-10-27 . Получено 2014-12-17 .
- ^ "LSD Blotter Acid Mimics (Actually contain 4-IODO-2,5-DIMETHOXYAMPHETAMINE (DOI) and 4-CHLORO-2,5-DIMETHOXYAMPHETAMINE (DOC)) in Lantana, Florida". DEA Microgram Bulletin . Вашингтон, округ Колумбия: Управление судебной экспертизы, Управление по борьбе с наркотиками. Июнь 2008 г. Архивировано из оригинала 2009-02-04 . Получено 12 февраля 2009 г.
- ^ Poulie CB, Jensen AA, Halberstadt AL, Kristensen JL (декабрь 2020 г.). «Классика DARK в химической нейронауке: NBOMes». ACS Chem Neurosci . 11 (23): 3860– 3869. doi :10.1021/acschemneuro.9b00528. PMC 9191638 . PMID 31657895.
Психоделические фенэтиламины обычно проявляют менее чем 5–10-кратную селективность для рецепторов 5-HT2A по сравнению с 5-HT2C.53,54 [...] Сообщаемая селективность 25CN-NBOH для 5-HT2A по сравнению с 5-HT2C варьируется в зависимости от экспериментальных условий,49,59,60 но 25CN-NBOH явно более селективен, чем DOI, который всего лишь примерно в 5 и 12 раз селективнее для 5-HT2A по сравнению с 5-HT2C на человеческих и мышиных рецепторах, соответственно.93–95 [...]
- ^ Мацумото Т., Маэно Ю., Като Х., Секо-Накамура Ю., Монма-Отаки Дж., Исиба А., Нагао М., Аоки Ю. (август 2014 г.). «Влияние циклозамещенных амфетаминов на мозг крыс, высвобождающее 5-гидрокситриптамин и дофамин: сравнительное исследование с использованием микродиализа in vivo». Eur Нейропсихофармакол . 24 (8): 1362–1370 . doi :10.1016/j.euroneuro.2014.04.009. ПМИД 24862256.
- ^ Bunzow JR, Sonders MS, Arttamangkul S, Harrison LM, Zhang G, Quigley DI, Darland T, Suchland KL, Pasumamula S, Kennedy JL, Olson SB, Magenis RE, Amara SG, Grandy DK (декабрь 2001 г.). «Амфетамин, 3,4-метилендиоксиметамфетамин, диэтиламид лизергиновой кислоты и метаболиты нейротрансмиттеров катехоламинов являются агонистами рецептора следовых аминов крысы». Mol Pharmacol . 60 (6): 1181– 1188. doi :10.1124/mol.60.6.1181. PMID 11723224.
- ^ abc Roth, BL ; Driscol, J (12 января 2011 г.). "PDSP Ki Database". Программа скрининга психоактивных препаратов (PDSP) . Университет Северной Каролины в Чапел-Хилл и Национальный институт психического здоровья США. Архивировано из оригинала 8 ноября 2013 г. . Получено 4 марта 2014 г. .
- ^ Miller KJ, Gonzalez HA (декабрь 1998 г.). «Активация рецептора серотонина 5-HT2A ингибирует стимулированную цитокинами индуцибельную синтазу оксида азота в клетках глиомы C6». Ann. NY Acad. Sci . 861 (1): 169– 73. Bibcode :1998NYASA.861..169M. doi :10.1111/j.1749-6632.1998.tb10188.x. PMID 9928254. S2CID 23264746.
- ^ Yu B, Becnel J, Zerfaoui M, Rohatgi R, Boulares AH, Nichols CD (ноябрь 2008 г.). «Активация рецептора серотонина 5-гидрокситриптамина (2A) с необычайной силой подавляет воспаление, вызванное фактором некроза опухоли альфа». J. Pharmacol. Exp. Ther . 327 (2): 316–23 . doi :10.1124/jpet.108.143461. PMID 18708586. S2CID 25374241.
- ^ Пеллетье М., Сигел Р. М. (декабрь 2009 г.). «Желание избавиться от воспаления? Новые связи между сигнализацией серотонина и ФНО». Mol. Interv . 9 (6): 299– 301. doi :10.1124/mi.9.6.5. PMC 2861806. PMID 20048135 .
- ^ "Исследования LSU Health New Orleans показывают, что психоделический препарат предотвращает развитие астмы у мышей". EurekAlert! .
- ^ Yu, B; Becnel, J; Zerfaoui, M; Rohatgi, R; Boulares, AH; Nichols, CD (2008). «Активация рецептора серотонина 5-гидрокситриптамина 2A с чрезвычайной силой подавляет воспаление, вызванное фактором некроза опухоли-α». Журнал фармакологии и экспериментальной терапии . 327 (2): 316– 323. doi : 10.1124/jpet.108.143461. PMID 18708586. S2CID 25374241.
- ^ Джонс, КА; Шривастава, ДП; Аллен, ДЖА; Страчан, РТ; Рот, БЛ; Пензес, П (17 ноября 2009 г.). «Быстрая модуляция морфологии позвоночника рецептором серотонина 5-HT2A через сигнализацию калирина-7». Труды Национальной академии наук . 106 (46): 19575– 19580. Bibcode : 2009PNAS..10619575J. doi : 10.1073/pnas.0905884106 . PMC 2780750. PMID 19889983 .
- ^ "Новое предупреждение о наркотиках, трое заболели". BBC News . 29 января 2007 г.
- ^ "Мужчина приговорен к тюремному заключению за непредумышленное убийство партнера, поскольку правительство принимает меры по закрытию "лазейки в защите" - ABC News". amp.abc.net.au . Получено 2024-09-06 .
- ^ Gill, A (22 июля 2013 г.). "POISONS STANDARD 2013" (PDF) . Управление по контролю за товарами терапевтического назначения. Департамент здравоохранения и старения правительства Австралии . Получено 4 марта 2014 г.
- ^ "Закон о контролируемых лекарственных средствах и веществах: история законодательства · Приложение I · Раздел 19: Трамадол [Предложено]; Амфетамины". isomerdesign.com . Архивировано из оригинала 2022-03-31 . Получено 2012-11-27 .
- ^ "Закон о контролируемых лекарственных средствах и веществах: определения и толкования". isomerdesign.com . Архивировано из оригинала 2013-11-10 . Получено 2012-11-27 .
- ^ [1] (на английском)
- ^ "Erowid DOC Vault: Правовой статус". www.erowid.org .
- ^ «FINLEX ® - Ajantasainen lainsäädäntö: Valtioneuvoston asetus kuluttajamarkkinoilta… 1130/2014» .
- ^ "Läkemedelsverkets föreskrifter - LVFS и HSLF-FS | Läkemedelsverket" (PDF) .
- ^ "ЧАСТЬ 1308 - Раздел 1308.11 Приложение I". www.deadiversion.usdoj.gov . Архивировано из оригинала 2009-08-27 . Получено 2014-12-17 .
- ^ ab «Списки контролируемых веществ: Размещение 2,5-диметокси-4-йодоамфетамина (DOI) и 2,5-диметокси-4-хлорамфетамина (DOC) в Списке I». www.regulations.gov .
- ^ Марио де ла Фуэнте Ревенга; Бохан Чжу; Кристофер А. Гевара; Джордж У. Хантли; Чанг Лу; Хавьер Гонсалес-Маесо (2021). «Длительные изменения эпигеномной и синаптической пластичности после однократного воздействия психоделика на мышей». Cell Reports . 37 (3): 109836. doi :10.1016/j.celrep.2021.109836. PMC 8582597 . PMID 34686347.
- ^ "Уставы и конституция: Просмотр уставов: Онлайн Sunshine". leg.state.fl.us .
Внешние ссылки
- Erowid о DOI
- Лицей о DOI
- Вход PiHKAL
- Запись DOI в PiHKAL • информация


