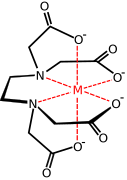
- комплекс металла с анионом ЭДТА
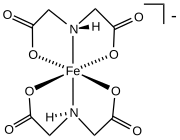
- Бис(иминодиацетат) железа
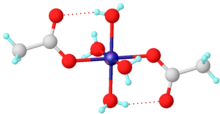
- Активный центр гемэритрина, карбоксилата железа, переносящего O2.
Комплекс карбоксилатов переходных металлов
Комплексы карбоксилатов переходных металлов представляют собой координационные комплексы с карбоксилатными (RCO 2 − ) лигандами . Отражая разнообразие карбоновых кислот, перечень карбоксилатов металлов велик. Многие из них полезны в коммерческом отношении, и многие привлекли пристальное внимание ученых. Карбоксилаты демонстрируют различные координационные режимы, наиболее распространенными из которых являются κ 1 - (O-монодентатный), κ 2 (O,O-бидентатный) и мостиковый.
Ацетат и родственные монокарбоксилаты
Структура и связь
Карбоксилаты связываются с отдельными металлами одним или обоими атомами кислорода, соответствующие обозначения κ 1 - и κ 2 -. С точки зрения подсчета электронов , κ 1 -карбоксилаты являются лигандами типа "X", т. е. псевдогалогенидными. κ 2 -карбоксилаты являются "лигандами LX", т. е. напоминают комбинацию основания Льюиса (L) и псевдогалогенида (X). Карбоксилаты классифицируются как жесткие лиганды в теории HSAB .
- Структуры некоторых ацетатов металлов
- Ацетат серебра
- Ацетат молибдена(II) , иллюстрирующий четверную связь Mo-Mo. [1]
- [CoO(ацетат)] 4 , " Das cubane "
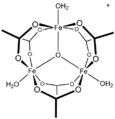
Для простых карбоксилатов иллюстративными являются ацетатные комплексы. Большинство ацетатов переходных металлов являются комплексами со смешанными лигандами. Одним из распространенных примеров является гидратированный ацетат никеля , Ni(O 2 CCH 3 ) 2 (H 2 O) 4 , который характеризуется внутримолекулярными водородными связями между некоординированными атомами кислорода и протонами лигандов aqua . Стехиометрически простые комплексы часто являются мультиметаллическими. Одно семейство — это основные ацетаты металлов со стехиометрией [M 3 O(OAc) 6 (H 2 O) 3 ] n+ . [2]

Гомолептические комплексы
Гомолептические карбоксилатные комплексы обычно являются координационными полимерами . Но существуют исключения.
- Молекулярный монокарбоксилат — это ацетат серебра , Ag2 ( OAc) 2 .
- Молекулярные диацетаты более распространены. Несколько диацетатов принимают структуру китайского фонарика . Хорошо изученные примеры включают диметаллические тетраацетаты (M 2 (OAc) 4 ), включая ацетат родия (II) , ацетат меди (II) , ацетат молибдена (II) и ацетат хрома (II) . Диацетат платины и диацетат палладия имеют ядра Pt 4 и Pd 3 , что дополнительно иллюстрирует тенденцию ацетатных лигандов стабилизировать мультиметаллические структуры.
- Мононуклеарные трикарбоксилаты включают производные 1-адамантанкарбоновой кислоты , которые имеют формулу [M(O 2 CC 10 H 11 ) 3 ] − (M = Co, Ni, Zn). Карбоксилаты являются бидентатными. [4]
Синтез
Многие методы позволяют синтезировать карбоксилаты металлов. Из предварительно сформированной карбоновой кислоты были продемонстрированы следующие пути: [5]
- кислотно-основные реакции: L n MOR' + RCO 2 H → L n MO 2 CR + R'OH
- протонолиз: L n Mалкил + RCO 2 H → L n MO 2 CR + алкан
- окислительное присоединение : L n M + RCO 2 H → L n (H)MO 2 CR
Из предварительно образованного карбоксилата обычно происходят реакции метатезиса соли :
- L n MCl + RCO 2 Na → L n MO 2 CR + NaCl
Карбоксилаты металлов можно получить путем карбонизации высокоосновных алкилов металлов:
- L n MR + CO 2 → L n MO 2 CR
Реакции
Распространенной реакцией карбоксилатов металлов является их вытеснение более основными лигандами. Ацетат является распространенной уходящей группой . Они особенно склонны к протонолизу, который широко используется для введения лигандов, вытесняя карбоновую кислоту. Таким образом, из димолибдентетраацетата получается октахлордимолибдат :
- Mo2 ( O2CCH3 ) 4 + 4HCl + 4KCl → K4 [ Mo2Cl8 ] + 4CH3CO2H
Предполагается, что ацетаты электрофильных металлов действуют как основания в реакциях депротонирования при совместном металлировании . [6]
Попытки приготовить некоторые карбоксилатные комплексы, особенно для электрофильных металлов, часто приводят к оксопроизводным. Примерами служат оксоацетаты Fe(III), Mn(III) и Cr(III). Пиролиз карбоксилатов металлов дает ангидриды кислот и оксид металла. Эта реакция объясняет образование основного ацетата цинка из безводного диацетата цинка .
В некоторых случаях монодентатные карбоксилаты подвергаются O-алкилированию с образованием эфиров. Требуются сильные алкилирующие агенты.
Другие карбоксилаты
Многие карбоксилаты образуют комплексы с переходными металлами. Алкил- и простые арилкарбоксилаты ведут себя подобно ацетатам. Трифторацетаты отличаются моноядерными комплексами, поскольку они обычно монодентатны, например, [Zn(κ 2 -O 2 CCH 3 ) 2 (OH 2 ) 2 ] против [Zn(κ 1 -O 2 CCF 3 ) 2 (OH 4 ) 2 ]. [7]
Приложения
Нафтенаты и этилгексаноаты металлов

Структура представительной нафтеновой кислоты, образующей разнообразные комплексы с переходными металлами.
Нафтеновые кислоты , смеси длинноцепочечных и циклических карбоновых кислот, извлеченных из нефти, образуют липофильные комплексы (часто называемые солями) с переходными металлами. Эти нафтенаты металлов , имеющие формулу M(naphthenate) 2 или M3O (naphthenate) 6 , имеют разнообразное применение [8] [9] , включая синтетические моющие средства , смазочные материалы , ингибиторы коррозии, присадки к топливу и смазочным маслам, консерванты для древесины , инсектициды , фунгициды , акарициды , смачивающие агенты , загустители и осушители масла . Промышленно полезные нафтенаты включают нафтенаты алюминия, магния, кальция, бария, кобальта, меди, свинца, марганца, никеля, ванадия и цинка.< [9] Показательным является использование нафтената кобальта для окисления тетрагидронафталина до гидропероксида. [10]
2.jpg/440px-Co(Ethexanoate)2.jpg)
Подобно нафтеновой кислоте, 2-этилгексановая кислота образует липофильные комплексы, которые используются в органическом и промышленном химическом синтезе . Они действуют как катализаторы в полимеризациях , а также в реакциях окисления в качестве масляных осушителей . [11] Этилгексаноаты металлов называются металлическими мылами. [12]
Аминополикарбоксилаты
Коммерчески важное семейство карбоксилатов металлов получено из аминополикарбоксилатов , например, ЭДТА 4- . С этими синтетическими хелатирующими агентами связаны аминокислоты , которые образуют большие семейства аминокислотных комплексов . Две аминокислоты, глутамат и аспартат, имеют карбоксилатные боковые цепи, которые функционируют как лиганды для железа в негемовых железосодержащих белках, таких как гемэритрин . [13]
Металлоорганические каркасы (МОК)
Металлоорганические каркасы , пористые, трехмерные координационные полимеры, часто получаются из кластеров карбоксилатов металлов. Эти кластеры, называемые вторичными связующими единицами (SBU), часто связаны сопряженными основаниями бензолди- и трикарбоновых кислот. [14]
Реагенты для органического синтеза

Утверждается, что «карбоксилаты кобальта являются наиболее широко используемыми гомогенными катализаторами в промышленности», поскольку они используются при окислении п-ксилола в терефталевую кислоту . [15]
Ацетат палладия(II) описывается как «один из наиболее широко используемых комплексов переходных металлов в металло-опосредованном органическом синтезе». Во многих реакциях сочетания используется этот реагент, который растворим в органических растворителях и содержит встроенное основание Бренстеда (ацетат). [16]
Диродий тетракис(трифторацетат) широко используется в качестве катализатора для реакций с участием диазосоединений. [17]
Похожие темы
Ссылки
- ^ Brignole, Alicia B.; Cotton, FA (1972). «Соединения рения и молибдена, содержащие четверные связи». Неорганические синтезы . 13 : 81–89 . doi :10.1002/9780470132449.ch15.
- ^ Каттерик, Джанет; Торнтон, Питер (1977). Структуры и физические свойства полинуклеарных карбоксилатов . Достижения в неорганической химии и радиохимии. Т. 20. С. 291– 362. doi :10.1016/S0065-2792(08)60041-2. ISBN 9780120236206.
- ^ Чжан, Гао; Линь, Цзянь; Го, Донг-Вэй; Яо, Ши-Янь; Тиан, Юнь-Ци (2010). «Полимеры бесконечной координации одно- и двумерных ацетатов кобальта». Zeitschrift für Anorganische und Allgemeine Chemie . 636 (7): 1401–1404 . doi :10.1002/zaac.200900457.
- ^ Фурсова, Е. Ю.; Романенко Г.В.; Толстиков С.Е.; Овчаренко, В.И. (2019). «Моноядерные адамантан-1-карбоксилаты переходных металлов». Российский химический вестник : 1669–1674 . doi :10.1007/s11172-019-2610-4. S2CID 203592748.
- ^ Гарсия-Родригес, Рауль; Хендрикс, Марк П.; Коссэрт, Брэнди М.; Лю, Хайтао; Оуэн, Джонатан С. (2013). «Реакции преобразования прекурсоров нанокристаллов халькогенида кадмия». Химия материалов . 25 (8): 1233– 1249. doi : 10.1021/cm3035642.
- ^ Акерман, Лутц (2011-03-09). "Carboxylate-Assisted Transition-Metal-Catalyzed C−H Bond Functionalizations: Mechanism and Scope". Chemical Reviews . 111 (3): 1315– 1345. doi :10.1021/cr100412j. ISSN 0009-2665. PMID 21391562.
- ^ Морозов, ИВ; Карпова Е.В.; Глазунова Т. Ю.; Болталин А.И.; Захаров, М.А.; Терещенко Д.С.; Федорова А.А.; Троянов, СИ (2016). «Трифторацетатные комплексы 3d-элементов: особенности синтеза и строения». Российский журнал координационной химии . 42 (10): 647–661 . doi : 10.1134/S107032841610002X.
- ^ М. Ландау. 1993. "Сиккативы и металлические мыла", в J. Kroschwitz, ed., Kirk-Othmer Encyclopedia of Chemical Technology . Нью-Йорк: John Wiley & Sons. Т. 8, стр. 432-445. doi :10.1002/0471238961.0418090512011404.a01
- ^ ab Нора, Анджело; Коенен, Гюнтер (2010). «Металлические мыла». Энциклопедия промышленной химии Ульмана . doi :10.1002/14356007.a16_361.pub2. ISBN 978-3-527-30385-4.
- ^ Найт, Х. Б.; Сверн, Дэниел (1954). «Гидропероксид тетралина». Органические синтезы . 34 : 90. doi :10.15227/orgsyn.034.0090.
- ^ Раджу, Равиндер; Прасад, Капа (2012). «Синтетические применения реагентов, полученных из 2-этилгексановой кислоты». Тетраэдр . 68 (5): 1341– 1349. doi :10.1016/j.tet.2011.10.078.
- ^ Нора, Анджело; Щепанек, Альфред; Кёнен, Гюнтер (2001). «Металлические мыла». Энциклопедия промышленной химии Ульмана . doi :10.1002/14356007.a16_361. ISBN 3527306730.
- ^ Ясневский, Эндрю Дж.; Ку, Лоуренс (2018). «Активация дикислорода негемовыми дижелезными ферментами: разнообразные дикислородные аддукты, высоковалентные промежуточные продукты и связанные модельные комплексы». Chemical Reviews . 118 (5): 2554– 2592. doi :10.1021/acs.chemrev.7b00457. PMC 5920527 . PMID 29400961.
- ^ Траншемонтань, Дэвид Дж.; Мендоса-Кортес, Хосе Л.; О'Киф, Майкл; Яги, Омар М. (2009). «Вторичные строительные единицы, сети и связи в химии металлоорганических каркасов». Обзоры химического общества . 38 (5): 1257– 1283. doi :10.1039/b817735j. PMID 19384437.
- ^ Битти, Джеймс К.; Хэмбли, Тревор В.; Клепетко, Джон А.; Мастерс, Энтони Ф.; Тернер, Питер (1997). «Химия ацетата кобальта — III. Выделение и характеристика кристаллической структуры олигомера октакобальта со смешанной валентностью, [Co8(O)4(CH3CO2)6(OMe)4]Cl4(OHn)4 · 6H2O (N = 1 или 2), полученного при получении ацетата кобальта (III)». Polyhedron . 16 (12): 2109– 2112. doi :10.1016/S0277-5387(96)00498-6.
- ^ Греннберг, Хелена; Фут, Джонатан С.; Банвелл, Мартин Г.; Роман, Даниэла Сустак (2001). "Ацетат палладия(II)". Энциклопедия реагентов для органического синтеза . С. 1–35 . doi :10.1002/047084289X.rp001.pub3. ISBN 978-0-470-84289-8.
- ^ Дойл, Майкл П.; Дэвис, Хью МЛ; Мэннинг, Джеймс Р. (2006). "Dirhodium(II) tetrakis(trifluoroacetate)". EEROS . doi :10.1002/047084289X.rd461.pub2. ISBN 0-471-93623-5.


![Ацетат молибдена(II), иллюстрирующий четверную связь Mo-Mo.[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/2/23/Mo2%28OAc%294.svg/120px-Mo2%28OAc%294.svg.png)
![[CoO(ацетат)]4, «Кубан»](http://upload.wikimedia.org/wikipedia/commons/thumb/d/da/DasCubane.svg/120px-DasCubane.svg.png)