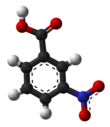
3-Нитробензойная кислота
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 3-Нитробензойная кислота | |||
| Другие имена м -Нитробензойная кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| ЧЭБИ |
| ||
| ChEMBL | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.004.099 | ||
CID PubChem |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С7Н5НО4 | |||
| Молярная масса | 167,12 г/моль | ||
| Появление | кремовый цвет твердого вещества | ||
| Плотность | 1,494 г/см 3 | ||
| Температура плавления | от 139 до 141 °C (от 282 до 286 °F; от 412 до 414 K) | ||
| 0,24 г/100 мл (15 °C) | |||
| Кислотность ( pK a ) | 3,47 (в воде) [1] | ||
| -80,22·10 −6 см 3 /моль | |||
| Родственные соединения | |||
Родственные соединения | Бензойная кислота Нитробензол Антраниловая кислота 3,5-Динитробензойная кислота 2-Нитробензойная кислота 4-Нитробензойная кислота | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
3-Нитробензойная кислота — органическое соединение с формулой C 6 H 4 (NO 2 )CO 2 H. Это ароматическое соединение, и при стандартных условиях это не совсем белое твердое вещество. Два заместителя находятся в мета-положении по отношению друг к другу, что дает альтернативное название м -нитробензойная кислота. Это соединение может быть полезным, поскольку оно является предшественником 3-аминобензойной кислоты , которая используется для получения некоторых красителей. [2]
Подготовка
Его получают путем нитрования бензойной кислоты при низких температурах. Как 2-нитробензойная кислота , так и 4-нитробензойная кислота производятся в качестве побочных продуктов с выходами приблизительно 20% и 1,5% соответственно. [2] Поскольку функциональные группы карбоновой кислоты являются электроноакцепторными , во время реакции электрофильного ароматического замещения нитрования заместители направляются в мета-положение, что объясняет эту региохимию.
Менее эффективный путь включает нитрование метилбензоата с последующим гидролизом. [3] В качестве альтернативы было продемонстрировано окислительное расщепление связи CC 3-нитроацетофенона до соответствующей арилкарбоновой кислоты. [4] Дальнейший синтез включает окисление 3-нитробензальдегида.
Характеристики
При ap K a 3,47 [1] 3-нитробензойная кислота примерно в десять раз более кислая, чем бензойная кислота . Сопряженное основание бензойной кислоты стабилизировано наличием электроноакцепторной нитрогруппы, что объясняет ее повышенную кислотность по сравнению с незамещенной бензойной кислотой. [5] Она обычно растворима в кислородсодержащих и хлорированных растворителях. [6]
Реактивность
Присутствие как карбоновой кислоты , так и нитрофункциональных групп дезактивирует кольцо по отношению к реакциям электрофильного ароматического замещения . Гидрирование дает 3-аминобензойную кислоту . [2]
Безопасность
Соединение, вероятно, имеет умеренную токсичность, с LD 50 (внутривенно, мышь) 640 мг/кг. Это соединение может вызывать раздражение кожи и глаз с симптомами воздействия, включая метгемоглобин, сенсибилизацию, раздражение и повреждение роговицы. [7]
Ссылки
- ^ ab "Константы диссоциации органических кислот и оснований" . Получено 11 апреля 2010 г.
- ^ abc Takao Maki, Kazuo Takeda (2002). "Бензойная кислота и ее производные". Энциклопедия промышленной химии Ульмана . Weinheim: Wiley-VCH. doi :10.1002/14356007.a03_555. ISBN 978-3-527-30673-2..
- ^ Оливер Камм и Дж. Б. Сегюр "м-нитробензойная кислота" Org. Synth. 1923, том 3, 73. doi :10.15227/orgsyn.003.0073
- ^ Ли, Мэйчао; Шэнь, Чжэньлу; Сюй, Лян; Ван, Шэнпэн; Чэнь, Бацзинь; Ху, Синьцюань; Ху, Баосян; Цзинь, Лицюнь; Сан, Нань (2018-05-16). «Окислительное расщепление связи C–C для синтеза арилкарбоновых кислот из арилалкилкетонов». Synlett . 29 (11): 1505– 1509. doi :10.1055/s-0037-1609751. ISSN 0936-5214. S2CID 104110049.
- ^ "20.4 Влияние заместителей на кислотность". Chemistry LibreTexts . 2017-08-25 . Получено 2018-09-25 .
- ^ Эшфорд, Эдит . Словарь художников Бенезита. Том 1. Oxford University Press. 2011-10-31. doi :10.1093/benz/9780199773787.article.b00007872.
- ^ "М-нитробензойная кислота". CAMEO Chemicals . Получено 25.09.2018 .