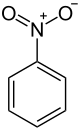
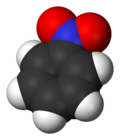
Нитробензол
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Нитробензол | |||
| Другие имена Нитробензол Нитритбензол Масло мирбана | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 507540 | |||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.002.469 | ||
| Номер ЕС |
| ||
| 50357 | |||
| КЕГГ | |||
CID PubChem |
| ||
| Номер RTECS |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С6Н5НО2 | |||
| Молярная масса | 123,11 г/моль | ||
| Появление | желтоватая, маслянистая жидкость [1] | ||
| Запах | едкий, как паста для обуви [1] до миндального | ||
| Плотность | 1,199 г/см 3 | ||
| Температура плавления | 5,7 °C (42,3 °F; 278,8 К) | ||
| Точка кипения | 210,9 °C (411,6 °F; 484,0 К) | ||
| 0,19 г/100 мл при 20 °C | |||
| Давление пара | 0,3 мм рт. ст. (25°С) [1] | ||
| -61,80·10 −6 см 3 /моль | |||
| Вязкость | 1,8112 мПа·с [2] | ||
| Опасности | |||
| Маркировка СГС : | |||
  | |||
| Опасность | |||
| Н301 , Н311 , Н331 , Н351 , Н360 , Н372 , Н412 | |||
| Р201 , Р202 , Р260 , Р261 , Р264 , Р270 , Р271 , Р273 , Р280 , Р281 , Р301+Р310 , Р302+Р352 , Р304+Р340 , Р308+Р313 , Р311 , Р312 , Р314 , Р321 , Р322 , Р330 , Р361 , Р363 , Р403+Р233 , Р405 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 88 °C (190 °F; 361 К) | ||
| 480 °C (896 °F; 753 К) | |||
| Пределы взрывоопасности | 1,8%-? [1] | ||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD 50 ( средняя доза ) | 780 мг/кг (крыса, перорально) 600 мг/кг (крыса, перорально) 590 мг/кг (мышь, перорально) [3] | ||
LD Lo ( самый низкий опубликованный ) | 750 мг/кг (собака, перорально) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (допустимый) | TWA 1 ppm (5 мг/м 3 ) [кожа] [1] | ||
РЕЛ (рекомендуется) | TWA 1 ppm (5 мг/м 3 ) [кожа] [1] | ||
IDLH (Непосредственная опасность) | 200 частей на миллион [1] | ||
| Родственные соединения | |||
Родственные соединения | Анилин Бензолдиазонийхлорид Нитрозобензол | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Нитробензол — ароматическое нитросоединение и простейший из нитробензолов с химической формулой C6H5NO2 . Это нерастворимое в воде бледно-желтое масло с запахом миндаля. Замерзает, образуя зеленовато-желтые кристаллы. Его производят в больших масштабах из бензола в качестве предшественника анилина . В лаборатории его иногда используют в качестве растворителя , особенно для электрофильных реагентов .
Производство
Нитробензол получают нитрованием бензола смесью концентрированной серной кислоты , воды и азотной кислоты . Эту смесь иногда называют «смешанной кислотой». Производство нитробензола является одним из самых опасных процессов, проводимых в химической промышленности из-за экзотермичности реакции (Δ H = −117 кДж/моль). [4]
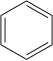 +
+

Мировые мощности по производству нитробензола в 1985 году составляли около 1 700 000 тонн . [4]
Процесс нитрования включает образование иона нитрония (NO 2 + ), за которым следует реакция электрофильного ароматического замещения его бензолом. Ион нитрония образуется в результате реакции азотной кислоты и кислотного дегидратирующего агента, обычно серной кислоты:
- HNO 3 + H + ⇌ NO 2 + + H 2 O
Использует
Приблизительно 95% нитробензола, производимого в промышленности, гидрогенизируется в анилин : [4]
- C6H5NO2 + 3H2 → C6H5NH2 + 2H2O
Анилин является предшественником уретановых полимеров, резиновых химикатов, пестицидов , красителей (особенно азокрасителей ), взрывчатых веществ и фармацевтических препаратов .

Большая часть анилина потребляется при производстве метилендианилина — предшественника полиуретанов.
Специализированные приложения
Нитробензол используется для маскировки неприятных запахов в кремах для обуви и полов, кожаных повязках, растворителях для красок и других материалах. Перегнанный, как масло мирбана, нитробензол использовался в качестве недорогой отдушки для мыла . Для этой цели его заменили менее токсичными химикатами. [5] Значительным рынком сбыта нитробензола является его использование в производстве анальгетика парацетамола (также известного как ацетаминофен). [6] Нитробензол также используется в ячейках Керра , поскольку он имеет необычно большую константу Керра . Имеются данные, указывающие на его использование в сельском хозяйстве в качестве стимулятора роста/цветения растений. [7]
Органические реакции
Помимо превращения в анилин, нитробензол может быть селективно восстановлен до азоксибензола , [8] азобензола , [9] нитрозобензола , [10] гидразобензола , [11] и фенилгидроксиламина . [12] Он использовался как мягкий окислитель в реакциях, таких как синтез хинолина Скраупа . [13]
Безопасность
Нитробензол очень токсичен ( предельно допустимая концентрация 5 мг/м3 ) и легко всасывается через кожу.
Длительное воздействие может вызвать серьезное повреждение центральной нервной системы , ухудшить зрение, вызвать повреждение печени или почек, анемию и раздражение легких. Вдыхание паров может вызвать головную боль, тошноту, усталость, головокружение, цианоз , слабость в руках и ногах, а в редких случаях может быть смертельным. Масло легко впитывается через кожу и может увеличить частоту сердечных сокращений, вызвать судороги или, в редких случаях, смерть. Проглатывание может также вызвать головные боли, головокружение, тошноту, рвоту и желудочно-кишечное раздражение, потерю чувствительности/использования в конечностях, а также вызвать внутреннее кровотечение. [10]
Нитробензол считается вероятным канцерогеном для человека Агентством по охране окружающей среды США [14] и классифицируется МАИР как канцероген группы 2B, который «возможно канцерогенен для человека». [15] Было показано, что он вызывает аденомы и карциномы печени, почек и щитовидной железы у крыс. [16]
В Соединенных Штатах он классифицируется как чрезвычайно опасное вещество , как определено в разделе 302 Закона США о планировании действий в чрезвычайных ситуациях и праве общества на информацию (42 USC 11002), и подлежит строгим требованиям отчетности со стороны предприятий, которые производят, хранят или используют его в значительных количествах. [17]
Ссылки
- ^ abcdefg Карманный справочник NIOSH по химическим опасностям. "#0450". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ахлувалия, Р.; Ванчоо, Р.К.; Шарма, С.К.; Вашишт, Дж.Л. (1996). «Плотность, вязкость и поверхностное натяжение бинарных жидких систем: этановая кислота, пропановая кислота и бутановая кислота с нитробензолом». Журнал химии растворов . 25 (9): 905–917. doi :10.1007/BF00972581. ISSN 0095-9782. S2CID 95126469.
- ^ ab "Нитробензол". Концентрации, представляющие немедленную опасность для жизни или здоровья (IDLH) . Национальный институт охраны труда (NIOSH).
- ^ abc Booth G (2007). "Нитросоединения, ароматические". Энциклопедия промышленной химии Ульмана (6-е изд.). Weinheim: Wiley-VCH. doi :10.1002/14356007.a17_411. ISBN 978-3-527-30385-4.
- ^ Hogarth CW (январь 1912 г.). «случай отравления маслом мирбана (нитробензола)». British Medical Journal . 1 (2665): 183. doi :10.1136/bmj.1.2665.183. PMC 2344391. PMID 20765985 .
- ^ Bhattacharya A, Purohit VC, Suarez V, Tichkule R, Parmer G, Rinaldi F (март 2006 г.). «Одношаговое восстановительное амидирование нитроаренов: применение в синтезе ацетаминофена». Tetrahedron Letters . 47 (11): 1861–1864. doi :10.1016/j.tetlet.2005.09.196.
- ^ «Состав стимулятора цветения с использованием нитробензола».
- ^ Бигелоу, Х. Э.; Палмер, Альберт (1931). «Азоксибензол». Органические синтезы . 11 : 16. doi :10.15227/orgsyn.011.0016.
- ^ Bigelow HE, Robinson DB (1955). "Азобензол". Органические синтезы; Собрание томов , т. 3, стр. 103.
- ^ ab Coleman GH, McCloskey CM, Stuart FA. "Нитрозобензол". Органические синтезы; Собрание томов , т. 3, стр. 668.
- ^ Karwa, Shrikant L.; Rajadhyaksha, Rajeev A. (январь 1988). «Селективное каталитическое гидрирование нитробензола в гидразобензол». Industrial & Engineering Chemistry Research . 27 (1): 21–24. doi :10.1021/ie00073a005. ISSN 0888-5885.
- ^ Камм О. «β-фенилгидроксиламин». Органические синтезы; Собрание томов , т. 1, стр. 445.
- ^ Кларк, HT; Дэвис, AW. «Хинолин». Органические синтезы . 1 : 478.
- ^ Отдел, US EPA, ORD, Интегрированная система информации о рисках. "Нитробензол CASRN 98-95-3 - IRIS - US EPA, ORD". cfpub.epa.gov . Получено 10 августа 2017 г. .
{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ "Агенты, классифицированные монографиями МАИР, Международное агентство по изучению рака" (PDF) . Получено 10 августа 2017 г.
- ^ Национальные институты здравоохранения · Министерство здравоохранения и социальных служб США, Номинация: Комитет по рассмотрению нитробензола, 02.02.2010
- ^ "40 CFR: Приложение A к Части 355 — Список чрезвычайно опасных веществ и их пороговые плановые количества" (PDF) (ред. от 1 июля 2008 г.). Правительственная типография . Архивировано из оригинала (PDF) 25 февраля 2012 г. Получено 29 октября 2011 г.
Внешние ссылки
- Международная карта химической безопасности 0065
- Карманный справочник NIOSH по химическим опасностям
- Монография МАИР: «Нитробензол»
- Информационный листок Агентства по охране окружающей среды США
- https://patents.google.com/patent/US9113628