Гексакарбонил вольфрама
 | |||
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гексакарбонилвольфрам | |||
| Другие имена Карбонил вольфрама Гексакарбонилвольфрам | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| Информационная карта ECHA | 100.034.423 | ||
| Номер ЕС |
| ||
CID PubChem |
| ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С 6 О 6 В | |||
| Молярная масса | 351,901 г/моль | ||
| Появление | Бесцветное твердое вещество | ||
| Плотность | 2,65 г/см 3 | ||
| Температура плавления | 170 °C (338 °F; 443 K) (разлагается) | ||
| нерастворимый | |||
| Растворимость | экономно в ТГФ | ||
| Опасности | |||
| Охрана труда и техника безопасности (OHS/OSH): | |||
Основные опасности | Горючий, источник CO | ||
| Опасности | |||
| NFPA 704 (огненный алмаз) | |||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности | ||
| Родственные соединения | |||
Другие катионы | Гексакарбонил хрома Гексакарбонил молибдена | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
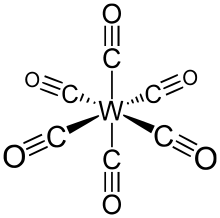
Гексакарбонил вольфрама (также называемый карбонилом вольфрама ) — металлоорганическое соединение с формулой W(CO) 6 . Этот комплекс дал начало первому примеру дигидрогенного комплекса . [2]
Подобно своим аналогам хрома и молибдена , это бесцветное соединение примечательно как летучее, устойчивое на воздухе производное вольфрама в нулевой степени окисления.
Приготовление, свойства и структура
Как и многие карбонилы металлов , W(CO) 6 обычно получают путем «восстановительного карбонилирования», которое включает восстановление галогенида металла в атмосфере оксида углерода . Как описано в обзоре методов 2023 года, «наиболее экономически эффективные пути синтеза гексакарбонилов группы 6 основаны на восстановлении хлоридов металлов (CrCl3 , MoCl5 или WCl6 ) порошками магния, цинка или алюминия... под давлением CO». [3] Соединение относительно стабильно на воздухе. Оно плохо растворяется в неполярных органических растворителях. Карбонил вольфрама широко используется в технике осаждения с помощью электронного пучка — он легко испаряется и разлагается электронным пучком, обеспечивая удобный источник атомов вольфрама. [4]
W(CO) 6 имеет октаэдрическую геометрию, состоящую из шести стержнеобразных лигандов CO , исходящих из центрального атома W с дипольным моментом 0 Дебай .
Реактивность
Все реакции W(CO) 6 начинаются с замещения некоторых лигандов CO в W(CO) 6 . W(CO) 6 ведет себя аналогично Mo(CO) 6 , но имеет тенденцию образовывать соединения, которые кинетически более устойчивы.
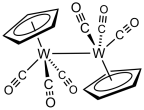
Обработка гексакарбонила вольфрама циклопентадиенидом натрия с последующим окислением полученного NaW(CO) 3 ( C5H5 ) дает димер трикарбонила циклопентадиенилвольфрама . [ 5]
Одним из производных является дигидрогенный комплекс W(CO) 3 [P( C6H11 ) 3 ] 2 (H2 ) . [2]
Три из этих лигандов CO могут быть замещены ацетонитрилом. [6] W(CO) 6 использовался для десульфуризации сероорганических соединений и в качестве предшественника катализаторов для метатезиса алкенов .
Безопасность и обращение
Как и все карбонилы металлов, W(CO) 6 является опасным источником летучих металлов, а также CO.
Ссылки
- ^ Эвен, Дж.; Якушев А.; Дуллманн, CE; Хаба, Х.; Асаи, М.; Сато, ТК; Брэнд, Х.; Ди Нитто, А.; Эйхлер, Р.; Фан, Флорида; Хартманн, В.; Хуанг, М.; Ягер, Э.; Кадзи, Д.; Канайя, Дж.; Канея, Ю.; Хуягбаатар Дж.; Киндлер, Б.; Крац, СП; Криер, Дж.; Кудо, Ю.; Курц, Н.; Ломмель, Б.; Мияшита, С.; Моримото, К.; Морита, К.; Мураками, М.; Нагаме, Ю.; Ниче, Х.; и др. (2014). «Синтез и обнаружение карбонильного комплекса сиборгия». Наука . 345 (6203): 1491–3. Bibcode : 2014Sci...345.1491E. doi : 10.1126/science.1255720. PMID: 25237098. S2CID : 206558746. (требуется подписка)
- ^ ab Kubas, GJ, Металлические дигидрогенные комплексы и σ-связи, Kluwer Academic/Plenum Publishers: Нью-Йорк, 2001
- ^ Бруно, София М.; Валенте, Анабела А.; Гонсалвес, Изабель С.; Пиллингер, Мартин (2023). «Группа 6 карбонильных комплексов N,O,P-лигандов как предшественников высоковалентных металл-оксокатализаторов для эпоксидирования олефинов». Coordination Chemistry Reviews . 478 : 214983. doi : 10.1016/j.ccr.2022.214983 . hdl : 10773/40120 . S2CID 255329673.
- ^ Рэндольф, С.; Фоулкс, Дж.; Рэк, П. (2006). «Фокусированное осаждение и травление, вызванное наночастицами электронного пучка». Критические обзоры твердотельных тел и материаловедения . 31 (3): 55. Bibcode : 2006CRSSM..31...55R. doi : 10.1080/10408430600930438. S2CID 93769658.
- ^ Manning, AR; Hacket, Paul; Birdwhistell, Ralph (1990). Гексакарбонилбис(η 5 -циклопентадиенил)дихром, молибден и вольфрам и их аналоги, M 2 (η 5 -C 5 H 4 R) 2 (CO) 6 (M = Cr, Mo и W; R = H, Me или PhCH 2 ) . Неорганические синтезы . Т. 28. С. 148–149. doi :10.1002/9780470132593.ch39. ISBN 978-0-470-13259-3.
- ^ Кубас, ГДж; ван дер Слёйс, ЛС (1990). «Трикарбонилтрис(нитрил) комплексы Cr, Mo и W». Неорганические синтезы . Т. 28. С. 29–33. doi :10.1002/9780470132593.ch6. ISBN 978-0-470-13259-3.





