Селициклиб
 | |
| Имена | |
|---|---|
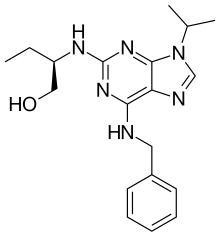
| Предпочтительное название ИЮПАК (2 R )-2-{[6-(Бензиламино)-9-(пропан-2-ил)-9 H -пурин-2-ил]амино}бутан-1-ол | |
| Другие имена Росковитин; CYC202 | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChEMBL | |
| ChemSpider | |
| |
| МеШ | росковитин |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С19Н26Н6О | |
| Молярная масса | 354,458 г·моль −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Seliciclib ( росковитин или CYC202 ) — экспериментальный кандидат на лекарственное средство в семействе фармакологических ингибиторов циклинзависимой киназы (CDK), которые преимущественно ингибируют несколько ферментных мишеней, включая CDK2 , CDK7 и CDK9 , которые изменяют фазу роста или состояние в клеточном цикле обработанных клеток . Seliciclib разрабатывается Cyclacel . Это фаза II, дозозависимое, многоцентровое, рандомизированное, двойное слепое, плацебо-контролируемое исследование.
Целью данного исследования является оценка безопасности увеличения доз росковитина, вводимого перорально в течение 4 циклов по 4 последовательных дня (лечение «включено»), разделенных 3-дневным периодом без лечения (лечение «выключено»), у взрослых пациентов с муковисцидозом, имеющих 2 мутации, вызывающие муковисцидоз, по крайней мере одну мутацию F508del-CFTR, и хронически инфицированных Pseudomonas aeruginosa.
В этом исследовании приняли участие 36 пациентов с муковисцидозом: 24 из них прошли лечение, а 12 вошли в контрольную группу. [1]
Селициклиб исследуется для лечения немелкоклеточного рака легких (НМРЛ), болезни Кушинга , лейкемии , ВИЧ-инфекции , болезни Паркинсона , инфекции простого герпеса , муковисцидоза [2] и механизмов хронических воспалительных заболеваний.
Селициклиб — 2,6,9-замещенный аналог пурина . Его структура в комплексе с CDK2 была определена в 1996 году. [3] Селициклиб ингибирует CDK2/E, CDK2/A, CDK7 и CDK9. [4]
Клинические испытания и лабораторные тесты
Этот раздел необходимо обновить . Пожалуйста ( Январь 2014 ) |
Лечение рака
Было обнаружено, что селициклиб вызывает апоптоз в обработанных раковых клетках немелкоклеточного рака легких (НМРЛ) и других видов рака. Селициклиб ранее прошел клинические испытания фазы IIa у 240 пациентов с НМРЛ в качестве комбинированной дозы с существующими методами лечения первой и второй линии. [4] [5] В текущем исследовании APPRAISE исследуемый препарат проходит клинические испытания фазы IIb в качестве монотерапии НМРЛ у пациентов третьей линии. [6] Побочные эффекты , зарегистрированные в испытаниях фазы I селициклиба для НМРЛ, включали « тошноту , рвоту, временное повышение уровня креатинина в сыворотке и параметров функции печени, а также временную гипокалиемию ». [5]
Иммунологические нарушения
Селициклиб также проходит клинические испытания для В-клеточных лимфом, включая множественную миелому . Было показано, что селициклиб ингибирует транскрипцию, зависимую от РНК-полимеразы II , и снижает регуляцию белка MCL1 . [7] [8]
Было показано, что селициклиб in vitro вызывает апоптоз в нейтрофильных гранулоцитах . [9] Если этот механизм окажется безопасным, надежным и эффективным in vivo , препарат может улучшить лечение хронических воспалительных заболеваний, таких как муковисцидоз и артрит . Обычно их лечат глюкокортикоидами , которые часто имеют серьезные побочные эффекты.
Неврологическая терапия
Было показано, что в нервной системе селициклиб подавляет активацию микроглии [10] и обеспечивает некоторую нейропротекцию в животных моделях церебральной ишемии . [11] [12] Кроме того, он увеличивает противоопухолевую активность темозоломида при лечении мультиформной глиобластомы и рассматривается как возможный терапевтический вариант для глиомы. [13]
Противовирусный эффект
Селициклиб также является возможным противовирусным средством . Он вызывает гибель клеток, инфицированных ВИЧ [14] [15] [16] и предотвращает репликацию вируса простого герпеса . [17] [18]
Производство яйцеклеток
Было показано, что селициклиб вызывает партеногенетическую активацию яиц. Однако он создает аномальные вторые полярные тельца и, следовательно, возможные анеуплоидные зиготы. Активация яиц обычно включает кальциевые колебания, однако этого не происходит с селициклибом. Сециклиб вызывает активацию яиц, ингибируя протеинкиназы, что приводит к инактивации фактора, способствующего созреванию (MPF). [19]
гипертрофия почек
Селициклиб снижает гипертрофию почек на 45% после нефрэктомии 5/6. [20]
Побочные эффекты
Вызывает серьезные побочные эффекты, которые невозможно переносить ежедневно. Побочные эффекты включают гипокалиемию и повышение уровня печеночных ферментов. [21] Из-за этих побочных эффектов Seliciclib не был одобрен USFDA.
Ссылки
- ^ «Фаза II, многоцентровое, двойное слепое, плацебо-контролируемое исследование с целью оценки безопасности и эффектов (R)-росковитина у взрослых пациентов с муковисцидозом, имеющих 2 мутации, вызывающие муковисцидоз, по крайней мере одну мутацию F508del-CFTR, и хронически инфицированных Pseudomonas Aeruginosa, исследование с участием 36 пациентов с муковисцидозом (24 прошедших лечение, 12 контрольных). ROSCO-CF». 11 декабря 2018 г.
- ^ Noel S, Faveau C, Norez C, Rogier C, Mettey Y, Becq F (2006). «Открытие производных пирроло[2,3-b]пиразинов как субмикромолярных активаторов сродства дикого типа, G551D и F508del кистозного фиброза трансмембранных регуляторов проводимости хлоридных каналов». J Pharmacol Exp Ther . 319 (1): 349–59 . doi :10.1124/jpet.106.104521. PMID 16829626. S2CID 1554921.
- ^ De Azevedo WF, Leclerc S, Meijer L, Havlicek L, Strnad M, Kim SH (1997). «Ингибирование циклин-зависимых киназ пуриновыми аналогами: кристаллическая структура человеческого cdk2 в комплексе с росковитином». Eur J Biochem . 243 ( 1– 2): 518– 526. doi : 10.1111/j.1432-1033.1997.0518a.x . PMID 9030780.
- ^ ab "Cyclacel начинает рандомизированное исследование фазы IIb селициклиба для ранее леченного немелкоклеточного рака легких". BIOWIRE. 29 июня 2006 г.
- ^ ab "Cyclacel сообщает промежуточные данные по фазе IIa Seliciclib на ASCO 2005". Business Wire. 15 мая 2005 г.
- ^ "Cyclacel Pharmaceuticals сообщает о финансовых результатах за второй квартал 2006 года". Business Wire. 14 августа 2006 г.
- ^ MacCallum DE, Melville J, Frame S, Watt K, Anderson S, Gianella-Borradori A, Lane DP, Green SR (2005). «Селициклиб (CYC202, R-Росковитин) вызывает гибель клеток множественной миеломы путем ингибирования транскрипции, зависящей от РНК-полимеразы II, и снижения регуляции Mcl-1». Cancer Research . 65 (12): 5399– 5407. doi :10.1158/0008-5472.CAN-05-0233. PMID 15958589.
- ^ Ноопур Радже, Шаджи Кумар, Теру Хидэсима, Альдо Роккаро, Кенджи Ишицука, Хироши Ясуи, Норихико Сираиси, Дхарминдер Чаухан, Никхил К. Мунши, Саймон Р. Грин, Кеннет К. Андерсон (1 августа 2005 г.). «Селициклиб (CYC202 или R-росковитин), низкомолекулярный ингибитор циклин-зависимой киназы, опосредует активность посредством подавления Mcl-1 при множественной миеломе». Кровь . 106 (3): 1042–1047 . doi :10.1182/blood-2005-01-0320. ПМК 1895150 . ПМИД 15827128.
- ^ Rossi AG, Sawatzky DA, Walker A, Ward C, Sheldrake TA, Riley NA, Caldicott A, Martinez-Losa M, Walker TR, Duffin R, Gray M, Crescenzi E, Martin MC, Brady HJ, Savill JS, Dransfield I, Haslett C (2006). «Ингибиторы циклинзависимой киназы усиливают разрешение воспаления, способствуя апоптозу воспалительных клеток». Nature Medicine . 12 (9): 1056–1064 . doi :10.1038/nm1468. PMID 16951685. S2CID 5875865.
- ^ Томов Н., Сурчев Л., Виденманн К., Дёбрёсси М., Никха Г. (август 2019 г.). «Росковитин, экспериментальный ингибитор CDK5, вызывает замедленное подавление микроглиального, но не астроглиального рекрутинга вокруг внутримозговых дофаминергических трансплантатов». Experimental Neurology . 318 : 135–144 . doi :10.1016/j.expneurol.2019.04.013. PMID 31028828. S2CID 129946710.
- ^ Menn B, Bach S, Blevins TL, Campbell M, Meijer L, Timsit S (2010-08-12). Manzoni OJ (ред.). "Отсроченное лечение системным (S)-росковитином обеспечивает нейропротекцию и ингибирует in vivo увеличение активности CDK5 в моделях инсульта у животных". PLOS ONE . 5 (8): e12117. Bibcode :2010PLoSO...512117M. doi : 10.1371/journal.pone.0012117 . ISSN 1932-6203. PMC 2920814 . PMID 20711428.
- ^ Rousselet E, Létondor A, Menn B, Courbebaisse Y, Quillé ML, Timsit S (июнь 2018 г.). «Устойчивая доставка (S)-росковитина способствует нейропротекции, связанной с функциональным восстановлением и уменьшением отека мозга в рандомизированном слепом исследовании очаговой церебральной ишемии». Журнал мозгового кровотока и метаболизма . 38 (6): 1070– 1084. doi :10.1177/0271678X17712163. ISSN 0271-678X. PMC 5998998. PMID 28569655 .
- ^ Pandey V, Ranjan N, Narne P, Babu PP (2019-03-21). «Росковитин эффективно усиливает противоопухолевую активность темозоломида in vitro и in vivo, опосредованную повышенной аутофагией и апоптозом, зависимым от каспазы-3». Scientific Reports . 9 (1): 5012. Bibcode :2019NatSR...9.5012P. doi :10.1038/s41598-019-41380-1. ISSN 2045-2322. PMC 6428853 . PMID 30899038.
- ^ Садаи MR, Майнер R, Донигер J (январь 2004 г.). «Новый подход к разработке лекарств против ВИЧ: адаптация ненуклеозидных противораковых химиотерапевтических средств». Antiviral Research . 61 (1): 1– 18. doi :10.1016/j.antiviral.2003.09.004. PMID 14670589.
- ^ Pumfery A, de la Fuente C, Berro R, Nekhai S, Kashanchi F, Chao SH (2006). «Потенциальное использование фармакологических ингибиторов циклинзависимой киназы в качестве терапевтических средств против ВИЧ». Curr Pharm Des . 12 (16): 1949– 61. doi :10.2174/138161206777442083. PMID 16787240.
- ^ Agbottah E, de La Fuente C, Nekhai S, Barnett A, Gianella-Borradori A, Pumfery A, Kashanchi F (28 января 2005 г.). "Противовирусная активность CYC202 в клетках, инфицированных ВИЧ-1". J. Biol. Chem . 280 (4): 3029– 42. doi : 10.1074/jbc.M406435200 . PMID 15531588.
- ^ Schang LM, Rosenberg A, Schaffer PA (2000). «Росковитин, специфический ингибитор клеточных циклин-зависимых киназ, ингибирует синтез ДНК вируса простого герпеса в присутствии вирусных ранних белков». J. Virol . 74 (5): 2107– 20. doi :10.1128/JVI.74.5.2107-2120.2000. PMC 111691 . PMID 10666240.
- ^ Diwan P, Lacasse JJ, Schang LM (2004). «Росковитин ингибирует активацию промоторов в геномах вируса простого герпеса типа 1 независимо от факторов, специфичных для промотора». J. Virol . 78 (17): 9352– 9365. doi :10.1128/JVI.78.17.9352-9365.2004. PMC 506918 . PMID 15308730.
- ^ Дори М., Галас С. (1994). «Циклинзависимые протеинкиназы и контроль деления клеток». FASEB J. 8 ( 14): 1114– 1121. doi : 10.1096/fasebj.8.14.7958616 . PMID 7958616. S2CID 3069118.
- ^ Ю, Алан С.Л., Чертоу, Гленн М., Люйкс, Валери А., Марсден, Филип А., Скорецки, Карл, Таал, Маартен В., ред. (25 сентября 2019 г.). Бреннер и Ректор - почка. Elsevier Науки о здоровье. ISBN 978-0-323-55085-7. OCLC 1122857051.
- ^ Ле Турно С, Фавр С, Лоуренс В, Дельбальдо С, Вера К, Жирре В, Чиао Дж, Армор С, Фрейм S, Грин С.Р., Джанелла-Боррадори А, Диерас В, Раймонд Э (декабрь 2010 г.). «Оценка I фазы селициклиба (R-росковитина), нового перорального ингибитора циклин-зависимой киназы, у пациентов с запущенными злокачественными новообразованиями». Европейский журнал рака . 46 (18): 3243–3250 . doi :10.1016/j.ejca.2010.08.001. ISSN 1879-0852. ПМИД 20822897.



