Органоиридиевая химия



Химия органоиридия - это химия металлоорганических соединений , содержащих химическую связь иридий - углерод . [2] Органоиридиевые соединения имеют отношение ко многим важным процессам, включая гидрирование олефинов и промышленный синтез уксусной кислоты. Они также представляют большой академический интерес из-за разнообразия реакций и их значимости для синтеза тонких химикатов. [3]
Классификация на основе основных степеней окисления
Органические соединения иридия имеют много общих характеристик с родием, но в меньшей степени с кобальтом. Иридий может существовать в степенях окисления от -III до +V, но иридий(I) и иридий(III) являются более распространенными. Соединения иридия(I) (конфигурация d 8 ) обычно встречаются с квадратной плоской или тригональной бипирамидальной геометрией, тогда как соединения иридия(III) (конфигурация d 6 ) обычно имеют октаэдрическую геометрию. [3]
Иридий(0)
Комплексы иридия(0) представляют собой бинарные карбонилы, основным членом которых является додекакарбонил тетраиридия , Ir 4 (CO) 12 . В отличие от родственного Rh 4 (CO) 12 , все лиганды CO являются концевыми в Ir 4 (CO) 12 , аналогично разнице между Fe 3 (CO) 12 и Ru 3 (CO) 12 . [4]
Иридий(I)
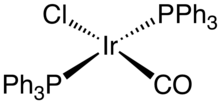
Известным примером является комплекс Васки , бис(трифенилфосфин)иридий карбонилхлорид. Хотя комплексы иридия(I) часто являются полезными гомогенными катализаторами , комплекс Васки таковым не является. Скорее, он является знаковым в разнообразии своих реакций. Другие распространенные комплексы включают Ir 2 Cl 2 (циклооктадиен) 2 , димер хлоробис(циклооктен)иридия , аналог катализатора Уилкинсона , IrCl(PPh 3 ) 3 ), подвергается ортометаллированию:
- IrCl ( PPh3 ) 3 → HIrCl ( PPh3 ) 2 ( PPh2C6H4 )
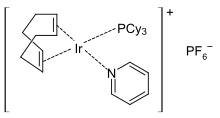
Это различие между RhCl(PPh 3 ) 3 и IrCl(PPh 3 ) 3 отражает в целом большую тенденцию иридия подвергаться окислительному присоединению . Подобную тенденцию демонстрируют RhCl(CO)(PPh 3 ) 2 и IrCl(CO)(PPh 3 ) 2 , только последний окислительно присоединяет O 2 и H 2 . [5] Олефиновые комплексы димер хлоробис(циклооктен)иридия и димер хлорида циклооктадиена иридия часто используются в качестве источников «IrCl», используя лабильность лигандов алкена или их восприимчивость к удалению путем гидрирования. Катализатор Крэбтри ([Ir(P(C 6 H 11 ) 3 )(пиридин)(циклооктадиен)]PF 6 ) является универсальным гомогенным катализатором для гидрирования алкенов. [6]
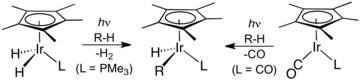
(η 5 - Cp )Ir(CO) 2 окислительно присоединяет связи CH при фотолитической диссоциации одного лиганда CO.
Иридий(II)
Как и в случае с родием(II), иридий(II) встречается редко. Одним из примеров является иридоцен, IrCp 2 . [7] Как и в случае с родоценом , иридоцен димеризуется при комнатной температуре. [8]
Иридий(III)
Иридий обычно поставляется в коммерческих целях в степенях окисления Ir(III) и Ir(IV). Важными исходными реагентами являются гидратированный трихлорид иридия и гексахлориридат аммония . Эти соли восстанавливаются при обработке CO, водородом и алкенами. Показательным является карбонилирование трихлорида: IrCl 3 (H 2 O) x + 3 CO → [Ir(CO) 2 Cl 2 ] − + CO 2 + 2 H + + Cl − + (x-1) H 2 O
Многие органоиридиевые (III) соединения генерируются из димера пентаметилциклопентадиенил иридиевого дихлорида . Многие из производных характеризуются кинетически инертными циклометаллированными лигандами. [9] Связанные полусэндвичевые комплексы были центральными в развитии активации CH . [10] [11]

Химия органоиридиевых соединений сыграла центральную роль в развитии активации CH , два примера которой приведены здесь.
Иридий(V)
Степень окисления выше III более распространена для иридия, чем для родия. Обычно они характеризуются лигандами сильного поля. Одним из часто цитируемых примеров является оксотримезитиллиридий(V). [12]
Использует
Доминирующее применение органоиридиевых комплексов – в качестве катализатора в процессе Cativa для карбонилирования метанола с целью получения уксусной кислоты . [13]

Оптические приборы и фоторедокс
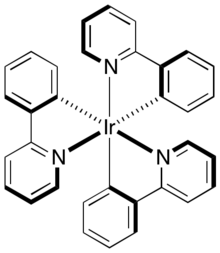
Комплексы иридия, такие как циклометаллированные, полученные из 2-фенилпиридинов, используются в качестве фосфоресцирующих органических светодиодов . [14] Родственные комплексы являются фотоокислительно-восстановительными катализаторами .
Потенциальные приложения
Комплексы иридия очень активны для гидрирования как напрямую, так и через трансферное гидрирование . Асимметричные версии этих реакций широко изучены.
Многие полусэндвичевые комплексы были исследованы как возможные противораковые препараты. Связанные комплексы являются электрокатализаторами для преобразования диоксида углерода в формиат. [9] [15] В академических лабораториях комплексы иридия широко изучаются, поскольку его комплексы способствуют активации CH , но такие реакции не используются ни в одном коммерческом процессе.
Смотрите также
Ссылки
- ^ SM Bischoff; RA Periana (2010). Кислород и углерод связанные ацетилацетонато иридиевые(III) комплексы . Неорганические синтезы. Т. 35. С. 173. doi : 10.1002/9780470651568 . ISBN 978-0-470-65156-8.
- ^ Синтез металлоорганических соединений: практическое руководство Сансиро Комия Ред. С. Комия, М. Хурано 1997
- ^ ab Crabtree, Robert H. (2005). Металлоорганическая химия переходных металлов (4-е изд.). США: Wiley-Interscience. ISBN 0-471-66256-9.
- ^ Гринвуд, NN; Эрншоу, А. (1997). Химия элементов (2-е изд.). Oxford: Butterworth-Heinemann. стр. 1113– 1143, 1294. ISBN 0-7506-3365-4.
- ^ Васка, Лаури ; ДиЛуцио, Дж. В. (1961). «Карбонильные и гидридо-карбонильные комплексы иридия по реакции со спиртами. Гидридокомплексы по реакции с кислотой». Журнал Американского химического общества . 83 (12): 2784– 2785. doi :10.1021/ja01473a054.
- ^ Крэбтри, Роберт Х. (1979). «Соединения иридия в катализе». Acc. Chem. Res . 12 (9): 331– 337. doi :10.1021/ar50141a005.
- ^ Келлер, HJ; Ваверсик, Х. (1967). «Spektroskopische Untersuruchungen an Komplexverbindungen. VI. ЭПР-спектр фон (C 5 H 5 ) 2 Rh и (C 5 H 5 ) 2 Ir». Дж. Органомет. хим. (на немецком языке). 8 (1): 185–188 . doi :10.1016/S0022-328X(00)84718-X.
- ^ Фишер, Э.О .; Ваверсик, Х. (1966). «Убер ароматенкомплекс фон Металлен. LXXXVIII. Убер мономеры и димеры дициклопентадиенилродия и дициклопентадиенилиридия и убер Ein Neues Verfahren Zur Darstellung Ungeladener Metall-Aromaten-Komplexe». Дж. Органомет. хим. (на немецком языке). 5 (6): 559–567 . doi :10.1016/S0022-328X(00)85160-8.
- ^ ab Liu, Zhe; Sadler, Peter J. (2014 ) . «Комплексы органоиридиевые: противораковые агенты и катализаторы». Accounts of Chemical Research . 47 (4): 1174– 1185. doi :10.1021/ar400266c. PMC 3994614. PMID 24555658.
- ^ Эндрю Х. Янович; Роберт Г. Бергман (1982). «Углерод-водородная активация в насыщенных углеводородах: прямое наблюдение M + R−H → M(R)(H)». J. Am. Chem. Soc . 104 : 352– 354. doi :10.1021/ja00365a091.
- ^ Грэм, Уильям АГ (1982). «Окислительное присоединение связей углерода и водорода неопентана и циклогексана к фотохимически полученному комплексу иридия (I)». Журнал Американского химического общества . 104 (13): 3723– 3725. doi :10.1021/ja00377a032.
- ^ Хей-Мазервелл, Р. С.; Уилкинсон, Г.; Хуссейн-Бейтс, Б.; Хёрстхаус, М. Б. (1993). «Синтез и рентгеновская кристаллическая структура оксотримезитил-иридия (V)». Polyhedron . 12 (16): 2009– 2012. doi :10.1016/S0277-5387(00)81474-6.
- ^ Cheung, Hosea; Tanke, Robin S.; Torrence, G. Paul (2000). "Уксусная кислота". Энциклопедия промышленной химии Ульмана . Wiley. doi :10.1002/14356007.a01_045. ISBN 3-527-30673-0.
- ^ Jaesang Lee; Hsiao-Fan Chen; Thilini Batagoda; Caleb Coburn; Peter I. Djurovich; Mark E. Thompson; Stephen R. Forrest (2016). «Deep Blue Phosphorescent Organic Light-Emitting Diodes with Very High Brightness and Efficiency». Nature Materials . 15 ( 1– 2): 92– 98. Bibcode : 2016NatMa..15...92L. doi : 10.1038/nmat4446. PMID 26480228.
- ^ Maenaka, Yuta; Suenobu, Tomoyoshi; Fukuzumi, Shunichi (2012). «Каталитическое взаимопревращение водорода и муравьиной кислоты при температуре окружающей среды и давлении». Energy & Environmental Science . 5 (6): 7360– 7367. doi :10.1039/c2ee03315a.