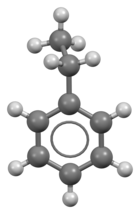
Этилбензол
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Этилбензол | |||
| Другие имена Этилбензол; Фенилэтан; альфа -метилтолуол; ЭБ | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| Сокращения | ЭБ | ||
| 1901871 | |||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Информационная карта ECHA | 100.002.591 | ||
| КЕГГ | |||
CID PubChem |
| ||
| Номер RTECS |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С 8 Н 10 | |||
| Молярная масса | 106,168 г·моль −1 | ||
| Появление | бесцветная жидкость | ||
| Запах | ароматический [1] | ||
| Плотность | 0,8665 г/мл | ||
| Температура плавления | −95 °C (−139 °F; 178 K) | ||
| Точка кипения | 136 °C (277 °F; 409 К) | ||
| 0,015 г/100 мл (20 °C) | |||
| лог P | 3.27 | ||
| Давление пара | 9,998 мм рт.ст. | ||
| -77,20·10 −6 см 3 /моль | |||
Показатель преломления ( nD ) | 1.495 | ||
| Вязкость | 0,669 сП при 20 °C | ||
| 0,58 Д [2] | |||
| Термохимия | |||
Теплоемкость ( С ) | 1,726 Дж/(гК) | ||
| Опасности | |||
| Охрана труда и техника безопасности (OHS/OSH): | |||
Основные опасности | Легковоспламеняющийся | ||
| Маркировка СГС : | |||
    | |||
| Опасность | |||
| Н225 , Н304 , Н320 , Н332 , Н335 , Н336 , Н351 , Н360 , Н373 , Н400 , Н411 | |||
| Р201 , Р202 , Р210 , Р233 , Р240 , Р241 , Р242 , Р243 , Р260 , Р261 , Р264 , Р271 , Р273 , Р280 , Р281 , Р301+Р310 , Р303+Р361+Р353 , Р304+Р312 , Р304+Р340 , Р305+Р351+Р338 , Р308+Р313 , Р312 , Р314 , Р331 , Р337+Р313 , Р370+Р378 , Р391 , Р403+Р233 , Р403+Р235 , Р405 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 22,22 °C (72,00 °F; 295,37 К) | ||
| 430 °C (806 °F; 703 К) | |||
| Пределы взрывоопасности | 1–7,8% | ||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD 50 ( средняя доза ) | 5460 мг/кг | ||
LC Lo ( самый низкий опубликованный ) | 4000 ppm (крыса, 4 часа) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (допустимый) | TWA 100 частей на миллион (435 мг/м 3 ) [1] | ||
РЕЛ (рекомендуется) | TWA 100 ppm (435 мг/м 3 ) ST 125 ppm (545 мг/м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 800 частей на миллион [1] | ||
| Родственные соединения | |||
Родственные ароматические углеводороды | стирол , толуол | ||
Родственные соединения | бензол этилциклогексан | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
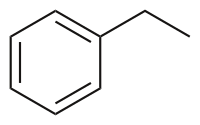
Этилбензол — органическое соединение с формулой C6H5CH2CH3 . Это легковоспламеняющаяся бесцветная жидкость с запахом, похожим на запах бензина. Этот моноциклический ароматический углеводород важен в нефтехимической промышленности как промежуточный продукт реакции при производстве стирола, предшественника полистирола , распространенного пластикового материала . В 2012 году более 99 % произведенного этилбензола было использовано при производстве стирола .
Возникновение и применение
Этилбензол встречается в природе в каменноугольной смоле и нефти . [4]
Доминирующее применение этилбензола - его роль в качестве промежуточного продукта в производстве полистирола. Каталитическая дегидрогенизация этилбензола дает водород и стирол :
- С
6ЧАС
5Ч.
2Ч.
3 → С6Н5СН = СН2 + Н
2
По состоянию на май 2012 года более 99% всего производимого этилбензола используется для этой цели.
Гидропероксид этилбензола , реагент и инициатор радикальной реакции, получают путем автоокисления этилбензола:
- С6Н5СН2СН3 + О2 → С6Н5СН ( О2Н ) СН3
Ниша использует
Этилбензол добавляют в бензин в качестве антидетонационной присадки для снижения стука двигателя и повышения октанового числа. Этилбензол часто встречается в других продуктах, включая пестициды , ацетат целлюлозы, синтетический каучук , краски и чернила. [4] Используемый при добыче природного газа, этилбензол может закачиваться в землю.
Производство
Этилбензол производится в больших масштабах путем соединения бензола и этилена в химической реакции, катализируемой кислотой :
- С
6ЧАС
6+ С
2ЧАС
4→ С
6ЧАС
5Ч.
2Ч.
3
В 2012 году более 99% этилбензола было произведено таким образом. [ необходима цитата ]
Небольшие количества этилбензола извлекаются из смеси ксилолов путем суперфракционирования, являющегося продолжением процесса дистилляции . [5]
В 1980-х годах процесс на основе цеолита с использованием алкилирования в паровой фазе обеспечивал более высокую чистоту и выход. Затем был внедрен жидкофазный процесс с использованием цеолитных катализаторов . Это обеспечивает низкое соотношение бензола к этилену, уменьшая размер необходимого оборудования и снижая производство побочных продуктов. [6]
Промышленные аварии
3 июня 2014 года в голландской промышленной зоне Мурдейк произошел взрыв . Это произошло в химическом реакторе компании Shell , который перегрелся из-за экзотермической реакции между катализатором на основе оксида металла и этилбензолом. [7]
Влияние на здоровье
Острая токсичность этилбензола низкая, LD 50 составляет около 4 граммов на килограмм веса тела. Долгосрочная токсичность и канцерогенность неоднозначны. [8] Чувствительность глаз и горла может возникнуть при высоком уровне воздействия этилбензола в воздухе. При более высоком уровне воздействия этилбензол может вызвать головокружение. [4] Попав в организм, этилбензол биоразлагается до 1-фенилэтанола, ацетофенона , фенилглиоксиловой кислоты , миндальной кислоты , бензойной кислоты и гиппуровой кислоты . [8] Воздействие этилбензола можно определить путем тестирования продуктов распада в моче .
По состоянию на сентябрь 2007 года Агентство по охране окружающей среды США (EPA) определило, что питьевая вода с концентрацией 30 частей на миллион (ppm) в течение одного дня или 3 ppm в течение десяти дней, как ожидается, не будет иметь никаких неблагоприятных последствий для детей. Пожизненное воздействие 0,7 ppm этилбензола, как ожидается, также не будет иметь никаких неблагоприятных последствий. Управление по охране труда и технике безопасности США (OSHA) ограничивает воздействие на работников в среднем 100 ppm для 8-часового рабочего дня, 40-часовой рабочей недели. [4]
Этилбензол классифицируется как возможный канцероген Международным агентством по изучению рака (IARC), однако EPA не определило этилбензол как канцероген. Национальная токсикологическая программа провела исследование ингаляции на крысах и мышах. Воздействие этилбензола привело к увеличению частоты опухолей почек и яичек у самцов крыс и тенденциям увеличения опухолей почек у самок крыс, опухолей легких у самцов мышей и опухолей печени у самок мышей.
Как и все органические соединения, пары этилбензола образуют взрывоопасную смесь с воздухом. [5] При транспортировке этилбензол классифицируется как легковоспламеняющаяся жидкость класса 3, группы упаковки II. [5]
Воздействие на окружающую среду
Этилбензол в основном встречается в виде пара в воздухе, так как он может легко перемещаться из воды и почвы. [4] Медианная концентрация 0,62 частей на миллиард (ppb) была обнаружена в городском воздухе в 1999 году. [9] Исследование, проведенное в 2012 году, показало, что в сельском воздухе медианная концентрация составила 0,01 ppb, а в помещении медианная концентрация составила 1,0 ppb. Он также может выделяться в воздух при сжигании угля , газа и нефти . Использование этилбензола в промышленности способствует образованию паров этилбензола в воздухе. Примерно через три дня нахождения в воздухе с помощью солнечного света другие химические вещества расщепляют этилбензол на химические вещества, которые можно найти в смоге . [4] Поскольку он нелегко связывается с почвой, он также может легко перемещаться в грунтовые воды . В поверхностных водах он распадается при реакции с химическими веществами, естественным образом содержащимися в воде. [10] Обычно этилбензол не содержится в питьевой воде, однако его можно обнаружить в колодцах с питьевой водой для жилых домов, если колодцы находятся вблизи свалок, подземных топливных резервуаров, которые протекают, или свалок. [4]
По состоянию на 2012 год, согласно Директиве ЕС об опасных веществах, этилбензол не классифицируется как опасный для окружающей среды. [5]
Этилбензол входит в состав табачного дыма . [11]
Биодеградация
Некоторые штаммы грибка Cladophialophora могут расти на этилбензоле. [12] Бактерия Aromatoleum fragranceum EbN1 была обнаружена благодаря своей способности расти на этилбензоле. [13]
Ссылки
- ^ abcd Карманный справочник NIOSH по химическим опасностям. "#0264". Национальный институт охраны труда и здоровья (NIOSH).
- ↑ Справочник по химии Ланге (15-е изд.). 1999.
- ^ "Этилбензол". Концентрации, представляющие немедленную опасность для жизни или здоровья (IDLH) . Национальный институт охраны труда (NIOSH).
- ^ abcdefg "Ethylbenzene ToxFAQs" (PDF) . Агентство по регистрации токсичных веществ и заболеваний . Получено 21 мая 2018 г. .
- ^ abcd "ЭТИЛБЕНЗОЛ: РУКОВОДСТВО ПО ОХРАНЕ ОКРУЖАЮЩЕЙ СРЕДЫ, ЗДОРОВЬЯ И БЕЗОПАСНОСТИ". CEFIC. Архивировано из оригинала 19 сентября 2014 года . Получено 14 февраля 2013 года .
- ^ "Процесс производства и изготовления этилбензола (ЭБ)". PIERS . Получено 14 февраля 2013 г. .
- ^ Резюме оболочки moerdijk onderzoeksraad.nl, июль 2018 г.
- ^ ab Винсент А. Уэлч, Кевин Дж. Фэллон, Хайнц-Питер Гельбке «Этилбензол», Энциклопедия промышленной химии Ульмана , Wiley-VCH, Weinheim, 2005. doi : 10.1002/14356007.a10_035.pub2
- ^ "Веб-сайт Technology Transfer Network Air Toxics: Ethylbenzene". Агентство по охране окружающей среды США . Получено 13 февраля 2013 г.
- ^ "Этилбензол". eco-usa.net. Архивировано из оригинала 25 декабря 2012 года . Получено 12 февраля 2013 года .
- ^ Талхаут, Рейнскье; Шульц, Томас; Флорек, Ева; Ван Бентем, Ян; Вестер, Пит; Опперхейзен, Антон (2011). «Опасные соединения в табачном дыме». Международный журнал экологических исследований и общественного здравоохранения . 8 (12): 613–628. дои : 10.3390/ijerph8020613 . ISSN 1660-4601. ПМК 3084482 . ПМИД 21556207.
- ^ Francesc X. PRENAFETA-BOLDU; Andrea KUHN; Dion MAM LUYKX; Heidrun ANKE; Johan W. van GROENESTIJN; Jan AM de BONT (апрель 2001 г.). «Выделение и характеристика грибов, растущих на летучих ароматических углеводородах как на единственном источнике углерода и энергии». Mycological Research . 105 (4): 477–484. doi :10.1017/s0953756201003719.
- ^ Рабус, Р.; Виддель, Ф. (1995). «Анаэробная деградация этилбензола и других ароматических углеводородов новыми денитрифицирующими бактериями». Архив микробиологии . 163 (2): 96–103. doi :10.1007/s002030050177. PMID 7710331.
- Национальная токсикологическая программа. Исследования токсикологии и канцерогенеза этилбензола (CAS № 100-41-4) на крысах F344/N и мышах B6C3F1 (исследования при вдыхании). TR № 466. Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Национальные институты здравоохранения, Бетесда, Мэриленд. 1999.
Внешние ссылки
- Национальный реестр загрязняющих веществ - Информационный листок об этибензоле
- Банк данных опасных веществ NLM – Этилбензол
- База данных химических веществ Агентства по охране окружающей среды
- База данных химикатов Intox
- Агентство по регистрации токсичных веществ и заболеваний
- CDC - Карманный справочник NIOSH по химическим опасностям