Регулятор трансмембранной проводимости при муковисцидозе
| ЦФТР | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
  | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | CFTR , ABC35, ABCC7, CF, CFTR/MRP, MRP7, TNR-dJ760C5.1, регулятор трансмембранной проводимости при муковисцидозе, регулятор трансмембранной проводимости при CF | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | ОМИМ : 602421; МГИ : 88388; Гомологен : 55465; GeneCards : CFTR; OMA :CFTR — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер ЕС | 5.6.1.6 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Регулятор трансмембранной проводимости при муковисцидозе ( CFTR ) — это мембранный белок и анионный канал у позвоночных, который кодируется геном CFTR . [5] [6]
Генетик Лап-Чи Цуй и его команда в 1989 году идентифицировали ген CFTR как ген, связанный с муковисцидозом ( муковисцидозом ). [7]
Ген CFTR кодирует белок ионного канала класса ABC-транспортера , который проводит ионы хлорида [8] и бикарбоната через мембраны эпителиальных клеток . Мутации гена CFTR , влияющие на функцию анионных каналов, приводят к нарушению регуляции транспорта эпителиальной выстилающей жидкости (слизи) в легких, поджелудочной железе и других органах, что приводит к муковисцидозу . Осложнения включают сгущение слизи в легких с частыми респираторными инфекциями и недостаточность поджелудочной железы, приводящую к недоеданию и диабету . [9] Эти состояния приводят к хронической инвалидности и сокращению продолжительности жизни. У пациентов мужского пола прогрессирующая обструкция и разрушение развивающихся семявыносящих протоков (семенного канатика) и придатка яичка, по-видимому, являются результатом аномальной интралюминальной секреции, [10] вызывающей врожденное отсутствие семявыносящих протоков и мужское бесплодие, и, как выяснилось, связаны с дисбалансом жирных кислот . [11]
Тканевая и внутриклеточная локализация
CFTR обнаружен в эпителиальных клетках многих органов, включая легкие , печень , поджелудочную железу , пищеварительный тракт, а также женский половой тракт [12] и мужской половой тракт, включая яички, клетки Сертоли, сперматозоиды [13] , придаток яичка [14] и семявыносящий проток [15] .
В дыхательных путях легких CFTR наиболее сильно экспрессируется редкими специализированными клетками, называемыми легочными ионоцитами . [16] [17] [18] В коже CFTR сильно экспрессируется в сальных и эккриновых потовых железах. [19] В эккриновых железах CFTR расположен на апикальной мембране эпителиальных клеток, которые составляют протоки этих потовых желез. [19]
Обычно белок обеспечивает перемещение ионов хлорида , бикарбоната и тиоцианата [20] (с отрицательным зарядом) из эпителиальной клетки в жидкость и слизь поверхности дыхательных путей . Положительно заряженные ионы натрия следуют пассивно, увеличивая общую концентрацию электролитов в слизи, что приводит к перемещению воды из клетки посредством осмоса .
В эпителиальных клетках с подвижными ресничками, выстилающих бронхи и яйцеводы, CFTR расположен на апикальной клеточной мембране, но не на ресничках. [12] Напротив, ENaC (эпителиальный натриевый канал) расположен по всей длине ресничек. [12]
В потовых железах дефектный CFTR приводит к снижению транспорта хлорида натрия и тиоцианата натрия [21] в резорбтивном протоке и, следовательно, к более соленому поту. Это основа клинически важного потового теста на кистозный фиброз, часто используемого в диагностических целях с генетическим скринингом. [22]
Ген

Ген, кодирующий человеческий белок CFTR, находится на хромосоме 7 , на длинном плече в позиции q31.2. [6] от пары оснований 116 907 253 до пары оснований 117 095 955. Ортологи CFTR [23] встречаются у челюстных позвоночных . [24] [ проверка не удалась ]
Каждый человек наследует две копии гена CFTR (муковисцидозный трансмембранный регулятор проводимости). Однако некоторые из унаследованных копий были изменены. До сих пор ген CFTR был связан с более чем 700 различными мутациями. Человек с CF наследует две дефектные копии гена CFTR . Эти мутации могут быть гетерозиготными, то есть они включают две разные мутации, и гомозиготными, то есть они включают одну и ту же мутацию. [25] Delta F508 является наиболее распространенной мутацией, на которую приходится более 70% всех мутаций. Те, кто гомозиготен по Delta F508, обычно страдают недостаточностью поджелудочной железы. [26]
Ген CFTR использовался у животных в качестве филогенетического маркера ядерной ДНК . [23] Большие геномные последовательности этого гена использовались для изучения филогении основных групп млекопитающих , [27] и подтвердили группировку плацентарных отрядов в четыре основные клады: Xenarthra , Afrotheria , Laurasiatheria и Euarchonta plus Glires .
Мутации
Описано около 1000 мутаций , вызывающих муковисцидоз . [28] Наиболее распространенная мутация, DeltaF508 (ΔF508), в первую очередь известна как мутация процессинга, которая возникает в результате делеции (Δ) трех нуклеотидов, что приводит к потере аминокислоты фенилаланина (F) в 508-й позиции белка. [29] В результате белок не сворачивается нормально и быстрее деградирует. Подавляющее большинство мутаций встречаются редко. Распределение и частота мутаций различаются среди разных популяций, что имеет значение для генетического скрининга и консультирования.
Открытие лекарств для терапии муковисцидоза у всех пациентов осложнено из-за большого количества мутаций, вызывающих заболевание. В идеале, для скрининга широкоактивных кандидатов на лекарства требуется библиотека клеточных линий и клеточных анализов, соответствующих всем мутантам. Методы клеточной инженерии, включая флуорогенные олигонуклеотидные сигнальные зонды, могут использоваться для обнаружения и изоляции клональных клеточных линий для каждого мутанта. [30]
Мутации состоят из замен, дупликаций, делеций или сокращений в гене CFTR . Это может привести к белкам, которые не могут функционировать, работать менее эффективно, быстрее разрушаться или присутствовать в недостаточных количествах. [31]
Была выдвинута гипотеза, что мутации в гене CFTR могут давать селективное преимущество гетерозиготным особям. Клетки, экспрессирующие мутантную форму белка CFTR, устойчивы к вторжению бактерии Salmonella typhi , возбудителя брюшного тифа , а мыши, несущие одну копию мутантного CFTR, устойчивы к диарее, вызванной холерным токсином. [32]
Наиболее распространенными мутациями, вызывающими муковисцидоз и недостаточность поджелудочной железы у людей, являются: [33]
| Название варианта кДНК (упорядочено от 5' к 3') | Название варианта белка | Вариант устаревшего имени | rsID | # аллели в CFTR2 | Частота аллелей в CFTR2 | % недостаточности поджелудочной железы | Окончательное определение варианта (июль 2020 г.) |
|---|---|---|---|---|---|---|---|
| c.1521_1523delCTT | стр.Phe508del | F508del | rs113993960 | 99061 | 0,69744 | 98% | вызывающий муковисцидоз |
| ок.1624Г>Т | п.Gly542X | G542X | rs113993959 | 3610 | 0,02542 | 98% | вызывающий муковисцидоз |
| ок.1652г>А | п.Gly551Asp | Г551Д | rs75527207 | 2986 | 0,02102 | 96% | вызывающий муковисцидоз |
| c.3909C>G | п.Asn1303Lys | Н1303К | rs80034486 | 2246 | 0,01581 | 98% | вызывающий муковисцидоз |
| с.350Г>А | p.Arg117Его | Р117Х | rs78655421 | 1854 | 0,01305 | 23% | Различные клинические последствия |
| c.3846G>A | стр.Trp1282X | W1282X | rs77010898 | 1726 | 0,01215 | 99% | вызывающий муковисцидоз |
| ок.489+1Г>Т | Нет названия белка | 621+1Г->Т | rs78756941 | 1323 | 0,00931 | 99% | вызывающий муковисцидоз |
| ок.1657С>Т | п.Arg553X | Р553Х | rs74597325 | 1323 | 0,00931 | 97% | вызывающий муковисцидоз |
| ок.1585-1G>A | Нет названия белка | 1717-1Г->А | rs76713772 | 1216 | 0,00856 | 97% | вызывающий муковисцидоз |
| ок.3718-2477С>Т | Нет названия белка | 3849+10kbC->T | rs75039782 | 1158 | 0,00815 | 33% | вызывающий муковисцидоз |
| ок.2657+5G>A | Нет названия белка | 2789+5G->A | rs80224560 | 1027 | 0,00723 | 43% | вызывающий муковисцидоз |
| c.1519_1521delATC | стр. Ile507del | I507del | rs121908745 | 651 | 0,00458 | 98% | вызывающий муковисцидоз |
| c.3484C>Т | п.Arg1162X | Р1162Х | rs74767530 | 651 | 0,00458 | 97% | вызывающий муковисцидоз |
| с.254Г>А | п.Gly85Glu | G85E | rs75961395 | 616 | 0,00434 | 85% | вызывающий муковисцидоз |
| c.3454G>C | p.Asp1152Его | Д1152Н | rs75541969 | 571 | 0,00402 | 24% | Различные клинические последствия |
| c.2051_2052delAAinsG | стр. Lys684SerfsX38 | 2183AA->G | rs121908799 | 542 | 0,00382 | 96% | вызывающий муковисцидоз |
| c.3528delC | стр. Lys1177SerfsX15 | 3659delC | rs121908747 | 539 | 0,00379 | 99% | вызывающий муковисцидоз |
| ок.1040G>C | п.Arg347Pro | Р347П | rs77932196 | 533 | 0,00375 | 68% | вызывающий муковисцидоз |
| ок.1210−12T[5] | Нет названия белка | 5Т | rs1805177 | 516 | 0,00363 | 28% | Различные клинические последствия |
| ок.2988+1G>A | Нет названия белка | 3120+1Г->А | rs75096551 | 501 | 0,00353 | 98% | вызывающий муковисцидоз |
| ок.1364С>А | п.Ala455Glu | А455Е | rs74551128 | 500 | 0,00352 | 34% | вызывающий муковисцидоз |
| ок.3140-26А>Г | Нет названия белка | 3272-26А->Г | rs76151804 | 470 | 0,00331 | 29% | вызывающий муковисцидоз |
| ок.1000С>Т | п.Arg334Trp | Р334В | rs121909011 | 429 | 0,00302 | 40% | вызывающий муковисцидоз |
| ок.1766+1Г>А | Нет названия белка | 1898+1Г->А | rs121908748 | 421 | 0,00296 | 99% | вызывающий муковисцидоз |
| c.54-5940_273+10250del21kb | стр.Ser18ArgfsX16 | CFTRdele2,3 | не найдено | 417 | 0,00294 | 100% | вызывающий муковисцидоз |
| ок.1679г>С | п.Arg560Thr | Р560Т | rs80055610 | 343 | 0,00241 | 98% | вызывающий муковисцидоз |
| с.617Т>Г | п. Leu206Trp | L206W | rs121908752 | 333 | 0,00234 | 20% | вызывающий муковисцидоз |
| c.2052dupA | стр.Gln685ThrfsX4 | 2184вставкиА | rs121908786 | 329 | 0,00232 | 85% | вызывающий муковисцидоз |
| c.262_263delTT | стр. Leu88IlefsX22 | 394delTT | rs121908769 | 307 | 0,00216 | 97% | вызывающий муковисцидоз |
| с.178Г>Т | п.Glu60X | Е60Х | rs77284892 | 296 | 0,00208 | 99% | вызывающий муковисцидоз |
| ок.1477С>Т | стр.Gln493X | Q493X | rs77101217 | 292 | 0,00206 | 98% | вызывающий муковисцидоз |
| ок.579+1Г>Т | Нет названия белка | 711+1Г->Т | rs77188391 | 274 | 0,00193 | 98% | вызывающий муковисцидоз |
| c.2052delA | стр. Lys684AsnfsX38 | 2184delA | rs121908746 | 255 | 0,00180 | 98% | вызывающий муковисцидоз |
| ок.200С>Т | п.Pro67Leu | П67Л | rs368505753 | 239 | 0,00168 | 34% | вызывающий муковисцидоз |
| c.3302T>A | п.Met1101Lys | М1101К | rs36210737 | 238 | 0,00168 | 69% | вызывающий муковисцидоз |
| ок.1408А>Г | п.Мет470Вал | М470В | rs213950 | 235 | 0,00165 | 46% | Не вызывает муковисцидоз |
| c.3276C>A или c.3276C>G | стр.Tyr1092X | Y1092X | rs121908761 | 225 | 0,00158 | 98% | вызывающий муковисцидоз |
| c.3196C>Т | п.Arg1066Cys | Р1066С | rs78194216 | 220 | 0,00155 | 98% | вызывающий муковисцидоз |
| c.1021_1022dupTC | стр.Phe342HisfsX28 | 1154insTC | rs387906360 | 214 | 0,00151 | 99% | вызывающий муковисцидоз |
| c.3773dupT | стр. Leu1258PhefsX7 | 3905insT | rs121908789 | 210 | 0,00148 | 97% | вызывающий муковисцидоз |
| ок.1646г>А | стр.Ser549Asn | С549Н | rs121908755 | 203 | 0,00143 | 84% | вызывающий муковисцидоз |
| ок.1040г>А | p.Arg347Его | Р347Х | rs77932196 | 199 | 0,00140 | 24% | вызывающий муковисцидоз |
| c.948delT | стр.Phe316LeufsX12 | 1078delT | rs121908744 | 184 | 0,00130 | 99% | вызывающий муковисцидоз |
| c.1210-33_1210-6GT[12]T[4] | Нет названия белка | 5Т;ТГ12 | не найдено | 182 | 0,00128 | 14% | Различные клинические последствия |
| c.3472C>Т | п.Arg1158X | Р1158Х | rs79850223 | 179 | 0,00126 | 99% | вызывающий муковисцидоз |
| c.2834C>Т | п.Ser945Leu | С945Л | rs397508442 | 167 | 0,00118 | 40% | вызывающий муковисцидоз |
| ок.1558г>т | стр. Val520Phe | V520F | rs77646904 | 156 | 0,00110 | 98% | вызывающий муковисцидоз |
| с.443Т>С | стр. Ile148Thr | И148Т | rs35516286 | 148 | 0,00104 | 88% | Не вызывает муковисцидоз |
| с.349С>Т | п.Arg117Cys | Р117С | rs77834169 | 146 | 0,00103 | 24% | вызывающий муковисцидоз |
ДельтаФ508
DeltaF508 ( ΔF508 ), полное название CFTRΔF508 или F508del-CFTR (rs113993960), представляет собой специфическую мутацию в гене CFTR, включающую делецию трех нуклеотидов, охватывающих кодоны для аминокислотных позиций 507 и 508 гена CFTR на хромосоме 7, что в конечном итоге приводит к потере одного кодона для аминокислоты фенилаланина (F). Человек с мутацией CFTRΔF508 будет производить аномальный белок CFTR, в котором отсутствует этот остаток фенилаланина и который не может правильно складываться . Большая часть этого мутировавшего белка не покидает эндоплазматический ретикулум для дальнейшей обработки. Небольшие количества, которые достигают плазматической мембраны, дестабилизируются, и анионный канал открывается нечасто. Наличие двух копий этой мутации (по одной унаследованной от каждого родителя) является наиболее распространенной причиной муковисцидоза (МВ), отвечая за почти две трети мутаций во всем мире. [34]
Эффекты
This section needs more reliable medical references for verification or relies too heavily on primary sources. (March 2019) |
Белок CFTR в значительной степени экспрессируется в клетках поджелудочной железы, кишечного и респираторного эпителия и всех экзокринных желез. При правильном сворачивании он перемещается к клеточной мембране, где становится трансмембранным белком, который образует водные каналы, позволяющие ионам хлорида и бикарбоната выходить из клеток; он также одновременно ингибирует поглощение ионов натрия другим канальным белком. Обе эти функции помогают поддерживать ионный градиент , который заставляет осмос вытягивать воду из клеток. [35] Мутация ΔF508 приводит к неправильному сворачиванию CFTR и его возможной деградации в ER . У организмов с двумя комплементами мутации белок почти полностью отсутствует в клеточной мембране, и эти критические функции транспорта ионов не выполняются. [36]
Наличие гомозиготной пары генов с мутацией ΔF508 не позволяет белку CFTR занять свое нормальное положение в клеточной мембране. Это вызывает повышенную задержку воды в клетках, соответствующую дегидратацию внеклеточного пространства и связанный с этим каскад эффектов на различные части тела. Эти эффекты включают: более толстые слизистые оболочки в эпителии пораженных органов; обструкцию узких дыхательных путей в результате более густой слизи и ингибирования свободного движения мукоцилий; врожденное отсутствие семявыносящих протоков из-за увеличения толщины слизи во время развития плода; недостаточность поджелудочной железы из-за закупорки протока поджелудочной железы слизью; и повышенный риск респираторной инфекции из-за накопления густой, богатой питательными веществами слизи, где процветают бактерии. Это симптомы кистозного фиброза , генетического заболевания; однако ΔF508 — не единственная мутация, вызывающая это заболевание. [37]
Будучи гетерозиготным носителем (имеющим одну копию ΔF508), мы снижаем потерю воды во время диареи , поскольку неисправные или отсутствующие белки CFTR не могут поддерживать стабильные ионные градиенты через клеточные мембраны. Типичное связывание нуклеотидов как ионов Cl − , так и ионов Na + внутри пораженных клеток, что создает гипотонический раствор снаружи клеток и заставляет воду диффундировать в клетки путем осмоса. Несколько исследований показывают, что гетерозиготные носители подвержены повышенному риску различных симптомов. Например, было показано, что гетерозиготность по муковисцидозу связана с повышенной реактивностью дыхательных путей, а гетерозиготы могут подвергаться риску плохой функции легких. Было показано, что гетерозиготы с хрипами подвержены более высокому риску плохой функции легких или развития и прогрессирования хронической обструктивной болезни легких . Одного гена муковисцидоза достаточно, чтобы вызвать легкие аномалии легких даже при отсутствии инфекции. [38]
Механизм
Ген CFTR расположен на длинном плече хромосомы 7, в позиции q31.2, и в конечном итоге кодирует последовательность из 1480 аминокислот. Обычно три пары оснований ДНК ATC (в паре с TAG на противоположной нити) в 507-й позиции гена образуют шаблон для кодона мРНК AUC для изолейцина , в то время как три пары оснований ДНК TTT (в паре с AAA) в соседней 508-й позиции образуют шаблон для кодона UUU для фенилаланина . [39] Мутация ΔF508 представляет собой делецию пары CG из позиции 507 вместе с первыми двумя парами TA из позиции 508, оставляя последовательность ДНК ATT (в паре с TAA) в позиции 507, которая транскрибируется в кодон мРНК AUU. Поскольку AUU также кодирует изолейцин, аминокислота в позиции 507 не меняется, а чистый эффект мутации эквивалентен делеции («Δ») последовательности, в результате чего в позиции 508 появляется кодон фенилаланина. [40]
Распространенность
ΔF508 присутствует по крайней мере в одной копии хромосомы 7 примерно у одного из 30 европеоидов . Наличие мутации в обеих копиях вызывает аутосомно-рецессивное заболевание кистозный фиброз. Ученые подсчитали, что исходная мутация произошла более 52 000 лет назад в Северной Европе, хотя известно , что пациенты с кистозным фиброзом других этнических групп также имеют мутацию. Молодой возраст аллеля может быть следствием прошлого отбора. Одна из гипотез относительно того, почему в противном случае пагубная мутация поддерживалась естественным отбором, заключается в том, что одна копия может представлять положительный эффект, уменьшая потерю воды во время холеры , хотя занос патогенного Vibrio cholerae в Европу произошел только в конце 18 века. [41] Другая теория утверждает, что носители CF (гетерозиготы по ΔF508) более устойчивы к брюшному тифу , поскольку было показано, что CFTR действует как рецептор для бактерий Salmonella typhi для проникновения в эпителиальные клетки кишечника. [42]
Гетерозиготы по муковисцидозу ΔF508 могут быть чрезмерно представлены среди людей с астмой и могут иметь более плохую функцию легких, чем неносители. [43] [44] Носители одной мутации CF имеют более высокую распространенность хронического риносинусита , чем общая популяция. [45] Примерно 50% случаев муковисцидоза в Европе вызваны гомозиготными мутациями ΔF508 (это сильно варьируется в зависимости от региона), [46] в то время как частота аллеля ΔF508 составляет около 70%. [47] Остальные случаи вызваны более чем 1500 другими мутациями, включая R117H, 1717-1G>A и 2789+56G>A. Эти мутации, в сочетании друг с другом или даже с одной копией ΔF508, могут вызывать симптомы CF. Генотип не имеет строгой корреляции с тяжестью муковисцидоза, хотя определенные симптомы связаны с определенными мутациями.
Структура

Ген CFTR имеет длину приблизительно 189 кб , содержит 27 экзонов и 26 интронов . [49] CFTR является гликопротеином и находится на поверхности многих эпителиальных клеток в организме. [50] CFTR состоит из пяти доменов, которые включают два трансмембранных или трансмембранных домена, два нуклеотидсвязывающих домена и регуляторный домен. [51] Каждый из трансмембранных доменов связан с нуклеотидсвязывающим доменом (NBD) в цитоплазме. Первый NBD связан со вторым трансмембранным доменом регуляторным доменом «R», который является уникальной особенностью CFTR, отсутствующей в других транспортерах ABC , который несет 19 предсказанных участков для протеинкиназы A (PKA). Сообщалось, что шесть из них фосфорилируются in vivo. [52] Ионный канал открывается только тогда, когда его R-домен фосфорилируется PKA, а АТФ связывается с NBD. Фосфорилирование вытесняет неупорядоченный домен R из положений, предотвращающих димеризацию и открытие NBD. [53] [54] Аминоконец является частью мотива лассо, который закрепляется в клеточной мембране. [52] Карбоксильный конец белка закреплен на цитоскелете с помощью домена , взаимодействующего с PDZ . [55]
Расположение и функция
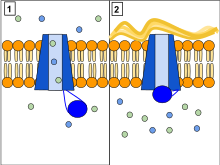
Ген CFTR состоит из 27 экзонов, которые кодируют его генный состав, и находится на длинном (q) плече хромосомы 7 в локусе 31.2. Экзоны представляют собой фрагменты ДНК, которые обеспечивают код для структуры белка. [50] CFTR функционирует как фосфорилирование и АТФ - управляемый анионный канал , увеличивая проводимость для определенных анионов (например, Cl− ) , чтобы течь по их электрохимическому градиенту . Управляемые АТФ конформационные изменения в CFTR открывают и закрывают ворота, позволяя трансмембранному потоку анионов по их электрохимическому градиенту . [5] Это контрастирует с другими белками ABC , в которых управляемые АТФ конформационные изменения подпитывают восходящий транспорт субстрата через клеточные мембраны. По сути, CFTR представляет собой ионный канал, который эволюционировал как «сломанный» транспортер ABC , который протекает в открытой конформации .
CFTR состоят из пяти доменов, включая два трансмембранных домена, каждый из которых связан с доменом связывания нуклеотидов. CFTR также содержит другой домен, называемый регуляторным доменом. Другие члены суперсемейства транспортеров ABC участвуют в поглощении питательных веществ у прокариот или в экспорте различных субстратов у эукариот. Транспортеры ABC эволюционировали, чтобы преобразовывать свободную энергию гидролиза АТФ в восходящее движение субстратов через клеточную мембрану. Они имеют две основные конформации: одну, в которой сайт связывания груза обращен к цитозолю или обращен внутрь (свободный АТФ), и другую, в которой он обращен наружу (связанный АТФ). АТФ связывается с каждым доменом связывания нуклеотидов, что приводит к последующей димеризации NBD, что приводит к перестройке трансмембранных спиралей. Это изменяет доступность сайта связывания груза с положения, обращенного внутрь, на положение, обращенное наружу. Связывание АТФ и последующий гидролиз приводят к альтернативному раскрытию сайта связывания груза, обеспечивая однонаправленный транспорт груза против электрохимического градиента . В CFTR чередование конформации, обращенной внутрь, и конформации, обращенной наружу, приводит к запиранию канала. В частности, димеризация NBD (благоприятствуемая связыванием АТФ) сопряжена с переходом в конформацию, обращенную наружу, в которой образуется открытый трансмембранный путь для анионов. [56] Последующий гидролиз (в каноническом активном сайте, сайте 2, включая мотивы Уокера NBD2) дестабилизирует димер NBD и способствует возврату к конформации, обращенной внутрь, в которой путь проникновения анионов закрыт. [5]
Клинические последствия
Различные мутации CFTR могут приводить к разной степени тяжести кистозного фиброза. Общие симптомы включают хронические инфекции легких, недостаточность поджелудочной железы и высокий уровень хлорида пота. Для устранения этих специфических генетических дефектов были разработаны методы лечения, специфичные для мутаций, такие как модуляторы CFTR. [57]
Взаимодействия
Было показано, что регулятор трансмембранной проводимости при муковисцидозе взаимодействует с:
Его подавляет противодиарейный препарат крофелемер .
Сопутствующие условия
- Врожденное двустороннее отсутствие семявыносящих протоков : у мужчин с врожденным двусторонним отсутствием семявыносящих протоков чаще всего наблюдается легкая мутация (изменение, которое обеспечивает частичную функцию гена) в одной копии гена CFTR и мутация, вызывающая муковисцидоз, в другой копии гена CFTR.
- Муковисцидоз : обнаружено более 1800 мутаций в гене CFTR [71], но большинство из них не связаны с муковисцидозом. [72] Большинство этих мутаций либо заменяют одну аминокислоту (строительный блок белков) на другую аминокислоту в белке CFTR, либо удаляют небольшое количество ДНК в гене CFTR. Наиболее распространенная мутация, называемая ΔF508, представляет собой делецию (Δ) одной аминокислоты (фенилаланина) в позиции 508 в белке CFTR. Этот измененный белок никогда не достигает клеточной мембраны, поскольку он разрушается вскоре после своего создания. Все вызывающие заболевание мутации в гене CFTR препятствуют правильному функционированию канала, что приводит к блокировке движения соли и воды в клетки и из них. В результате этой блокировки клетки, выстилающие проходы легких, поджелудочной железы и других органов, вырабатывают аномально густую, липкую слизь. Эта слизь закупоривает дыхательные пути и железы, вызывая характерные признаки и симптомы муковисцидоза. Кроме того, только жидкая слизь может быть удалена ресничками ; густая слизь не может, поэтому она задерживает бактерии, которые вызывают хронические инфекции.
- Холера : АДФ-рибозилирование, вызванное холерным токсином, приводит к увеличению продукции циклического АМФ , который, в свою очередь, открывает канал CFTR, что приводит к избыточной секреции Cl− . Na + и H2O следуют за Cl− в тонкий кишечник, что приводит к обезвоживанию и потере электролитов. [73]
Цель наркотиков
CFTR был лекарственной мишенью в попытках найти методы лечения связанных с ним состояний. Ивакафтор (торговая марка Kalydeco, разработанный как VX-770) — это лекарство , одобренное FDA в 2012 году для людей с муковисцидозом , у которых есть определенные мутации CFTR. [74] [75] Ивакафтор был разработан Vertex Pharmaceuticals совместно с Фондом муковисцидоза и является первым лекарством, которое лечит основную причину, а не симптомы заболевания. [76] [77] и «чудо-лекарство» [78]
Комбинация ванзакафтор/тезакафтор/дейтивакафтор (торговая марка Alyftrek) была одобрена для медицинского применения в Соединенных Штатах в декабре 2024 года. [79]
Ссылки
- ^ abc GRCh38: Ensembl выпуск 89: ENSG00000001626 – Ensembl , май 2017 г.
- ^ abc GRCm38: Ensembl выпуск 89: ENSMUSG00000041301 – Ensembl , май 2017 г.
- ^ "Human PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ "Mouse PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ abc Csanády L, Vergani P, Gadsby DC (январь 2019). «Структура, управление и регуляция анионного канала CFTR». Physiological Reviews . 99 (1): 707– 738. doi : 10.1152/physrev.00007.2018 . PMID 30516439.
- ^ ab Rommens JM , Iannuzzi MC, Kerem B, Drumm ML, Melmer G, Dean M и др. (сентябрь 1989 г.). «Идентификация гена муковисцидоза: ходьба и прыжки хромосом». Science . 245 (4922): 1059– 1065. Bibcode :1989Sci...245.1059R. doi :10.1126/science.2772657. PMID 2772657.
- ^ "Ген регулятора трансмембранной проводимости при муковисцидозе (CFTR) | Энциклопедия проекта "Эмбрион"". Embryo.asu.edu . Получено 26 сентября 2022 г. .
- ^ Riordan JR, Rommens JM, Kerem B, Alon N, Rozmahel R, Grzelczak Z, et al. (сентябрь 1989). «Идентификация гена кистозного фиброза: клонирование и характеристика комплементарной ДНК». Science . 245 (4922): 1066– 1073. Bibcode :1989Sci...245.1066R. doi :10.1126/science.2475911. PMID 2475911. S2CID 84566748.
- ^ Riordan JR, Rommens JM, Kerem B, Alon N, Rozmahel R, Grzelczak Z, et al. (сентябрь 1989). «Идентификация гена кистозного фиброза: клонирование и характеристика комплементарной ДНК». Science . 245 (4922): 1066– 1073. doi :10.1016/0168-9525(89)90155-8. PMID 2475911.
- ^ Marcorelles P, Gillet D, Friocourt G, Ledé F, Samaison L, Huguen G и др. (март 2012 г.). «Экспрессия белка-регулятора трансмембранной проводимости при муковисцидозе в системе мужских выводных протоков во время развития». Human Pathology . 43 (3): 390–397 . doi :10.1016/j.humpath.2011.04.031. PMID 21840567.
- ^ Bregman T, Fride E (июнь 2011 г.). «Лечение тетрагидроканнабинолом (ТГК) предотвращает бесплодие у мышей-самцов с кистозным фиброзом». Журнал базовой и клинической физиологии и фармакологии . 22 ( 1– 2): 29– 32. doi : 10.1515/jbcpp.2011.004. PMID 22865360. S2CID 19335113.
- ^ abc Enuka Y, Hanukoglu I, Edelheit O, Vaknine H, Hanukoglu A (март 2012 г.). «Эпителиальные натриевые каналы (ENaC) равномерно распределены на подвижных ресничках яйцевода и дыхательных путей». Histochemistry and Cell Biology . 137 (3): 339– 353. doi :10.1007/s00418-011-0904-1. PMID 22207244. S2CID 15178940.
- ^ Шарма С., Ханукоглу А., Ханукоглу И. (апрель 2018 г.). «Локализация эпителиального натриевого канала (ENaC) и CFTR в зародышевом эпителии яичек, клетках Сертоли и сперматозоидах». Журнал молекулярной гистологии . 49 (2): 195–208 . doi :10.1007/s10735-018-9759-2. PMID 29453757. S2CID 3761720.
- ^ Шарма С., Ханукоглу И. (апрель 2019 г.). «Картирование участков локализации эпителиального натриевого канала (ENaC) и CFTR в сегментах придатка яичка млекопитающих». Журнал молекулярной гистологии . 50 (2): 141– 154. doi :10.1007/s10735-019-09813-3. PMID 30659401. S2CID 58026884.
- ^ Sharma S, Kumaran GK, Hanukoglu I (февраль 2020 г.). «Высокоразрешающая визуализация актинового цитоскелета и эпителиального натриевого канала, CFTR и локализации аквапорина-9 в семявыносящих протоках». Mol Reprod Dev . 87 (2): 305–319 . doi :10.1002/mrd.23317. PMID 31950584.
- ^ «Исследование CF обнаруживает новые клетки, называемые ионоцитами, несущие высокий уровень гена CFTR». Новости о муковисцидозе сегодня . 3 августа 2018 г.
- ^ Монторо Д.Т., Хабер А.Л., Битон М., Винарский В., Лин Б., Биркет С.Е. и др. (август 2018 г.). «Пересмотренная иерархия эпителия дыхательных путей включает ионоциты, экспрессирующие CFTR». Природа . 560 (7718): 319–324 . Бибкод : 2018Natur.560..319M. дои : 10.1038/s41586-018-0393-7. ПМК 6295155 . ПМИД 30069044.
- ^ Plasschaert LW, Žilionis R, Choo-Wing R, Savova V, Knehr J, Roma G и др. (август 2018 г.). «Атлас одноклеточного эпителия дыхательных путей выявляет богатые CFTR легочные ионоциты». Nature . 560 (7718): 377– 381. Bibcode :2018Natur.560..377P. doi :10.1038/s41586-018-0394-6. PMC 6108322 . PMID 30069046.
- ^ ab Hanukoglu I, Boggula VR, Vaknine H, Sharma S, Kleyman T, Hanukoglu A (июнь 2017 г.). «Экспрессия эпителиального натриевого канала (ENaC) и CFTR в человеческом эпидермисе и эпидермальных придатках». Histochemistry and Cell Biology . 147 (6): 733– 748. doi :10.1007/s00418-016-1535-3. PMID 28130590. S2CID 8504408.
- ^ Moskwa P, Lorentzen D, Excoffon KJ, Zabner J, McCray PB, Nauseef WM и др. (январь 2007 г.). «Новая система защиты дыхательных путей хозяина дефектна при кистозном фиброзе». American Journal of Respiratory and Critical Care Medicine . 175 (2): 174– 183. doi :10.1164/rccm.200607-1029OC. PMC 2720149. PMID 17082494 .
- ^ Xu Y, Szép S, Lu Z (декабрь 2009 г.). «Антиоксидантная роль тиоцианата в патогенезе муковисцидоза и других заболеваний, связанных с воспалением». Труды Национальной академии наук Соединенных Штатов Америки . 106 (48): 20515– 20519. Bibcode : 2009PNAS..10620515X. doi : 10.1073/pnas.0911412106 . PMC 2777967. PMID 19918082 .
- ^ Yonei Y, Tanaka M, Ozawa Y, Miyazaki K, Tsukada N, Inada S и др. (апрель 1992 г.). «Первичная гепатоцеллюлярная карцинома с тяжелой гипогликемией: участие инсулиноподобных факторов роста». Liver . 12 (2): 90– 93. doi :10.1111/j.1600-0676.1992.tb00563.x. PMID 1320177.
- ^ ab "OrthoMaM phylogenetic marker: CFTR coding sequence". Архивировано из оригинала 2 марта 2016 года . Получено 12 марта 2010 года .
- ^ Davies R, Conroy SJ, Davies WL, Potter IC, Trezise AE (19–23 июня 2005 г.). "Эволюция и регуляция гена кистозного фиброза" (конференциальная статья) . Конференция по молекулярной биологии и эволюции (MBE05) . Получено 28 июля 2014 г.
- ^ Welsh MJ, Smith AE (июль 1993 г.). «Молекулярные механизмы дисфункции хлоридных каналов CFTR при муковисцидозе». Cell . 73 (7): 1251– 1254. doi :10.1016/0092-8674(93)90353-r. PMID 7686820.
- ^ "Генетика и муковисцидоз". Центр муковисцидоза в Стэнфорде (на самоанском) . Получено 23 октября 2022 г.
- ^ Prasad AB, Allard MW, Green ED (сентябрь 2008 г.). «Подтверждение филогении млекопитающих с помощью больших сравнительных наборов данных о последовательностях». Молекулярная биология и эволюция . 25 (9): 1795–1808 . doi :10.1093/molbev/msn104. PMC 2515873. PMID 18453548 .
- ^ "Клиническая и функциональная ТРАНСЛЯЦИЯ CFTR (CFTR2): История списка вариантов CFTR2". Фонд CF США, Университет Джонса Хопкинса, Центр муковисцидоза в Детской больнице Торонто . Получено 2 августа 2017 г.[ постоянная мертвая ссылка ]
- ^ Guimbellot J, Sharma J, Rowe SM (ноябрь 2017 г.). «На пути к инклюзивной терапии с модуляторами CFTR: прогресс и проблемы». Детская пульмонология . 52 (S48): S4 – S14 . doi :10.1002/ppul.23773. PMC 6208153. PMID 28881097 .
- ^ Шекдар К, Лангер Дж, Венкатачалан С, Шмид Л, Анобиле Дж, Шах П и др. (Май 2021 г.). «Метод клеточной инженерии с использованием флуорогенных олигонуклеотидных сигнальных зондов и проточной цитометрии». Biotechnology Letters . 43 (5): 949–958 . doi :10.1007/s10529-021-03101-5. PMC 7937778. PMID 33683511 .
- ^ Rowe SM, Miller S, Sorscher EJ (май 2005 г.). «Кистозный фиброз». The New England Journal of Medicine . 352 (19): 1992–2001 . doi :10.1056/NEJMra043184. PMID 15888700.
- ^ Kavic SM, Frehm EJ, Segal AS (1999). «Исследования случаев холеры: уроки истории медицины и науки». Йельский журнал биологии и медицины . 72 (6): 393–408 . PMC 2579035. PMID 11138935 .
- ^ "CFTR2" . Получено 8 июля 2021 г. .
- ^ Bobadilla JL, Macek M, Fine JP, Farrell PM (июнь 2002 г.). «Кистозный фиброз: всемирный анализ мутаций CFTR — корреляция с данными о заболеваемости и применение к скринингу». Human Mutation . 19 (6): 575– 606. doi : 10.1002/humu.10041 . PMID 12007216.
- ^ Verkman AS, Song Y, Thiagarajah JR (январь 2003 г.). «Роль жидкости поверхности дыхательных путей и подслизистых желез при кистозном фиброзе легких». American Journal of Physiology. Cell Physiology . 284 (1): C2-15. doi :10.1152/ajpcell.00417.2002. PMID 12475759.
- ^ "Направления исследований кистозного фиброза". Национальный институт диабета, заболеваний органов пищеварения и почек (NIDDK). Архивировано из оригинала 25 мая 2003 г.
- ^ Boyle MP, De Boeck K (апрель 2013 г.). «Новая эра в лечении муковисцидоза: коррекция основного дефекта CFTR». The Lancet. Респираторная медицина . 1 (2): 158– 163. doi :10.1016/s2213-2600(12)70057-7. PMID 24429096.
- ^ Maurya N, Awasthi S, Dixit P (апрель 2012 г.). "Ассоциация мутации гена CFTR с бронхиальной астмой" (PDF) . The Indian Journal of Medical Research . 135 (4): 469– 478. PMC 3385229 . PMID 22664493. Архивировано из оригинала (PDF) 12 марта 2020 г. . Получено 16 марта 2019 г. .
- ^ Отчет CCDS для консенсусного CDS: Отчет для CCDS5773.1 (текущая версия) NCBI
- ^ Bartoszewski RA, Jablonsky M, Bartoszewska S, Stevenson L, Dai Q, Kappes J, et al. (сентябрь 2010 г.). «Синонимический однонуклеотидный полиморфизм в DeltaF508 CFTR изменяет вторичную структуру мРНК и экспрессию мутантного белка». Журнал биологической химии . 285 (37): 28741– 28748. doi : 10.1074/jbc.M110.154575 . PMC 2937902. PMID 20628052 .
- ^ «Re: Есть ли связь между муковисцидозом и холерой?».
- ^ Pier GB, Grout M, Zaidi T, Meluleni G, Mueschenborn SS, Banting G, et al. (май 1998). "Salmonella typhi использует CFTR для проникновения в эпителиальные клетки кишечника". Nature . 393 (6680): 79– 82. Bibcode :1998Natur.393...79P. doi :10.1038/30006. PMID 9590693. S2CID 5894247.
- ^ Dahl M, Nordestgaard BG, Lange P, Tybjaerg-Hansen A (май 2001 г.). «Пятнадцатилетнее наблюдение за функцией легких у лиц, гетерозиготных по делеции фенилаланина-508 при кистозном фиброзе». Журнал аллергии и клинической иммунологии . 107 (5): 818– 823. doi : 10.1067/mai.2001.114117 . PMID 11344348.
- ^ Dahl M, Tybjaerg-Hansen A, Lange P, Nordestgaard BG (июнь 1998 г.). «Гетерозиготность DeltaF508 при муковисцидозе и восприимчивости к астме». Lancet . 351 (9120): 1911– 1913. doi :10.1016/s0140-6736(97)11419-2. PMID 9654257. S2CID 22970136.
- ^ Wang X, Kim J, McWilliams R, Cutting GR (март 2005 г.). «Повышенная распространенность хронического риносинусита у носителей мутации кистозного фиброза». Архивы отоларингологии–хирургии головы и шеи . 131 (3): 237– 240. doi : 10.1001/archotol.131.3.237 . PMID 15781764.
- ^ Ежегодный отчет ECFS: что это значит для Великобритании. Архивировано 1 мая 2018 г. в Wayback Machine Cystic Fibrosis Trust.
- ^ Моррал Н., Бертранпети Дж., Эстивилл Х., Нуньес В., Казальс Т., Хименес Дж. и др. (июнь 1994 г.). «Происхождение основной мутации муковисцидоза (дельта F508) в европейском населении». Природная генетика . 7 (2): 169–175 . doi : 10.1038/ng0694-169. PMID 7920636. S2CID 38005421.
- ^ "5UAK: Дефосфорилированный, свободный от АТФ регулятор трансмембранной проводимости человека при муковисцидозе (CFTR)". RCSB Protein Data Bank . 19 декабря 2016 г. Получено 24 декабря 2024 г.
- ^ База данных мутаций при муковисцидозе. "Геномная последовательность ДНК". Архивировано из оригинала 22 августа 2016 г. Получено 6 апреля 2013 г.
- ^ ab "CFTR". Центр муковисцидоза Джонса Хопкинса . Получено 9 октября 2022 г.
- ^ Sheppard DN, Welsh MJ (январь 1999). «Структура и функция хлоридного канала CFTR». Physiological Reviews . 79 (1 Suppl): S23 – S45 . doi : 10.1152/physrev.1999.79.1.S23 . PMID 9922375.
- ^ ab Zhang Z, Liu F, Chen J (декабрь 2018 г.). «Молекулярная структура связанного с АТФ фосфорилированного человеческого CFTR». Труды Национальной академии наук Соединенных Штатов Америки . 115 (50): 12757– 12762. Bibcode : 2018PNAS..11512757Z. doi : 10.1073/pnas.1815287115 . PMC 6294961. PMID 30459277 .
- ^ Чжан З, Лю Ф, Чэнь Дж (июль 2017 г.). «Конформационные изменения CFTR при фосфорилировании и связывании АТФ». Cell . 170 (3): 483–491.e8. doi : 10.1016/j.cell.2017.06.041 . PMID 28735752. S2CID 5361509.
- ^ Sheppard DN, Welsh MJ (январь 1999). «Структура и функция хлоридного канала CFTR». Physiological Reviews . 79 (1 Suppl): S23 – S45 . doi : 10.1152/physrev.1999.79.1.S23 . PMID 9922375.
- ^ ab Short DB, Trotter KW, Reczek D, Kreda SM, Bretscher A, Boucher RC и др. (Июль 1998 г.). «Апикальный белок PDZ прикрепляет регулятор трансмембранной проводимости кистозного фиброза к цитоскелету». Журнал биологической химии . 273 (31): 19797– 19801. doi : 10.1074/jbc.273.31.19797 . PMID 9677412.
- ^ Vergani P, Lockless SW, Nairn AC, Gadsby DC (2005). «Открытие канала CFTR с помощью АТФ-управляемой плотной димеризации его нуклеотид-связывающих доменов». Nature . 433 (7028): 876– 80. Bibcode :2005Natur.433..876V. doi :10.1038/nature03313. PMC 2756053 . PMID 15729345. S2CID 4383918.
- ^ Boyle MP, De Boeck K (апрель 2013 г.). «Новая эра в лечении муковисцидоза: коррекция основного дефекта CFTR». The Lancet. Респираторная медицина . 1 (2): 158– 163. doi :10.1016/s2213-2600(12)70057-7. PMID 24429096.
- ^ Zhang H, Peters KW, Sun F, Marino CR, Lang J, Burgoyne RD и др. (август 2002 г.). «Цистеиновый цепочечный белок взаимодействует с регулятором трансмембранной проводимости кистозного фиброза и модулирует его созревание». Журнал биологической химии . 277 (32): 28948– 28958. doi : 10.1074/jbc.M111706200 . PMID 12039948.
- ^ Cheng J, Moyer BD, Milewski M, Loffing J, Ikeda M, Mickle JE и др. (февраль 2002 г.). «Ассоциированный с аппаратом Гольджи белок домена PDZ модулирует экспрессию трансмембранного регулятора плазматической мембраны кистозного фиброза». Журнал биологической химии . 277 (5): 3520– 3529. doi : 10.1074/jbc.M110177200 . PMID 11707463.
- ^ ab Gentzsch M, Cui L, Mengos A, Chang XB, Chen JH, Riordan JR (февраль 2003 г.). «PDZ-связывающий хлоридный канал ClC-3B локализуется в аппарате Гольджи и ассоциируется с белками PDZ, взаимодействующими с регулятором трансмембранной проводимости кистозного фиброза». Журнал биологической химии . 278 (8): 6440– 6449. doi : 10.1074/jbc.M211050200 . PMID 12471024.
- ^ Wang S, Yue H, Derin RB, Guggino WB, Li M (сентябрь 2000 г.). «Вспомогательный белок способствовал взаимодействию CFTR-CFTR, молекулярный механизм потенцирования активности хлоридного канала». Cell . 103 (1): 169– 179. doi : 10.1016/S0092-8674(00)00096-9 . PMID 11051556. S2CID 16697781.
- ^ Liedtke CM, Yun CH, Kyle N, Wang D (июнь 2002 г.). «Регулирование трансмембранного регулятора муковисцидоза, зависящее от протеинкиназы C, включает связывание с рецептором активированной киназы C (RACK1) и связывание RACK1 с регуляторным фактором обмена Na+/H+». Журнал биологической химии . 277 (25): 22925– 22933. doi : 10.1074/jbc.M201917200 . PMID 11956211.
- ^ ab Park M, Ko SB, Choi JY, Muallem G, Thomas PJ, Pushkin A и др. (декабрь 2002 г.). «Регулятор трансмембранной проводимости при муковисцидозе взаимодействует с изоформой 3 человеческого Na+-HCO3-котранспортера HCO3- и регулирует ее активность». Журнал биологической химии . 277 (52): 50503– 50509. doi : 10.1074/jbc.M201862200 . PMID 12403779.
- ^ ab Cormet-Boyaka E, Di A, Chang SY, Naren AP, Tousson A, Nelson DJ и др. (сентябрь 2002 г.). «CFTR хлоридные каналы регулируются комплексом SNAP-23/синтаксин 1A». Труды Национальной академии наук Соединенных Штатов Америки . 99 (19): 12477– 12482. Bibcode : 2002PNAS ...9912477C. doi : 10.1073/pnas.192203899 . PMC 129470. PMID 12209004.
- ^ Hegedüs T, Sessler T, Scott R, Thelin W, Bakos E, Váradi A и др. (март 2003 г.). «C-концевое фосфорилирование MRP2 модулирует его взаимодействие с белками PDZ». Biochemical and Biophysical Research Communications . 302 (3): 454– 461. doi :10.1016/S0006-291X(03)00196-7. PMID 12615054.
- ^ Wang S, Raab RW, Schatz PJ, Guggino WB, Li M (май 1998). «Консенсус связывания пептида домена NHE-RF-PDZ1 соответствует C-концевой последовательности трансмембранного регулятора проводимости кистозного фиброза (CFTR)». FEBS Letters . 427 (1): 103– 108. Bibcode : 1998FEBSL.427..103W. doi : 10.1016/S0014-5793(98)00402-5 . PMID 9613608. S2CID 20803242.
- ^ Moyer BD, Duhaime M, Shaw C, Denton J, Reynolds D, Karlson KH и др. (сентябрь 2000 г.). «PDZ-взаимодействующий домен регулятора трансмембранной проводимости кистозного фиброза необходим для функциональной экспрессии в апикальной плазматической мембране». Журнал биологической химии . 275 (35): 27069– 27074. doi : 10.1074/jbc.M004951200 . PMID 10852925.
- ^ Hall RA, Ostedgaard LS, Premont RT, Blitzer JT, Rahman N, Welsh MJ и др. (июль 1998 г.). «C-концевой мотив, обнаруженный в бета2-адренергическом рецепторе, рецепторе P2Y1 и регуляторе трансмембранной проводимости кистозного фиброза, определяет связывание с семейством регуляторных факторов обмена Na+/H+ белков PDZ». Труды Национальной академии наук Соединенных Штатов Америки . 95 (15): 8496– 8501. Bibcode : 1998PNAS ...95.8496H. doi : 10.1073/pnas.95.15.8496 . PMC 21104. PMID 9671706.
- ^ Sun F, Hug MJ, Lewarchik CM, Yun CH, Bradbury NA, Frizzell RA (сентябрь 2000 г.). «E3KARP опосредует связь эзрина и протеинкиназы A с регулятором трансмембранной проводимости при кистозном фиброзе в клетках дыхательных путей». Журнал биологической химии . 275 (38): 29539– 29546. doi : 10.1074/jbc.M004961200 . PMID 10893422.
- ^ Naren AP, Nelson DJ, Xie W, Jovov B, Pevsner J, Bennett MK и др. (ноябрь 1997 г.). «Регулирование хлоридных каналов CFTR синтаксином и изоформами Munc18». Nature . 390 (6657): 302– 305. Bibcode :1997Natur.390..302N. doi :10.1038/36882. PMID 9384384. S2CID 4395005.
- ^ Egan ME (март 2016 г.). «Генетика кистозного фиброза: клинические аспекты». Clinics in Chest Medicine . 37 (1): 9– 16. doi :10.1016/j.ccm.2015.11.002. PMID 26857764.
- ^ De Boeck K, Amaral MD (август 2016 г.). «Прогресс в терапии муковисцидоза». The Lancet. Респираторная медицина . 4 (8): 662– 674. doi :10.1016/S2213-2600(16)00023-0. PMID 27053340.
- ^ Thiagarajah JR, Verkman AS (сентябрь 2012 г.). «Ингибиторы CFTR для лечения диарейных заболеваний». Клиническая фармакология и терапия . 92 (3): 287– 290. doi :10.1038/clpt.2012.114. PMC 3643514. PMID 22850599 .
- ^ Jones AM, Helm JM (октябрь 2009 г.). «Новые методы лечения муковисцидоза». Drugs . 69 (14): 1903– 1910. doi :10.2165/11318500-0000000000-00000. PMID 19747007. S2CID 23344660.
- ^ McPhail GL, Clancy JP (апрель 2013 г.). «Ивакафтор: первая терапия, действующая на основную причину муковисцидоза». Drugs of Today . 49 (4): 253– 260. doi :10.1358/dot.2013.49.4.1940984. PMID 23616952.
- ^ «Исследование фазы 3 VX-770 показывает заметное улучшение функции легких среди людей с муковисцидозом с мутацией G551D» (пресс-релиз). Фонд муковисцидоза. 23 февраля 2011 г.
- ^ Herper M (27 декабря 2012 г.). «Самый важный новый препарат 2012 года». Forbes .
- ^ Nocera J (18 июля 2014 г.). «Лекарство за 300 000 долларов». The New York Times .
- ^ «Vertex объявляет об одобрении FDA США препарата Alyftrek, модулятора CFTR нового класса для лечения муковисцидоза один раз в день» (пресс-релиз). Vertex. 20 декабря 2024 г. Получено 24 декабря 2024 г. – через Business Wire.
Дальнейшее чтение
- Boyle MP (2000). «Уникальные проявления и хронические осложнения при муковисцидозе у взрослых: учат ли они нас чему-либо о CFTR?». Respiratory Research . 1 (3): 133– 135. doi : 10.1186/rr23 . PMC 59552. PMID 11667976 .
- Брэдбери NA (2001). «Сигнальные каскады цАМФ и CFTR: есть ли еще чему поучиться?». Pflügers Archiv . 443 (Suppl 1): S85 – S91 . doi :10.1007/s004240100651. PMID 11845310. S2CID 19373036.
- Cohn JA, Mitchell RM, Jowell PS (март 2005 г.). «Влияние муковисцидоза и мутаций гена PSTI/SPINK1 на восприимчивость к хроническому панкреатиту». Clinics in Laboratory Medicine . 25 (1): 79– 100. doi :10.1016/j.cll.2004.12.007. PMID 15749233.
- Cohn JA, Noone PG, Jowell PS (сентябрь 2002 г.). «Идиопатический панкреатит, связанный с CFTR: сложное наследование и идентификация гена-модификатора». Journal of Investigative Medicine . 50 (5): 247S – 255S . doi :10.1136/jim-50-suppl5-01. PMID 12227654. S2CID 34017638.
- Cuppens H, Cassiman JJ (октябрь 2004 г.). «Мутации и полиморфизмы CFTR при мужском бесплодии». Международный журнал андрологии . 27 (5): 251– 256. doi : 10.1111/j.1365-2605.2004.00485.x . PMID 15379964.
- Dahan D, Evagelidis A, Hanrahan JW, Hinkson DA, Jia Y, Luo J и др. (2001). «Регулирование канала CFTR путем фосфорилирования». Pflügers Archiv . 443 (Suppl 1): S92 – S96 . doi :10.1007/s004240100652. PMID 11845311. S2CID 8144727.
- Devidas S, Guggino WB (октябрь 1997 г.). «CFTR: домены, структура и функция». Журнал биоэнергетики и биомембран . 29 (5): 443– 451. doi :10.1023/A:1022430906284. PMID 9511929. S2CID 6000695.
- Драмм МЛ, Коллинз ФС (1993). «Молекулярная биология муковисцидоза». Молекулярная генетическая медицина . 3 : 33–68 . doi :10.1016/b978-0-12-462003-2.50006-7. ISBN 9780124620032. PMID 7693108.
- Greger R, Schreiber R, Mall M, Wissner A, Hopf A, Briel M и др. (2001). «Кистозный фиброз и CFTR». Pflügers Archiv . 443 (Suppl 1): S3 – S7 . doi :10.1007/s004240100635. PMID 11845294. S2CID 8057614.
- Кандула Л., Уиткомб Д.К., Лоу М.Э. (июнь 2006 г.). «Генетические проблемы детского панкреатита». Current Gastroenterology Reports . 8 (3): 248– 253. doi :10.1007/s11894-006-0083-8. PMID 16764792. S2CID 23606613.
- Керем Б., Керем Э. (1996). «Молекулярная основа изменчивости заболеваний при муковисцидозе». European Journal of Human Genetics . 4 (2): 65–73 . doi :10.1159/000472174 (неактивен 22 декабря 2024 г.). PMID 8744024. S2CID 41476164.
{{cite journal}}: CS1 maint: DOI inactive as of December 2024 (link) - Kulczycki LL, Kostuch M, Bellanti JA (январь 2003 г.). «Клиническая перспектива муковисцидоза и новые генетические открытия: связь мутаций CFTR с проявлениями генотипа-фенотипа». American Journal of Medical Genetics. Часть A. 116A ( 3): 262– 267. doi :10.1002/ajmg.a.10886. PMID 12503104. S2CID 9245855.
- Marcet B, Boeynaems JM (декабрь 2006 г.). «Связь между регулятором трансмембранной проводимости при муковисцидозе, внеклеточными нуклеотидами и муковисцидозом». Фармакология и терапия . 112 (3): 719– 732. doi :10.1016/j.pharmthera.2006.05.010. PMID 16828872.
- McIntosh I, Cutting GR (июль 1992 г.). «Регулятор трансмембранной проводимости при муковисцидозе и этиология и патогенез муковисцидоза». FASEB Journal . 6 (10): 2775– 2782. doi : 10.1096/fasebj.6.10.1378801 . PMID 1378801. S2CID 24932803.
- Нагель Г (декабрь 1999 г.). «Дифференциальная функция двух доменов связывания нуклеотидов на регуляторе трансмембранной проводимости при муковисцидозе». Biochimica et Biophysica Acta (BBA) - Биомембраны . 1461 (2): 263– 274. doi : 10.1016/S0005-2736(99)00162-5 . PMID 10581360.
- Шварц М (февраль 2003 г.). "[Ген трансмембранного регулятора проводимости при муковисцидозе (CFTR): мутации и клинические фенотипы]". Ugeskrift for Laeger . 165 (9): 912–916 . PMID 12661515.
- Southern KW, Peckham D (2004). «Установление диагноза муковисцидоза». Хронические респираторные заболевания . 1 (4): 205–210 . doi : 10.1191/1479972304cd044rs . PMID 16281647.
- Tsui LC (1992). «Мутации и вариации последовательностей, обнаруженные в гене трансмембранного регулятора проводимости при кистозном фиброзе (CFTR): отчет Консорциума по генетическому анализу кистозного фиброза». Human Mutation . 1 (3): 197– 203. doi : 10.1002/humu.1380010304 . PMID 1284534. S2CID 35904538.
- Vankeerberghen A, Cuppens H, Cassiman JJ (март 2002 г.). «Регулятор трансмембранной проводимости при кистозном фиброзе: интригующий белок с плейотропными функциями». Журнал кистозного фиброза . 1 (1): 13–29 . doi : 10.1016/S1569-1993(01)00003-0 . PMID 15463806.
- Wilschanski M, Durie PR (август 2007 г.). «Модели заболеваний ЖКТ у взрослых, связанные с мутациями в гене CFTR». Gut . 56 (8): 1153– 1163. doi :10.1136/gut.2004.062786. PMC 1955522 . PMID 17446304.
- Wong LJ, Alper OM, Wang BT, Lee MH, Lo SY (июль 2003 г.). «Две новые нулевые мутации у тайваньского пациента с муковисцидозом и обзор мутаций CFTR в Восточной Азии». Американский журнал медицинской генетики. Часть A. 120A ( 2): 296– 298. doi :10.1002/ajmg.a.20039. PMID 12833420. S2CID 41060230.
- Savant A, Lyman B, Bojanowski C, Upadia J (август 2024 г.). «Кистозный фиброз». Вашингтонский университет, Сиэтл. PMID 20301428.
Внешние ссылки
- Обзор всей структурной информации, доступной в PDB для UniProt : P13569 (регулятор трансмембранной проводимости при муковисцидозе человека) на сайте PDBe-KB .
- Обзор всей структурной информации, доступной в PDB для UniProt : P26361 (регулятор трансмембранной проводимости мышиного муковисцидоза) на сайте PDBe-KB .








