Кислотный краситель
Раздел лида статьи , возможно, необходимо переписать . ( Февраль 2023 ) |

Кислотный краситель — это краситель , который обычно наносится на текстиль при низком pH. Они в основном используются для окрашивания шерсти, а не хлопчатобумажных тканей. [1] Некоторые кислотные красители используются в качестве пищевых красителей, [2] [3] , а некоторые также могут использоваться для окрашивания органелл в медицинской сфере.
Кислотные красители являются анионными, растворимыми в воде и в основном наносятся из кислотной ванны. Эти красители обладают кислотными группами, такими как SO3H и COOH, и наносятся на шерсть, шелк и нейлон, когда между протонированной группой –NH2 волокна и кислотной группой красителя устанавливается ионная связь. Общая устойчивость к стирке плохая, хотя светостойкость довольно хорошая. Поскольку краситель и волокно имеют противоположную электрическую природу, скорость удара и поглощение кислотного красителя на этих волокнах происходит быстрее; электролит в более высокой концентрации добавляется для замедления поглощения красителя и формирования ровных оттенков. Кислота генерирует катион на волокне, а температура помогает заменить отрицательную часть кислоты молекулами анионных красителей. [4]
Описание
Кислотные красители обычно делятся на три класса в зависимости от требований к стойкости, способности к миграции и pH окрашивания. [5]
Кислотные красители прикрепляются к волокнам с помощью водородных связей , сил Ван-дер-Ваальса [6] и ионных связей . Хотя некоторые кислотные красители работают в воде, многие предпочитают активировать красители в кислотных красильных ваннах. Согласно кислотно-основной теории Бренстеда-Лоури , кислота — это молекула или ион, способные отдавать протон, и это определяется константой диссоциации кислоты . По сравнению с большинством кислот, вода имеет гораздо более высокое значение pKa , что означает, что она диссоциирует с образованием H + с большим трудом. В этом контексте, если вместо воды используется кислота, то ион водорода (H + ) легче диссоциирует, чтобы вступить в реакцию с анионом анилинового красителя, позволяя красителю раствориться.
Волокна животного белка и синтетическое волокно нейлон содержат много катионных участков, которые связывают анионный краситель. Прочность (устойчивость) этой связи отражает прочность этого ионного взаимодействия.
Использует
Волокна
В лаборатории, дома или художественной студии кислотой, используемой в красильной ванне, часто является уксус ( уксусная кислота ) или лимонная кислота . Скорость поглощения красителя контролируется с помощью хлорида натрия. В текстильной промышленности кислотные красители эффективны для белковых волокон, т. е. волокон животных волос, таких как шерсть , альпака и мохер . Они также эффективны для шелка . [7] Они эффективны при окрашивании синтетического волокна нейлона , но представляют минимальный интерес для окрашивания любых других синтетических волокон.


Гистология
При окрашивании во время микроскопического исследования для диагностики или исследования кислотные красители используются для окрашивания основных белков тканей. Напротив, основные красители используются для окрашивания ядер клеток и некоторых других кислых компонентов тканей. [8] Что касается клеточных структур, кислотные красители будут окрашивать ацидофильные структуры, которые имеют чистый положительный заряд из-за того, что у них есть отрицательно заряженный хромофор . Ацидофильные структуры включают цитоплазму , коллаген и митохондрии . Эти два имеют сродство друг к другу из-за конфликтующих зарядов. [9] [10] Примеры кислотных красителей, используемых в медицине, включают: [11]
- Окраска по Ли (пятна красновато-розовые).
- Окраска гематоксилином фосфорновольфрамовой кислоты (PTAH) (окрашивает в синий цвет).
- Окраска эозином (окрашивает в розовато-оранжевый цвет).
Пищевая промышленность
Кислотные красители также могут использоваться в качестве пищевых красителей, помогая повысить привлекательность определенных продуктов питания и, таким образом, делая их более привлекательными для покупателей. Некоторые примеры включают эритрозин , тартразин , желтый закат и красный очарование , и это лишь некоторые из них, многие из которых являются азокрасителями . [12] Эти красители могут использоваться в глазури, печенье, хлебе, приправах или напитках. Чтобы предотвратить опасность для здоровья, краситель должен быть одобрен для потребления, прежде чем он может быть маркирован как съедобный. Некоторые методы разделения, которые могут использоваться для идентификации неодобренных красителей, включают процесс твердофазной экстракции , процесс тонкослойной хроматографии под избыточным давлением и использование обращенно-фазовых пластин . [13]
Структуры
Химия кислотных красителей сложна и разнообразна. Большинство кислотных красителей по своей базовой структуре относятся к следующим:
- Тип антрахинона : Многие кислотные красители синтезируются из химических промежуточных соединений, которые образуют в качестве конечного состояния структуры, подобные антрахинону. Многие синие красители имеют эту структуру в качестве своей базовой формы. Структура преобладает в выравнивающем классе кислотных красителей.
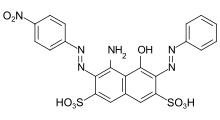
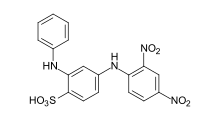
- Азокрасители : Структура азокрасителей содержит азогруппу (RN=N−R. Большинство азокрасителей не являются кислотными красителями, но многие кислотные красители являются азокрасителями. Многие кислотные красители азотипа имеют красный цвет. [14]
- Триарилметановый краситель : Они преобладают в классе красителей для фрезерования. Существует много желтых и зеленых красителей, которые коммерчески применяются для волокон и связаны с трифенилметаном.
Классы кислотных красителей
Кислотные красители можно классифицировать по их красящему поведению. Это включает их устойчивость к влаге, способность к миграции и pH окрашивания: [1]
- Выравнивающие кислотные красители: Эти красители имеют относительно низкий молекулярный вес. Следовательно, они легче мигрируют перед фиксацией и демонстрируют низкую устойчивость к влаге. Обычно они не подходят для использования в качестве тканей для одежды. Для них требуется кислотная красильная ванна, часто с использованием смесей серной кислоты и сульфата натрия (pH2-4), [7] вместе с выравнивающими агентами, такими как этоксилированные жирные амины .
- Красители для фрезерования: Эти красители имеют высокую молекулярную массу, в результате чего они медленно мигрируют. Следовательно, они обладают устойчивостью к влаге, что полезно для окрашивания шерстяных материалов. Красители для фрезерования кислот иногда называют «нейтральными кислотными красителями», поскольку они не требуют кислотной красильной ванны. Обычно их наносят с использованием уксусной кислоты (pH4-7). [7]
- Металлокомплексные кислотные красители: Эти красители состоят из молекул кислотного красителя, связанных с ионом металла, которым обычно является хром или кобальт. Металлокомплексные кислотные красители имеют высокую молекулярную массу, что обеспечивает им низкую подвижность и высокую устойчивость к влаге. Благодаря этому их обычно используют на нейлоновых и синтетических полиамидных волокнах. Металлокомплексные кислотные красители экономичны. Однако они дают относительно тусклые оттенки. Металлокомплексные кислотные красители принимают более широкий диапазон pH в красильной ванне (pH2-7). [7]
Безопасность
Некоторые красители являются мутагенными и канцерогенными, включая метиловый оранжевый , кислотный красный 26 и трипановый синий . [15] [16]
Ссылки
- ^ ab Booth, Gerald (2000). "Dyes, General Survey". Энциклопедия промышленной химии Ульмана . Weinheim: Wiley-VCH. doi :10.1002/14356007.a09_073. ISBN 3527306730.
- ^ Троубридж Филиппоне, Пегги. "Добавки пищевых красителей". Архивировано из оригинала 5 апреля 2015 г. Получено 8 сентября 2016 г.
- ^ Клаус Хангер, изд. (2003), Промышленные красители: химия, свойства, применение (на немецком языке), Вайнхайм: WILEY-VCH Verlag, стр. 276 и далее, ISBN 978-3-662-01950-4
- ^ AK Roy Choudhary, «Подготовка и крашение текстиля», Science Publishers, США (2006)
- ^ "Механизм крашения кислотными красителями". Textile Learner . Mazharul Islam Kiron . Получено 2012-01-08 .
- ^ Кларк, Джим (2012). «Межмолекулярная связь - силы Ван дер Ваальса». chemguide.co.uk . Проверено 15 июня 2014 г.
- ^ abcd "Как работает кислотный краситель" . Получено 21 октября 2019 г.
- ^ Брукнер, Моника З. "Базовое клеточное окрашивание" . Получено 12 декабря 2013 г.
- ^ "Окрашивание и общеупотребительные красители". Система обучения гистологии . Бостонский университет . Получено 2019-11-05 .
- ^ Гохале, С (2008). Фармацевтическая биология . Махараштра, Индия: Pragati Books Pvt. ООО
- ^ "Окрашивание и общеупотребительные красители". Система обучения гистологии . Бостонский университет . Получено 2019-11-05 .
- ^ Фрейзер, РА (2007). КАПИЛЛЯРНЫЙ ЭЛЕКТРОФОРЕЗ | Пищевые добавки . Elsevier Ltd.
- ^ Вега, М. (2000). Энциклопедия науки о разделении . Elsevier Ltd.
- ^ Голод, Клаус; Мишке, Питер; Рипер, Вольфганг; Рауэ, Родерих; Кунде, Клаус; Энгель, Алоис (2005). «Азокрасители». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH . дои : 10.1002/14356007.a03_245. ISBN 3527306730.
- ^ Prival, MJ; Bell, SJ; Mitchell, VD; Peiperl, MD; Vaughan, VL (1984). «Мутагенность бензидина и конгенерных бензидиновых красителей и выбранных моноазокрасителей в модифицированном анализе Salmonella». Mutation Research . 136 (1): 33– 47. doi :10.1016/0165-1218(84)90132-0. PMID 6371512.
- ^ Бансал, Мегха; Ядав, Раджеш Кумар (2016). «ОПАСНОСТИ ДЛЯ ЗДОРОВЬЯ НА ПРОИЗВОДСТВЕ И ОСВЕДОМЛЕННОСТЬ О БЕЗОПАСНОСТИ ТРУДА СРЕДИ РАБОТНИКОВ ТЕКСТИЛЬНЫХ КРАШИЛЬНЫХ ПРОМЫШЛЕННОСТЕЙ В ДЖАЙПУРЕ, ИНДИЯ». Suresh Gyan Vihar University International Journal of Environment, Science and Technology . 2 (2): 30–38 . S2CID 37596329.