Феноксиэтанол
 | |
 | |
| Имена | |
|---|---|
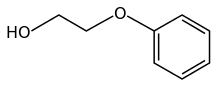
| Предпочтительное название ИЮПАК 2-феноксиэтан-1-ол | |
| Другие имена Феноксиэтанол Монофениловый эфир этиленгликоля Фенокситоларозол Дованол EP / EPH Протектол PE Эмери 6705 Эфир розы 1-гидрокси-2-феноксиэтан β-гидроксиэтилфениловый эфир Фенилцеллозольв Феноксетол® | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| Информационная карта ECHA | 100.004.173 |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С8Н10О2 | |
| Молярная масса | 138,166 г·моль −1 |
| Появление | Бесцветная маслянистая жидкость |
| Запах | слабый розоподобный |
| Плотность | 1.102 г/см 3 |
| Температура плавления | −2 °C (28 °F; 271 К) |
| Точка кипения | 247 °C (477 °F; 520 К) |
| 26 г/кг | |
| Растворимость | Хлороформ , щелочь , диэтиловый эфир : растворим |
| Растворимость в арахисовом масле | немного |
| Растворимость в оливковом масле | немного |
| Растворимость в ацетоне | смешивающийся |
| Растворимость в этаноле | смешивающийся |
| Растворимость в глицерине | смешивающийся |
| Давление пара | 0,001 кПа (0,00015 фунт/кв. дюйм) |
| Теплопроводность | 0,169 Вт/(м⋅К) |
Показатель преломления ( nD ) | 1,534 (20 °С) |
| Опасности | |
| Охрана труда и техника безопасности (OHS/OSH): | |
Основные опасности | Вредно при проглатывании. Вызывает серьезное раздражение глаз. |
| Маркировка СГС : | |
 | |
| Предупреждение | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 126 °C (259 °F; 399 К) |
| 430 °C (806 °F; 703 К) | |
| Смертельная доза или концентрация (ЛД, ЛК): | |
LD 50 ( средняя доза ) | 1850 мг/кг (крыса, перорально) |
| Родственные соединения | |
Родственные соединения | фенетол |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Феноксиэтанол — органическое соединение с формулой C 6 H 5 OC 2 H 4 OH. Это бесцветная маслянистая жидкость. Его можно классифицировать как гликолевый эфир и фенольный эфир . Это распространенный консервант в вакцинных составах. [4] Он имеет слабый аромат розы. [5]
Использовать
Феноксиэтанол обладает бактерицидными и бактериостатическими свойствами. [6] Его часто используют вместе с четвертичными аммониевыми соединениями .
Феноксиэтанол используется как фиксатор духов ; средство от насекомых ; антисептик ; [7] растворитель для ацетата целлюлозы , красителей, чернил и смол; консервант для фармацевтических препаратов, косметики и смазочных материалов; [8] анестетик в рыбоводстве; [ 9 ] [10] и в органическом синтезе .
Это альтернатива консервантам, выделяющим формальдегид . [11] В Японии и Европейском Союзе его концентрация в косметике ограничена 1%. [12]
История и синтез
Феноксиэтанол был впервые получен WH Perkin Jr. и его аспирантом Edward Haworth в 1896 году. [13] Они провели реакцию натрия , фенола и 2-хлорэтанола в безводном этаноле. [14] Начиная с 1920-х годов он стал коммерчески доступен как растворитель ацетата целлюлозы под торговой маркой «Phenyl cellosolve». [15]
Соединение получают в промышленности путем гидроксиэтилирования фенола ( синтез Уильямсона ), например, в присутствии гидроксидов щелочных металлов или борогидридов щелочных металлов. [1]
Эффективность
Феноксиэтанол эффективен против грамотрицательных и грамположительных бактерий , а также дрожжей Candida albicans . [16]
| Ароматный спирт | Концентрация (%) | Время контакта (минуты) | |||
|---|---|---|---|---|---|
| Escherichia coli | Синегнойная палочка | Протей чудесный | Золотистый стафилококк | ||
| Бензиловый спирт | 1 | >30 | >30 | >30 | >30 |
| Фенилэтиловый спирт | 1.25 | 2.5 | 2.5 | 2.5 | >30 |
| 2.5 | 2.5 | 2.5 | 2.5 | 5 | |
| Феноксиэтанол | 1.25 | 15 | 2.5 | 2.5 | >30 |
| 2.5 | 2.5 | 2.5 | 2.5 | >30 | |
Безопасность
Феноксиэтанол — консервант вакцины и потенциальный аллерген, который может вызвать узелковую реакцию в месте инъекции. Возможные симптомы включают сыпь, экзему и возможную смерть. [17] Он обратимо ингибирует ионные токи, опосредованные NMDAR . [18]
Экологические соображения
Ввиду широкого использования феноксиэтанола, его биодеградация была изучена. Один путь включает начальное преобразование в фенол и ацетальдегид. [19]
Ссылки
- ^ аб Хельмут Фиге; Хайнц-Вернер Фогес; Тошиказу Хамамото; Сумио Умемура; Тадао Ивата; Хисая Мики; Ясухиро Фудзита; Ханс-Йозеф Буйш; Доротея Гарбе; Вильфрид Паулюс (2007). «Производные фенола». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_313. ISBN 978-3-527-30673-2.
- ^ Комиссия, Британская фармакопея (2009), «Феноксиэтанол», Британская фармакопея , т. 2, Канцелярия, ISBN 978-0-11-322799-0
- ^ Дэвид Р. Лид, ред. (2010), CRC Handbook of Chemistry and Physics (90-е изд.), CRC Press
- ^ Мейер, Брайан К.; Ни, Алекс; Ху, Бинхуа; Ши, Ли (2007). «Использование противомикробных консервантов в парентеральных препаратах: прошлое и настоящее». Журнал фармацевтических наук . 96 (12): 3155–3167 . doi :10.1002/jps.20976. ПМИД 17722087.
- ^ ab Ганс-П. Харке (2007), «Дезинфицирующие средства», Энциклопедия промышленной химии Ульмана (7-е изд.), Wiley, стр. 1–17 , doi :10.1002/14356007.a08_551, ISBN 978-3-527-30673-2
- ^ Нолан, Ричард А.; Нолан, Уильям Г. (1972). «Феноксиэтанол как экстрагент и консервант грибковых ферментов». Mycologia . 64 (6): 1344– 1349. doi :10.2307/3757974. ISSN 0027-5514. JSTOR 3757974.
- ^ Розенберг, Херб (1992). «Улучшение лабораторных условий с помощью нейтрализующего агента». Американский учитель биологии . 54 (6): 327. doi :10.2307/4449498. ISSN 0002-7685. JSTOR 4449498.
- ^ Nakanishi, Mikiye; Wilson, Allan C.; Nolan, Richard A.; Gorman, George C.; Bailey, George S. (1969). «Феноксиэтанол: белковый консервант для таксономистов». Science . 163 (3868): 681– 683. Bibcode :1969Sci...163..681N. doi :10.1126/science.163.3868.681. ISSN 0036-8075. JSTOR 1726343. PMID 5762931.
- ^ Руни, Шон М.; Уайтман, Глен; О'Кончуир, Руайри; Кинг, Джеймс Дж. (2015). «Поведение морской миноги (Petromyzon marinus L.) у искусственных препятствий во время нерестовой миграции вверх по реке: использование телеметрии для оценки эффективности модификаций плотин для улучшения прохода». Биология и окружающая среда: Труды Королевской Ирландской академии . 115B (2): 125– 136. doi :10.3318/bioe.2015.14. ISSN 0791-7945. JSTOR 10.3318/bioe.2015.14.
- ^ Данабас, Дурали; Йылдырым, Нуран Джикчикоглу; Йылдирим, Нуман; Онал, Айтен Озтуфекчи; Услу, Гульсад; Унлу, Эрхан; Данабас, Севаль; Эргин, Джемиль; Тайхан, Нилгун (2016). «Цитокиновые реакции в жабрах Capoeta umbla как биомаркеры загрязнения окружающей среды». Исследования водной среды . 88 (3): 217–222 . Бибкод : 2016WaEnR..88..217D. дои : 10.2175/106143016X14504669767616. ISSN 1061-4303. JSTOR 44134400. PMID 26931532.
- ^ Wineski LE, English AW (1989). «Феноксиэтанол как нетоксичный консервант в лаборатории препарирования». Acta Anat (Базель) . 136 (2): 155– 8. doi :10.1159/000146816. PMID 2816264.
- ^ Токунага Х, Такеучи О, Ко Р, Учино Т, Андо М (2003). «Исследования по анализу феноксиэтанола» и парабены в коммерческих лосьонах] (PDF) . Кокурицу Иякухин Сёкухин Эйсэй Кенкюдзё Хококу (на японском языке) (121): 25–9 . PMID 14740401.
- ↑ Тезисы трудов Химического общества. Химическое общество. 1895.
- ^ Бентли, Уильям Генри; Хаворт, Эдвард; Перкин, Уильям Генри (1896). «О γ-феноксипроизводных малоновой и уксусной кислот, а также различных соединениях, используемых в синтезе этих кислот». Журнал химического общества, Труды . 69 : 161– 175. doi :10.1039/CT8966900161. ISSN 0368-1645.
- ^ Корпорация Union Carbide (1929). Отчет.
- ^ Lowe I, Southern J (1994). «Антимикробная активность феноксиэтанола в вакцинах». Lett Appl Microbiol . 18 (2): 115– 6. doi :10.1111/j.1472-765X.1994.tb00820.x. PMID 7764595. S2CID 12124463.
- ^ MH Beck; SM Wilkinson (2010), «Контактный дерматит: аллергический», в Tony Burns; Stephen Breathnach; Neil Cox; Christopher Griffiths (ред.), Rook's Textbook of Dermatology , т. 2 (8-е изд.), Wiley-Blackwell, стр. 26.46, ISBN 978-1-4051-6169-5
- ^ Schmuck G, Steffens W, Bomhard E (июль 2000 г.). «2-феноксиэтанол: нейротоксикант?». Архив токсикологии . 74 ( 4–5 ): 281–7 . Bibcode : 2000ArTox..74..281S. doi : 10.1007/s002040000110. PMID 10959804. S2CID 6999187.
- ^ Ghattas, Ann-Kathrin; Fischer, Ferdinand; Wick, Arne; Ternes, Thomas A. (2017). «Анаэробная биодеградация (возникающих) органических загрязнителей в водной среде». Water Research . 116 : 268–295 . Bibcode : 2017WatRe.116..268G. doi : 10.1016/j.watres.2017.02.001 . PMID 28347952.



