УВА-101
 | |
| Правовой статус | |
|---|---|
| Правовой статус |
|
| Идентификаторы | |
| |
| Номер CAS |
|
| CID PubChem |
|
| ChemSpider |
|
| УНИИ |
|
| ChEMBL |
|
| Панель инструментов CompTox ( EPA ) |
|
| Химические и физические данные | |
| Формула | С13Н17Н2 |
| Молярная масса | 219,284 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| |
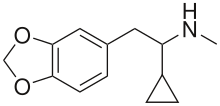
UWA-101 (также известный как α-циклопропил-MDMA ) — производное фенэтиламина , исследуемое как потенциальное средство для лечения болезни Паркинсона . Его химическая структура очень похожа на структуру нелегального наркотика MDMA , единственное отличие заключается в замене α- метильной группы на α- циклопропильную группу. В исследованиях на животных и несанкционированных экспериментах на людях было обнаружено, что MDMA эффективен в краткосрочном облегчении побочных эффектов терапии болезни Паркинсона, в частности, дискинезии, вызванной леводопой. [1] [2] [3] [4] Однако нелегальный статус MDMA и опасения по поводу его потенциала для рекреационного использования, нейротоксичности и потенциально опасных побочных эффектов означают, что его вряд ли будут исследовать для медицинского использования в этом приложении, поэтому были исследованы альтернативные аналоги. [5]
Замена α-метила на циклопропил резко снижает сродство к переносчику норадреналина и рецептору 5-HT 2A , сохраняя при этом высокое сродство к переносчику серотонина и заметно увеличивая сродство к переносчику дофамина (и, таким образом, это один из немногих селективных ингибиторов обратного захвата серотонина-дофамина ). Это изменение приводит к тому, что UWA-101 теряет цитотоксичность и поведенческие эффекты, подобные MDMA, у животных, сохраняя при этом аналогичную или слегка улучшенную антидискинетическю эффективность по сравнению с MDMA. [6] Это исследование стало продолжением более ранней работы той же группы под руководством химика-медика Мэтью Пигготта из Университета Западной Австралии, которая показала, что замена α-метильной группы MDMA на более крупные ароматические кольцевые системы приводит к образованию соединений, которые не обладают психоактивностью и нейротоксичностью, но обладают мощным противораковым действием против клеток лимфомы Беркитта in vitro . [7] [8]
UWA-121 является ( R ) -энантиомером UWA-101, а ( S )-энантиомером является UWA-122. [9] Оба являются активными ингибиторами обратного захвата моноаминов. [9] UWA-121 является селективным ингибитором обратного захвата дофамина с 10-кратным преимуществом в ингибировании обратного захвата дофамина по сравнению с обратным захватом серотонина, в то время как UWA-122 является высокоселективным ингибитором обратного захвата серотонина . [9]
Другим родственником является UWA-104 («α-изопропил-MDMA»), который также активен. [6] Это селективный ингибитор обратного захвата дофамина , с более чем 30-кратной селективностью по сравнению с другими транспортерами моноаминов или рецептором серотонина 5-HT 2A . [6] Другие аналоги включают UWA-091 («α-пропил-MDMA»), UWA-102 («α- трет -бутил-MDMA») и UWA-001 («α-фенил-MDMA»). [6] Сообщалось о фармакологической активности UWA-101, UWA-104 и UWA-001 in vitro. [ 6 ]
Смотрите также
- МБДБ
- Метил-К (UWA-091)
- Изогексилон
- УВА-001
- Зилофурамин
- RTI-83 — еще один препарат, который избирательно повышает уровень дофамина и серотонина, не влияя на норадреналин.
Ссылки
- ^ Schmidt WJ, Mayerhofer A, Meyer A, Kovar KA (сентябрь 2002 г.). «Экстази противодействует каталепсии у крыс, антипаркинсонический эффект?». Neuroscience Letters . 330 (3): 251– 4. doi :10.1016/s0304-3940(02)00823-6. PMID 12270640. S2CID 41609012.
- ^ Iravani MM, Jackson MJ, Kuoppamäki M, Smith LA, Jenner P (октябрь 2003 г.). «3,4-метилендиоксиметамфетамин (экстази) подавляет проявление дискинезии и нормализует двигательную активность у приматов, леченных 1-метил-4-фенил-1,2,3,6-тетрагидропиридином». The Journal of Neuroscience . 23 (27): 9107– 15. doi :10.1523/JNEUROSCI.23-27-09107.2003. PMC 6740822 . PMID 14534244.
- ^ Lebsanft HB, Kohles T, Kovar KA, Schmidt WJ (март 2005 г.). «3,4-Метилендиоксиметамфетамин противодействует акинезии энантиоселективно при вращательном поведении крыс и каталепсии». Synapse . 55 (3): 148– 55. doi :10.1002/syn.20102. PMID 15602749. S2CID 24601744.
- ^ Huot P, Johnston TH, Lewis KD, Koprich JB, Reyes MG, Fox SH и др. (май 2011 г.). «Характеристика энантиомеров 3,4-метилендиоксиметамфетамина (МДМА) in vitro и у приматов с поражением MPTP: R-MDMA снижает тяжесть дискинезии, тогда как S-MDMA увеличивает продолжительность ON-time». The Journal of Neuroscience . 31 (19): 7190– 8. doi :10.1523/JNEUROSCI.1171-11.2011. PMC 6703214 . PMID 21562283.
- ↑ Jerome I (весна 2008 г.). «MDMA и болезнь Паркинсона: много исследований, мало практических ответов» (PDF) . MAPS . XVI (1): 16– 18. Архивировано (PDF) из оригинала 2011-09-15 . Получено 2012-04-09 .
- ^ abcde Johnston TH, Millar Z, Huot P, Wagg K, Thiele S, Salomonczyk D и др. (май 2012 г.). «Новый аналог MDMA, UWA-101, не обладающий психоактивностью и цитотоксичностью, усиливает действие L-DOPA на приматов, страдающих паркинсонизмом». FASEB Journal . 26 (5): 2154– 63. doi : 10.1096/fj.11-195016 . PMID 22345403. S2CID 37589231.
- ^ Gandy MN, McIldowie M, Lewis K, Wasik AM, Salomonczyk D, Wagg K и др. (2010). «Перепроектирование дизайнерского наркотика экстази: непсихоактивные аналоги MDMA, проявляющие цитотоксичность при лимфоме Беркитта». MedChemComm . 1 (4): 287– 293. doi :10.1039/c0md00108b.
- ^ Wasik AM, Gandy MN, McIldowie M, Holder MJ, Chamba A, Challa A и др. (август 2012 г.). «Усиление противолимфомного потенциала 3,4-метилендиоксиметамфетамина («экстази») посредством итеративной химической переработки: механизмы и пути к гибели клеток» (PDF) . Investigational New Drugs . 30 (4): 1471– 83. doi :10.1007/s10637-011-9730-5. PMID 21850491. S2CID 20880580. Архивировано (PDF) из оригинала 2020-03-10 . Получено 2019-09-18 .
- ^ abc Huot P, Johnston TH, Lewis KD, Koprich JB, Reyes MG, Fox SH и др. (июль 2014 г.). «UWA-121, смешанный ингибитор обратного захвата дофамина и серотонина, усиливает противопаркинсоническое действие L-ДОФА, не ухудшая дискинезию или психозоподобное поведение у мартышек с поражением MPTP». Neuropharmacology . 82 : 76– 87. doi : 10.1016/j.neuropharm.2014.01.012. PMID 24447715. S2CID 37160397.
Внешние ссылки
- Танцуют ли неврологи? Личный опыт болезни Паркинсона и МДМА, Тим Лоуренс, 2003