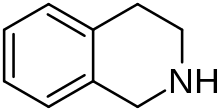
Тетрагидроизохинолин
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 1,2,3,4-Тетрагидроизохинолин | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| Сокращения | ТИК, ТИК |
| ChEMBL | |
| ChemSpider | |
| Информационная карта ECHA | 100.001.864 |
| Номер ЕС |
|
CID PubChem |
|
| Номер RTECS |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С 9 Н 11 Н | |
| Молярная масса | 133,19 г/моль |
| Появление | Жидкость темно-желтого цвета |
| Плотность | 1,05 г/мл |
| Температура плавления | −30 °C (−22 °F; 243 К) |
| Точка кипения | 235–239 °C (455–462 °F; 508–512 K) |
| Опасности | |
| Маркировка СГС : [1] | |
   | |
| Опасность | |
| Н301 , Н310 , Н314 , Н332 , Н371 , Н412 | |
| P260 , P261 , P262 , P264 , P270 , P271 , P273 , P280 , P301+P310 , P301+P330+P331 , P302+P350 , P302+P352 , P303+P361+P353 , P304+P312 , P304+P340 , P305+P351+P338 , P309+P311 , P310 , P312 , P322 , P330 , P332+P313 , P337+P313 , P361 , P362 , P363 , P403+P233 , P405 , П501 | |
| точка возгорания | 99 °C (210 °F; 372 K) (закрытый тигель) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Тетрагидроизохинолин ( TIQ или THIQ ) — органическое соединение с химической формулой C9H11N . Классифицируется как вторичный амин , его получают из изохинолина путем гидрирования. Это бесцветная вязкая жидкость, смешивающаяся с большинством органических растворителей. Скелет тетрагидроизохинолина встречается в ряде биологически активных соединений и лекарственных препаратов. [ 2] [3]
Реакции
Как вторичный амин, тетрагидроизохинолин обладает слабоосновными свойствами и образует соли с сильными кислотами. Он может быть дегидрирован с образованием изохинолина и гидрирован до декагидроизохинолина . Как и другие вторичные амины, тетрагидроизохинолин может быть окислен до соответствующего нитрона с использованием перекиси водорода , катализируемой диоксидом селена . [4]
Токсикология
Производные тетрагидроизохинолина могут образовываться в организме как метаболиты некоторых препаратов, и когда-то считалось, что это связано с развитием алкоголизма . [5] Эта теория в настоящее время дискредитирована и больше не является общепринятой в научном сообществе, [6] но эндогенное производство нейротоксичных производных тетрагидроизохинолина, таких как норсалсолинол, продолжает исследоваться как возможные причины некоторых состояний, таких как болезнь Паркинсона . [7] [8] [9] [10] [11] [12]
Тетрагидроизохинолины
Тетрагидроизохинолиновый скелет присутствует в ряде препаратов, [3] таких как тубокурарин , один из четвертичных аммониевых миорелаксантов . Препараты на основе 4-замещенных тетрагидроизохинолинов включают номифензин [13] и диклофензин . Их можно получить путем N -алкилирования бензиламинов галогенацетофенонами . [ 14] Природные тетрагидроизохинолины включают чериллин [15] и латифин.
Эспрохин [16], который проявляет гипотензивную активность благодаря своим α-адреноблокирующим свойствам, производится из THIQ.
Ссылки
- ^ "1,2,3,4-Тетрагидроизохинолин". pubchem.ncbi.nlm.nih.gov . Получено 12 декабря 2021 г. .
- ^ Митченсон, Эндрю (2000). «Насыщенные азотсодержащие гетероциклы». Журнал химического общества, Perkin Transactions 1 (17): 2862– 2892. doi :10.1039/A908537H.
- ^ ab Скотт, Джек Д.; Уильямс, Роберт М. (2002). «Химия и биология противоопухолевых антибиотиков тетрагидроизохинолина». Chemical Reviews . 102 (5): 1669– 1730. doi :10.1021/cr010212u. PMID 11996547.
- ^ Мурахаши, С. (1987). «Окисление вторичных аминов, катализируемое диоксидом селена перекисью водорода. Простой синтез нитронов из вторичных аминов». Tetrahedron Letters . 28 (21): 2383– 2386. doi :10.1016/S0040-4039(00)96130-6.
- ^ Блум, К.; Гамильтон, МГ; Хёрст, М.; Уоллес, ДЖ. Э. (1978). «Предполагаемая роль изохинолиновых алкалоидов в алкоголизме: связь с опиатами». Алкоголизм: клинические и экспериментальные исследования . 2 (2): 113– 120. doi :10.1111/j.1530-0277.1978.tb04710.x. PMID 350073., Альтшулер, ХЛ; Шиппенберг (1982). «Тетрагидроизохинолин и опиоидные субстраты действия алкоголя». Прогресс в клинических и биологических исследованиях . 90 : 329–344 . PMID 7202207., Майерс, РД (1989). «Изохинолины, бета-карболины и употребление алкоголя: участие опиоидных и дофаминергических механизмов». Experientia . 45 (5): 436– 443. doi :10.1007/BF01952025. PMID 2656285. S2CID 1513683.
- ^ Майерс, РД (1996). «Тетрагидроизохинолины и алкоголизм: где мы сегодня?». Алкоголизм: клинические и экспериментальные исследования . 20 (3): 498– 500. doi :10.1111/j.1530-0277.1996.tb01081.x. PMID 8727243., Musshoff, F.; Daldrup, T.; Bonte, W.; Leitner, A.; Lesch, OM (1996). «Формальдегид-производные тетрагидроизохинолины и тетрагидро-бета-карболины в моче человека». Журнал хроматографии B. 683 ( 2): 163– 176. doi :10.1016/0378-4347(96)00106-5. PMID 8891913., Sällström Baum, S.; Hill, R.; Kiianmaa, K.; Rommelspacher, H. (1999). "Влияние этанола на (R)- и (S)-сальсолинол, сальсолин и THP в прилежащем ядре крыс AA и ANA". Alcohol (Фейетвилл, Нью-Йорк) . 18 ( 2–3 ): 165–169 . doi :10.1016/S0741-8329(98)00080-9. PMID 10456568., Musshoff, F.; Lachenmeier, DW; Schmidt, P.; Dettmeyer, R.; Madea, B. (2005). "Систематическое региональное исследование уровней дофамина, норсалсолинола и (R/S)-салсолинола в областях человеческого мозга алкоголиков". Алкоголизм: клинические и экспериментальные исследования . 29 (1): 46– 52. doi :10.1097/01.ALC.0000150011.81102.C2. PMID 15654290.
- ^ Kotake Y, Tasaki Y, Makino Y, Ohta S, Hirobe M (декабрь 1995 г.). «1-Бензил-1,2,3,4-тетрагидроизохинолин как агент, вызывающий паркинсонизм: новый эндогенный амин в мозге мышей и паркинсонической спинномозговой жидкости». Journal of Neurochemistry . 65 (6): 2633– 8. doi :10.1046/j.1471-4159.1995.65062633.x. PMID 7595560. S2CID 39449026.
- ^ McNaught KS, Carrupt PA, Altomare C, Cellamare S, Carotti A, Testa B, Jenner P, Marsden CD (октябрь 1998 г.). «Производные изохинолина как эндогенные нейротоксины в этиологии болезни Паркинсона». Биохимическая фармакология . 56 (8): 921– 33. doi :10.1016/S0006-2952(98)00142-7. PMID 9776302.
- ^ Lorenc-Koci E, Smiałowska M, Antkiewicz-Michaluk L, Gołembiowska K, Bajkowska M, Wolfarth S (2000). «Влияние острого и хронического введения 1,2,3,4-тетрагидроизохинолина на мышечный тонус, метаболизм дофамина в полосатом теле и иммуноцитохимию тирозингидроксилазы в черной субстанции у крыс». Neuroscience . 95 (4): 1049– 59. doi :10.1016/S0306-4522(99)00511-4. PMID 10682712. S2CID 13549697.
- ^ Storch A, Ott S, Hwang YI, Ortmann R, Hein A, Frenzel S, Matsubara K, Ohta S, Wolf HU, Schwarz J (март 2002 г.). «Селективная дофаминергическая нейротоксичность производных изохинолина, связанная с болезнью Паркинсона: исследования с использованием гетерологичных систем экспрессии транспортера дофамина». Biochemical Pharmacology . 63 (5): 909– 20. doi :10.1016/S0006-2952(01)00922-4. PMID 11911843.
- ^ Lorenc-Koci E, Antkiewicz-Michaluk L, Kamińska A, Lenda T, Zieba B, Wierońska J, Smiałowska M, Schulze G, Rommelspacher H (октябрь 2008 г.). «Влияние острого и хронического введения 1,2-диметил-6,7-дигидрокси-1,2,3,4-тетрагидроизохинолина на функцию нигростриарной дофаминергической системы у крыс». Neuroscience . 156 (4): 973– 86. doi :10.1016/j.neuroscience.2008.08.050. PMID 18809471. S2CID 44658852.
- ^ Kobayashi H, Fukuhara K, Tada-Oikawa S, Yada Y, Hiraku Y, Murata M, Oikawa S (январь 2009 г.). «Механизмы окислительного повреждения ДНК и апоптоза, вызванного норсалсолинолом, эндогенным производным тетрагидроизохинолина, связанным с болезнью Паркинсона». Journal of Neurochemistry . 108 (2): 397– 407. doi : 10.1111/j.1471-4159.2008.05774.x . PMID 19012744.
- ^ Шнайдер, CS; Вебер, KH; Дэниел, H.; Бехтель, WD; Бёке-Кун, K. (1984). «Синтез и антидепрессантная активность производных 4-арилтетрагидротиено[2,3-c]пиридина». Журнал медицинской химии . 27 (9): 1150– 1155. doi :10.1021/jm00375a011. PMID 6471069.
- ^ БГ 49761
- ^ шериллин
- ^ Грей, Аллан П.; Шили, Ричард Х. (1973). «Подготовка и сердечно-сосудистые действия группы производных тетрагидроизохинолина». Журнал медицинской химии . 16 (7): 859– 861. doi :10.1021/jm00265a028. ISSN 0022-2623. PMID 4146907.


