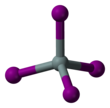
Тетраиодид кремния
 | |||
 | |||
| Имена | |||
|---|---|---|---|
| Другие имена тетраиодид кремния Тетраиодосилан | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| ChemSpider | |||
| Информационная карта ECHA | 100.033.355 | ||
| Номер ЕС |
| ||
CID PubChem |
| ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| SiI 4 | |||
| Молярная масса | 535,7034 г/моль | ||
| Появление | белый порошок | ||
| Плотность | 4,198 г/см 3 | ||
| Температура плавления | 120,5 °C (248,9 °F; 393,6 К) | ||
| Точка кипения | 287,4 °C (549,3 °F; 560,5 К) | ||
| реагирует | |||
| Растворимость в органических растворителях | растворимый | ||
| Структура | |||
| тетраэдрический | |||
| Опасности | |||
| Маркировка СГС : | |||
    | |||
| Опасность | |||
| Н301 , Н311 , Н314 , Н317 , Н334 , Н360 | |||
| Р201 , Р202 , Р260 , Р261 , Р264 , Р270 , Р272 , Р280 , Р281 , Р285 , Р301+Р310 , Р301+Р330+Р331 , Р302+Р352 , Р303+Р361+Р353 , Р304+Р340 , Р304+Р341 , Р305+Р351+Р338 , Р308+Р313 , Р310 , Р312 , Р321 , Р322 , Р330 , Р333+Р313 , Р342+Р311 , Р361 , Р363 , Р405 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Другие анионы | Тетрафторид кремния Тетрахлорид кремния Тетрабромид кремния | ||
Другие катионы | Тетраиодид углерода Тетраиодид германия Иодид олова(IV) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Тетраиодид кремния — химическое соединение с формулой Si I 4 . Это тетраэдрическая молекула с длиной связей Si-I 2,432(5) Å. [1]
SiI 4 является предшественником амидов кремния с формулой Si(NR 2 ) 4 (R = алкил). [2] Он также представляет интерес при производстве и травлении кремния в микроэлектронике .
Синтез и реакции
Это соединение получают путем обработки смеси кремния и меди йодом: [3]
- Si + I2 → SiI4
Быстро реагирует с водой и влагой воздуха.
Его также можно производить в больших масштабах путем реакции кремния или карбида кремния с йодом при нагревании примерно до 200 °C. Более академический интерес представляет реакция силана с парами йода при 130–150 °C, так как в результате образуется ряд соединений от йодсилана SiH 3 I до дийодсилана SiH 2 I 2 и трийодсилана SiHI 3 . Эти соединения представляют собой бесцветные жидкости при комнатной температуре. [4] Последнее можно легко отличить от похожего углеродного соединения, йодоформа , который при комнатной температуре представляет собой желтое твердое вещество.
Сравнение с другими SiX4соединения
| SiH4 | SiF4 | SiCl4 | SiBr4 | SiI 4 | |
|---|---|---|---|---|---|
| температура кипения (˚C) [5] | -111,9 | -90,3 | 56.8 | 155.0 | 290.0 |
| т.пл. (˚C) [5] | -185 | -95.0 | -68,8 | 5.0 | 155.0 |
| Длина связи Si-X (Å) | >0,74 [6] | 1.55 | 2.02 | 2.20 | 2.43 |
| Энергия связи Si-X (кДж/моль) [7] | 384 | 582 | 391 | 310 | 234 |
Ссылки
- ^ Колониц, Мария; Харгиттай, Магдолна (1998). «Молекулярная структура тетраиодида кремния». Структурная химия . 9 (5): 349–352. doi :10.1023/A:1022462926682. S2CID 96658381.
- ^ Баннерджи, Чиранджиб; Уэйд, Кейси Р.; Соулет, Аксель; Юрсич, Грегори; МакЭндрю, Джеймс; Бело, Джон А. (2006). «Прямой синтез и полная характеристика тетракис(диалкиламино)силанов, не содержащих галогенидов». Inorganic Chemistry Communications . 9 (7): 761. doi :10.1016/j.inoche.2006.04.027.
- ^ PW Schenk (1963). «Кремний и германий». В G. Brauer (ред.). Справочник по препаративной неорганической химии, 2-е изд . Т. 2стр.=689. Нью-Йорк, Нью-Йорк: Academic Press.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ ab Кремниевые соединения, Галогениды кремния. Коллинз, У.: Энциклопедия химической технологии Кирка-Отмера; John Wiley & Sons, Inc, 2001.
- ^ "Какова длина связи HH?". Answers.com .
- ^ Эбсворт, EAV В Летучие соединения кремния; Таубе, H.; Мэддок, AG; Неорганическая химия; Pergamon Press Book: Нью-Йорк, штат Нью-Йорк, 1963; Том 4.
Внешние ссылки
- страница веб-элементов