Гексафторид рения
 | |
| Имена | |
|---|---|
| Название ИЮПАК фторид рения(VI) | |
| Другие имена гексафторид рения | |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| Информационная карта ECHA | 100.030.144 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| Ф 6 Ре | |
| Молярная масса | 300,20 г/моль |
| Появление | жидкость или желтое кристаллическое вещество [1] |
| Плотность | 4,94 г/мл [2] |
| Температура плавления | 18,5 °C (65,3 °F; 291,6 К) [1] |
| Точка кипения | 33,7 °C (92,7 °F; 306,8 К) [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гексафторид рения , также фторид рения(VI) (ReF6 ) — соединение рения и фтора , один из семнадцати известных бинарных гексафторидов .
Химия
Гексафторид рения получают путем соединения гептафторида рения с дополнительным металлическим рением при температуре 300 °C в сосуде под давлением . [2]
- 6 Реф
7+ Ре → 7 РеФ
6
Соединение является кислотой Льюиса и сильным окислителем, образуя аддукт фторида калия и окисляя оксид азота до нитрозила: [3]
- 2КФ + РеФ 6 → К 2 РеФ 8
- НЕТ + ReF 6 → [НЕТ][ReF 6 ]
Описание
Гексафторид рения — жидкость при комнатной температуре. При 18,5 °C он замерзает, превращаясь в желтое твердое вещество. Температура кипения — 33,7 °C. [1]
Твердая структура, измеренная при −140 °C, является орторомбической пространственной группой Pnma . Параметры решетки a = 9,417 Å , b = 8,570 Å и c = 4,965 Å. На элементарную ячейку приходится четыре формульные единицы (в данном случае дискретные молекулы) , что дает плотность 4,94 г·см −3 . [2]
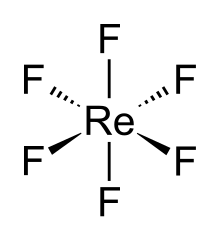
Сама молекула ReF 6 (форма, важная для жидкой или газовой фазы) имеет октаэдрическую молекулярную геометрию , которая имеет точечную группу ( O h ). Длина связи Re–F составляет 1,823 Å. [2]
Использовать
Гексафторид рения — коммерческий материал, используемый в электронной промышленности для нанесения пленок рения. [3]
Ссылки
- ^ abcd CRC Handbook of Chemistry and Physics , 90-е издание, CRC Press, Бока-Ратон, Флорида, 2009, ISBN 978-1-4200-9084-0 , Раздел 4, Физические константы неорганических соединений , стр. 4-85.
- ^ abcd T. Drews, J. Supeł, A. Hagenbach, K. Seppelt: «Твердотельные молекулярные структуры гексафторидов переходных металлов», в: Неорганическая химия , 2006 , 45 (9) , S. 3782–3788; doi :10.1021/ic052029f; PMID 16634614.
- ^ ab Meshri, DT (2000). "Соединения фтора, неорганические, рений". Энциклопедия химической технологии Кирка-Отмера . doi :10.1002/0471238961.1808051413051908.a01. ISBN 0471238961.
Дальнейшее чтение
- Gmelins Handbuch der anorganischen Chemie , System Nr. 70, Рений, Часть А, стр. 102–105.
Внешние ссылки
- Гексафторид рения на webelements.com.
