Тетрагидропиран
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Оксан | |||
| Другие имена Тетрагидропиран, Оксациклогексан, 1,5-эпоксипентан | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 102436 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| DrugBank | |||
| Информационная карта ECHA | 100.005.048 | ||
| Номер ЕС |
| ||
CID PubChem |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С5Н10О | |||
| Молярная масса | 86,134 г·моль −1 | ||
| Появление | Бесцветная жидкость. | ||
| Плотность | 0,880 г/см 3 | ||
| Температура плавления | −45 °C (−49 °F; 228 K) | ||
| Точка кипения | 88 °C (190 °F; 361 К) | ||
| Опасности | |||
| Охрана труда и техника безопасности (OHS/OSH): | |||
Основные опасности | Легковоспламеняющийся, вызывает раздражение кожи | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −15,6 °C (3,9 °F; 257,5 К) | ||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD Lo ( самый низкий опубликованный ) | 3000 мг/кг (перорально, крыса) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Тетрагидропиран ( THP ) — это органическое соединение, состоящее из насыщенного шестичленного кольца, содержащего пять атомов углерода и один атом кислорода. Он назван в честь пирана , который содержит две двойные связи и может быть получен из него путем добавления четырех атомов водорода. В 2013 году его предпочтительное название по ИЮПАК было установлено как оксан . [1] Соединение представляет собой бесцветную летучую жидкость. Однако производные тетрагидропирана более распространены. 2-Тетрагидропиранильные (THP-) эфиры, полученные в результате реакции спиртов и 3,4-дигидропирана, обычно используются в качестве защитных групп в органическом синтезе . [2] Кроме того, тетрагидропирановая кольцевая система , т. е. пять атомов углерода и кислород, является ядром пиранозных сахаров, таких как глюкоза .
Структура и подготовка
В газовой фазе THP существует в своей самой низкой энергетической конформации кресла симметрии C s . [3]
Одной из классических процедур органического синтеза тетрагидропирана является гидрирование 3,4- изомера дигидропирана с никелем Ренея . [4 ]
Тетрагидропиранилпроизводные
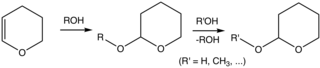
Хотя тетрагидропиран является малоизвестным соединением, тетрагидропираниловые эфиры обычно используются в органическом синтезе . В частности, группа 2-тетрагидропиранила (THP) является распространенной защитной группой для спиртов . [5] [6] Спирты реагируют с 3,4-дигидропираном, давая 2-тетрагидропираниловые эфиры. Эти эфиры устойчивы к различным реакциям. Спирт впоследствии может быть восстановлен путем кислотно-катализируемого гидролиза . Этот гидролиз преобразует исходный спирт, а также 5-гидроксипентаналь. Эфиры THP, полученные из хиральных спиртов, образуют диастереомеры. Другая нежелательная особенность заключается в том, что эфиры демонстрируют сложные спектры ЯМР, которые мешают анализу. [2]
В типичной процедуре спирт обрабатывают 3,4-дигидропираном и п -толуолсульфоновой кислотой в дихлорметане при температуре окружающей среды. [2]

Альтернативно, эфир THP может быть получен в условиях, близких к условиям реакции Мицунобу . Таким образом, спирт обрабатывают 2-гидрокситетрагидропиранилом, трифенилфосфином и диэтилазодикарбоксилатом (DEAD) в тетрагидрофуране (THF).
Обычно защиту эфиров ТГФ снимают с помощью уксусной кислоты в растворе ТГФ/вода, п -толуолсульфоновой кислоты в воде или п- толуолсульфоната пиридиния (PPTS) в этаноле .
Оксаны
Оксаны — это класс гексациклических эфирных колец с тетрагидропираном в качестве корневого химического вещества. Оксаны имеют один или несколько атомов углерода, замененных атомом кислорода. [8] Предпочтительным названием ИЮПАК для тетрагидропирана в настоящее время является оксан . [9]
Оксан — это также торговая марка цис -2-метил-4-пропил-1,3-оксатиана, коммерческого ароматизатора. [10]
Смотрите также
- Пиран
- Диоксан и триоксан , которые имеют два и три атома кислорода в составе своих шестичленных колец соответственно
Ссылки
- ^ «Новая органическая номенклатура ИЮПАК — БЮЛЛЕТЕНЬ химической информации» (PDF) .
- ^ abc Wuts, Peter GM; Greene, Theodora W. (2006). «Защита гидроксильной группы, включая 1,2- и 1,3-диолы». Greene's Protective Groups in Organic Synthesis (4-е изд.). стр. 16–366 . doi :10.1002/9780470053485.ch2. ISBN 9780470053485.
- ^ Builth-Williams, JD; Bellm, SM; Chiari, L.; Thorn, PA; Jones, DB; Chaluvadi, H.; Madison, DH; Ning, CG; Lohmann, B. (2013). "Динамическое (e,2e) исследование структурно связанных циклических эфиров тетрагидрофурана, тетрагидропирана и 1,4-диоксана" (PDF) . Journal of Chemical Physics . 139 (3): 034306. Bibcode :2013JChPh.139c4306B. doi :10.1063/1.4813237. hdl : 2328/26887 . PMID 23883026. S2CID 205181690.
- ^ Андрус, Д. В.; Джонсон, Джон Р. (1943). «Тетрагидропиран». Органические синтезы . 23 : 90. doi :10.15227/orgsyn.023.0090; Собрание томов , т. 3, стр. 794.
- ^ Эрл, РА; Таунсенд, ЛБ (1981). "Метил 4-гидрокси-2-бутиноат". Органические синтезы . 60 : 81. doi :10.15227/orgsyn.060.0081; Собрание томов , т. 7, стр. 334.
- ^ Клюге, Артур Ф. (1986). "Диэтил [(2-Тетрагидропиранилокси)метил]фосфонат". Органические синтезы . 64 : 80. doi :10.15227/orgsyn.064.0080; Собрание томов , т. 7, стр. 160.
- ^ Робинсон, Анна; Аггарвал, Вариндер К. (2010). «Асимметричный полный синтез соланделактона E: стереоконтролируемый синтез ядра 2-ен-1,4-диола через последовательность литиирования–борилирования–аллилирования». Angewandte Chemie International Edition . 49 (37): 6673– 6675. doi :10.1002/anie.201003236. PMID 20683835.
- ^ Ференц Нотеис, Михай Барток, «Гидрогенолиз связей C–O, C–N и C–X», с. 416 в, Р.А. Шелдон, Герман ван Беккум (редакторы), Fine Chemicals Through Heterogeneous Catalesis , John Wiley & Sons, 2008 ISBN 3527612971 .
- ^ «Новая органическая номенклатура ИЮПАК — БЮЛЛЕТЕНЬ химической информации» (PDF) .
- ^ Пантен, Йоханнес; Сурбург, Хорст (2016). «Ароматизаторы и отдушки, 3. Ароматические и гетероциклические соединения». Энциклопедия промышленной химии Ульмана . С. 1– 45. doi :10.1002/14356007.t11_t02. ISBN 978-3-527-30673-2.