Органопалладий химия
Химия органопалладия — это раздел металлоорганической химии , который занимается органическими соединениями палладия и их реакциями. Палладий часто используется в качестве катализатора при восстановлении алкенов и алкинов водородом . Этот процесс включает образование ковалентной связи палладий- углерод . Палладий также играет важную роль в реакциях углерод-углеродного сопряжения , как показано в тандемных реакциях . [1]
Хронология химии органопалладия
- 1873 г. — А.Н. Зайцев сообщает о восстановлении бензофенона над палладием водородом.
- 1894 - Фрэнсис Филлипс сообщает, что хлорид палладия(II) восстанавливается до металлического палладия при контакте с этиленом . [2]
- 1907 г. — Внедренная Владимиром Ипатьевым автоклавная технология позволяет проводить гидрирование под высоким давлением.
- 1956 г. — В процессе Ваккера этилен и кислород реагируют с образованием ацетальдегида в присутствии катализатора PdCl2 / CuCl2 .
- 1957 г. — Малатеста и Анголетта сообщают о тетракис(трифенилфосфин)палладии(0).
- 1972 - Реакция Хека представляет собой реакцию сочетания галогенида с олефином. В ней участвуют промежуточные соединения Pd(0).
- 1973 - Асимметричное аллильное алкилирование Троста представляет собой нуклеофильное замещение .
- 1975 — Реакция сочетания Соногаширы представляет собой реакцию сочетания терминальных алкинов с арил- или винилгалогенидами.
- 1994 г. — Аминирование Бухвальда-Хартвига, катализируемое Pd, для реакций образования связи CN.
sample.jpg/440px-PdCl2(cod)sample.jpg)
Палладий(II)
Комплексы алкенов
В отличие от Ni(II), но подобно Pt(II), галогениды Pd(II) образуют множество алкеновых комплексов. Главным примером является дихлор(1,5-циклооктадиен)палладий . В этом комплексе диен легко замещается, что делает его предпочтительным предшественником катализаторов. В промышленно важном процессе Ваккера этилен превращается в ацетальдегид посредством нуклеофильной атаки гидроксида на промежуточный продукт Pd(II)-этилен с последующим образованием комплекса винилового спирта. Лиганды фуллерена также связываются с палладием(II).

Ацетат палладия(II) и родственные соединения являются распространенными реагентами, поскольку карбоксилаты являются хорошими уходящими группами с основными свойствами. Например, было показано, что трифторацетат палладия эффективен в ароматическом декарбоксилировании : [3]
Аллиловые комплексы
Знаковым комплексом в этой серии является димер хлорида аллилпалладия (APC). Аллильные соединения с подходящими уходящими группами реагируют с солями палладия(II) с образованием пи-аллильных комплексов с тактильностью 3. Эти промежуточные соединения также реагируют с нуклеофилами, например, с карбанионами, полученными из эфиров малоновой кислоты [4] или с аминами в аллильном аминировании [5], как показано ниже [6]
Промежуточные соединения аллилпалладия также участвуют в асимметричном аллильном алкилировании Троста и перегруппировке Кэрролла , а также в оксо-вариации окисления Саэгусы .
Палладий-углеродные сигма-связанные комплексы
Различные органические группы могут связываться с палладием и образовывать стабильные сигма-связанные комплексы. Устойчивость связей с точки зрения энергии диссоциации связи следует тенденции: Pd-Алкинил > Pd-Винил ≈ Pd-Арил > Pd-Алкил, а длина связи металл-углерод изменяется в противоположном направлении: Pd-Алкинил < Pd-Винил ≈ Pd-Арил < Pd-Алкил. [7]
Соединения палладия(0)
Соединения Pd(0) с нулевой валентностью включают трис(дибензилиденацетон)дипалладий(0) и тетракис(трифенилфосфин)палладий(0) . Эти комплексы реагируют с галогенуглеродом RX в окислительном присоединении к промежуточным соединениям R-Pd-X с ковалентными связями Pd-C. Эта химия составляет основу большого класса органических реакций, называемых реакциями сочетания (см. реакции сочетания, катализируемые палладием ). Примером является реакция Соногаширы :
Органопалладий(IV)
Первое органопалладий(IV) соединение было описано в 1986 году. Этот комплекс представляет собой Me 3 Pd(IV)(I)bpy (bpy = бидентатный 2,2'-бипиридиновый лиганд) [8]. Он был синтезирован путем окислительного присоединения метилйодида к Me 2 Pd(II)bpy.
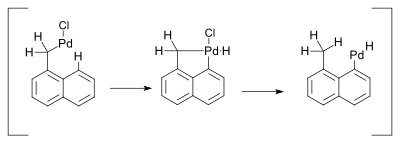
Соединения палладия обязаны своей реакционной способностью легкости взаимопревращения между промежуточными соединениями Pd(0) и палладия(II). Однако нет убедительных доказательств участия превращений Pd(II) в Pd(IV) в металлоорганических реакциях, опосредованных палладием. [9] Одна реакция, включающая такой механизм, была описана в 2000 году и касалась реакции Хека . Эта реакция сопровождалась 1,5-водородным сдвигом в присутствии аминов: [10]
Предполагалось, что гидридный сдвиг будет происходить через металлоцикл Pd(IV) :
В смежной работе промежуточным соединением, связанным с гидридным сдвигом, остается Pd(II): [11]
и в другой работе (новый синтез индолов с двумя миграциями Pd) равновесия постулируются между различными палладациклами: [12] [13]
и в некоторых внутримолекулярных связях синтетическая ценность была продемонстрирована независимо от степени окисления: [14]
Смотрите также
Ссылки
- ^ Справочник по палладийорганической химии для органического синтеза Эй-Негиши Джон Уайли (2002) ISBN 0-471-31506-0
- ^ Филлипс, Фрэнсис К. (март–июнь 1894 г.). «ИССЛЕДОВАНИЯ ЯВЛЕНИЙ ОКИСЛЕНИЯ И ХИМИЧЕСКИХ СВОЙСТВ ГАЗОВ». American Chemical Journal . 16 ( 3– 6): 163– 187, 255– 277, 340– 365, 406– 429 – через Google Books.
Реакция между этиленом и хлоридом палладия в растворе является реакцией второго класса и полной, газ быстро поглощается. Палладий осаждается в виде черного порошка, но никаких следов окисления до углекислого газа не происходит. Реакция почти такая же на холоде и при 100°. Газ, выделяющийся из раствора хлорида палладия (после полного восстановления до металлического палладия), не дает осадка в известковой воде. Реакция между хлоридом палладия и этиленом приводит к образованию альдегида.
- ^ Джошуа С. Дикштейн; Кэрол А. Малруни; Эрин М. О'Брайен; Барбара Дж. Морган и Мариса К. Козловски (2007). «Развитие каталитической реакции ароматического декарбоксилирования». Org. Lett. 9 (13): 2441– 2444. doi :10.1021/ol070749f. PMID 17542594.
- ^ Ян-Э. Бэквалл и Ян О. Вогберг (1993). "Стереоселективные 1,4-функционализации сопряженных диенов: цис- и транс-1-ацетокси-4-(дикарбометоксиметил)-2-циклогексен". Органические синтезы; Собрание томов , т. 8, стр. 5.
- ^ Игорь Дубовик; Иэн Д. Г. Уотсон и Андрей К. Юдин (2007). «Преследование виновника протона из катализируемого палладием аллилового аминирования». J. Am. Chem. Soc. 129 (46): 14172– 14173. doi :10.1021/ja076659n. PMID 17960935.
- ^ Реагенты: триэтилфосфитный лиганд, DBU (как сообщается, поглощает протоны амина, которые в противном случае вызвали бы изомеризацию) в ТГФ
- ^ В. П. Анаников и др., Металлоорганика, 2005, 24, 715 doi :10.1021/om0490841.
- ^ Питер К. Байерс; Аллан Дж. Кэнти; Брайан В. Скелтон; Аллан Х. Уайт (1986). «Окислительное присоединение йодметана к [PdMe2(bpy)] и рентгеновская структура продукта органопалладия(IV) fac-[PdMe3(bpy)l](bpy = 2,2-бипиридил)». Chem. Commun. (23): 1722– 1724. doi :10.1039/C39860001722.
- ^ Антонио Дж. Мота и Ален Дедье (2007). «Внутримолекулярная перегруппировка палладия в пространстве в замещенных арильных комплексах: теоретическое исследование процесса миграции арила в алкилпалладий». J. Org. Chem. 72 (25): 9669– 9678. doi :10.1021/jo701701s. PMID 18001098.
- ^ Ляньшэн Ван; И Пан; Синь Цзян; Хунвэнь Ху (2000). «Реакция α-хлорметилнафталина с олефинами, катализируемая палладием». Tetrahedron Letters . 41 (5): 725– 727. doi :10.1016/S0040-4039(99)02154-1.
- ^ Активация CH и миграция палладия в биарилах в условиях реакции Хека Гюнтер Кариг, Мария-Тереза Мун, Ноппорн Тасана и Тимоти Галлахер Org. Lett., том 4, № 18, 2002 3116 doi :10.1021/ol026426v
- ^ Синтез замещенных карбазолов с помощью миграции винильного палладия в арил с участием процессов активации домино CH Цзянь Чжао и Ричард К. Ларок Org. Lett. , том 7, № 4, 701 2005 doi :10.1021/ol0474655
- ^ Реагенты: дифенилацетилен , ацетат палладия , бис(дифенилфосфино)метан (dppm) и цезиевая соль пивалевой кислоты (CsPiv)
- ^ Миграция и циклизация алкила в арил, катализируемая Pd: эффективный синтез конденсированных полициклов с помощью множественной активации CH Циньхуа Хуан, Алессия Фацио, Гуансю Дай, Марино А. Кампо и Ричард К. Ларок J. Am. Chem. Soc. 2004 , 126, 7460-7461 doi :10.1021/ja047980y