Органическая радикальная батарея
Органическая радикальная батарея (ORB) — это тип батареи, впервые разработанный в 2005 году. [1] По состоянию на 2011 год этот тип батареи, как правило, не был доступен для потребителя, хотя их разработка в то время считалась приближающейся к практическому использованию. [2] ORB потенциально более экологичны, чем обычные батареи на основе металла , поскольку они используют органические радикальные полимеры (гибкие пластики) для обеспечения электропитания вместо металлов. ORB считаются мощной альтернативой литий-ионной батарее . Функциональные прототипы батареи были исследованы и разработаны различными исследовательскими группами и корпорациями, включая японскую корпорацию NEC . [1]
Органические радикальные полимеры, используемые в ORB, являются примерами стабильных радикалов , которые стабилизируются стерическими и/или резонансными эффектами. [2] Например, радикал нитроксила в (2,2,6,6-тетраметилпиперидин-1-ил)оксиле (TEMPO), наиболее распространенной субъединице, используемой в ORB, является стабильным молекулярным радикалом с центром на кислороде. Здесь радикал стабилизируется путем делокализации электронов с азота на кислород. Радикалы TEMPO могут быть присоединены к полимерным остовам с образованием поли(2,2,6,6-тетраметилпипериденилоксила-4-илметакрилата) (PTMA). ORB на основе PTMA имеют плотность заряда немного выше, чем у обычных литий-ионных аккумуляторов , что теоретически должно позволить ORB обеспечить больший заряд, чем литий-ионный аккумулятор аналогичного размера и веса. [2]
По состоянию на 2007 год исследования ORB были направлены в основном на гибридные ORB/Li-ion батареи, поскольку органические радикальные полимеры с подходящими электрическими свойствами для анода трудно синтезировать. [3]
Приложения
По состоянию на 2015 год ORB все еще находились в стадии разработки и не использовались в коммерческих целях. [ требуется ссылка ] Теоретически ORB могли бы заменить литий-ионные аккумуляторы как более экологически чистые батареи с аналогичной или более высокой емкостью заряда и аналогичным или более коротким временем зарядки. [2] Это сделало бы ORB хорошо подходящими для портативных электронных устройств.
Органические радикальные батареи были впервые исследованы и разработаны NEC в 2005 году с намерением широко использоваться для питания крошечных гаджетов в ближайшем будущем. [1] Они начинались с размера 0,3 мм и чрезвычайно быстрого времени зарядки. С самого начала разработки смарт-карты и RFID- метки были основными целями для использования ORB. [4] NEC также работала над более крупной батареей 0,7 мм, которая толще, но также имеет высокую зарядную емкость 5 мАч. [5]
Учитывая быструю окислительно-восстановительную химию радикалов нитроксила, [2] ORB оказались полезными для поддержания работы компьютера в течение короткого времени после отключения питания. Хотя количество дополнительного времени, предоставляемого в качестве резервного, невелико, его вполне достаточно, чтобы компьютер мог сделать резервную копию любых важных данных перед полным отключением. [1]
Функция
Радикальные полимерные батареи полагаются на окислительно-восстановительную реакцию органического радикала для генерации электрохимического потенциала . Наиболее изученным примером такой органической радикальной окислительно-восстановительной реакции является реакция нитроксидных радикалов, например, обнаруженная в молекуле, называемой (2,2,6,6-тетраметилпиперидин-1-ил)оксил , также известной как TEMPO. Нитроксидный радикал может быть окислен до катиона оксаммония или восстановлен до аниона гидроксиламина.


Положительный электрод использует окислительно-восстановительную пару катионов нитроксида и оксаммония для создания электрохимического потенциала , т. е. когда батарея разряжается, радикал нитроксида окисляется до катиона оксаммония, а когда батарея заряжается, катион оксаммония восстанавливается обратно до нитроксида. Окислительно-восстановительные потенциалы для нитроксида показывают некоторые вариации, и для нитроксида TEMPO для этой окислительно-восстановительной пары потенциал окисления составляет +0,87 В. Положительный электрод часто принимает форму геля, изготовленного из органических радикальных твердых веществ и графита , пропитанного электролитами. [1] Графит смешивают с полимером для увеличения проводимости. [6]
Отрицательный электрод использует окислительно-восстановительную пару нитроксид-гидроксиламин-анион для создания электрохимического потенциала, т. е. когда батарея разряжается, радикал нитроксида восстанавливается до гидроксиламин-аниона, а когда батарея заряжается, анион гидроксиламина окисляется обратно до нитроксида. Эта полуреакция имеет окислительный потенциал -0,11 В. Поскольку эта полуреакция не является легко обратимой, как полуреакция на положительном электроде, несколько исследовательских групп отказались от использования чистых органических радикальных батарей и вместо этого используют гибридные батареи металл/ORB, которые обычно состоят из радикального полимерного катода и того же анода, который используется в перезаряжаемых литий-ионных батареях . [2] [3] [7]
Подобно традиционной батарее, такой как литий-ионная батарея , органическая радикальная батарея состоит из катода и анода, которые разделены пористой пленкой и погружены в электролит. В чистой органической радикальной батарее обе клеммы сделаны из органических радикальных полимеров (полимер p-типа и n-типа), в то время как гибридная батарея металл/ORB обычно имеет катод из радикального полимера и анод из литий-иона/графита. [8]
Синтез радикальных полимеров
Несколько синтетических подходов были использованы в синтезе полирадикальных видов для использования в органических радикальных батареях. Следующие методы были использованы для синтеза поли(2,2,6,6-тетраметилпиперидинилокси-4-илметакрилата) (ПТМА) и других нитроксидных полимеров.
Свободнорадикальная полимеризация
Первоначальные попытки синтезировать ПТМА включали синтез полимера без радикальной функциональности посредством свободнорадикальной полимеризации . После синтеза полимера функция нитроксила может быть введена путем окисления. [3]
Несколько групп описали синтез PTMA (4) с использованием свободнорадикальной полимеризации 2,2,6,6-тетраметилпиперидинметакрилата ( 2) с 2,2'-азобисиобутрионитрилом ( AIBN ) в качестве радикального инициатора. Мономер был получен через 2,2,6,6-тетраметил-4-пиперидинол (1) и метакрилоилхлорид . Предшественник нейтрального полимера (3) был окислен до стабильного радикального полимера (4) 3-хлорпероксибензойной кислотой (mCPBA). [9] [10] Аналогичные синтетические подходы были предложены с использованием 4-метакрилоилокси-N-гидрокси-2,2,6,6-тетраметилпиперидина в качестве мономера, а не 2,2,6,6-тетраметилпиперидинметакрилата. [11]

Свободнорадикальная полимеризация как синтетический подход имеет несколько недостатков. Наиболее существенным ограничением является тот факт, что окисление полимера-предшественника никогда не достигает 100%. В результате синтезированный ПТМА имеет от 65% до 81% теоретически возможного количества нитроксидных групп. Уменьшение количества нитроксидных групп отрицательно влияет на зарядную емкость полимера и ограничивает его эффективность в органических радикальных батареях. [3] Мало того, что присутствует меньше нитроксидных групп, но и побочные реакции между неокисленными группами и катионами оксаммония снижают окислительно-восстановительную обратимость соединения.
Трудности свободнорадикальной полимеризации ПТМА можно было бы избежать, если бы этап окисления не был необходим. Однако, поскольку нитроксильные радикалы будут реагировать с любыми углеродными радикалами, образующимися во время полимеризации, использование мономера с нитроксильным радикалом нецелесообразно. [3]
RAFT-опосредованная полимеризация
Одним из последних методов синтеза ПТМА является тип свободнорадикальной полимеризации, известный как полимеризация, опосредованная обратимой передачей цепи присоединения-фрагментации (RAFT). [12]

RAFT-опосредованная полимеризация PTMA использует тот же исходный мономер, что и свободно-радикальная полимеризация. Использование RAFT-опосредованного подхода для полимеризации 2,2,6,6-тетраметил-4-пиперидинилметакрилата (TMPM), исходного мономера, генерирует поли(2,2,6,6-тетраметил-4-пиперидинилметакрилат) или PTMPM-RAFT. Прямое окисление PTMPM-RAFT до PTMA нецелесообразно, так как прямое окисление вызывает побочные реакции с участием концевой группы тиокаронилтиола PTMPM-RAFT, чтобы реагировать с образованием нерастворимого гелеобразного продукта. Вместо этого избыток AIBN используется для удаления реакционноспособного конца с образованием PTMPM, который затем может быть окислен мета-хлорпербензойной кислотой до желаемого PTMA. [12]
Несмотря на обещания полимеризации с помощью RAFT, сообщаемая концентрация радикалов составила всего 69 ± 4% [12] .
Полимеризация, катализируемая родием
Катализируемая родием полимеризация мономеров, содержащих ТЕМПО , позволяет избежать некоторых проблем, связанных со свободнорадикальной полимеризацией, поскольку не требуется стадия окисления для генерации радикала.
Структура (2,2,6,6-тетраметилпиперидин-1-ил)оксила или ТЕМПО показана ниже.

Следующие мономеры (1-3) могут быть синтезированы путем реакции конденсации между карбоксильными группами с амино- или гидроксильной группой производных ацетилена и различных производных ТЕМПО. Полимеризация мономеров завершается с использованием родиевого катализатора (nbd)Rh + [n 6 -C 6 H 5 B − (C 6 H 5 ) 3 ]. [8] Родиевый катализируемый синтез полимеров, содержащих ТЕМПО, был выполнен с высоким количественным выходом.

Хотя использование родиевого катализатора может быть выгодным из-за его высокого выхода, использование металлического катализатора создает дополнительную проблему, связанную с необходимостью отделения катализатора от конечного продукта. [12]
Анионная полимеризация
Прямая анионная полимеризация нитроксилсодержащих мономеров также использовалась для синтеза ПТМА. Анионная полимеризация не идеальна, поскольку она должна проводиться с использованием очень строгих процедур, чтобы избежать побочных реакций. Использование 1,1-дифенилгексиллития в качестве инициатора реакции устраняет некоторые побочные реакции за счет стерических эффектов, [13] однако необходимые процедуры не поддаются крупномасштабному синтезу. [3]
Полимеризация с переносом группы
Полимеризация с переносом группы, как и полимеризация ПТМА, катализируемая родием, позволяет полимеризовать мономеры нитроксильных радикалов. В отличие от мономеров, катализируемых родием, полимеризация с переносом группы использует кремний для катализа полимеризации.
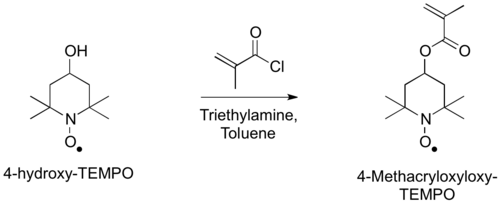
Получение мономера 4-метакрилоксилокси-ТЕМПО может быть осуществлено путем ацилирования 4-гидрокси-ТЕМПО метакрилоилхлоридом. [3]

Полимеризация с использованием 1-метокси-2-метил-1-триметилсилилокси-пропена (МТС) в качестве катализатора протекает быстро при комнатной температуре с образованием ПТМА. В качестве дополнительного катализатора используется фторид тетрабутиламмония (ТБАФ).
Ниже приводится обоснование полимеризации с переносом группы.

Преимущества
Органические радикальные батареи намного более экологичны, чем литий-ионные батареи , поскольку ORB не содержат металлов, которые создают проблему правильной утилизации. ORB нетоксичны и не воспламеняются, и не требуют дополнительной осторожности при обращении. [1] Сжигание полимеров нитроксидных радикалов дает углекислый газ, воду и оксид азота без золы или запаха. [6]
Будучи экологически чистыми, они обладают свойствами, которые в остальном сопоставимы с литий-ионными аккумуляторами : ORB имеют теоретическую емкость 147 мА·ч.г −1 , что немного выше, чем у литий-ионных аккумуляторов с 140 мА·ч.г −1 . [2] ORB также показывают сопоставимое время зарядки и хорошо сохраняют зарядно-разрядную емкость, соответствуя литий-ионным аккумуляторам при 75% от их первоначального заряда после 500 циклов. [14] Кроме того, концентрация радикалов в ORB достаточно стабильна в условиях окружающей среды, чтобы оставаться неизменной в течение года. [6] ORB также более гибки, чем литий-ионные аккумуляторы , что делает их более адаптируемыми к различным конструктивным ограничениям, таким как изогнутые устройства. [15]
Недостатки и трудности, возникающие в процессе развития
Основной трудностью в разработке ORB является сложность синтеза соответствующего отрицательного электрода. Этот недостаток возникает из-за того, что окислительно-восстановительная реакция отрицательного электрода не является полностью обратимой. Гибридные ORB/Li-ion батареи, в которых отрицательный электрод заменен на тот, что находится в литий-ионной батарее , были предложены в качестве компромисса для преодоления этой трудности. [2] [3]
Реакции полимеризации стабильного мономера, содержащего радикалы, также оказались областью трудностей в разработке. Стабильные органические радикалы, которые имеют решающее значение для функционирования батареи, иногда расходуются в побочных реакциях различных реакций полимеризации. Однако исследовательская группа успешно синтезировала сшитый органический радикальный полимер, потеряв при этом всего 0,4% органических радикалов в синтезе полимера. [3]
Смотрите также
Ссылки
- ^ abcdef "Что такое органическая радикальная батарея?". Conjecture Corporation . Получено 8 ноября 2012 г.
- ^ abcdefgh Накахара, К.; Ояидзу, К.; Нишиде, Х. Chemistry Letters 2011, 40 (3), 222–227. doi:10.1246/cl.2011.222
- ^ abcdefghi Буньон, Л.; Мортон, CJH; Новак П.; Веттер, Дж.; Несвадба, П. Хим. Матер. 2007, 19 (11), 2910–2914. дои: 10.1021/cm063052h
- ^ Фоли, Дайан. «NEC разрабатывает новую ультратонкую, гибкую, перезаряжаемую батарею, способную заряжаться сверхбыстро». NEC Corporation . Получено 5 ноября 2012 г.
- ^ Джаспер, Джозеф. "NEC разрабатывает органическую радикальную батарею для практического использования". NEC Corporation . Получено 6 ноября 2012 г.
- ^ abc Нишиде, Х.; Суга, Т. Интерфейс электрохимического общества 2005, № Зима, 32–36
- ^ Нишиде, Х.; Иваса, С.; Пу, Ю.-Ж.; Шуга, Т.; Накахара, К.; Сато, М. Electrochimica Acta 2004, 50 (2–3), 827–831. doi: 10.1016/j.electacta.2004.02.052
- ^ аб Кацумата, Т.; Сато, М.; Вада, Дж.; Сиоцуки, М.; Санда, Ф.; Масуда, Т. Макромол. Быстрая коммуникация. 2006, 27 (15), 1206–1211. дои: 10.1002/marc.200600286
- ^ Куросаки, Т.; Ли, К. В.; Окавара, М. Дж. Polym. Sci. A-1 Polym. Chem. 1972, 10 (11), 3295–3310. doi: 10.1002/pol.1972.170101116
- ^ Накахара, К.; Иваса, С.; Сато, М.; Мориока, Ю.; Ирияма, Дж.; Сугуро, М.; Хасэгава, Э. Письма по химической физике, 2002, 359 (5–6), 351–354. doi: 10.1016/S0009-2614(02)00705-4
- ^ Куросаки, Т.; Такахаши, О.; Окавара, М. Дж. Полим. Наука. Полим. Химия. Ред. 1974, 12 (7), 1407–1420. doi: 10.1002/pol.1974.170120705
- ^ abcd Ростро, Л.; Барадвадж, АГ; Будурис, BW ACS Appl. Матер. Интерфейсы 2013, 5 (20), 9896–9901. дои: 10.1021/am403223s
- ^ Аллгайер, Дж.; Финкельманн, Х. Макромол. хим., Rapid Commun. 1993, 14 (5), 267–271. дои: 10.1002/marc.1993.030140502
- ^ Фоли, Дайан. «NEC разрабатывает новую ультратонкую, гибкую, перезаряжаемую батарею, способную заряжаться сверхбыстро». NEC Corporation . Получено 30 октября 2012 г.
- ^ Стоддарт, Элисон. «Гибкое питание от батареи». RSC Publishing . Получено 30 октября 2012 г.