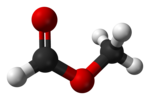
Метилформиат
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Метилформиат | |||
| Систематическое название ИЮПАК Метилметаноат | |||
| Другие имена Р-611 | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| ЧЭБИ | |||
| ChEMBL | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.003.166 | ||
| Номер ЕС |
| ||
CID PubChem |
| ||
| УНИИ | |||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С2Н4О2 | |||
| Молярная масса | 60,052 г·моль −1 | ||
| Появление | Бесцветная жидкость. | ||
| Запах | приятный [1] | ||
| Плотность | 0,98 г/см 3 | ||
| Температура плавления | −100 °C (−148 °F; 173 К) | ||
| Точка кипения | 32 °C (90 °F; 305 К) | ||
| 30% (20°С) [1] | |||
| Давление пара | 634 гПа (476 мм рт. ст.) (20°C) [1] | ||
| -32,0·10 −6 см 3 /моль | |||
| Опасности | |||
| Маркировка СГС : [3] | |||
  | |||
| Опасность | |||
| Х224 , Х302 , Х319 , Х332 , Х335 | |||
| Р210 , Р233 , Р240 , Р241 , Р242 , Р243 , Р261 , Р264 , Р270 , Р271 , Р280 , Р301+Р312 , Р303+Р361+Р353 , Р304+Р312 , Р304+Р340 , Р305+Р351+Р338 , Р312 , Р330 , Р337+Р313 , Р370+Р378 , Р403+Р233 , Р403+Р235 , Р405 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −19 °C; −2 °F; 254 К [1] | ||
| Пределы взрывоопасности | 4,5%-23% [1] | ||
| Смертельная доза или концентрация (ЛД, ЛК): | |||
LD 50 ( средняя доза ) | 1622 мг/кг (перорально, кролик) [2] | ||
LC Lo ( самый низкий опубликованный ) | 50 000 ppm (морская свинка, 20 мин) [2] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (допустимый) | TWA 100 частей на миллион (250 мг/м 3 ) [1] | ||
РЕЛ (рекомендуется) | TWA 100 ppm (250 мг/м 3 ) ST 150 ppm (375 мг/м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 4500 частей на миллион [1] | ||
| Паспорт безопасности (SDS) | Оксфордский паспорт безопасности | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Метилформиат , также называемый метилметаноатом , является метиловым эфиром муравьиной кислоты . Простейший пример карбоксилатного эфира, это бесцветная жидкость с эфирным запахом, высоким давлением паров и низким поверхностным натяжением . Он является предшественником многих других соединений, представляющих коммерческий интерес. [4]
Производство
В лаборатории метилформиат можно получить реакцией конденсации метанола и муравьиной кислоты следующим образом:
- HCOOH + CH 3 OH → HCOOCH 3 + H 2 O
Однако промышленный метилформиат обычно получают путем сочетания метанола и оксида углерода ( карбонилирование ) в присутствии сильного основания, такого как метоксид натрия : [4]
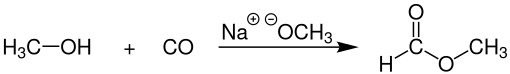
Этот процесс, коммерчески практикуемый BASF и другими компаниями, дает 96% селективности по отношению к метилформиату. Катализатор этого процесса чувствителен к воде, которая может присутствовать в исходном сырье оксида углерода , который обычно получают из синтез-газа . Поэтому очень сухой оксид углерода имеет важное значение. [5]
Использует
Метилформиат используется в основном для производства формамида , диметилформамида и муравьиной кислоты . Эти соединения являются предшественниками или строительными блоками для многих полезных производных.
Из-за высокого давления паров он используется для быстросохнущих покрытий и в качестве вспенивающего агента для некоторых видов полиуретановой пены (например, Ecomate ®, производимый Foam Supplies Inc.) [6] и в качестве замены для CFC , HCFC и HFC . Метилформиат имеет близкий к нулю потенциал истощения озонового слоя и нулевой потенциал глобального потепления , а также короткую жизнь в атмосфере — 3 дня. [7]
Он также используется как инсектицид . [ необходима ссылка ]
Историческое применение метилформиата, которое иногда привлекает к нему внимание, было в холодильной технике. До появления менее токсичных хладагентов метилформиат использовался в качестве альтернативы диоксиду серы в бытовых холодильниках, таких как некоторые модели знаменитого GE Monitor Top.
Ссылки
- ^ abcdefgh Карманный справочник NIOSH по химическим опасностям. "#0417". Национальный институт охраны труда и здоровья (NIOSH).
- ^ ab "Метилформиат". Концентрации, представляющие немедленную опасность для жизни или здоровья (IDLH) . Национальный институт охраны труда (NIOSH).
- ^ "Methyl formate". pubchem.ncbi.nlm.nih.gov . Архивировано из оригинала 19 декабря 2021 г. . Получено 19 декабря 2021 г. .
- ^ ab Вернер Ройтеманн и Хайнц Кечка «Муравьиная кислота» в Энциклопедии промышленной химии Ульмана , 2002, Wiley-VCH, Вайнхайм. дои : 10.1002/14356007.a12_013
- ^ В. Куто, Ж. Рамиулль, патент США US4216339.
- ^ "Ecomate". Ecomate . Foam Supplies, Inc. Архивировано из оригинала 2023-05-05 . Получено 2023-06-14 .
- ^ Wypych, George (2017). "2. Химическое происхождение пенообразователей". Справочник по пенообразователям и пенообразователям . Торонто: ChemTec Publishing. стр. 3–28 . doi :10.1016/B978-1-895198-99-7.50004-0. ISBN 9781895198997ЭКОЛОГИЧЕСКОЕ
ВОЗДЕЙСТВИЕ Жизнь в атмосфере, дней: 3 Соответствие Киотскому протоколу: да Соответствие Монреальскому протоколу: да Потенциал глобального потепления: <1,5 Потенциал разрушения озонового слоя: 0
Внешние ссылки
- NIST Chemistry WebBook: Метилформиат
- Запись на ChemicalLand21.com о МЕТИЛФОРМИАТЕ
- CDC - Карманный справочник NIOSH по химическим опасностям