Мезомерный эффект
В химии мезомерный эффект (или резонансный эффект ) является свойством заместителей или функциональных групп в химическом соединении . Он определяется как полярность , создаваемая в молекуле взаимодействием двух пи-связей или между пи-связью и неподеленной парой электронов , присутствующих на соседнем атоме. [1] Это изменение в расположении электронов приводит к образованию резонансных структур , которые гибридизируются в истинную структуру молекулы. Затем пи-электроны перемещаются от или к определенной замещающей группе. Мезомерный эффект сильнее в соединениях с более низким потенциалом ионизации . Это связано с тем, что состояния переноса электронов будут иметь более низкие энергии.
Представления мезомерного эффекта
Эффект используется качественно и описывает электроноакцепторные или электровысвобождающие свойства заместителей на основе соответствующих резонансных структур и обозначается буквой M. [2] Мезомерный эффект отрицателен ( –M ), когда заместитель является электроноакцепторной группой , и положителен ( +M ), когда заместитель является электронодонорной группой . Ниже приведены два примера эффекта +M и –M . Кроме того, ниже приведены функциональные группы, которые вносят вклад в каждый тип резонанса.
+М эффект
Эффект +M, также известный как положительный мезомерный эффект, возникает, когда заместитель является группой, отдающей электроны. Группа должна иметь одно из двух: неподеленную пару электронов или отрицательный заряд. При эффекте +M пи-электроны переносятся из группы в сопряженную систему, увеличивая плотность системы. Из-за увеличения электронной плотности сопряженная система будет развивать более отрицательный заряд. В результате система под эффектом +M будет более реакционноспособной по отношению к электрофилам , которые могут забрать отрицательный заряд, чем нуклеофил . [ необходима цитата ]

+M порядок эффекта: [1]
-М эффект
Эффект -M, также известный как отрицательный мезомерный эффект, возникает, когда заместитель является электроноакцепторной группой. Для того чтобы возник отрицательный мезомерный (-M) эффект, группа должна иметь положительный заряд или пустую орбиталь, чтобы притягивать к себе электроны. При эффекте -M π-электроны перемещаются от сопряженной системы к группе, притягивающей электроны. В сопряженной системе плотность электронов уменьшается, и общий заряд становится более положительным. При эффекте -M группы и соединения становятся менее реакционноспособными по отношению к электрофилам и более реакционноспособными по отношению к нуклеофилам, которые могут отдавать электроны и уравновешивать положительный заряд. [3]
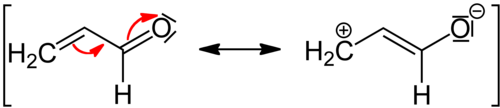
-M порядок эффекта:
Мезомерный эффект против индуктивного эффекта
Чистый поток электронов от или к заместителю определяется также индуктивным эффектом . [3] Мезомерный эффект как результат перекрытия p - орбиталей (резонанс) абсолютно не влияет на этот индуктивный эффект, поскольку индуктивный эффект имеет отношение исключительно к электроотрицательности атомов и их топологии в молекуле (какие атомы с какими связаны). В частности, индуктивный эффект - это тенденция заместителей отталкивать или притягивать электроны исключительно на основе электроотрицательности и не имеет отношения к перестройке. Мезомерный эффект, однако, имеет дело с перестройкой и возникает, когда электронная пара заместителей смещается. Индуктивный эффект действует только на альфа-углероды, в то время как мезомерный использует пи-связи между атомами. [4] Хотя эти два пути часто приводят к похожим молекулам и резонансным структурам, механизм различен. Таким образом, мезомерный эффект сильнее индуктивного эффекта. [5]
Понятия мезомерного эффекта, мезомерии и мезомера были введены Ингольдом в 1938 году как альтернатива синонимичной концепции резонанса Полинга . [6] «Мезомерия» в этом контексте часто встречается в немецкой и французской литературе, но в английской литературе доминирует термин «резонанс».
Мезомерия в сопряженных системах
Мезомерный эффект может передаваться по любому числу атомов углерода в сопряженной системе . Это объясняет резонансную стабилизацию молекулы из-за делокализации заряда. [7] Важно отметить, что энергия фактической структуры молекулы, т. е. резонансного гибрида, может быть ниже, чем у любой из канонических структур, вносящих вклад. Разница в энергии между фактической индуктивной структурой и (наиболее стабильной структурой, вносящей вклад) наихудшей кинетической структурой называется резонансной энергией или энергией резонансной стабилизации. [8] Для количественной оценки силы мезомерного/резонансного эффекта используются различные константы заместителей, т. е. резонансная константа Суэйна-Лаптона, резонансная константа Тафта или параметр pEDA Озиминского и Добровольского .
Кроме того, полученные резонансные структуры могут придать молекуле свойства, которые изначально не очевидны при взгляде на одну структуру. Некоторые из этих свойств включают различную реактивность, локальное диамагнитное экранирование в ароматических соединениях, деэкранирование, а также кислотную и щелочную силу. [9]
Ссылки
- ^ ab Murrell, JN (1955-11-01). "Электронный спектр ароматических молекул VI: Мезомерный эффект". Труды Физического общества. Раздел A. 68 ( 11): 969–975. Bibcode :1955PPSA...68..969M. doi :10.1088/0370-1298/68/11/303. ISSN 0370-1298.
- ^ Гровер, Нитика; Эманди, Ганапати; Твэмли, Брендан; Хурана, Бхавья; Сол, Винсент; Сенге, Матиас О. (08 ноября 2020 г.). «Синтез и структура мезозамещенных дибензигомопорфиринов». Европейский журнал органической химии . 2020 (41): 6489–6496. дои : 10.1002/ejoc.202001165. ISSN 1434-193Х. ПМК 7702178 . ПМИД 33328793.
- ^ ab Химия (ИЮПАК), Международный союз теоретической и прикладной химии. "ИЮПАК - мезомерный эффект (M03844)". goldbook.iupac.org . doi : 10.1351/goldbook.M03844 . Получено 25.10.2022 .
- ^ Кларк, Д.Т.; Мюррелл, Дж.Н.; Теддер, Дж.М. (1963). «234. Величины и знаки индуктивных и мезомерных эффектов галогенов». Журнал химического общества (возобновление) : 1250–1253. doi :10.1039/jr9630001250. ISSN 0368-1769.
- ^ Улицы, ГД; Сезар, Джеральд П. (октябрь 1973 г.). «Индуктивные и мезомерные эффекты на π-орбиталях галогенбензолов». Молекулярная физика . 26 (4): 1037–1052. Бибкод : 1973MolPh..26.1037S. дои : 10.1080/00268977300102271. ISSN 0026-8976.
- ^ Кербер, Роберт С. (2006-02-01). "Если это резонанс, что такое резонирование?". J. Chem. Educ. 83 (2): 223. Bibcode :2006JChEd..83..223K. doi :10.1021/ed083p223. Архивировано из оригинала 2006-10-04.
- ^ Балчи, Метин (2005-01-01), Балчи, Метин (ред.), "12 - Химический сдвиг", Базовая 1H- и 13C-ЯМР-спектроскопия , Амстердам: Elsevier Science, стр. 283–292, doi :10.1016/b978-044451811-8.50012-7, ISBN 978-0-444-51811-8, получено 2022-10-25
- ^ "Глава 2-2 - Теория химического сдвига". Elsevier Enhanced Reader. Международная серия по органической химии. Pergamon. Январь 1969. С. 61–113. doi :10.1016/B978-0-08-022953-9.50011-9. ISBN 9780080229539. Получено 2022-10-25 .
{{cite book}}:|website=проигнорировано ( помощь ) - ^ Питер, К.; Фоллхардт, К. (январь 1978 г.). "Обзор: "Место переходных металлов в органическом синтезе. Ред. Д. В. Слокум. Анналы Нью-Йоркской академии наук, том 295, Нью-Йорк, штат Нью-Йорк, 1977 г., XXIV + 282 стр. $3 2,00"". Синтез и реакционная способность в неорганической и металлоорганической химии . 8 (5–6): 505–506. doi :10.1080/00945717808057443. ISSN 0094-5714.