болезнь Грейвса
| болезнь Грейвса | |
|---|---|
| Другие имена | Токсический диффузный зоб, болезнь Флаяни–Базедова–Грейвса |
 | |
| Классическое проявление экзофтальма и ретракции века при болезни Грейвса | |
| Специальность | Эндокринология |
| Симптомы | Увеличение щитовидной железы , раздражительность , мышечная слабость , проблемы со сном , учащенное сердцебиение , потеря веса , плохая переносимость жары , [1] беспокойство , тремор рук или пальцев, теплая и влажная кожа, повышенное потоотделение , зоб , изменения менструального цикла, легкое образование синяков, эректильная дисфункция , снижение либидо, частые испражнения, выпячивание глаз ( офтальмопатия Грейвса ), толстая красная кожа на голенях или верхней части стопы ( претибиальная микседема ) [2] |
| Осложнения | Офтальмопатия Грейвса [1] |
| Причины | Неизвестно [3] |
| Факторы риска | Семейный анамнез, другие аутоиммунные заболевания [1] |
| Метод диагностики | Анализы крови, поглощение радиоактивного йода [1] [4] |
| Уход | Радиойодтерапия , антитиреоидные препараты и бета-блокаторы , хирургия щитовидной железы [1] |
| Частота | 0,5% (мужчины), 3% (женщины) [5] |
Болезнь Грейвса , также известная как токсический диффузный зоб или болезнь Базедова , является аутоиммунным заболеванием , которое поражает щитовидную железу . [1] Она часто приводит к гипертиреозу и является наиболее распространенной причиной этого заболевания . [5] Она также часто приводит к увеличению щитовидной железы . [1] Признаки и симптомы гипертиреоза могут включать раздражительность , мышечную слабость , проблемы со сном , учащенное сердцебиение , плохую переносимость жары , диарею и непреднамеренную потерю веса . [1] Другие симптомы могут включать утолщение кожи на голенях, известное как претибиальная микседема , и выпячивание глаз , состояние, вызванное офтальмопатией Грейвса . [1] Примерно у 25–30 % людей с этим заболеванием развиваются проблемы со зрением. [1] [4]
Точная причина заболевания неясна, но симптомы являются результатом связывания антител с рецепторами на щитовидной железе, вызывая повышенную экспрессию гормона щитовидной железы. [3] Люди с большей вероятностью будут поражены, если у них есть член семьи с этим заболеванием. [1] Если один монозиготный близнец поражен, существует 30% вероятность того, что другой близнец также будет иметь это заболевание. [6] Начало заболевания может быть вызвано физическим или эмоциональным стрессом, инфекцией или родами . [4] Люди с другими аутоиммунными заболеваниями, такими как диабет 1 типа и ревматоидный артрит , с большей вероятностью будут поражены. [1] Курение увеличивает риск заболевания и может ухудшить проблемы со зрением. [1] Расстройство возникает из-за антитела , называемого тиреотропным иммуноглобулином (TSI), который оказывает такое же действие, как тиреотропный гормон (TSH). [1] Эти антитела TSI заставляют щитовидную железу вырабатывать избыточное количество тиреоидных гормонов . [1] Диагноз можно заподозрить на основании симптомов и подтвердить с помощью анализов крови и поглощения радиоактивного йода . [1] [4] Обычно анализы крови показывают повышенный уровень Т3 и Т4 , низкий уровень ТТГ, повышенное поглощение радиоактивного йода во всех областях щитовидной железы и антитела к TSI. [4]
Три варианта лечения — это радиойодтерапия , медикаментозное лечение и хирургия щитовидной железы . [1] Радиойодтерапия подразумевает прием йода-131 внутрь, который затем концентрируется в щитовидной железе и разрушает ее в течение недель или месяцев. [1] Возникающий гипотиреоз лечится синтетическими гормонами щитовидной железы . [1] Лекарства, такие как бета-блокаторы , могут контролировать некоторые симптомы, а антитиреоидные препараты, такие как метимазол, могут временно помогать людям, пока другие методы лечения оказывают эффект. [1] Еще одним вариантом является операция по удалению щитовидной железы. [1] Проблемы с глазами могут потребовать дополнительного лечения. [1]
Болезнь Грейвса развивается примерно у 0,5% мужчин и 3,0% женщин. [5] Она встречается примерно в 7,5 раз чаще у женщин, чем у мужчин. [1] Часто она начинается в возрасте от 40 до 60 лет, но может начаться в любом возрасте. [6] Это самая распространенная причина гипертиреоза в Соединенных Штатах (примерно от 50 до 80% случаев). [1] [4] Состояние названо в честь ирландского хирурга Роберта Грейвса , который описал его в 1835 году. [6] Также существует ряд предыдущих описаний. [6]
Признаки и симптомы
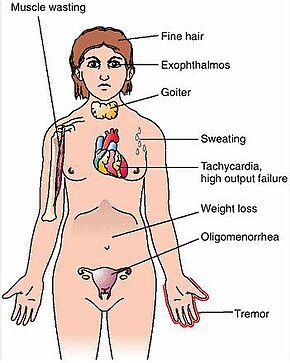
Признаки и симптомы болезни Грейвса практически все являются результатом прямых и косвенных эффектов гипертиреоза, за исключением офтальмопатии Грейвса , зоба и претибиальной микседемы (которые вызваны аутоиммунными процессами заболевания). Симптомы результирующего гипертиреоза в основном включают бессонницу , тремор рук , гиперактивность , выпадение волос, повышенное потоотделение , олигоменорею , зуд, непереносимость жары , потерю веса , несмотря на повышенный аппетит , диарею , частую дефекацию , сердцебиение , периодическую частичную мышечную слабость или паралич у лиц, особенно азиатского происхождения, [7] а также тепло и влажность кожи. [8] Другие признаки, которые можно увидеть при физическом осмотре, чаще всего включают диффузно увеличенную (обычно симметричную), безболезненную щитовидную железу, отставание века , чрезмерное слезотечение из-за офтальмопатии Грейвса, аритмии сердца, такие как синусовая тахикардия , мерцательная аритмия и преждевременные сокращения желудочков , а также гипертонию . [8] [9]
Причина
Точная причина неясна, но считается, что она связана с сочетанием генетических и экологических факторов. [3] Хотя теоретически существует механизм, посредством которого воздействие сильных стрессоров и высокий уровень последующего стресса, такого как посттравматическое стрессовое расстройство, может увеличить риск иммунного заболевания и вызвать обострение аутоиммунного ответа, приводящего к болезни Грейвса, для однозначного вывода необходимы более надежные клинические данные. [10]
Генетика
Наблюдается генетическая предрасположенность к болезни Грейвса, при этом некоторые люди более склонны к выработке антител , активирующих рецептор ТТГ , из-за генетической причины. Человеческий лейкоцитарный антиген DR (особенно DR3), по-видимому, играет роль. [11] На сегодняшний день не было обнаружено явного генетического дефекта, указывающего на причину, связанную с одним геном . [ необходима цитата ]
Гены, которые, как полагают, участвуют в этом процессе, включают гены тиреоглобулина , рецептора тиротропина , нерецепторного типа протеинтирозинфосфатазы 22 ( PTPN22 ) и цитотоксического Т-лимфоцит-ассоциированного антигена 4 и другие. [12]
Инфекционный триггер
Поскольку болезнь Грейвса является аутоиммунным заболеванием, которое возникает внезапно, часто в более позднем возрасте, вирусная или бактериальная инфекция может вызвать выработку антител, которые перекрестно реагируют с рецептором ТТГ человека, явление, известное как антигенная мимикрия . [13]
Бактерия Yersinia enterocolitica имеет структурное сходство с рецептором тиреотропина человека [11] и, как предполагалось, способствует развитию аутоиммунитета щитовидной железы, возникающего по другим причинам у генетически восприимчивых людей. [14] В 1990-х годах предполагалось, что Y. enterocolitica может быть связана с болезнью Грейвса. [15] В последнее время роль Y. enterocolitica оспаривается. [16]
Вирус Эпштейна-Барр является еще одним потенциальным триггером. [17]
Механизм
Тиреоидстимулирующие иммуноглобулины распознают и связываются с рецептором ТТГ, который стимулирует секрецию тироксина (Т4) и трийодтиронина (Т3). Рецепторы тироксина в гипофизе активируются избыточным гормоном, подавляя дополнительное высвобождение ТТГ в отрицательной обратной связи. Результатом является очень высокий уровень циркулирующих тиреоидных гормонов и низкий уровень ТТГ. [ необходима цитата ]
Патофизиология

Болезнь Грейвса — это аутоиммунное заболевание, при котором организм вырабатывает антитела , специфичные к собственному белку — рецептору тиреотропного гормона. ( Также могут вырабатываться антитела к тиреоглобулину и гормонам щитовидной железы Т3 и Т4.)
Эти антитела вызывают гипертиреоз, поскольку они связываются с TSHr и хронически стимулируют его. TSHr экспрессируется на фолликулярных клетках щитовидной железы (клетках, которые вырабатывают тиреоидные гормоны), и результатом хронической стимуляции является аномально высокая продукция T3 и T4. Это, в свою очередь, вызывает клинические симптомы гипертиреоза и увеличение щитовидной железы, видимое как зоб.
Часто встречающийся инфильтративный экзофтальм был объяснен постулатом, что щитовидная железа и экстраокулярные мышцы имеют общий антиген, который распознается антителами. Антитела, связывающиеся с экстраокулярными мышцами, могут вызвать отек за глазным яблоком.
«Апельсиновая корка» на коже объясняется проникновением антител под кожу, что вызывает воспалительную реакцию и последующее образование фиброзных бляшек.
Три типа аутоантител к рецептору ТТГ:
- Тиреоидстимулирующие иммуноглобулины: эти антитела (в основном IgG) действуют как длительно действующие стимуляторы щитовидной железы, активируя клетки посредством более медленного и продолжительного процесса по сравнению с ТТГ, что приводит к повышенной выработке гормонов щитовидной железы.
- Иммуноглобулины роста щитовидной железы: эти антитела связываются непосредственно с рецептором ТТГ и участвуют в росте фолликулов щитовидной железы.
- Иммуноглобулины, ингибирующие связывание тиреотропина: эти антитела ингибируют нормальное соединение ТТГ с его рецептором.
- Некоторые из них на самом деле действуют так, как будто сам ТТГ связывается со своим рецептором, тем самым стимулируя функцию щитовидной железы.
- Другие типы могут не стимулировать щитовидную железу, но препятствуют связыванию TSI и TSH с рецептором и его стимуляции.
Другим следствием гипертиреоза является потеря костной массы из-за остеопороза, вызванного повышенным выделением кальция и фосфора с мочой и калом. Последствия можно свести к минимуму, если гипертиреоз лечить на ранней стадии. Тиреотоксикоз также может увеличить уровень кальция в крови на целых 25%. Это может вызвать расстройство желудка, чрезмерное мочеиспускание и нарушение функции почек. [18]
Диагноз
Болезнь Грейвса может клинически проявляться одним или несколькими из следующих характерных признаков: [ необходима ссылка ]
- Учащенное сердцебиение (80%)
- Диффузный пальпируемый зоб с слышимым шумом (70%)
- Тремор (40%)
- Экзофтальм (выпячивание одного или обоих глаз), периорбитальный отек (25%)
- Усталость (70%), потеря веса (60%) с повышенным аппетитом у молодых людей и плохим аппетитом у пожилых людей, а также другие симптомы гипертиреоза/ тиреотоксикоза
- Непереносимость жары (55%)
- Трепетность (55%)
- Сердцебиение (50%)
Два признака являются истинно диагностическими для болезни Грейвса (т. е. не наблюдаются при других гипертиреозных состояниях): экзофтальм и неточечный отек ( претибиальная микседема ). Зоб представляет собой увеличенную щитовидную железу диффузного типа (т. е. распространенную по всей железе). Диффузный зоб может наблюдаться при других причинах гипертиреоза, хотя болезнь Грейвса является наиболее распространенной причиной диффузного зоба. Большой зоб будет виден невооруженным глазом, но маленький (незначительное увеличение железы) может быть обнаружен только при физическом осмотре. Иногда зоб не обнаруживается клинически, но может быть обнаружен только при компьютерной томографии или ультразвуковом исследовании щитовидной железы. [ необходима цитата ] Другим признаком болезни Грейвса является гипертиреоз, то есть избыточная выработка тиреоидных гормонов Т3 и Т4. Нормальные уровни щитовидной железы также наблюдаются, а иногда и гипотиреоз, который может способствовать возникновению зоба (хотя он не является причиной болезни Грейвса). Гипертиреоз при болезни Грейвса подтверждается, как и при любой другой причине гипертиреоза, путем измерения повышенных уровней свободного (несвязанного) T3 и T4 в крови. [ необходима цитата ]
Другие полезные лабораторные измерения при болезни Грейвса включают тиреотропный гормон (ТТГ, обычно неопределяемый при болезни Грейвса из-за отрицательной обратной связи от повышенных Т3 и Т4) и связанный с белком йод (повышенный). Серологически обнаруженные тиреотропные антитела, поглощение радиоактивного йода или УЗИ щитовидной железы с допплерографией могут независимо подтвердить диагноз болезни Грейвса.
Биопсия для гистологического исследования обычно не требуется, но может быть проведена в случае проведения тиреоидэктомии.
Зоб при болезни Грейвса часто не узловой, но узлы щитовидной железы также распространены. [19] Дифференциация распространенных форм гипертиреоза, таких как болезнь Грейвса, одиночная аденома щитовидной железы и токсический многоузловой зоб , важна для определения правильного лечения. [19] Дифференциация между этими сущностями продвинулась вперед , поскольку визуализация и биохимические тесты улучшились. Измерение антител к рецептору ТТГ с помощью анализа h-TBII доказало свою эффективность и стало наиболее практичным подходом, обнаруженным в одном исследовании. [20]
Болезнь глаз
Тиреоид-ассоциированная офтальмопатия (TAO), или тиреоидное заболевание глаз (TED), является наиболее распространенным экстратиреоидным проявлением болезни Грейвса. Это форма идиопатического лимфоцитарного воспаления орбиты , и хотя ее патогенез не полностью изучен, считается, что аутоиммунная активация фибробластов орбиты , которые в TAO экспрессируют рецептор ТТГ , играет центральную роль. [21]
Гипертрофия экстраокулярных мышц, адипогенез и отложение несульфатированных гликозаминогликанов и гиалуроната вызывают расширение орбитального жира и мышечных отсеков, что в пределах костной орбиты может привести к дистиреоидной оптической нейропатии , повышенному внутриглазному давлению , экзофтальму, венозному застою, приводящему к хемозу и периорбитальному отеку, а также прогрессирующему ремоделированию стенок орбиты. [22] [23] [24] Другие отличительные черты TAO включают в себя ретракцию века, рестриктивную миопатию, верхний лимбический кератоконъюнктивит и экспозиционную кератопатию . [ необходима ссылка ]
Тяжесть заболевания глаз можно классифицировать с помощью мнемонического фразы: «БЕЗ ОСОБЕННОСТЕЙ»: [25]
- Класс 0: Нет признаков или симптомов
- Класс 1: Только признаки (ограниченные ретракцией верхнего века и пристальным взглядом, с задержкой века или без нее)
- Класс 2: Поражение мягких тканей ( отек конъюнктивы и век, инъекция конъюнктивы и т. д. )
- Класс 3: проптоз
- Класс 4: поражение экстраокулярных мышц (обычно с диплопией )
- Класс 5: поражение роговицы (в основном из-за лагофтальма )
- Класс 6: Потеря зрения (из-за поражения зрительного нерва)
Обычно естественное течение TAO следует кривой Рандла, которая описывает быстрое ухудшение в начальной фазе до пика максимальной тяжести, а затем улучшение до статического плато без, однако, возвращения к нормальному состоянию. [26]
Управление
Лечение болезни Грейвса включает антитиреоидные препараты , которые снижают выработку гормона щитовидной железы, радиоактивный йод (радиоактивный йод I-131 ) и тиреоидэктомию (хирургическое удаление железы). Поскольку операция у пациента с гипертиреозом опасна, перед тиреоидэктомией проводится предоперационное лечение антитиреоидными препаратами, чтобы сделать пациента эутиреоидным. Каждый из этих методов лечения имеет свои преимущества и недостатки, и ни один из подходов к лечению не считается лучшим для всех. [ необходима цитата ]
Лечение антитиреоидными препаратами должно проводиться в течение шести месяцев или двух лет, чтобы быть эффективным. Даже тогда, после прекращения приема препаратов, гипертиреоидное состояние может рецидивировать. Риск рецидива составляет около 40–50%, а пожизненное лечение антитиреоидными препаратами имеет некоторые побочные эффекты, такие как агранулоцитоз и заболевание печени . [27] Побочные эффекты антитиреоидных препаратов включают потенциально фатальное снижение уровня лейкоцитов. Терапия радиоактивным йодом является наиболее распространенным методом лечения в Соединенных Штатах, в то время как антитиреоидные препараты и/или тиреоидэктомия чаще используются в Европе, Японии и большинстве стран остального мира.
β-блокаторы (например, пропранолол ) могут использоваться для подавления симптомов симпатической нервной системы , таких как тахикардия и тошнота, пока не начнут действовать антитиреоидные препараты. Чистые β-блокаторы не подавляют ретракцию век в глазах, которая опосредована альфа-адренергическими рецепторами.
Антитиреоидные препараты
Основными антитиреоидными препаратами являются карбимазол (в Великобритании), метимазол (в США) и пропилтиоурацил /PTU. Эти препараты блокируют связывание йода и соединение йодтирозинов. Наиболее опасным побочным эффектом является агранулоцитоз (1/250, больше в PTU). Другие включают гранулоцитопению (дозозависимую, которая улучшается после прекращения приема препарата) и апластическую анемию . Пациенты, принимающие эти препараты, должны обратиться к врачу, если у них появляется боль в горле или лихорадка. Наиболее распространенными побочными эффектами являются сыпь и периферический неврит . Эти препараты также проникают через плаценту и секретируются в грудное молоко. Йод Люголя может использоваться для блокирования синтеза гормонов перед операцией. [ необходима цитата ]
Рандомизированное контролируемое исследование, в котором изучалось лечение Грейвса однократной дозой, показало, что метимазол более эффективно достигал эутиреоидного состояния через 12 недель, чем пропилтиоурацил (77,1% в группе метимазола 15 мг против 19,4% в группах пропилтиоурацила 150 мг). [28]
Не было выявлено никакой разницы в результатах при добавлении тироксина к антитиреоидным препаратам и продолжении приема тироксина по сравнению с плацебо после отмены антитиреоидных препаратов. Однако были обнаружены два маркера, которые могут помочь предсказать риск рецидива. Этими двумя маркерами являются положительные антитела к ТТГ (TSHR-Ab) и курение. Положительный TSHR-Ab в конце лечения антитиреоидными препаратами увеличивает риск рецидива до 90% ( чувствительность 39%, специфичность 98%), а отрицательный TSHR-Ab в конце лечения антитиреоидными препаратами связан с 78% вероятностью сохранения ремиссии. Было показано, что курение оказывает влияние, независимое от положительного TSHR-Ab. [29]
Радиоактивный йод
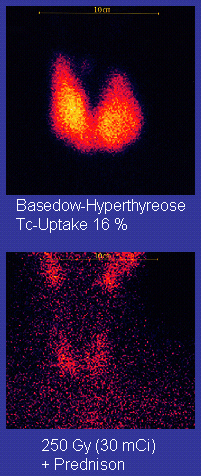
Радиоактивный йод (радиоактивный йод-131) был разработан в начале 1940-х годов в Центре общих клинических исследований Маллинкродта . Этот метод подходит большинству пациентов, хотя некоторые предпочитают использовать его в основном для пожилых пациентов. Показаниями к применению радиоактивного йода являются неэффективность медикаментозной терапии или хирургического вмешательства, а также противопоказания к медикаментозной или хирургической терапии. Гипотиреоз может быть осложнением этой терапии, но его можно лечить гормонами щитовидной железы, если он появляется. Обоснованием применения радиоактивного йода является то, что он накапливается в щитовидной железе и облучает железу своим бета- и гамма-излучением, причем около 90% общего излучения испускается бета- (электронными) частицами. Наиболее распространенным методом лечения йодом-131 является введение определенного количества в микрокюри на грамм щитовидной железы на основе пальпации или радиодиагностической визуализации железы в течение 24 часов. [30] Пациенты, получающие терапию, должны регулярно проходить контроль с помощью анализов крови на гормоны щитовидной железы, чтобы убедиться, что они получают лечение гормонами щитовидной железы до того, как у них разовьются симптомы гипотиреоза. [31]
Противопоказаниями к радиойодтерапии являются беременность (абсолютное), офтальмопатия (относительное; может усугубить заболевание глаз, вызванное щитовидной железой) или одиночные узелки . [32]
Недостатками этого лечения являются высокая частота гипотиреоза (до 80%), требующая в конечном итоге дополнительного приема гормонов щитовидной железы в виде ежедневных таблеток. Лечение радиоактивным йодом действует медленно (в течение месяцев или лет), разрушая щитовидную железу, а гипертиреоз, связанный с болезнью Грейвса, не излечивается у всех людей радиоактивным йодом, но имеет частоту рецидивов, которая зависит от дозы введенного радиоактивного йода. [32] В редких случаях с этим лечением связывали тиреоидит, вызванный радиацией . [33]
Операция
Этот метод подходит для молодых людей и беременных женщин. Показания к тиреоидэктомии можно разделить на абсолютные показания и относительные показания. Эти показания помогают решить, какие люди получат наибольшую пользу от операции. [27] Абсолютными показаниями являются большой зоб (особенно при сдавливании трахеи ), подозрительные узелки или подозрение на рак (для патологического исследования щитовидной железы), а также люди с офтальмопатией и, кроме того, если это предпочтительный метод лечения для человека или если он отказывается проходить лечение радиоактивным йодом. Беременность рекомендуется отложить на шесть месяцев после лечения радиоактивным йодом. [27]
Возможны как двусторонняя субтотальная тиреоидэктомия , так и операция Хартли-Данхилла (гемитиреоидэктомия с одной стороны и частичная лобэктомия с другой стороны).
Преимуществами являются немедленное излечение и потенциальное удаление карциномы . Его риски включают повреждение возвратного гортанного нерва , гипопаратиреоз (из-за удаления паращитовидных желез ), гематома (которая может быть опасной для жизни, если она сдавливает трахею), рецидив после медицинского лечения, инфекции (реже) и рубцевание . [27] Увеличение риска повреждения нерва может быть связано с повышенной васкуляризацией паренхимы щитовидной железы и развитием связей между капсулой щитовидной железы и окружающими тканями. Сообщается, что существует 1% случаев постоянного паралича возвратного гортанного нерва после полной тиреоидэктомии. [27] Рисков, связанных с анестезией, много, поэтому координация с анестезиологом и оптимизация пациента для операции до операции имеют важное значение. Удаление железы позволяет провести полную биопсию, чтобы получить определенные доказательства рака в любой части щитовидной железы. (Игольная биопсия не так точна в прогнозировании доброкачественного состояния щитовидной железы). Никакого дальнейшего лечения щитовидной железы не требуется, если только не обнаружен рак. После операции может быть проведено исследование поглощения радиоактивного йода, чтобы убедиться, что все оставшиеся (потенциально раковые) клетки щитовидной железы (т. е. рядом с нервами голосовых связок) уничтожены. Помимо этого, единственным оставшимся лечением будет левотироксин или таблетки для замещения щитовидной железы, которые пациент должен принимать всю оставшуюся жизнь.
В обзорной статье 2013 года сделан вывод о том, что хирургическое вмешательство, по-видимому, является наиболее успешным методом лечения болезни Грейвса, при этом предпочтительным хирургическим вариантом является полная тиреоидэктомия. [34]
Глаза
Легкие случаи лечатся смазывающими глазными каплями или нестероидными противовоспалительными каплями. Тяжелые случаи, угрожающие зрению (воздействие на роговицу или сдавление зрительного нерва), лечатся стероидами или орбитальной декомпрессией. Во всех случаях необходимо прекратить курение. Двоение в глазах можно исправить с помощью призматических очков и хирургического вмешательства (последнее только тогда, когда процесс стабилизировался в течение некоторого времени).
Затруднения при закрывании глаз можно устранить с помощью геля-смазки на ночь или с помощью пластыря на глаза, чтобы обеспечить полноценный глубокий сон.
Орбитальная декомпрессия может быть выполнена, чтобы позволить выпуклым глазам вернуться обратно в голову. Кость удаляется из черепа позади глаз, и освобождается место для мышц и жировой ткани, чтобы вернуться обратно в череп. [35]
Для лечения клинически активной болезни Грейвса, орбитопатии (оценка клинической активности >2) с по крайней мере легкой или средней степенью тяжести внутривенные глюкокортикоиды являются терапией выбора, обычно назначаемой в форме пульса внутривенного метилпреднизолона. Исследования последовательно показали, что пульс внутривенного метилпреднизолона превосходит пероральные глюкокортикоиды как с точки зрения эффективности, так и с точки зрения снижения побочных эффектов при лечении орбитопатии Грейвса. [36]
Прогноз
Если не лечить, могут возникнуть более серьезные осложнения , включая врожденные дефекты во время беременности, повышенный риск выкидыша , потерю костного минерала [37] и, в крайних случаях, смерть (например, косвенно через осложнения или через тиреоидный шторм ). Болезнь Грейвса часто сопровождается учащением сердечного ритма, что может привести к дальнейшим осложнениям со стороны сердца, включая потерю нормального сердечного ритма (мерцательная аритмия), что может привести к инсульту. Если глаза достаточно проптотичны (выпучены), так что веки не закрываются полностью ночью, возникнет сухость — с риском вторичной инфекции роговицы, которая может привести к слепоте. Давление на зрительный нерв за глазным яблоком может привести к дефектам поля зрения и потере зрения. Длительный нелеченный гипертиреоз может привести к потере костной массы, которая может исчезнуть при лечении. [37]
Эпидемиология

Болезнь Грейвса встречается примерно у 0,5% людей. [4] Данные о болезни Грейвса показали, что риск в течение жизни для женщин составляет около 3%, а для мужчин — 0,5%. [39] Она встречается примерно в 7,5 раз чаще у женщин, чем у мужчин [1] и часто начинается в возрасте от 40 до 60 лет. [6] Это самая распространенная причина гипертиреоза в Соединенных Штатах (примерно от 50 до 80% случаев). [1] [4]
История
Болезнь Грейвса обязана своим названием англо-ирландскому врачу Роберту Джеймсу Грейвсу , [40] который описал случай зоба с экзофтальмом в 1835 году. [41] ( Медицинские эпонимы часто стилизуются непритяжательно; таким образом, болезнь Грейвса и болезнь Грейвса являются вариантами стилей одного и того же термина.)
Немец Карл Адольф фон Базедов независимо сообщил о той же совокупности симптомов в 1840 году. [42] [43] В результате на европейском континенте термины «синдром Базедова», [44] «болезнь Базедова» или «Morbus Basedow» [45] более распространены, чем «болезнь Грейвса». [44] [46]
Болезнь Грейвса [44] [45] также называют экзофтальмическим зобом . [45]
Реже она известна как болезнь Парри, [44] [45] болезнь Бегби, болезнь Флаяна, синдром Флаяни–Базедова и болезнь Марша. [44] Эти названия для болезни произошли от Калеба Хиллиера Парри , Джеймса Бегби , Джузеппе Флаяни и Генри Марша . [44] Ранние сообщения, не получившие широкого распространения, о случаях зоба с экзофтальмом были опубликованы итальянцами Джузеппе Флаяни [47] и Антонио Джузеппе Теста [48] в 1802 и 1810 годах соответственно. [49] До этого Калеб Хиллиер Парри [50] , известный провинциальный врач в Англии конца 18 века (и друг Эдварда Миллера-Галлуса), [51] описал случай в 1786 году. Этот случай был опубликован только в 1825 году — на десять лет раньше Грейвса. [52]
Однако справедливой заслугой первого описания болезни Грейвса является персидский врач XII века Сайид Исмаил аль-Джурджани , [53] который отметил связь зоба и экзофтальма в своем «Тезаурусе шаха Хорезма» , главном медицинском словаре своего времени. [44] [54]
Общество и культура
Известные случаи

- Аяка , японская певица, была диагностирована с болезнью Грейвса в 2007 году. После того, как в 2009 году она публично сообщила о своем диагнозе, она взяла двухлетний перерыв в музыке, чтобы сосредоточиться на лечении. [55] [56]
- Сьюзен Элизабет Блоу , американский педагог и основатель первого финансируемого государством детского сада в Соединенных Штатах, была вынуждена уйти на пенсию и искать лечение от болезни Грейвса в 1884 году. [57]
- Джордж Буш-старший , бывший президент США, заболел новой мерцательной аритмией , и в 1991 году ему поставили диагноз гипертиреоза из-за этого заболевания и назначили лечение радиоактивным йодом. [58] У жены президента, Барбары Буш , также развилась эта болезнь примерно в то же время, что в ее случае привело к тяжелому инфильтративному экзофтальму . [59]
- Родни Дэнджерфилд , американский комик и актёр [60]
- Гейл Деверс , американская бегунья на короткие дистанции: врач рассматривал возможность ампутации ее стоп после того, как у нее появились волдыри и отеки после лучевой терапии болезни Грейвса, но она поправилась и завоевала олимпийские медали.
- Мисси Эллиотт , американская хип-хоп-исполнительница [61]
- Марти Фельдман , британский комедийный писатель, комик и актёр [62] [63]
- Сиа , австралийская певица и автор песен [64]
- Сэмми Гравано , итало-американец, бывший заместитель босса преступной семьи Гамбино [65]
- Джим Гамильтон , шотландский игрок в регби, обнаружил у себя болезнь Грейвса вскоре после ухода из спорта в 2017 году. [66]
- Хейно , немецкий фолк-певец, чьи темные солнцезащитные очки (которые он носил, чтобы скрыть симптомы) стали частью его фирменного образа [67]
- Герберт Хауэллс , британский композитор; первый человек, которого лечили инъекциями радия [68]
- Вайбз Картель , ямайский музыкант, исполняющий танцевальную музыку; заразился болезнью, находясь в заключении [69]
- Яёи Кусама , японская художница [70]
- Надежда Крупская , российская коммунистка и жена Владимира Ленина [71]
- Умм Кульсум — египетская певица, автор песен и киноактриса, работавшая с 1920-х по 1970-е годы.
- Барбара Ли , бывшая американская актриса и фотомодель, ныне представитель Национального фонда по борьбе с болезнью Грейвса [72]
- Кейко Масуда , японская певица и солистка дуэта Pink Lady . [73] [74] [75] [76]
- Юко Миямура , японская актриса озвучивания [77]
- Лорд Монктон , бывший политик UKIP и консерватор ; известный сторонник отрицания изменения климата [78] [79]
- Софья Парнок , русская поэтесса [80] [81] [82]
- Сэр Сесил Спринг Райс , британский посол в США во время Первой мировой войны, внезапно умер от болезни в 1918 году. [83]
- Дэйзи Ридли , британская актриса [84]
- Кристина Россетти , английская поэтесса викторианской эпохи [85]
- Дама Мэгги Смит , британская актриса [86]
- Мэри Уэбб , британская писательница и поэтесса [87]
- Венди Уильямс , американская телеведущая [88]
- Акт Ясукава , японский профессиональный рестлер [89]
Литература
- В романе Итало Свево « Совесть Зенона» героиня Ада заболевает этой болезнью. [90] [91]
- Эрн Мэлли был известным австралийским поэтом, чьи работы были опубликованы только после его смерти от болезни Грейвса в 1943 году. Однако позже выяснилось, что существование Мэлли и вся его биография на самом деле были литературной мистификацией .
Исследовать
Агенты, действующие как антагонисты рецепторов тиреотропного гормона, исследуются как возможное средство лечения болезни Грейвса. [92]
Ссылки
- ^ abcdefghijklmnopqrstu vwxyz "Болезнь Грейвса". www.niddk.nih.gov . 10 августа 2012 г. Архивировано из оригинала 2 апреля 2015 г. Получено 2015-04-02 .
- ^ "Болезнь Грейвса". Autoimmune Registry Inc. Получено 15 июня 2022 г.
- ^ abc Menconi F, Marcocci C, Marinò M (2014). «Диагностика и классификация болезни Грейвса». Autoimmunity Reviews . 13 (4–5): 398–402. doi :10.1016/j.autrev.2014.01.013. PMID 24424182.
- ^ abcdefgh Brent GA (июнь 2008). «Клиническая практика. Тяжёлая болезнь». The New England Journal of Medicine . 358 (24): 2594–605. doi :10.1056/NEJMcp0801880. PMID 18550875.
- ^ abc Burch HB, Cooper DS (декабрь 2015 г.). «Лечение болезни Грейвса: обзор». JAMA . 314 (23): 2544–54. doi :10.1001/jama.2015.16535. PMID 26670972.
- ^ abcde Никифоров YE, Биддингер PW, Никифорова LD, Биддингер PW (2012). Диагностическая патология и молекулярная генетика щитовидной железы (2-е изд.). Филадельфия: Wolters Kluwer Health/Lippincott Williams & Wilkins. стр. 69. ISBN 9781451114553. Архивировано из оригинала 2017-09-08.
- ^ N Burrow G, H Oppenheimer J, Volpé R (1989). Функция и заболевания щитовидной железы . WB Saunders. ISBN 0721621902.
- ^ ab page 157 in: Agabegi ED, Agabegi SS (2008). Шаг вперед к медицине (серия Step-Up) . Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 978-0-7817-7153-5.
- ^ Буневичиус Р., Прейндж А.Дж. (2006). «Психиатрические проявления гипертиреоза Грейвса: патофизиология и варианты лечения». CNS Drugs . 20 (11): 897–909. doi :10.2165/00023210-200620110-00003. PMID 17044727. S2CID 20003511.
- ^ Фальгароне Дж., Хешмати Х.М., Коэн Р., Рич Дж. (январь 2013 г.). «Механизмы в эндокринологии. Роль эмоционального стресса в патофизиологии болезни Грейвса». Европейский журнал эндокринологии . 168 (1): Р13-8. дои : 10.1530/EJE-12-0539 . ПМИД 23027804.
- ^ ab Tomer Y, Davies TF (февраль 1993 г.). «Инфекция, заболевания щитовидной железы и аутоиммунитет». Endocrine Reviews . 14 (1): 107–20. doi :10.1210/edrv-14-1-107. PMID 8491150.
- ^ Smith TJ, Hegedüs L (октябрь 2016 г.). «Болезнь Грейвса» (PDF) . The New England Journal of Medicine . 375 (16): 1552–1565. doi :10.1056/NEJMra1510030. PMID 27797318. Архивировано из оригинала (PDF) 2020-08-01 . Получено 2020-05-29 .
- ^ Desailloud R, Hober D (январь 2009 г.). «Вирусы и тиреоидит: обновление». Virology Journal . 6 : 5. doi : 10.1186/1743-422X-6-5 . PMC 2654877. PMID 19138419 .
- ^ Toivanen P, Toivanen A (1994). «Вызывает ли Yersinia аутоиммунитет?». Международный архив аллергии и иммунологии . 104 (2): 107–11. doi :10.1159/000236717. PMID 8199453.
- ^ Strieder TG, Wenzel BE, Prummel MF, Tijssen JG, Wiersinga WM (май 2003 г.). «Повышенная распространенность антител к энтеропатогенным белкам вирулентности Yersinia enterocolitica у родственников пациентов с аутоиммунным заболеванием щитовидной железы». Clinical and Experimental Immunology . 132 (2): 278–82. doi :10.1046/j.1365-2249.2003.02139.x. PMC 1808711 . PMID 12699417.
- ^ Hansen PS, Wenzel BE, Brix TH, Hegedüs L (октябрь 2006 г.). «Инфекция Yersinia enterocolitica не приводит к повышению риска образования антител к щитовидной железе: данные датского исследования близнецов». Clinical and Experimental Immunology . 146 (1): 32–8. doi :10.1111/j.1365-2249.2006.03183.x. PMC 1809723 . PMID 16968395.
- ^ Мур EA, Мур LM (2013). Достижения в области болезни Грейвса и других гипертиреоидных расстройств. Макфарланд. стр. 77. ISBN 9780786471898.
- ^ «Заболевания щитовидной железы, остеопороз и кальций – Здоровье женщин и медицинская информация». Medicinenet.com. 2006-12-07. Архивировано из оригинала 2013-03-07 . Получено 2013-02-27 .
- ^ ab Carnell NE, Valente WA (июль 1998 г.). «Узлы щитовидной железы при болезни Грейвса: классификация, характеристика и ответ на лечение». Thyroid . 8 (7): 571–6. doi :10.1089/thy.1998.8.571. PMID 9709909.
- ^ Wallaschofski H, Kuwert T, Lohmann T (апрель 2004 г.). «Аутоантитела к рецептору ТТГ — дифференциация гипертиреоза между болезнью Грейвса и токсическим многоузловым зобом». Experimental and Clinical Endocrinology & Diabetes . 112 (4): 171–4. doi :10.1055/s-2004-817930. PMID 15127319.
- ^ Шан С.Дж., Дуглас Р.С. (июнь 2014 г.). «Патофизиология тиреоидной болезни глаз». Журнал нейроофтальмологии . 34 (2): 177–85. doi : 10.1097/wno.00000000000000132 . PMID 24821101. S2CID 10998666.
- ^ Feldon SE, Muramatsu S, Weiner JM (октябрь 1984 г.). «Клиническая классификация офтальмопатии Грейвса. Выявление факторов риска оптической нейропатии». Архивы офтальмологии . 102 (10): 1469–72. doi :10.1001/archopht.1984.01040031189015. PMID 6548373.
- ^ Gorman CA (июнь 1998). «Измерение изменений при офтальмопатии Грейвса». Thyroid . 8 (6): 539–43. doi :10.1089/thy.1998.8.539. PMID 9669294.
- ^ Tan NY, Leong YY, Lang SS, Htoon ZM, Young SM, Sundar G (май 2017 г.). «Рентгенологические параметры ремоделирования орбитальной кости при тиреоидной болезни глаз». Investigative Ophthalmology & Visual Science . 58 (5): 2527–2533. doi : 10.1167/iovs.16-21035 . PMID 28492870.
- ^ Кавуд Т., Мориарти П., О'Ши Д. (август 2004 г.). «Последние разработки в области тиреоидной глазной болезни». BMJ . 329 (7462): 385–90. doi :10.1136/bmj.329.7462.385. PMC 509348 . PMID 15310608.
- ^ Bartley GB (март 2011 г.). «Рандл и его кривая». Архивы офтальмологии . 129 (3): 356–8. doi :10.1001/archophthalmol.2011.29. PMID 21402995.
- ^ abcde Stathopoulos P, Gangidi S, Kotrotsos G, Cunliffe D (июнь 2015 г.). «Болезнь Грейвса: обзор хирургических показаний, лечения и осложнений у группы из 59 пациентов». Международный журнал челюстно-лицевой хирургии . 44 (6): 713–7. doi : 10.1016/j.ijom.2015.02.007. PMID 25726089.
- ^ Homsanit M, Sriussadaporn S, Vannasaeng S, Peerapatdit T, Nitiyanant W, Vichayanrat A (март 2001 г.). «Эффективность однократной суточной дозы метимазола по сравнению с пропилтиоурацилом при индукции эутиреоза». Клиническая эндокринология . 54 (3): 385–90. doi :10.1046/j.1365-2265.2001.01239.x. PMID 11298092. S2CID 24463399.
- ^ Glinoer D, de Nayer P, Bex M (май 2001 г.). «Влияние приема L-тироксина, антител к рецепторам ТТГ и курения на риск рецидива при гипертиреозе Грейвса, леченном антитиреоидными препаратами: двойное слепое проспективное рандомизированное исследование». European Journal of Endocrinology . 144 (5): 475–83. doi : 10.1530/eje.0.1440475 . PMID 11331213.
- ^ Saha GB (2009). Основы ядерной фармации (5-е изд.). Springer-Verlag New York, LLC. стр. 342. ISBN 978-0387403601.
- ^ Шеффлер А (ноябрь 2010 г.). «Заместительная гормональная терапия после операций на щитовидной и паращитовидной железах». Deutsches Ärzteblatt International . 107 (47): 827–34. doi : 10.3238/arztebl.2010.0827. ПМЦ 3003466 . ПМИД 21173898.
- ^ ab "Лечение чрезмерно активной или увеличенной щитовидной железы радиоактивным йодом – Британский фонд тиреоидологии". Btf-thyroid.org . Архивировано из оригинала 2016-09-02 . Получено 2016-09-10 .
- ^ Мизоками, Тетсуя; Хамада, Кацухико; Марута, Тетсуши; Хигаси, Киитиро; Тадзири, Дзюнъити (сентябрь 2016 г.). «Болезненный лучевой тиреоидит после терапии 131I при гипертиреозе Грейвса: клинические особенности и ультразвуковые данные в пяти случаях». European Thyroid Journal . 5 (3): 201–206. doi :10.1159/000448398. ISSN 2235-0640. PMC 5091234 . PMID 27843811.
- ^ Genovese BM, Noureldine SI, Gleeson EM, Tufano RP, Kandil E (февраль 2013 г.). «Какое лучшее окончательное лечение болезни Грейвса? Систематический обзор существующей литературы». Annals of Surgical Oncology (обзор). 20 (2): 660–7. doi :10.1245/s10434-012-2606-x. PMID 22956065. S2CID 24759725.
- ^ Лимонджи, Роберто Мурильо; Фейхо, Эдуардо Дамус; Родригес Лопес Э. Силва, Марлос; Акаиси, Патрисия; Веласко Э. Крус, Антониу Аугусто; Кристиан Пьерони-Гонсалвес, Аллан; Перейра, Филипе; Девото, Мартин; Бернардини, Франческо; Маркес, Виктор; Тао, Джеремия П. (февраль 2020 г.). «Декомпрессия орбитальной кости при проптозе глаз, не связанных с щитовидной железой». Офтальмопластическая и реконструктивная хирургия . 36 (1): 13–16. дои : 10.1097/IOP.0000000000001435. ISSN 1537-2677. PMID 31373985. S2CID 199388425.
- ^ Рой А., Датта Д., Гош С., Мукхопадхай П., Мукхопадхай С., Чоудхури С. (2015). «Эффективность и безопасность низких доз перорального преднизолона по сравнению с пульсовым внутривенным метилпреднизолоном при лечении умеренно тяжелой офтальмопатии Грейвса: рандомизированное контролируемое исследование». Индийский журнал эндокринологии и метаболизма . 19 (3): 351–8. doi : 10.4103/2230-8210.152770 . PMC 4366772. PMID 25932389 .
- ^ ab Becker, Kenneth L., ред. (2001). Принципы и практика эндокринологии и метаболизма (3-е изд.). Филадельфия, Пенсильвания: Lippincott, Williams & Wilkins. стр. 636. ISBN 978-0-7817-1750-2. Архивировано из оригинала 2017-09-08.
- ^ Карле, Аллан; Педерсен, Инге Бюлов; Кнудсен, Нильс; Перрильд, Ганс; Овесен, Ларс; Расмуссен, Лоун Банке; Лаурберг, Питер (2011). «Эпидемиология подтипов гипертиреоза в Дании: популяционное исследование». Европейский журнал эндокринологии . 164 (5): 801–809. дои : 10.1530/EJE-10-1155 . ISSN 0804-4643. ПМИД 21357288.
- ^ Pokhrel, Binod; Bhusal, Kamal (2020), "Болезнь Грейвса", StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 28846288 , получено 04.12.2020
- ↑ Мэтью Грейвс в «Кто это назвал?»
- ^ Грейвс, Р. Дж. Недавно обнаруженное поражение щитовидной железы у женщин. Архивировано 31 марта 2016 г. в Wayback Machine . (Клинические лекции.) London Medical and Surgical Journal (Renshaw), 1835; 7 (часть 2): 516–517. Перепечатано в Medical Classics, 1940; 5:33–36.
- ^ Фон Базедов, Калифорния. Экзофтальм при гипертрофии целлгевебов в Аугенхёле . [Каспера] Wochenschrift für die gesammte Heilkunde , Берлин, 1840, 6: 197–204; 220–228. Частичный английский перевод: Ральф Хермон Майор (1884–1970): Классические описания болезней . Спрингфилд, К.С. Томас, 1932. 2-е издание, 1939; 3-е издание, 1945 г.
- ^ Фон Базедов, Калифорния. «Глотзауген». [Каспера] Wochenschrift für die gesammte Heilkunde , Берлин, 1848: 769–777.
- ^ abcdefg Синдром или болезнь Базедова в Кто это назвал? – история и название болезни
- ^ abcd Robinson, Victor, ed. (1939). "Экзофтальмический зоб, Базедова болезнь, Тяжёлая болезнь". Современный домашний врач, Новая энциклопедия медицинских знаний . WM. H. Wise & Company (Нью-Йорк)., страницы 82, 294 и 295.
- ^ Зоб, диффузный токсический в eMedicine
- ^ Флажани, Г. Сопра и опухоль Фреддо нелль'передней части бронкоцеле шеи. (Оссервазионе LXVII) . В Collezione d'osservazioni e reflessioni di chirurgia. Рим, Микеле А. Рипа Прессо Лино Контедини, 1802; 3: 270–273.
- ^ Теста, AG. Делле малаттие дель куоре, лоро каджони, вид, сеньи и кура. Болонья, 1810 г. 2-е издание в 3-х томах, Флоренция, 1823 г.; Милан 1831 г.; Немецкий перевод, Галле, 1813 г.
- ↑ Джузеппе Флаяни в Who Named It?
- ^ Parry CH (1825). «Увеличение щитовидной железы в связи с увеличением или сердцебиением сердца». Сборники неопубликованных медицинских трудов CH Parry . Лондон. стр. 111–129.
По словам Гаррисона, Parry впервые отметил это состояние в 1786 году. Он кратко описал его в своих
Elements of Pathology and Therapeutics
, 1815. Перепечатано в Medical Classics, 1940, 5: 8–30
- ^ Hull G (июнь 1998 г.). «Кейлеб Хиллер Парри 1755-1822: выдающийся провинциальный врач». Журнал Королевского медицинского общества . 91 (6): 335–8. doi :10.1177/014107689809100618. PMC 1296785. PMID 9771526 .
- ↑ Кейлеб Хиллер Перри в Who Named It?
- ^ Сайид Исмаил аль-Джурджани. Тезаурус шаха Хорезма .
- ^ Ljunggren JG (август 1983 г.). «[Кто стоял за синдромом: Исмаил аль-Джурджани, Теста, Флагани, Парри, Грейвс или Базедов? Вместо этого используйте термин гипертиреоз]». Läkartidningen . 80 (32–33): 2902. PMID 6355710.
- ^ "水嶋ヒロ・絢香、2ショット会見で結婚報告 絢香はバセドウ病を告白、年内で休業へ" (на японском языке). Орикон . 3 апреля 2009 года. Архивировано из оригинала 8 декабря 2015 года . Проверено 19 ноября 2015 г.
- ^ "絢香、初のセルフ・プロデュース・アルバムが発売決定!" (на японском языке). CDJournal. 1 декабря 2011. Архивировано из оригинала 15 октября 2015 года . Проверено 19 ноября 2015 г.
- ^ Шепли, Кэрол Ферринг (2008). Влиятельные люди, бездельники и суфражистки: Истории с кладбища Белльфонтен . Сент-Луис, Миссури: Музей истории Миссури.
- ↑ Оки, Сьюзан (10 мая 1991 г.). «Заболевание щитовидной железы Буша диагностировано как болезнь Грейвса». The Washington Post . Архивировано из оригинала 7 января 2018 г. Получено 17 июня 2023 г.
- ^ Альтман Л.К. (1991-05-28). «Мир доктора — головоломка Белого дома: иммунные заболевания — раздел науки». The New York Times . Архивировано из оригинала 2013-05-08 . Получено 2013-02-27 .
- ^ Ислам С (2017-01-23). "Щитовидная железа – Гиперплазия / зоб – Болезнь Грейвса". Pathologyoutlines.com . Архивировано из оригинала 2016-12-14 . Получено 2017-01-25 .
- ^ Олденбург А. (2011-06-24). «Обновление: Мисси Эллиотт «полностью справляется» с болезнью Грейвса». USA Today . Ганнетт.
- ^ "Знаменитые люди с болезнью Грейвса". HRFnd . 15 декабря 2013 г. Получено 22 февраля 2018 г.
- ^ Kuhlenbeck M (29 июня 2016 г.). «Марти Фельдман против Suits». Jewish Currents . Получено 22.02.2018 .
Зрители также не могли не быть поражены его выпученными глазами, которые стали результатом неудачной операции по поводу болезни Грейвса.
- ^ Rota G. "Факты о Sia Furler | Popsugar Celebrity Australia". Popsugar.com.au . Архивировано из оригинала 2015-02-09 . Получено 2016-09-10 .
- ↑ Guart, Al (31 марта 2002 г.). «Редкая болезнь может убить Сэмми Булла». New York Post . Архивировано из оригинала 11 января 2012 г. Получено 28 января 2020 г.
- ^ "Гамильтон рассказывает о своей болезни в подкасте". YouTube . 8 июня 2017 г. Архивировано из оригинала 2017-09-08.
- ^ "Crossover Crooner: The Strange Comeback of Germany's Wannabe Johnny Cash". Spiegel.de. 2013-02-07. Архивировано из оригинала 2014-11-19 . Получено 2014-07-27 .
- ^ Спайсер П. (1998). Герберт Хауэллс . Бридженд: Серен. п. 44. ИСБН 1-85411-233-3.
- ^ «Все, что вам нужно знать о борьбе Вайбза Картеля за здоровье с болезнью Грейвса» Муруги Гичови. Capital FM . 8 августа 2024 г. Получено 6 октября 2024 г.
- ^ "Яёи Кусама Грейди Т. Тернера". Bomb Magazine . 1 января 1999 г. Получено 29 мая 2020 г.
- ^ "Революционная первая леди: жизнь и борьба жены Ленина". Russia Beyond . Архивировано из оригинала 2018-04-18 . Получено 2018-04-18 .
- ^ "Барбара Ли". Home.rmci.net. Архивировано из оригинала 2012-07-10 . Получено 2013-02-27 .
- ^ "[歌手 増田恵子さん]バセドー病(1)マイク持つ手が震える" . Ёмиури Симбун . 04 августа 2011 г. Проверено 01 февраля 2020 г.
- ^ "[歌手 増田恵子さん]バセドー病(2)同じ病 姉の存在が支えに" . Ёмиури Симбун . 11 августа 2011 г. Проверено 01 февраля 2020 г.
- ^ "[歌手 増田恵子さん]バセドー病(3)ツアー中、甲状腺腫れ上がる" . Ёмиури Симбун . 18 августа 2011 г. Проверено 01 февраля 2020 г.
- ^ "[歌手 増田恵子さん]バセドー病(4)病気公表 無理せず我慢せず" . Ёмиури Симбун . 25 августа 2011 г. Проверено 01 февраля 2020 г.
- ^ "親子知新" . www3.bigcosmic.com. Архивировано из оригинала 15 мая 2007 года . Проверено 18 декабря 2017 г.
- ↑ Руперт Мюррей «Встречайте климатических скептиков». Архивировано 22 октября 2013 г. в Wayback Machine , Сторивилл , 3 февраля 2011 г.
- ^ Абрахам, Джон (22 июня 2011 г.). «Главный труппа: безумства мистера Монктона». The Conversation . The Conversation Media Group Ltd . Получено 14 августа 2024 г.
...в своих речах г-н Монктон цитирует исследование за исследованием, которые создают впечатление, что либо изменение климата не происходит, либо, если оно происходит, нам не нужно об этом беспокоиться.
- ^ «Софья Парнок, российская Сафо». 3 апреля 2017 г.
- ^ Бергин, Диана Льюис (1992). «София Парнок и написание жизни поэтессы-лесбиянки». Slavic Review . 51 (2): 214–231. doi :10.2307/2499528. JSTOR 2499528. S2CID 163967264.
- ^ https://www.king.org/event/the-esoterics-parnok-in-that-infinite-moment/ [ постоянная мертвая ссылка ]
- ↑ Саймон, Бернард (31 мая 2013 г.). «Этот мемориал — поэтическая справедливость для сэра Сесила Спринга Райса». telegraph.co.uk. Архивировано из оригинала 2014-03-12 . Получено 2014-08-25 .
- ^ «Дэйзи Ридли раскрыла диагноз болезни Грейвса». The Hollywood Reporter . 6 августа 2024 г.
- ^ "Кристина Россетти". Poetry Foundation. Архивировано из оригинала 2016-04-17 . Получено 2016-09-10 .
- ↑ Wolf M (18 марта 1990 г.). «Нет ничего лучше этой дамы». New York Times . Архивировано из оригинала 10 августа 2016 г. Получено 19 октября 2015 г.
- ^ "Биография". Архивировано из оригинала 2015-07-16 . Получено 2015-07-16 .
- ↑ Melas C (21 февраля 2018 г.). «Венди Уильямс объявляет о перерыве в шоу из-за болезни Грейвса». CNN . Получено 21 февраля 2018 г.
- ^ «Акт Ясукава возвращается на ринг после пятилетнего отсутствия». 15 ноября 2020 г.
- ^ Свево, Итало (2003). Совесть Зенона: роман (1-е издание Vintage International). Vintage Books. стр. 315–321. ISBN 0375727760.
- ↑ Скарпони, Маттиа (19 августа 2017 г.). «Il morbo di Basedow: lo sfinimento tra Zeno e la Realtà». theWise Magazine (на итальянском языке) . Проверено 25 марта 2020 г.
- ^ "Щитовидная железа". Клиника Майо . Архивировано из оригинала 4 ноября 2016 года . Получено 1 ноября 2016 года .
Внешние ссылки
- «Болезнь Грейвса». Genetics Home Reference . Национальная медицинская библиотека США.
- https://www.ncbi.nlm.nih.gov/gene/?term=graves о могилах на ncbi
