Фибродисплазия оссифицирующая прогрессирующая
| Фибродисплазия оссифицирующая прогрессирующая | |
|---|---|
| Другие имена | Болезнь каменного человека, болезнь Мюнхмейера |
 | |
| Скелет Гарри Рэймонда Истлака , пациента с прогрессирующей оссифицирующей фибродисплазией, демонстрирующий характерный аномальный рост костей. | |
| Специальность | Медицинская генетика , ревматология |
| Симптомы | Непрерывный рост костей |
| Обычное начало | До 10 лет |
| Продолжительность | жизнь |
| Причины | врожденный, точная причина неизвестна |
| Дифференциальная диагностика | Фиброзная дисплазия |
| Уход | Никто |
| Медикамент | Паловаротене , торговая марка Sohonos. |
| Прогноз | Средняя продолжительность жизни составляет около 40 лет (при правильном управлении) |
| Частота | 801 подтвержденный случай во всем мире (2017 г.); уровень заболеваемости оценивается в 0,5 случая на миллион человек (1 из 2 миллионов) |
| Летальные исходы | 60 |
Прогрессирующая оссифицирующая фибродисплазия ( / ˌ f aɪ b r oʊ d ɪ ˈ s p l eɪ ʒ ( i ) ə ɒ ˈ s ɪ f ɪ k æ n z p r ə ˈ ɡ r ɛ s ɪ v ə / ; [1] сокр. ФОП ), также называемая болезнью Мюнхмейера или ранее миозитом оссифицирующим прогрессивным , является чрезвычайно редким заболеванием соединительной ткани , при котором волокнистая соединительная ткань, такая как мышцы , сухожилия и связки, превращается в костную ткань ( окостенение ). Это единственное известное заболевание, при котором одна система органов превращается в другую. [2] Это тяжелое, инвалидизирующее заболевание, не поддающееся лечению.
FOP вызывается мутацией гена ACVR1 . Мутация влияет на механизм восстановления организма, заставляя фиброзную ткань , включая мышцы , сухожилия и связки, окостенеть либо спонтанно, либо при повреждении в результате травмы. Во многих случаях, в противном случае, незначительные травмы могут привести к тому, что суставы станут постоянно сращенными, поскольку образуются новые кости, заменяющие поврежденную мышечную ткань. Это новое костное образование (известное как «гетеротопическое окостенение») в конечном итоге образует вторичный скелет и постепенно ограничивает способность пациента двигаться. Кость, образованная в результате этого процесса, идентична «нормальной» кости, просто в неправильных местах. Косвенные доказательства свидетельствуют о том, что заболевание может вызывать деградацию суставов отдельно от характерного для него роста костей. [3]
Хирургическое удаление лишнего костного нароста, как было показано, заставляет организм «ремонтировать» пораженную область дополнительной костью. Хотя скорость роста костей может различаться в зависимости от пациента, в конечном итоге это состояние делает больных обездвиженными, поскольку новая кость заменяет мускулатуру и срастается с существующим скелетом. Это принесло ФОП прозвище « болезнь каменного человека ». [4]
Признаки и симптомы
По неизвестным причинам дети, рожденные с ФОП, часто имеют неправильно сформированные большие пальцы ног , иногда отсутствует сустав или, в других случаях, просто проявляется заметная опухоль на малом суставе. [5] Первое «вспышка», которая приводит к образованию кости ФОП, обычно происходит до 10 лет. [5] Рост костей обычно прогрессирует от верхней части тела вниз, так же, как кости растут у плодов. У ребенка с ФОП обычно развиваются дополнительные кости, начиная с шеи, затем в плечах, руках, области груди и, наконец, в ступнях. [6]
В частности, окостенение обычно сначала наблюдается в дорсальной, аксиальной, краниальной и проксимальной областях тела. Позже заболевание прогрессирует в вентральной, аппендикулярной, каудальной и дистальной областях. [5] Однако это не обязательно происходит в этом порядке из-за обострений, вызванных травмой. Часто опухолевидные уплотнения, характерные для обострения заболевания, появляются внезапно.
Рост костей, происходящий во время обострений, может привести к потере подвижности пораженных суставов, включая, если затронута челюсть/нижняя челюсть, невозможность полностью открыть рот, что ограничивает речь и прием пищи. Конкретное проявление обострения этого состояния в суставах стопы/голеностопного сустава может привести к ограниченной возможности поставить ногу на землю. [ необходима цитата ] Рост костей также может привести к иммобилизации бедра или колена, что влияет на способность человека ходить. Дополнительное образование костей вокруг грудной клетки ограничивает расширение легких и диафрагмы, вызывая респираторные осложнения. [5]
Поскольку это расстройство встречается невероятно редко, встречаясь только у 1 из 2 миллионов человек, его можно ошибочно диагностировать как рак или фиброз . Это может привести к тому, что врачи назначат биопсию , что может усугубить рост кости ФОП. [7] Наличие деформированных пальцев ног или больших пальцев рук у тех, кто родился с ФОП, помогает отличить это расстройство от других проблем со скелетом. [8]
При правильном медицинском лечении медиана выживаемости составляет 40 лет. Однако задержка диагностики, травмы и инфекции могут снизить продолжительность жизни. [9]
Причины
FOP вызывается аутосомно- доминантным аллелем на хромосоме 2q23-24. [10] Аллель имеет вариабельную экспрессивность , но полную пенетрантность . Большинство случаев вызваны спонтанной мутацией в гаметах ; большинство людей с FOP не могут или предпочитают не иметь детей. Похожее, но менее катастрофическое заболевание — фиброзная дисплазия , которая вызывается постзиготической мутацией .
За заболевание отвечает мутация в гене ACVR1 (также известном как активин-подобная киназа 2 (ALK2)). [10] ACVR1 кодирует рецептор активина типа 1, рецептор BMP типа 1. Мутация вызывает замену кодона 206 с аргинина на гистидин в белке ACVR1. [11] [12] Эта замена вызывает аномальную активацию ACVR1, что приводит к трансформации соединительной ткани и мышечной ткани во вторичный скелет. Это заставляет эндотелиальные клетки трансформироваться в мезенхимальные стволовые клетки , а затем в кость. [13] Обычно ген ACVR1 кодирует трансмембранную киназу рецептора активина типа 1 , которая связывает рецепторы BMP (BMPR типа I и BMPR типа II) для передачи сигналов хондрогенеза . BMP относятся к суперсемейству белков, известных как белки трансформирующего фактора роста бета ( TGF- β ). Связывание белка ACVR1 с рецепторами BMP запускает каскад сигналов, который имеет решающее значение для индукции формирования эндохондральной кости во время развития, а также для гомеостаза скелета и тканей . [14]
Генетика
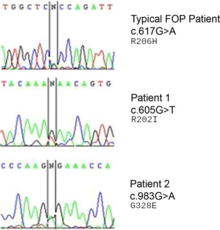
ФОП — это аутосомно-доминантное заболевание. Таким образом, ребенок пораженного гетерозиготного родителя и здорового родителя имеет 50% вероятность быть пораженным. Два пораженных человека могут произвести здоровых детей. Два здоровых человека могут произвести пораженное потомство в результате мутации гена. Гомозиготная доминантная форма более тяжелая, чем гетерозиготная форма. [15]
Белок, вызывающий окостенение, обычно дезактивируется ингибиторным белком после того, как кости плода формируются в утробе матери, но у пациентов с ФОП белок продолжает работать. Аберрантное формирование костей у пациентов с ФОП происходит, когда поврежденные соединительные ткани или мышечные клетки в местах повреждения или роста неправильно экспрессируют фермент для восстановления костей во время апоптоза (саморегулируемая гибель клеток), в результате чего лимфоциты содержат избыток костного морфогенетического белка 4 (BMP4), предоставляемого во время реакции иммунной системы. Кость, которая получается, возникает независимо от нормального скелета, образуя свои собственные дискретные скелетные элементы. Эти элементы, однако, могут сливаться с нормальной скелетной костью. [16] Диафрагма, язык и экстраокулярные мышцы остаются в этом процессе, как и сердечная и гладкая мускулатура . [5] Поскольку неправильный фермент остается неразрешенным в рамках иммунного ответа, организм продолжает предоставлять неправильные лимфоциты, содержащие BMP4. BMP4 — это продукт, который способствует развитию скелета у нормального эмбриона. [17]
Ген ACVR1 кодирует рецептор костного морфогенетического белка (BMP); этот ген мутирует при FOP. Он отвечает за рост и развитие костей и мышц. Типичная мутация, R202H, заставляет ингибитор FKBP1A менее прочно связываться с активационной петлей GS. [18] В результате ACVR1 не выключается эффективно, и происходит чрезмерный рост костей и хрящей, а также сращение суставов. [19] Атипичные мутации, затрагивающие другие остатки, работают аналогичным образом. В некоторых случаях рецептор может в конечном итоге сигнализировать о своей активности, не будучи связанным со своим активирующим лигандом. [20]
Большинство случаев ФОП являются результатом новой генной мутации: у этих людей не было истории этого конкретного расстройства в их семье. Есть некоторые случаи, когда человек унаследовал мутацию от одного из пораженных родителей. [19]
Диагноз
Как правило, ФОП можно диагностировать с помощью рентгенограмм . Ранняя диагностика этого расстройства с помощью рентгенологии очень важна, чтобы избежать ненужных инвазивных исследований, таких как биопсия . Самая маленькая или тривиальная травма или внутримышечные инъекции могут усилить прогрессирование заболевания через воспаление, отсюда и благоприятность рентгенологии. Клиницисты должны знать об этой редкой сущности, так как ее часто ошибочно диагностируют как рак или другие доброкачественные образования, такие как инфекция, что приводит к биопсии, которая часто может ускорить прогрессирование заболевания. [21]
Вспышки заболевания можно оценить клинически по повышенным уровням щелочной фосфатазы и костно-специфической щелочной фосфатазы . [22] Другим явным признаком ФОП является укороченный большой палец ноги с деформированной дистальной первой плюсневой костью и отсутствующей или аномальной первой фалангой и/или межфаланговым суставом. [23]
Уход
В то время как ФОП остается неизлечимым, многообещающим прорывом является одобренное лечение Sohonos ( паловаротен ). [24] Примечательно, что попытки хирургического удаления кости у пациента с ФОП могут привести к взрывному росту новой кости. [25] Во время анестезии люди с ФОП могут столкнуться с трудностями при интубации , рестриктивным заболеванием легких и изменениями в системе электропроводности сердца . [26] Следует избегать действий, которые повышают риск падения или повреждения мягких тканей, поскольку даже незначительная травма может спровоцировать гетеротопическую оссификацию . [27]
Хотя эффективных методов окончательного лечения этого расстройства не существует, существуют периодические методы лечения, такие как противовоспалительные препараты для подавления воспаления в результате обострений или воспаления из-за повреждения мышц. В настоящее время хирургическое вмешательство обычно не рекомендуется для людей с ФОП, поскольку оно может спровоцировать быстрое формирование костей в местах разрезов или там, где были наложены швы на мышцы или соединительную ткань. Можно рассмотреть возможность проведения спасающей жизнь операции, однако разработка хирургического плана с участием специалиста по ФОП может считаться наилучшей практикой. Хирургическое устранение контрактур суставов, как правило, безуспешно и сопряжено с риском новой гетеротопической оссификации, вызванной травмой. [28]
Антисмысловая терапия, в частности, с использованием аллель-селективных LNA-гэпмеров, стала многообещающей стратегией для FOP [29] . Этот подход нацелен на мутировавший ген ACVR1, который вызывает гетеротопическую оссификацию, реагируя аберрантно на активин А. В недавних исследованиях LNA-гэпмеры эффективно снижали экспрессию патогенного транскрипта ACVR1R206H, сохраняя при этом дикий тип гена ACVR1, таким образом, избирательно подавляя остеогенную дифференциацию, связанную с FOP. Этот новый антисмысловой подход предлагает потенциал для терапевтического применения при FOP, представляя собой прорыв в целевом генетическом лечении этого и потенциально других аутосомно-доминантных заболеваний
Эпидемиология
По состоянию на 2017 год [обновлять]во всем мире было подтверждено около 800 случаев ФОП, что делает ФОП одним из самых редких известных заболеваний. [30] Предполагаемая заболеваемость ФОП составляет 0,5 случая на миллион человек и затрагивает все этнические группы. [30]
История
Медицинские отчеты, описывающие людей, страдающих ФОП, датируются доктором Гаем Патеном в 1692 году. [30] ФОП изначально назывался миозитом оссифицирующим прогрессирующим и считалось, что он вызывается мышечным воспалением ( миозитом ), которое вызывает образование костей. [30] Заболевание было переименовано Виктором А. МакКьюсиком в 1970 году после открытия того, что мягкие ткани, помимо мышц (например, связки ), также поражаются процессом заболевания. [30]
Самый известный случай ФОП — случай Гарри Истлака (1933–1973). Его заболевание начало развиваться в возрасте десяти лет, и к моменту его смерти от пневмонии в ноябре 1973 года, за шесть дней до его 40-летия, его тело полностью окостенело, и он мог двигать только губами. Истлак никогда не встречал другого человека с ФОП в течение своей жизни. [31]
Истлак пожертвовал свое тело науке, и его скелет сейчас находится в Музее Мюттера в Филадельфии , и оказался бесценным источником информации в изучении ФОП. Другой человек с ФОП, Кэрол Орзел (20 апреля 1959 г. – февраль 2018 г.), также пожертвовала свое тело музею, и ее скелет был выставлен там, рядом со скелетом Истлака, в феврале 2019 г. [32] [33]
Исследовать
Клинические испытания изотретиноина , этидроната с пероральными кортикостероидами и пергексилина малеата не смогли продемонстрировать эффективность, хотя изменчивое течение заболевания и малая распространенность вызывают неопределенность. [22]
Несколько фармацевтических компаний, специализирующихся на редких заболеваниях, в настоящее время находятся на разных стадиях исследования различных терапевтических подходов к лечению ФОП.
В августе 2015 года Управление по разработке орфанных препаратов Управления по контролю за продуктами питания и лекарственными средствами США (FDA) предоставило компании La Jolla Pharmaceuticals статус орфанного препарата для двух новых соединений для лечения ФОП. Соединения представляют собой низкомолекулярные ингибиторы протеинкиназы , предназначенные для селективной блокировки ACVR1 (ALK2). [39]
В августе 2015 года компания Clementia Pharmaceuticals также начала набор детей (в возрасте от 6 лет и старше) в клиническое исследование II фазы паловаротена для лечения ФОП. [40] Доклинические исследования показали, что паловаротен, агонист гамма-рецептора ретиноевой кислоты, блокировал аномальное формирование костей у животных моделей путем ингибирования вторичных мессенджерных систем в пути BMP. [41] Clementia лицензировала паловаротен у Roche Pharmaceuticals, которая ранее оценивала это соединение у более чем 800 человек, включая здоровых добровольцев и пациентов с хронической обструктивной болезнью легких. Паловаротен получил статус Fast Track от FDA и статус орфанного препарата для лечения ФОП как от FDA, так и от Европейского агентства по лекарственным средствам (EMA). [40]
В сентябре 2015 года компания Regeneron объявила о новом взгляде на механизм заболевания, включающего активацию рецептора ACVR1 активином А. В 2016 году компания инициировала исследование фазы 1 своего антитела к активину, REGN 2477 , на здоровых добровольцах; исследование фазы 2 на пациентах с ФОП было проведено в 2017 году. [42]
Другой потенциальный терапевтический подход включает аллель-специфическую РНК-интерференцию , которая нацелена на мутировавшую мРНК для деградации, сохраняя при этом нормальную экспрессию гена ACVR1. [43]
Дальнейшее изучение механизмов гетеротопического костеобразования при ФОП может помочь в разработке методов лечения других заболеваний, связанных с образованием внескелетной костной ткани.
Фибро/адипогенные предшественники (FAP) могут быть типом клеток, вызывающих заболевание, ответственным за эктопическое образование костей, зависящее от активина А, как в мышцах, так и в сухожилиях мышей, имеющих мутацию ACVR1(R206H), вызывающую FOP. [44]
В декабре 2019 года компания Ipsen частично приостановила проведение клинических исследований для лиц младше 14 лет из-за сообщений о раннем сращении зон роста.
Недавно, в 2021 году [обновлять], потенциальный терапевтический кандидат, саракатиниб , находится на III фазе клинических испытаний в качестве мощного ингибитора гетеротопической оссификации у мышей дикого типа и мышей с мутацией ACVR1. [45]
Смотрите также
- Международная ассоциация FOP – американская организация
- Несовершенный остеогенез — группа генетических нарушений, приводящих к хрупкости костей, состояние, характеризующееся необычайно легкой ломкостью костей, вызванное мутациями в генах, связанных с генами, ответственными за ФОП.
- Прогрессирующая костная гетероплазия – редкое генетическое заболевание, характеризующееся кожной или подкожной оссификацией.
- FOP Friends – британская благотворительная организацияСтраницы, отображающие описания викиданных в качестве резерва
Ссылки
- ^ "Медицинское определение фибродисплазии оссифицирующей прогрессирующей". www.merriam-webster.com . Получено 8 мая 2022 г. .
- ^ Каплан, Фредерик С.; Шен, Ци; Лунев, Виталий; Зееманн, Петра; Гроппе, Джей; Катагири, Такенобу; Пиньоло, Роберт Дж.; Шор, Эйлин М. (2008). «Метаморфозы скелета при прогрессирующей фибродисплазии оссифицирующей (ФОП)». Журнал костного и минерального метаболизма . 26 (6): 521–530. doi :10.1007/s00774-008-0879-8. PMC 3620015. PMID 18979151 .
- ^ Pinkowski, Jen (1 марта 2019 г.). «Вот что происходит, когда ткани вашего тела превращаются в кости». National Geographic . Архивировано из оригинала 3 марта 2019 г.
- ^ Верма, Амит Кумар; Ага, Паллави; Сингх, Шайлеш Кумар; Сингх, Рагини (2012). «Болезнь каменного человека: прогрессирующая оссифицирующая фибродисплазия: пересмотр визуализации». Отчеты о случаях в BMJ . 2012 : bcr2012006422. doi : 10.1136/bcr-2012-006422. PMC 4543882. PMID 22843760 .
- ^ abcde Каплан, Фредерик С.; Ле Меррер, Мартин; Глейзер, Дэвид Л.; Пиньоло, Роберт Дж.; Голдсби, Роберт Э.; Киттерман, Джозеф А.; Гроппе, Джей; Шор, Эйлин М. (март 2008 г.). "Fibrodysplasia ossificans progressiva". Best Practice & Research Clinical Rheumatology . 22 (1): 191–205. doi :10.1016/j.berh.2007.11.007. PMC 2424023. PMID 18328989 .
- ^ "Fibrodysplasia ossificans progressiva: MedlinePlus Genetics". medlineplus.gov . Получено 31 декабря 2022 г. .
- ^ Обамуйиде, HA; Огунладе, SO (март 2015 г.). «Опухоль, при которой хирургическое вмешательство принесет больше вреда, чем пользы: отчет о случае прогрессирующей оссифицирующей фибродисплазии». Нигерийский последипломный медицинский журнал . 22 (1): 83–8. doi : 10.4103/1117-1936.163373 . PMID 25875418. S2CID 33239264. ProQuest 1850178336.
- ^ "Fibrodysplasia ossificans progressiva". Lister Hill National Center for Biomedical Communications . Получено 12 декабря 2013 г.
- ^ Салех, Мохаммед; Командер, Йост; Боччарди, Рената; Кинабо, Грейс; Хамель, Бен (2015). «Прогрессирующая оссифицирующая фибродисплазия с незначительной односторонней аномалией большого пальца стопы в спорадическом случае из Северной Танзании с распространенной мутацией ACVR1c.617G>A». Pan African Medical Journal . 22 : 299. doi : 10.11604/pamj.2015.22.299.8032. PMC 4769042. PMID 26966495 .
- ^ ab Shore, Eileen M; Xu, Meiqi; Feldman, George J; Fenstermacher, David A; Cho, Tae-Joon; Choi, In Ho; Connor, J Michael; Delai, Patricia; Glaser, David L; LeMerrer, Martine; Morhart, Rolf; Rogers, John G; Smith, Roger; Triffitt, James T; Urtizberea, J Andoni; Zasloff, Michael; Brown, Matthew A; Kaplan, Frederick S (май 2006 г.). «Рекуррентная мутация в рецепторе BMP типа I ACVR1 вызывает наследственную и спорадическую прогрессирующую оссифицирующую фибродисплазию». Nature Genetics . 38 (5): 525–527. doi :10.1038/ng1783. PMID 16642017. S2CID 41579747.
- ^ «Исследователи Пенсильванского университета обнаружили ген, который создает второй скелет» (пресс-релиз). Медицинская школа Пенсильванского университета. 23 апреля 2006 г.
- ^ Hatsell, Sarah J.; Idone, Vincent; Wolken, Dana M. Alessi; Huang, Lily; Kim, Hyon J.; Wang, Lili; Wen, Xialing; Nannuru, Kalyan C.; Jimenez, Johanna; Xie, Liqin; Das, Nanditha; Makhoul, Genevieve; Chernomorsky, Rostislav; D'Ambrosio, David; Corpina, Richard A.; Schoenherr, Christopher J.; Feeley, Kieran; Yu, Paul B.; Yancopoulos, George D.; Murphy, Andrew J.; Economides, Aris N. (2 сентября 2015 г.). «Мутация рецептора ACVR1 R206H вызывает прогрессирующую оссифицирующую фибродисплазию, придавая чувствительность к активину A». Science Translational Medicine . 7 (303): 303ra137. doi : 10.1126/scitranslmed.aac4358. PMC 6164166. PMID 26333933 .
- ^ van Dinther, Maarten; Visser, Nils; de Gorter, David JJ; Doorn, Joyce; Goumans, Marie-José; de Boer, Jan; ten Dijke, Peter (23 ноября 2009 г.). «Мутация ALK2 R206H, связанная с Fibrodysplasia Ossificans Progressiva, придает конститутивную активность рецептору BMP типа I и повышает чувствительность мезенхимальных клеток к дифференцировке остеобластов и формированию кости, вызванной BMP». Journal of Bone and Mineral Research . 25 (6): 091211115834058–35. doi : 10.1359/jbmr.091110 . PMID 19929436. S2CID 207269687.
- ^ Линь, Шусянь; Свобода, Кэти КХ; Фэн, Цзянь Цюань; Цзян, Синьцюань (5 апреля 2016 г.). «Биологическая функция рецепторов типа I костного морфогенетического белка в кости». Bone Research . 4 (1): 16005. doi :10.1038/boneres.2016.5. ISSN 2095-6231. PMC 4820739. PMID 27088043 .
- ^ Каммингс, Майкл Р. Человеческая наследственность: принципы и проблемы Cengage Learning, 2011, [2009]. стр. 77
- ^ Шор, Эйлин М.; Каплан, Фредерик С. (2008). «Взгляд на редкое генетическое нарушение формирования внескелетной кости, прогрессирующую оссифицирующую фибродисплазию (FOP)». Bone . 43 (3): 427–443. doi :10.1016/j.bone.2008.05.013. PMC 2601573 . PMID 18590993.
- ^ Кирзенбаум, Абрахам (2002). Гистология и клеточная биология . Нью-Йорк: Мосби. ISBN 978-0-323-01639-1.
- ^ «AVCR1», Genetics Home Reference , Национальная медицинская библиотека США, август 2007 г. Доступ 18 февраля 2014 г.
- ^ ab "Fibrodysplasia ossificans progressiva", Genetics Home Reference , Национальная медицинская библиотека США, август 2007 г. Доступ 18 февраля 2014 г.
- ^ Petrie, KA; Lee, WH; Bullock, AN; Pointon, JJ; Smith, R; Russell, RG; Brown, MA; Wordsworth, BP; Triffitt, JT (2009). «Новые мутации в ACVR1 приводят к атипичным признакам у двух пациентов с прогрессирующей оссифицирующей фибродисплазией». PLOS ONE . 4 (3): e5005. Bibcode : 2009PLoSO...4.5005P. doi : 10.1371 /journal.pone.0005005 . PMC 2658887. PMID 19330033.
- ^ Ямин, Гиам; Дагиги, Шади; Мафи, Махмуд (31 мая 2021 г.). «Прогрессирующая оссифицирующая фибродисплазия (FOP), проявляющаяся в виде быстро растущей некальцифицированной массы шеи». Журнал радиологических отчетов . 15 (5): 10–16. doi : 10.3941/jrcr.v15i5.4103. ISSN 1943-0922. PMC 8253151. PMID 34276874 .
- ^ аб Кито, Хироши; Ачива, Масатака; Канеко, Хироши; Мисима, Кеничи; Мацусита, Масаки; Кадоно, Изуми; Горовиц, Джон Д.; Саллюстио, Бенедетта С; Оно, Кинджи; Исигуро, Наоки (2013). «Малеат пергексилина в лечении прогрессирующей оссифицирующей фибродисплазии: открытое клиническое исследование». Сиротский журнал редких заболеваний . 8 (1): 163. дои : 10.1186/1750-1172-8-163 . ПМК 4015865 . ПМИД 24131551.
- ^ "Fibrodysplasia Ossificans Progressiva". Август 2020 г.
- ^ Исследования, Центр оценки лекарственных средств и (17 августа 2023 г.). "FDA одобряет первое лечение прогрессирующей оссифицирующей фибродисплазии". FDA .
- ^ Американская академия хирургов-ортопедов (май 2006 г.). «Прогрессирующая оссифицирующая фибродисплазия (FOP)». orthoinfo.aaos.org. Архивировано из оригинала 21 июня 2012 г. Получено 7 октября 2011 г.
- ^ Newton, MC; Allen, PW; Ryan, DC (февраль 1990 г.). «Fibrodysplasia Ossificans Progressiva». British Journal of Anaesthesia . 64 (2): 246–250. doi : 10.1093/bja/64.2.246 . PMID 2317429.
- ^ «Медицинское лечение прогрессирующей оссифицирующей фибродисплазии: современные аспекты лечения» (PDF) . Международная ассоциация по прогрессирующей оссифицирующей фибродисплазии. Январь 2020 г.
- ^ Каплан, Фредерик С.; Ле Меррер, Мартин; Глейзер, Дэвид Л.; Пиньоло, Роберт Дж.; Голдсби, Роберт; Киттерман, Джозеф А.; Гроппе, Джей; Шор, Эйлин М. (март 2008 г.). "Fibrodysplasia ossificans progressiva". Best Practice & Research. Clinical Rheumatology . 22 (1): 191–205. doi :10.1016/j.berh.2007.11.007. ISSN 1521-6942. PMC 2424023. PMID 18328989 .
- ^ Маруяма, Рика; Нгуен, Куинь; Рошми, Рохини Рой; Тузник, Александр; Йокота, Тошифуми (июнь 2022 г.). «Аллель-селективные LNA-гапмеры для лечения прогрессирующей оссифицирующей фибродисплазии подавляют патогенный транскрипт ACVR1R206H и подавляют остеогенную дифференциацию». Nucleic Acid Therapeutics . 32 (3): 185–193. doi :10.1089/nat.2021.0009. ISSN 2159-3345. PMID 35085461.
- ^ abcdefg Мартелли, Андерсон; Сантос, Арнальдо Родригес (3 июля 2014 г.). «Клеточные и морфологические аспекты прогрессирующей оссифицирующей фибродисплазии: уроки формирования, восстановления и биоинженерии костей». Органогенез . 10 (3): 303–311. doi :10.4161/org.29206. PMC 4750545. PMID 25482313 .
- ^ Каплан, ФС (2013). Скелет в шкафу. Джин, 528(1), 7–11. https://doi.org/10.1016/j.gene.2013.06.022
- ^ Маккалоу, Мари (28 февраля 2019 г.). «Новая экспозиция Музея Мюттера исполняет последнее желание женщины, которая превратилась в кость». The Philadelphia Inquirer . Получено 28 февраля 2019 г.
- ^ «Музей Мюттера представляет новый экспонат: скелет женщины из Филадельфии с редким заболеванием костей». Музей Мюттера . 5 марта 2019 г. Архивировано из оригинала 28 августа 2021 г. Получено 7 марта 2020 г.
- ^ "Dr. Frederick Kaplan, MD 2017 Rare Impact Award Honoree". Национальная организация по редким заболеваниям . 15 марта 2017 г. Получено 8 мая 2022 г.
- ^ "Frederick Kaplan: Rare Impact Award" (PDF) . Альманах . 63 (32). Университет Пенсильвании : 7. 25 апреля 2017 г. Получено 8 мая 2022 г.
- ^ "An FOP Timeline". Penn Medicine . Университет Пенсильвании . Получено 8 мая 2022 г.
- ^ "AP: Ученые раскрывают тайну редкого заболевания костей". NBC News . 24 апреля 2006 г. Получено 8 мая 2022 г.
- ↑ Мейдер, Томас (1 февраля 1998 г.). «Несколько сотен людей превратились в кости». The Atlantic . Получено 8 мая 2022 г.
- ^ «La Jolla Pharmaceutical Company получает статус орфанного препарата для двух новых соединений для лечения прогрессирующей оссифицирующей фибродисплазии» (пресс-релиз). La Jolla Pharmaceutical Company. 18 августа 2015 г.
- ^ ab "Clementia Pharmaceuticals расширяет текущее исследование фазы 2, чтобы включить детей с прогрессирующей оссифицирующей фибродисплазией (FOP)" (пресс-релиз). Clementia Pharmaceuticals. 25 августа 2015 г.
- ^ "Pipeline". www.clementiapharma.com . Архивировано из оригинала 29 сентября 2015 г. Получено 22 ноября 2015 г.
- ^ «Regeneron делится новостями о своей текущей программе исследований ФОП». Международная ассоциация фибродисплазии оссифицирующей прогрессирующей фибродисплазии. 9 марта 2017 г.
- ^ JW Lowery; V. Rosen (2012). «Аллель-специфическая РНК-интерференция при FOP. Подавление чувствительности гена FOP». Генная терапия . 19 (7): 701–702. doi : 10.1038/gt.2011.190 . PMID 22130446. S2CID 24990800.
- ^ Лис-Шепард, Джон Б.; Ямамото, Масакадзу; Бисвас, Арпита А.; Стоессель, Шон Дж.; Николас, Сара-Энн Э.; Когсуэлл, Кэти А.; Девараконда, Парвати М.; Шнайдер, Майкл Дж.; Камминс, Саманта М.; Лежандр, Николас П.; Ямамото, Шоко; Каартинен, Веса; Хантер, Джеффри В.; Голдхамер, Дэвид Дж. (декабрь 2018 г.). «Активин-зависимая сигнализация в фибро/адипогенных предшественниках вызывает прогрессирующую оссифицирующую фибродисплазию». Nature Communications . 9 (1): 471. Bibcode :2018NatCo...9..471L. doi :10.1038/s41467-018-02872-2. PMC 5797136. PMID 29396429 .
- ^ Уильямс, Элеанор; Багарова, Яна; Керр, Джорджина; Ся, Донг-Донг; Плейс, Элси С.; Дей, Девавина; Шен, Юэ; Бокобо, Джеффри А.; Мохедас, Агустин Х.; Хуан, Сюли; Сандерсон, Филип Э. (2021). «Саракатиниб — эффективный клинический кандидат для лечения прогрессирующей оссифицирующей фибродисплазии». JCI Insight . 6 (8): e95042. doi :10.1172/jci.insight.95042. ISSN 2379-3708. PMC 8119212. PMID 33705358 .

