Эластография
This article needs more reliable medical references for verification or relies too heavily on primary sources. (April 2018) |
This article needs to be updated. (April 2018) |
| Эластография | |
|---|---|
 Обычная ультрасонография (нижнее изображение) и эластография (сверхзвуковая сдвиговая визуализация; верхнее изображение) папиллярной карциномы щитовидной железы , злокачественного рака. Рак (красный) намного жестче здоровой ткани. | |
| МеШ | Д054459 |
Эластография — это класс методов медицинской визуализации , которые отображают упругие свойства и жесткость мягких тканей . [1] [2] Основная идея заключается в том, что независимо от того, является ли ткань твердой или мягкой, это даст диагностическую информацию о наличии или состоянии заболевания . Например, раковые опухоли часто будут тверже, чем окружающие ткани, а больная печень жестче, чем здоровая. [1] [2] [3] [4]
Наиболее известные методы используют ультразвуковую или магнитно-резонансную томографию (МРТ) для создания как карты жесткости, так и анатомического изображения для сравнения. [ необходима ссылка ]
Историческая справка
_(3).jpg/440px-Breast_self-exam_illustration_(series_of_6)_(3).jpg)
Пальпация — это практика ощупывания жесткости тканей человека или животного руками врача. Ручная пальпация восходит как минимум к 1500 году до нашей эры, и египетские папирус Эберса и папирус Эдвина Смита дают инструкции по диагностике с помощью пальпации. В Древней Греции Гиппократ дал инструкции по многим формам диагностики с использованием пальпации, включая пальпацию молочных желез, ран, кишечника, язв, матки, кожи и опухолей. В современном западном мире пальпация стала считаться уважаемым методом диагностики в 1930-х годах. [1] С тех пор практика пальпации стала широко распространенной и считается эффективным методом обнаружения опухолей и других патологий.
Ручная пальпация имеет несколько важных ограничений: она ограничена тканями, доступными руке врача, она искажается любой промежуточной тканью и является качественной, а не количественной. Эластография, измерение жесткости тканей, стремится решить эти проблемы.
Как это работает
Существует множество методов эластографии, находящихся на стадиях разработки от ранних исследований до широкого клинического применения. Каждый из этих методов работает по-своему. Все методы объединяет то, что они создают искажение в ткани, наблюдают и обрабатывают реакцию ткани, чтобы сделать вывод о механических свойствах ткани, а затем отображают результаты оператору, обычно в виде изображения. Каждый метод эластографии характеризуется тем, как он делает каждую из этих вещей.
Вызывая искажение
Чтобы визуализировать механические свойства ткани, нам нужно увидеть, как она ведет себя при деформации. Существует три основных способа вызвать искажение для наблюдения. Это:
- Надавливание/деформация или вибрация поверхности тела ( кожи ) или органа ( простаты ) зондом или инструментом,
- Использование акустической радиационной импульсной визуализации с использованием ультразвука для удаленного создания «толчка» внутри ткани, и
- Использование искажений, создаваемых нормальными физиологическими процессами, например, пульсом или сердцебиением.
Наблюдение за реакцией
Основной способ классификации эластографических методов — это то, какой метод визуализации (тип) они используют для наблюдения за ответом. Эластографические методы используют ультразвук , магнитно-резонансную томографию (МРТ) и датчики давления/стресса в тактильной визуализации (TI) с использованием тактильного датчика (ов). Существует также несколько других методов.
Наблюдение за реакцией ткани может принимать различные формы. С точки зрения полученного изображения, оно может быть 1-D (т. е. линия), 2-D (плоскость), 3-D (объем) или 0-D (отдельное значение), и это может быть видео или отдельное изображение. В большинстве случаев результат отображается оператору вместе с обычным изображением ткани, которое показывает, где в ткани возникают различные значения жесткости.
Обработка и презентация
После того, как реакция была замечена, жесткость может быть рассчитана по ней. Большинство методов эластографии определяют жесткость ткани на основе одного из двух основных принципов:
- При заданной приложенной силе ( напряжении ) более жесткая ткань деформируется ( напрягается ) меньше, чем более мягкая ткань.
- Механические волны (в частности, сдвиговые волны ) распространяются через более жесткие ткани быстрее, чем через более мягкие ткани.
Некоторые методы просто отображают искажение и/или реакцию, или скорость волны оператору, в то время как другие вычисляют жесткость (в частности, модуль Юнга или аналогичный модуль сдвига ) и отображают его. Некоторые методы представляют результаты количественно, в то время как другие представляют только качественные (относительные) результаты.
Ультразвуковая эластография
Существует множество методов ультразвуковой эластографии. Наиболее известные из них приведены ниже.
Квазистатическая эластография/деформационная визуализация

Квазистатическая эластография (иногда называемая просто «эластографией» по историческим причинам) является одним из самых ранних методов эластографии. В этом методе к тканям применяется внешняя компрессия, и сравниваются ультразвуковые изображения до и после компрессии. Наименее деформированные области изображения являются наиболее жесткими, в то время как наиболее деформированные области являются наименее жесткими. [3] Как правило, то, что отображается оператору, представляет собой изображение относительных искажений ( деформаций ), что часто имеет клиническую полезность. [1]
Однако из изображения относительного искажения часто желательно сделать количественную карту жесткости. Для этого необходимо сделать предположения о природе визуализируемой мягкой ткани и о ткани за пределами изображения. Кроме того, при сжатии объекты могут перемещаться в изображение или из него или вокруг него, вызывая проблемы с интерпретацией. Другим ограничением этой техники является то, что, как и при ручной пальпации, она испытывает трудности с органами или тканями, которые не находятся близко к поверхности или легко сжимаются. [4]
Акустическая лучевая импульсная визуализация (ARFI)

Акустическая радиационная импульсная визуализация (ARFI) [5] использует ультразвук для создания качественной 2-мерной карты жесткости ткани. Это происходит путем создания «толчка» внутри ткани с помощью акустической радиационной силы от сфокусированного ультразвукового луча. Количество ткани, проталкиваемой вниз вдоль оси луча, отражает жесткость ткани; более мягкая ткань легче проталкивается, чем более жесткая. ARFI показывает качественное значение жесткости вдоль оси проталкивающего луча. Путем нажатия во многих разных местах создается карта жесткости ткани. Виртуальная сенсорная квантификация визуализации (VTIQ) успешно использовалась для выявления злокачественных шейных лимфатических узлов. [6]
Визуализация упругости сдвиговой волной (SWEI)
В визуализации упругости сдвиговой волной (SWEI), [7] подобной ARFI, «толчок» индуцируется глубоко в ткани силой акустического излучения . Возмущение, создаваемое этим толчком, распространяется вбок через ткань в виде сдвиговой волны . Используя модальность изображения, такую как ультразвук или МРТ, чтобы увидеть, как быстро волна достигает различных боковых положений, можно сделать вывод о жесткости промежуточной ткани. Поскольку термины «визуализация упругости» и «эластография» являются синонимами, исходный термин SWEI, обозначающий технологию картирования упругости с использованием сдвиговых волн, часто заменяется на SWE. Принципиальное различие между SWEI и ARFI заключается в том, что SWEI основан на использовании сдвиговых волн, распространяющихся латерально от оси пучка, и создании карты упругости путем измерения параметров распространения сдвиговой волны, тогда как ARFI получает информацию об упругости от оси толкающего пучка и использует множественные толчки для создания двухмерной карты жесткости. В ARFI не задействованы сдвиговые волны, а в SWEI не задействована оценка осевой упругости. SWEI применяется в сверхзвуковой сдвиговой визуализации (SSI).
Сверхзвуковая сдвиговая визуализация (SSI)
_supersonic_shear_imaging_of_hand_muscle_stiffness.tif/lossy-page1-440px-Killian_Bouillard,_Nordez_A,_Hug_F_(2011)_supersonic_shear_imaging_of_hand_muscle_stiffness.tif.jpg)
Сверхзвуковая сдвиговая визуализация (SSI) [8] [9] дает количественную двумерную карту жесткости ткани в реальном времени. SSI основана на SWEI: она использует силу акустического излучения, чтобы вызвать «толчок» внутри интересующей ткани, генерируя сдвиговые волны, а жесткость ткани вычисляется на основе того, насколько быстро результирующая сдвиговая волна проходит через ткань. Карты локальной скорости ткани получаются с помощью обычной техники отслеживания спеклов и предоставляют полный фильм о распространении сдвиговой волны через ткань. В SSI реализованы два основных нововведения. Во-первых, используя множество почти одновременных толчков, SSI создает источник сдвиговых волн, который перемещается через среду со сверхзвуковой скоростью. Во-вторых, сгенерированная сдвиговая волна визуализируется с помощью сверхбыстрой техники визуализации. Используя алгоритмы инверсии, сдвиговая эластичность среды отображается количественно из фильма о распространении волны. SSI — первая технология ультразвуковой визуализации, способная достигать более 10 000 кадров в секунду для глубоко расположенных органов. SSI предоставляет набор количественных и in vivo параметров, описывающих механические свойства тканей: модуль Юнга, вязкость, анизотропия.
Этот подход продемонстрировал клиническую пользу при визуализации молочной железы, щитовидной железы, печени, простаты и опорно-двигательного аппарата . SSI используется для обследования молочной железы с использованием ряда линейных датчиков высокого разрешения. [10] Крупное многоцентровое исследование визуализации молочной железы продемонстрировало как воспроизводимость [11] , так и значительное улучшение классификации [12] поражений молочной железы, когда изображения сдвиговой волновой эластографии добавляются к интерпретации стандартных ультразвуковых изображений в B-режиме и цветовом режиме.
Транзиентная эластография
В пищевой промышленности низкоинтенсивный ультразвук уже используется с 1980-х годов для получения информации о концентрации, структуре и физическом состоянии компонентов в таких продуктах питания, как овощи, мясо и молочные продукты, а также для контроля качества, [13] например, для оценки реологических свойств сыра. [14]

Транзиентная эластография изначально называлась импульсной эластографией с временным разрешением [15] , когда она была представлена в конце 1990-х годов. Метод основан на переходной механической вибрации, которая используется для индуцирования сдвиговой волны в ткани. Распространение сдвиговой волны отслеживается с помощью ультразвука для оценки скорости сдвиговой волны, из которой выводится модуль Юнга в соответствии с гипотезой однородности, изотропии и чистой эластичности (E=3ρV²). Важным преимуществом транзиентной эластографии по сравнению с методами гармонической эластографии является разделение сдвиговых волн и волн сжатия. [16] Метод может быть реализован в 1D [17] и 2D, что потребовало разработки сверхбыстрого ультразвукового сканера. [18]
Транзиентная эластография дает количественное одномерное (т. е. линейное) изображение жесткости «ткани». Он функционирует, вибрируя кожу с помощью двигателя, чтобы создать проходящее искажение в ткани ( волну сдвига ), и визуализируя движение этого искажения по мере того, как оно проходит глубже в тело, используя одномерный ультразвуковой луч. Затем он отображает количественную линию данных жесткости ткани ( модуль Юнга ). [19] [20] Этот метод используется в основном системой Fibroscan, которая используется для оценки печени, [21] например, для диагностики цирроза . [22] Специальная реализация одномерной транзиентной эластографии, называемая VCTE, была разработана для оценки средней жесткости печени, которая коррелирует с фиброзом печени, оцененным с помощью биопсии печени. [23] [24] Этот метод реализован в устройстве, которое также может оценивать контролируемый параметр затухания (CAP), который является хорошим суррогатным маркером стеатоза печени . [25]
Магнитно-резонансная эластография (МРЭ)

Магнитно-резонансная эластография (МРЭ) [26] была введена в середине 1990-х годов, и были исследованы многочисленные клинические применения. В МРЭ механический вибратор используется на поверхности тела пациента; это создает сдвиговые волны, которые перемещаются в более глубокие ткани пациента. Используется последовательность получения изображений, которая измеряет скорость волн, и это используется для определения жесткости ткани ( модуль сдвига ). [27] [28] Результатом сканирования МРЭ является количественная трехмерная карта жесткости ткани, а также обычное трехмерное изображение МРТ.
Одной из сильных сторон MRE является результирующая 3-D карта эластичности, которая может охватывать весь орган. [2] Поскольку МРТ не ограничена воздухом или костью, она может получить доступ к некоторым тканям, которые не может получить ультразвук, в частности, к мозгу. Она также имеет преимущество в том, что более однородна для всех операторов и менее зависима от навыков оператора, чем большинство методов ультразвуковой эластографии.
За последние несколько лет МР-эластография достигла значительных успехов, сократив время получения данных до минуты или меньше, и использовалась в различных медицинских приложениях, включая кардиологические исследования на живых человеческих сердцах. Короткое время получения данных МР-эластографии также делает ее конкурентоспособной по сравнению с другими методами эластографии.
Оптическая эластография
Оптическая эластография — это новая технология, которая использует оптическую микроскопию для получения изображений тканей. Наиболее распространенная форма оптической эластографии, оптическая когерентная эластография (OCE), основана на оптической когерентной томографии (OCT), которая сочетает интерферометрию с боковым сканированием луча для быстрого получения трехмерного изображения и достигает пространственного разрешения 5-15 мкм. [29] Для OCE механическая нагрузка прикладывается к ткани, а результирующая деформация измеряется с помощью отслеживания спеклов или фазочувствительного обнаружения. [30] Ранние реализации OCE включали применение квазистатического сжатия к ткани, [31] хотя в последнее время динамическая нагрузка достигалась путем применения синусоидальной модуляции через контактный преобразователь или акустическую волну. [29] Другие методы визуализации с большим оптическим разрешением также были введены для оптической эластографии для исследования микромасштаба между клетками и целыми тканями. [29] ОКТ использует более длинные волны, 850–1050 нм, и, следовательно, обеспечивает более низкое оптическое разрешение по сравнению с обычной световой микроскопией, которая использует видимые длины волн 400–700 нм и обеспечивает латеральное пространственное разрешение <1 мкм. Примеры анализа с более высоким разрешением включают использование конфокальной и световой микроскопии соответственно для механической характеристики многоклеточных сфероидов [32] и для структурного анализа трехмерных органоидов с разрешением одной клетки. [33] При использовании этих методов визуализации квазистатическое сжатие может быть вызвано в образце ткани с помощью микроиндентирующего устройства, такого как микропинцет. [32] Результирующая деформация может быть измерена по изображениям микроскопии с использованием алгоритмов отслеживания узлов на основе изображений, [32] [33] а механические свойства могут быть распознаны с помощью анализа методом конечных элементов (FEM).
Приложения
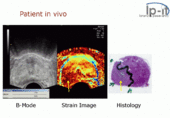
Эластография используется для исследования многих заболеваний во многих органах. Она может использоваться для получения дополнительной диагностической информации по сравнению с простым анатомическим изображением, а также может использоваться для направления биопсий или, все чаще, для их полной замены. Биопсии являются инвазивными и болезненными, несут риск кровотечения или инфекции, тогда как эластография полностью неинвазивна.
Эластография используется для исследования заболеваний печени. Жесткость печени обычно указывает на фиброз или стеатоз ( жировую болезнь печени ), которые, в свою очередь, указывают на многочисленные заболевания, включая цирроз и гепатит . Эластография особенно полезна в этом случае, поскольку, когда фиброз диффузный (распространяется скоплениями, а не сплошным рубцеванием), биопсия может легко пропустить образец пораженной ткани, что приводит к ложноотрицательному диагнозу.
Естественно, эластография находит применение для органов и заболеваний, где ручная пальпация уже была широко распространена. Эластография используется для обнаружения и диагностики рака груди , щитовидной железы и простаты . Некоторые типы эластографии также подходят для визуализации опорно-двигательного аппарата , и они могут определять механические свойства и состояние мышц и сухожилий .
Поскольку эластография не имеет тех же ограничений, что и ручная пальпация, она исследуется в некоторых областях, для которых нет истории диагностики с помощью ручной пальпации. Например, магнитно-резонансная эластография способна оценить жесткость мозга , [ 34] и появляется все больше научной литературы по эластографии здорового и больного мозга.
В 2015 году были опубликованы предварительные отчеты об эластографии, используемой на трансплантированных почках для оценки кортикального фиброза, которые показали многообещающие результаты. [35] В исследовании Бристольского университета «Дети 90-х» у 2,5% из 4000 человек, родившихся в 1991 и 1992 годах, с помощью ультразвукового сканирования в возрасте 18 лет была обнаружена неалкогольная жировая болезнь печени; пять лет спустя транзиторная эластография обнаружила более 20% жировых отложений на печени стеатоза, что указывает на неалкогольную жировую болезнь печени; половина из них была классифицирована как тяжелая. Сканирование также показало, что у 2,4% было рубцевание печени из-за фиброза , которое может привести к циррозу . [36]
Другие методы включают эластографию с оптической когерентной томографией [37] (т.е. световой).
Тактильное изображение включает в себя перевод результатов цифрового «прикосновения» в изображение. Многие физические принципы были исследованы для реализации тактильных датчиков : резистивные, индуктивные, емкостные, оптоэлектрические, магнитные, пьезоэлектрические и электроакустические принципы в различных конфигурациях. [38]
Примечания
- † ^ В случае визуализации эндогенного движения вместо возникновения возмущений наблюдаются возмущения, естественным образом создаваемые физиологическими процессами.
Ссылки
- ^ abcd Wells, PNT (июнь 2011 г.). «Медицинский ультразвук: визуализация деформации и эластичности мягких тканей». Журнал Королевского общества, Интерфейс . 8 (64): 1521– 1549. doi :10.1098/rsif.2011.0054. PMC 3177611. PMID 21680780 .
- ^ abc Сарвазян А., Холл Т.Дж., Урбан М.В., Фатеми М., Аглямов СР., Гарра Б.С. Обзор эластографии – развивающейся отрасли медицинской визуализации. Current Medical Imaging Reviews, 2011, 7(4):255-282.
- ^ ab Ophir, J.; Céspides, I.; Ponnekanti, H.; Li, X. (апрель 1991 г.). «Эластография: количественный метод визуализации эластичности биологических тканей». Ultrasonic Imaging . 13 (2): 111– 134. doi :10.1016/0161-7346(91)90079-W. PMID 1858217.
- ^ ab Parker, KJ; Doyley, MM; Rubens, DJ (февраль 2011 г.). «Визуализация упругих свойств ткани: перспектива 20 лет». Physics in Medicine and Biology . 56 (2): R1 – R29 . Bibcode :2012PMB....57.5359P. doi : 10.1088/0031-9155/57/16/5359 . PMID 21119234.
- ^ Найтингейл KR , Палмери ML, Найтингейл RW и Трейхи GE, О возможности дистанционной пальпации с использованием акустической радиационной силы. J. Acoust. Soc. Am. 2001; 110: 625-34
- ^ Рюгер, Хольгер; Психогиос, Георгиос; Йеринг, Моника; Зенк, Йоханнес (октябрь 2020 г.). «Мультимодальное ультразвуковое исследование, включающее количественную оценку виртуальной сенсорной визуализации для дифференциации шейных лимфатических узлов». Ультразвук в медицине и биологии . 46 (10): 2677– 2682. doi : 10.1016/j.ultrasmedbio.2020.06.005. PMID 32651021. S2CID 220484342.
- ^ Сарвазян А.П., Руденко О.В., Свонсон С.Д., Фоулкс Дж.Б., Емельянов С.Ю. Визуализация сдвиговой волны упругости: новая ультразвуковая технология медицинской диагностики. Ультразвуковая мед. биология. 1998; 24(9): 1419-35.
- ^ Сверхзвуковая сдвиговая визуализация: новый метод картирования эластичности мягких тканей. Bercoff J. et al., IEEE Transactions on Ultrasonics, Ferroelectrics, and Frequency Control, Vol. 51, No. 4, April 2004.
- ^ Акустоупругость в мягких твердых телах: Оценка нелинейного модуля сдвига с помощью акустической радиационной силы, J.-L. Gennisson,a M. Rénier, S. Catheline, C. Barrière, J. Bercoff, M. Tanter и M. Fink, J. Acoust. Soc. Am. 122 [1]6, декабрь 2007 г.
- ^ Мендельсон ЭБ, Чен Дж, Карстедт П. Оценка жесткости тканей может повысить специфичность визуализации молочной железы. Диагностическая визуализация. 2009;31(12):15-17.
- ^ Косгроув, Дэвид О.; Берг, Венди А.; Доре, Кэролайн Дж.; Скайба, Дэнни М.; Генри, Жан-Пьер; Гей, Джоэл; Коэн-Бакри, Клод; Исследовательская группа BE1 (2012). «Эластография сдвиговой волны для масс в груди имеет высокую воспроизводимость». Европейская радиология . 22 (5): 1023– 1032. doi :10.1007/s00330-011-2340-y. PMC 3321140. PMID 22210408 .
{{cite journal}}: CS1 maint: numeric names: authors list (link) - ^ Берг, Венди А.; Косгроув, Дэвид О.; Доре, Кэролайн Дж.; Шефер, Фриц К. В.; Свенссон, Уильям Э.; Хули, Регина Дж.; Олингер, Ральф; Мендельсон, Эллен Б.; Балу-Маэстро, Кэтрин; Локателли, Мартина; Турасс, Кристоф; Кавано, Барбара К.; Юхан, Валери; Ставрос, А. Томас; Тардивон, Энн (2012). «Эластография сдвиговой волны улучшает специфичность УЗИ молочной железы: многонациональное исследование BE1 939 новообразований». Радиология . 262 (2): 435– 449. doi :10.1148/radiol.11110640. PMID 22282182.
- ^ Povey, MJW; McClements, DJ (1988-01-01). "Ультразвук в пищевой инженерии. Часть I: Введение и экспериментальные методы". Журнал пищевой инженерии . 8 (4): 217– 245. doi :10.1016/0260-8774(88)90015-5. ISSN 0260-8774.
- ^ Ли, ХО; Луан, Х.; Даут, ДГ (1992). «Использование ультразвуковой техники для оценки реологических свойств сыра и теста». Журнал пищевой инженерии . 16 (1/2): 127– 150. doi :10.1016/s0260-8774(01)00073-5. ISSN 0260-8774.
- ^ Сандрин, Лоран; Кэтлин, Стефан; Тантер, Майкл; Хеннекин, Ксавье; Финк, Матиас (1999). «Импульсная эластография с временным разрешением и сверхбыстрой ультразвуковой визуализацией». Ultrasonic Imaging . 21 (4): 259– 272. doi :10.1177/016173469902100402. PMID 10801211. S2CID 40873227.
- ^ Catheline, Stefan; Wu, Francois; Fink, Mathias (1999). «Решение проблемы дифракционных смещений в соноупругости: метод акустического импульса». Журнал акустического общества Америки . 105 (5): 2941– 2950. Bibcode : 1999ASAJ..105.2941C. doi : 10.1121/1.426907. PMID 10335643.
- ^ Сандрин, Лоран; Тантер, Майкл; Дженниссон, Жан-Люк; Кателин, Стефан; Финк, Матиас (2002). «Измерение упругости сдвига для мягких тканей с помощью одномерной переходной эластографии». Труды IEEE по ультразвуку, сегнетоэлектрикам и управлению частотой . 49 (4): 436– 446. doi :10.1109/58.996561. PMID 11989699. S2CID 26431531.
- ^ Сандрин, Лоран; Тантер, Майкл; Кэтлин, Стефан; Финк, Матиас (2002). «Визуализация модуля сдвига с помощью 2D-транзиентной эластографии». Труды IEEE по ультразвуку, сегнетоэлектрикам и управлению частотой . 49 (4): 426– 435. doi :10.1109/58.996560. PMID 11989698. S2CID 24131440.
- ^ Catheline, Stefan; Wu, Francois; Fink, Mathias (1999). «Решение проблемы дифракционных смещений в соноупругости: метод акустического импульса». Журнал акустического общества Америки . 105 (5): 2941– 2950. Bibcode : 1999ASAJ..105.2941C. doi : 10.1109/58.996561. PMID 11989699. S2CID 26431531.
- ^ Сандрин, Лоран; Тантер, Микаэль; Генниссон, Жан-Люк; Кателин, Стефан; Финк, Матиас (апрель 2002 г.). «Зонд упругости сдвига для мягких тканей с одномерной переходной эластографией». Труды IEEE по ультразвуку, сегнетоэлектрикам и управлению частотой . 49 (4): 436– 446. doi :10.1109/58.996561. PMID 11989699. S2CID 26431531.
- ^ Ганн-Каррие Н.; Зиол М.; де Лединген В.; и др. (2006). «Точность измерения жесткости печени для диагностики цирроза у пациентов с хроническими заболеваниями печени». Гепатология . 44 (6): 1511– 7. doi : 10.1002/hep.21420 . PMID 17133503. S2CID 21900022.
- ^ Jung, Kyu Sik; Kim, Seung Up (2012). «Клиническое применение транзиентной эластографии». Клиническая и молекулярная гепатология . 18 (2): 163–73 . doi :10.3350/cmh.2012.18.2.163. PMC 3415879. PMID 22893866 .
- ^ Сандрин, Лоран; Фурке, Бертран; Аскеноф, Жан-Мишель; Йон, Сильвен; Фурнье, Селин; Мэл, Фредерик; Кристидис, Христос; Зиол, Марианна; Пуле, Брюно; Каземи, Фархад; Богранд, Мишель; Палау, Роберт (2003). «Транзиентная эластография: новый неинвазивный метод оценки фиброза печени». Ультразвук в медицине и биологии . 29 (12): 1705–1713 . doi :10.1016/j.ultrasmedbio.2003.07.001. ПМИД 14698338.
- ^ Ziol, Marianne; Handra-Luca, Adriana; Kettaneh, Adrien; Christidis, Christos; Mal, Frédéric; Kazemi, Farhad; de Ledinghen, Victor; Marcellin, Patrick; Dhumeaux, Daniel; Trinchet, Jean-Claude (2005). «Неинвазивная оценка фиброза печени по измерениям жесткости: перспективное многоцентровое исследование у пациентов с хроническим гепатитом C». Гепатология . 41 (1): 48–54 . doi : 10.1002/hep.20506 . PMID 15690481. S2CID 23294239.
- ^ Сассо, Магали; Богран, Мишель; де Лединген, Виктор; Дувен, Катрин; Марселлин, Патрик; Пупон, Рауль; Сандрин, Лоран; Миетт, Вероник (2010). «Контролируемый параметр затухания (CAP): новое ультразвуковое измерение затухания под управлением VCTE для оценки стеатоза печени: предварительное исследование и проверка на группе пациентов с хроническим заболеванием печени по разным причинам». Ультразвук в медицине и биологии . 36 (11): 1825– 1835. doi :10.1016/j.ultrasmedbio.2010.07.005. PMID 20870345.
- ^ Сарвазян, AP; Сковорода, AR; Емельянов, SY; Фоулкс, JB; Пайп, JG; Адлер, RS; Бакстон, RB; Карсон, PL (1995). "Биофизические основы визуализации упругости". Акустическая визуализация . Т. 21. С. 223– 240. doi :10.1007/978-1-4615-1943-0_23. ISBN 978-1-4613-5797-1.
- ^ Muthupillai R, Lomas DJ, Rossman PJ, et al. Магнитно-резонансная эластография с прямой визуализацией распространяющихся акустических волн деформации. Science 1995; 269: 1854-7.[49, 219, 220].
- ^ Manduca A, Oliphant TE, Dresner MA и др. Магнитно-резонансная эластография: неинвазивное картирование эластичности тканей. Med Image Anal 2001; 5: 237-54.
- ^ abc Kennedy, Brendan F.; Wijesinghe, Philip; Sampson, David D. (апрель 2017 г.). «Возникновение оптической эластографии в биомедицине». Nature Photonics . 11 (4): 215– 221. Bibcode : 2017NaPho..11..215K. doi : 10.1038/nphoton.2017.6. hdl : 10023/28354 . ISSN 1749-4893.
- ^ Кеннеди, Брендан Ф.; Кеннеди, Келси М.; Сэмпсон, Дэвид Д. (март 2014 г.). «Обзор оптической когерентной эластографии: основы, методы и перспективы». Журнал IEEE Selected Topics in Quantum Electronics . 20 (2): 272– 288. Bibcode : 2014IJSTQ..20..272K. doi : 10.1109/JSTQE.2013.2291445. ISSN 1077-260X.
- ^ Шмитт, Джозеф М. (1998). «ОКТ-эластография: визуализация микроскопической деформации и напряжения ткани». Optics Express . 3 (6): 199– 211. Bibcode : 1998OExpr...3..199S. doi : 10.1364/oe.3.000199. PMID 19384362. Получено 28.08.2024 .
- ^ abc Jaiswal, Devina; Moscato, Zoe; Tomizawa, Yuji; Claffey, Kevin P.; Hoshino, Kazunori (2019). «Эластография многоклеточных сфероидов с использованием 3D световой микроскопии». Biomedical Optics Express . 10 (5): 2409– 2418. doi :10.1364/boe.10.002409 . PMC 6524572. PMID 31143496. Получено 28.08.2024 .
- ^ ab Томизава, Юджи; Вали, Хадиджа Х.; Сурти, Манав; Сухаил, Ясир; Кшитиз; Хошино, Казунори (2024-05-07). «Микроскопия Lightsheet объединяет оптическую вискоэластографию отдельных клеток и флуоресцентную цитометрию трехмерных живых тканей». bioRxiv 10.1101/2024.04.20.590392 .
- ^ "Магнитно-резонансная эластография - обзор | Темы ScienceDirect". www.sciencedirect.com . Получено 2024-01-07 .
- ^ Содержание изначально скопировано из: Hansen, Kristoffer; Nielsen, Michael; Ewertsen, Caroline (2015). "Ultrasonography of the Kidney: A Pictorial Review". Diagnostics . 6 (1): 2. doi : 10.3390/diagnostics6010002 . ISSN 2075-4418. PMC 4808817. PMID 26838799 . (CC-BY 4.0)
- ^ Сара Босли (12 апреля 2019 г.). «Эксперты предупреждают об «эпидемии» жировой болезни печени среди молодых людей». The Guardian .
- ^ Кеннеди Б.Ф., Кеннеди К.М., Сэмпсон Д.Д. [1] Обзор оптической когерентной эластографии: основы, методы и перспективы. Журнал IEEE по избранным темам квантовой электроники 2014; 20(2):7101217.
- ^ Тегин, Дж.; Викандер, Дж. (2005). «Тактильное зондирование в интеллектуальных роботизированных манипуляциях – обзор». Industrial Robot . 32 (1): 64–70 . doi :10.1108/01439910510573318. S2CID 17274884.


