Перекись диэтилового эфира
 | |
 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) |
|
| ChemSpider | |
CID PubChem |
|
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С4Н10О3 | |
| Молярная масса | 106,121 г·моль −1 |
| Появление | бесцветная жидкость |
| Плотность | 1,005 г/см 3 |
| Точка кипения | 62–64 °C (144–147 °F; 335–337 K) при 18,7 гПа (пониженное давление) |
| Опасности | |
| Охрана труда и техника безопасности (OHS/OSH): | |
Основные опасности | Взрывоопасный |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
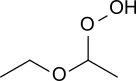
Гидропероксид диэтилового эфира — органическое соединение с формулой C2H5OCH ( OOH)CH3 . Это бесцветная жидкость. Гидропероксид диэтилового эфира и продукты его конденсации ответственны за взрывоопасные органические пероксиды , которые медленно образуются при воздействии на диэтиловый эфир окружающего воздуха и температурных условий. [ 1] [2]
Синтез и реакции
Гидропероксид диэтилового эфира может быть образован фотоокислением диэтилового эфира. Это радикальный процесс, вызванный УФ-возбуждением молекулярного кислорода в более реактивную форму. Его образование обычно нежелательно из-за связанного с этим риска взрыва. По этой причине коммерческие образцы диэтилового эфира обычно содержат антиоксиданты, такие как BHT , и содержатся в материале, способном блокировать УФ-лучи, таком как янтарное стекло.
Его можно намеренно получить с высоким выходом путем кислотно-катализируемого присоединения перекиси водорода к этилвиниловому эфиру : [1]
- C 2 H 5 OCH=CH 2 + H 2 O 2 → C 2 H 5 OCH(OOH)CH 3
Аналогичным образом можно получить родственные гидропероксиды.
Гидропероксид диэтилового эфира при нагревании в воде разлагается до ацетальдегида :
- C 2 H 5 OCH(OOH)CH 3 → CH 3 CHO + C 2 H 5 OH + H 2 O 2
Гидропероксид диэтилового эфира образует полимеры, известные как пероксид диэтилового эфира или пероксид этилидена :
Перекись водорода представляет собой бесцветное масло, которое является чрезвычайно бризантным и чувствительным к трению взрывчатым веществом , однако полимерные материалы являются твердыми, что делает их более опасными, поскольку испарение летучего диэтилового эфира может оставлять тонкие пленки чистого взрывчатого вещества.
Тесты
Пероксиды диэтилового эфира можно обнаружить с помощью раствора йодида калия (KI) в уксусной кислоте или йодида калия / крахмальной бумаги. Положительный тест приводит к образованию йода (I2 ) , который вызывает желтый или коричневый цвет эфирной фазы или темно-синеватое пятно на бумажной полоске. [3]
Ссылки
- ^ ab Milas, Nicholas A.; Peeler, Robert L.; Mageli, Orville L. (1954). «Органические пероксиды. XIX. α-Гидропероксиэфиры и родственные пероксиды». Журнал Американского химического общества . 76 (9): 2322–2325. doi :10.1021/ja01638a012.
- ^ А. Рич, Р. Мейстер (1936). «Modellversuche zur Autoxidation der Äther». Angewandte Chemie (на немецком языке). 49 (5): 101–103. Бибкод : 1936AngCh..49..101R. дои : 10.1002/ange.19360490502.
- ^ "Peroxide Forming Solvents". Sigma-Aldrich . Получено 2014-07-09 .





