Тетрафторид дибора
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Тетрафторид дибора | |||
| Систематическое название ИЮПАК Тетрафтордиборан(4) | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) |
| ||
| ChemSpider |
| ||
CID PubChem |
| ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| Б 2 Ф 4 | |||
| Молярная масса | 97,61 г·моль −1 | ||
| Появление | Бесцветный газ. | ||
| Плотность | 4,3 кг/м 3 (газ) | ||
| Температура плавления | −56 °C (−69 °F; 217 K) | ||
| Точка кипения | −34 °C (−29 °F; 239 K) | ||
| Термохимия | |||
Теплоемкость ( С ) | 79,1 Дж/моль К | ||
Стандартная молярная энтропия ( S ⦵ 298 ) | 317,3 Дж/моль К | ||
Стандартная энтальпия образования (Δ f H ⦵ 298 ) | -1440,1 кДж/моль | ||
Свободная энергия Гиббса (Δ f G ⦵ ) | -1410,4 кДж/моль | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Тетрафторид дибора — неорганическое соединение с формулой (BF 2 ) 2 . Бесцветный газ, период полураспада соединения составляет несколько дней при комнатной температуре. Это наиболее стабильный из тетрагалогенидов дибора, [1] и не разлагается заметно при стандартных условиях . [2]
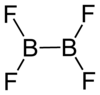
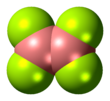
Структура и связь
Тетрафторид дибора — плоская молекула с расстоянием связи BB 172 пм. [1] Хотя он является электронодефицитным, ненасыщенные центры бора стабилизированы пи-связями с терминальными фторидными лигандами. Соединение изоэлектронно с оксалатом .
Синтез и реакции
Тетрафторид дибора может быть образован путем обработки монофторида бора трифторидом бора при низких температурах, при этом необходимо следить за тем, чтобы не образовывались более высокие полимеры. [3] В качестве альтернативы тетрахлорид дибора может быть фторирован трифторидом сурьмы . [2]
Добавление тетрафторида дибора к комплексу Васки было использовано для получения раннего примера комплекса борила переходного металла : [4]
- 2 B 2 F 4 + IrCl(CO)(PPh 3 ) 2 → Ir(BF 2 ) 3 (CO)(PPh 3 ) 2 + ClBF 2
Историческая литература
- Луи Трефонас и Уильям Н. Липскомб (1958). «Кристаллическая и молекулярная структура тетрафторида дибора, B2F4». J. Chem. Phys . 28 (1): 54– 55. Bibcode :1958JChPh..28...54T. doi : 10.1063/1.1744079 .
- Гейлс, Дж. Н.; Селф, Дж. (1964). «Инфракрасный спектр тетрафторида дибора в газообразном и твердом состояниях». Журнал химической физики . 40 (12): 3530–3539 . Bibcode : 1964JChPh..40.3530G. doi : 10.1063/1.1725048.
- AK Holliday; FB Taylor (1964). «Тетрафторид дибора. Часть II. Реакции с некоторыми оксидами и металлоорганическими соединениями». J. Chem. Soc. : 2731– 2734. doi :10.1039/JR9640002731.
- Вернон Х. Дибелер; Сьюзен К. Листон (1968). «Масс-спектрометрическое исследование фотоионизации. XII. Трифторид бора и тетрафторид дибора». J. Chem. Soc . 7 (9): 1742– 1746. doi :10.1021/ic50067a010.
Ссылки
- ^ ab Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ ab Артур Финч и Герман Ирвинг Шлезингер (1958). «Тетрафторид дибора». J. Am. Chem. Soc . 80 (14): 3573– 3574. doi :10.1021/ja01547a020.
- ^ Тиммс, П. Л. (1972). "Низкотемпературная конденсация высокотемпературных видов как синтетический метод" . Достижения в неорганической химии и радиохимии . Academic Press: 143. doi :10.1016/S0065-2792(08)60006-0. ISBN 0-12-023614-1.
- ^ Neeve, Emily C.; Geier, Stephen J.; Mkhalid, Ibraheem AI; Westcott, Stephen A.; Marder, Todd B. (2016). «Соединения диборона (4): от структурного любопытства до синтетической рабочей лошадки». Chemical Reviews . 116 (16): 9091–9161 . doi : 10.1021/acs.chemrev.6b00193 . hdl : 1807/78811 . PMID 27434758.
Внешние ссылки
- Тетрафторид дибора в webelements