Дескриптор (химия)
В химической номенклатуре дескриптор — это нотационный префикс, помещаемый перед систематическим названием вещества , который описывает конфигурацию или стереохимию молекулы . [1] Некоторые из перечисленных дескрипторов не следует использовать в публикациях , поскольку они больше не соответствуют рекомендациям ИЮПАК . Стереодескрипторы часто используются в сочетании с локантами для четкой и однозначной идентификации химической структуры .
Дескрипторы, обычно размещаемые в начале систематического названия, при алфавитной сортировке не учитываются.
Конфигурационные дескрипторы
цис,транс
См.: цис–транс-изомерия


Дескрипторы цис (лат. cis, по эту сторону ) [2] и транс (лат. trans, по ту сторону ) [3] используются в различных контекстах для описания химических конфигураций: [4] [5]
В органической структурной химии конфигурация двойной связи может быть описана с помощью цис и транс , в случае, если она имеет простую схему замещения только с двумя остатками. Положение двух остатков относительно друг друга в разных точках кольцевой системы или более крупной молекулы также может быть описано с помощью цис и транс, если конфигурация структуры жесткая и не допускает простой инверсии.
В химии неорганических комплексов дескрипторы цис и транс используются для характеристики позиционных изомеров в октаэдрических комплексах с конфигурацией A 2 B 4 X или квадратных плоских комплексах с конфигурацией A 2 B 2 X.
- Октаэдрический комплекс с цис- конфигурацией
- Октаэдрический комплекс с трансконфигурацией
- Квадратно-плоский комплекс: цисплатин
Типографское представление цис- и транс-элементов осуществляется курсивом и строчными буквами.
Цис / транс номенклатура не является однозначной для более высокозамещенных двойных связей и в настоящее время в значительной степени заменена номенклатурой ( E ) /( Z ). [6]
(Э), (З)
См.: обозначение E - Z
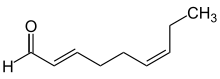
Дескрипторы ( E ) (от немецкого entgegen , «напротив») и ( Z ) (от немецкого zusammen , «вместе») используются для предоставления отдельного описания модели замещения для алкенов , кумуленов или других систем с двойной связью, таких как оксимы . [7]
Для атрибуции ( E ) или ( Z ) основано на относительном положении двух заместителей наивысшего приоритета, находящихся по обе стороны двойной связи, в то время как приоритет основан на номенклатуре CIP. Номенклатура ( E )/( Z ) может быть применена к любым системам двойных связей (включая гетероатомы ), но не к замещенным кольцевым системам . Дескрипторы ( E ) и ( Z ) всегда пишутся с заглавной буквы, набираются курсивом и заключаются в скобки, которые устанавливаются как обычные, как дополнительные локанты или запятые.
о-,м-,п-
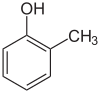 |  |  |
| о -Крезол | м -Крезол | п -Крезол |
Сокращение o - (сокращение от орто , от греч. orthós — вертикальный, прямой), [8] m - ( мета , от греч. (приблизительно) — между) [9] и p - ( пара , от греч. pará — примыкающий, сбоку) [10] описывают три возможных позиционных изомера двух заместителей в бензольном кольце . Обычно это два независимых одиночных заместителя, но в случае конденсированных кольцевых систем также упоминается орто -конденсация, если только в названии не рассматривается схема замещения, как в [2.2]парациклофане . В текущей систематической номенклатуре o -, m - и p - часто заменяются с использованием локантов ( 1,2-диметилбензол вместо о -ксилола).
о- , м- и п- (пишется орто- , мета- и пара- ) пишутся строчными буквами и курсивом.
экзо,эндо
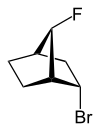 | 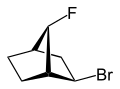 |
| 2- эндо -бром-7 -син -фтор- бицикло[2.2.1]гептан | 2- экзо -бром-7- син -фтор- бицикло[2.2.1]гептан |
 |  |
| 2- эндо -бром-7- анти -фтор- бицикло[2.2.1]гептан | 2- экзо -бром-7- анти -фтор- бицикло[2.2.1]гептан |
exo (от греч. = снаружи) [11] или endo (от греч. endon = внутри) [12] обозначает относительную конфигурацию мостиковых бициклических соединений. Положение заместителя в главном кольце относительно самого короткого мостика имеет решающее значение для назначения экзо или эндо (согласно ИЮПАК: мост с наивысшими локантными цифрами [13] в мостиковой кольцевой системе). Заместитель, который должен быть классифицирован, приписывается дескриптором экзо , если он обращен к мостику. Он имеет эндо- конфигурацию, если он обращен от мостика. Если два разных заместителя расположены на одном и том же атоме С, назначение экзо / эндо основывается на заместителе с более высоким приоритетом в соответствии с правилами CIP.
син,анти
Если мостиковая бициклическая система несет заместитель в самом коротком мостике, экзо- или эндо -дескриптор не может быть использован для его назначения. Такие изомеры классифицируются с помощью син- / анти -обозначения. [13] Если заместитель, который должен быть назначен, указывает на кольцо с наибольшим числом сегментов, он имеет син- конфигурацию (от греч. syn = вместе). [14] В противном случае ему присваивается анти- дескриптор (греч. anti = против). [15] Если оба кольца обладают равным числом сегментов, выбирается кольцо с наиболее значимым заместителем в соответствии с правилами CIP.

Использование син и анти для обозначения конфигурации двойных связей в настоящее время устарело, особенно в случае альдоксимов и гидразонов, полученных из альдегидов . Здесь соединения были обозначены как син -конфигурированные, когда альдегид H и O (оксима) или N (гидразона) были выровнены в цис -положении. Эти соединения теперь описываются номенклатурой ( E )/( Z ). Альдоксимы и гидразоны, классифицированные как син , поэтому теперь описываются как ( E )-конфигурированные. [14]
Когда речь идет о диастереомерах, син и анти используются для описания групп на тех же или противоположных участках в зигзагообразной проекции, см. Диастереомер#Син / анти
Син и анти всегда пишутся строчными буквами и курсивом, локанты (если используются) ставятся перед словом и разделяются дефисами.
фейс,мер
Термины fac (от лат. facies , «внешняя грань») [16] и mer (от «меридиональный») [17] могут указывать на расположение трех идентичных лигандов вокруг центрального атома в октаэдрических комплексах. Сегодня эта номенклатура считается устаревшей, но все еще допустима. [18] [19] Префикс fac описывает ситуацию, когда три идентичных лиганда занимают три вершины треугольной поверхности октаэдра. В конфигурации mer три лиганда охватывают плоскость , в которой расположен центральный атом.
- фэк -[CoCl 3 (NH 3 ) 3 ]
- мер -[CoCl 3 (NH 3 ) 3 ]
Перед именем комплекса ставятся префиксы fac и mer , набранные строчными буквами курсивом.
н,изо,нео, цикло
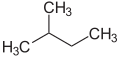
Префиксы n (нормальный), iso (от греч. ísos = равный), [20] neo (греч. néos = молодой, новый) [21] и cyclo (греч. kyklos = круг) [22] в основном используются для описания расположения атомов, обычно атомов углерода в углеродном скелете. n , iso и neo больше не используются в систематической номенклатуре, но по-прежнему часто встречаются в тривиальных названиях и в лабораторном жаргоне.
Префикс n описывает углеродный скелет с прямой цепью без разветвлений, тогда как iso описывает разветвленный скелет, без указания каких-либо дополнительных деталей. В более общем смысле iso — это соединение, которое изомерно соединению n (соединение, в котором отдельные атомы или атомные группы перегруппированы)
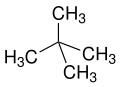
neo — неспецифический термин для «новых», обычно синтетически полученных веществ или изомеров давно известных n соединений или природных веществ (например, неоментол, полученный из ментола , или неоабиетиновая кислота из абиетиновой кислоты ). Согласно ИЮПАК, neo рекомендуется только в неопентане или неопентиловом остатке. [23] [24]
cyclo — часто используемый префикс для всех циклических и гетероциклических соединений. Во многих собственных названиях химических веществ cyclo используется не как префикс, а как непосредственная часть названия, например, в циклогексане или циклооктатетраене.
В то время как n , iso и neo пишутся строчными и курсивными буквами, для cyclo это имеет место только в неорганических соединениях. [25] В органических соединениях «cyclo» часто используется как компонент имени, не разделяется дефисом и также учитывается при алфавитной сортировке.
сек-,трет-
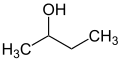
Префиксы sec и tert используются для указания окружения заместителя в молекуле. Таким образом, описывается не точное положение заместителя, а только схема замещения соседнего атома (обычно атома углерода). В n- бутаноле группа OH присоединена к первичному атому углерода, во sec -бутаноле — к вторичному атому углерода, а в tert -бутаноле — к третичному атому углерода.
Термины sec и tert считаются устаревшими и должны использоваться только для незамещенных групп sec-butoxy, sec-butyl [26] [27] или tert-butyl. [28] [27] Существуют различные варианты написания, такие как «sec-butyl», «s-butyl», «sBu» или «bus», которые также считаются устаревшими. [29] [30]
спиро

Префикс «спиро», за которым следует дескриптор Фон-Байера, описывает в номенклатуре органических соединений кольцевые системы, связанные только одним общим атомом — спироатомом. Если в молекуле присутствует несколько спироатомов, префикс «спиро» снабжается префиксом («диспиро», «триспиро» и т. д.), соответствующим числу спироатомов. Обычно «спиро» устанавливается как обычно. [31]
катена
Термин катена (лат. «цепь») используется в неорганической номенклатуре [32] для описания линейных, цепочевидных полимеров из идентичных многоатомных единиц. [33] Одним из примеров являются катенатрифосфазены. [34] [35] Родственными соединениями в органической химии являются катенаны .
сн
Обозначение sn означает стереоспецифическую нумерацию и указывает на особый способ нумерации атомов углерода в молекуле на основе глицерина.
Стереодескрипторы абсолютных конфигураций
(Р), (С)
См.: Правила приоритета Кана–Ингольда–Прелога

Стереохимические дескрипторы ( R ) (от лат. rectus = правый) и ( S ) (от лат. sinister = левый) [36] используются для описания абсолютной конфигурации стереоцентра (обычно хирального атома углерода). [37] Для этой цели все заместители в стереоцентре имеют приоритет в соответствии с правилами CIP, и заместитель с самым низким приоритетом («D») направлен назад (от направления взгляда). Стереоцентр имеет конфигурацию ( S ), если остальные заместители описывают круг, убывающий по приоритету («A» → «B» → «C») влево. Конфигурация ( R ) присваивается стереоцентру, если направление вращения направлено вправо.
Если одна молекула содержит несколько стереоцентров, локант должен быть помещен перед дескриптором (например, в (1 R , 2 S )-2-амино-1-фенилпропан-1-ол, систематическое обозначение норэфедрина ). Если все стереоцентры сконфигурированы одинаково, наименование локантов может быть опущено в пользу написания «все- R » или «(все- S )».
В типографике ( R ) и ( S ) пишутся заглавными буквами и курсивом; часто предшествующие им пробелы, окружающие круглые скобки и запятые, напротив, пишутся как обычно.
(г), (с)
Дескрипторы ( r ) и ( s ) используются для описания абсолютной конфигурации псевдоасимметричных центров. [38] Псевдоасимметрия возникает, когда к одному атому углерода присоединены четыре различных заместителя, два из которых отличаются только своей абсолютной стереохимической конфигурацией. Примерами таких соединений являются мезосоединения , такие как тропановые алкалоиды; исходное соединение — тропин , систематическое название которого (1 R , 3 r , 5 S )-8-метил-8-азабицикло[3.2.1]октан-3-ол. В этой структуре атом C3 — углерод, к которому присоединена гидроксильная группа — является псевдоасимметричным; поэтому стереохимический дескриптор в систематическом названии пишется строчными курсивными буквами, а не заглавными курсивными буквами, как для обычных хиральных атомов.
Д-,Л-
См.: Проекция Фишера
- Построение проекции Фишера
- D - глюкоза в проекции Фишера.
Красный: Группа с наивысшим приоритетом,
Синий: Для определения D -/ L - релевантной группы,
Фиолетовый: Группа с ахиральным атомом углерода
Стереоскрипторы D - (от лат. dexter, правый) и L - (от лат. laevus, левый) используются для описания конфигурации α-аминокислот и сахаров. [39] Во-первых, трехмерная молекула должна быть преобразована в определенную нотацию как двумерное изображение («проекция Фишера»). [40] Для этого атом C с наивысшим приоритетом в соответствии с обычными правилами номенклатуры располагается сверху, а дальнейшая углеродная цепь располагается вертикально под ним. Хиральный атом C, наиболее удаленный от группы с наивысшим приоритетом, используется для назначения D - или L -. Если остаток, расположенный на этом атоме углерода (обычно группа ОН), указывает влево, молекула происходит из L -ряда. Если остаток указывает вправо, используется дескриптор D -. [41]
Дескрипторы D - и L - пишутся маленькими заглавными буквами и отделяются дефисом от остальной части имени. [42]
г-,л-
Иногда упомянутые выше стереодескрипторы с заглавными буквами D и L ошибочно путают с устаревшими курсивными стереодескрипторами d и l , которые эквивалентны правовращающему и левовращающему оптическому вращению , т. е. (+)- и (−)- стереодескрипторам соответственно.
Ссылки
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «stereodescriptor». doi :10.1351/goldbook.S05976
- ^ "RÖMPP - цис- - Georg Thieme Verlag KG". roempp.thieme.de . Получено 28.12.2016 .
- ^ "транс-". 2016-02-12.
- ^ Руководства ИЮПАК E-2, E-3 (PDF; 542 кБ).
- ^ Рекомендации ИЮПАК R-7.1.1.
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «цис, транс». doi :10.1351/goldbook.C01092
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «E, Z». doi :10.1351/goldbook.E01882
- ^ "Орто-". 2012-09-14.
- ^ "Встречен(а)..." 2012-09-14.
- ^ "Para-". 2016-02-12.
- ^ "exo-". 2016-02-12.
- ^ "эндо-". 2016-02-12.
- ^ ab IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «endo, exo, syn, anti». doi :10.1351/goldbook.E02094
- ^ ab "syn-". 2016-02-12.
- ^ "Анти-". 2016-02-12.
- ^ "fac-". 2016-02-12.
- ^ "Мэр". 2016-02-12.
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «fac-». doi :10.1351/goldbook.F02313
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «mer-». doi :10.1351/goldbook.M03828
- ^ "Iso..." 2016-02-12.
- ^ «Нео...» 2016-02-12.
- ^ "Велосипед..." 2016-02-12.
- ^ Рекомендации ИЮПАК A-2.1, A-2.25.
- ^ IUPAC-Regel R-9.1, Таблица 19b Архивировано 08.02.2014 на Wayback Machine .
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «cyclo-». doi :10.1351/goldbook.C01495
- ^ Руководства ИЮПАК A-2.25, C-205.1, R-5.5.1.1.
- ^ ab ИЮПАК-Регель R-9.1, Таблица 26b.
- ^ IUPAC-Regel A-2.25.
- ^ "sec-". 2016-02-12.
- ^ "трет-Бутил..." 2016-02-12.
- ^ ИЮПАК: Nomenklatur von Spiro-Verbindungen, получено 23 мая 2016 г.
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «catena-». doi :10.1351/goldbook.C00903
- ^ "catena-". 2016-02-12.
- ^ S. Gorter и GC Verschoor: Кристаллическая структура катена-три-µ 2 -(1,12-додекандинитрил)меди(II)гексахлороантимоната(V) Cu(C 12 H 20 N 2 ) 3 (SbCl 6 ) 2 . В: Acta Crystallogr. (1976). B32, 1704-1707, doi :10.1107/S0567740876006262.
- ^ Руководства ИЮПАК D-4.4, I-9.7.3 и I-10.8.3.5.
- ^ "CIP-Regeln". 2016-02-12.
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «R,S». doi :10.1351/goldbook.R05423
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «псевдоасимметричный атом углерода». doi :10.1351/goldbook.P04921
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «d, l, dl». doi :10.1351/goldbook.D01512
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. (The "Gold Book") (1997). Онлайн-исправленная версия: (2006–) "Fischer–Rosanoff convention (or Rosanoff convention)". doi :10.1351/goldbook.F02392
- ^ "d". 2016-02-12.
- ^ IUPAC Chemical Nomenclature and Structure Representation Division (2013). "P-102.3.2". В Favre, Henri A.; Powell, Warren H. (ред.). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. IUPAC – RSC . ISBN 978-0-85404-182-4.



![fac-[CoCl3(NH3)3]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/69/Fac-trichlorotriamminecobalt%28III%29.png/109px-Fac-trichlorotriamminecobalt%28III%29.png)
![мер-[CoCl3(NH3)3]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/54/Mer-trichlorotriamminecobalt%28III%29.png/120px-Mer-trichlorotriamminecobalt%28III%29.png)