Циклогептатриен
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Циклогепта-1,3,5-триен [1] | |||
| Другие имена 1,3,5-Циклогептатриен 1 H -[7]Аннулен CHT Тропилиден | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 506066 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| Информационная карта ECHA | 100.008.061 | ||
| Номер ЕС |
| ||
| 1943 | |||
CID PubChem |
| ||
| УНИИ | |||
| Номер ООН | 2603 | ||
Панель инструментов CompTox ( EPA ) |
| ||
| |||
| |||
| Характеристики | |||
| С 7 Н 8 | |||
| Молярная масса | 92,141 г·моль −1 | ||
| Появление | Бесцветная жидкость. | ||
| Плотность | 0,888 г/мл при 25 °C | ||
| Температура плавления | −80 °C (−112 °F; 193 К) | ||
| Точка кипения | 116 °C (241 °F; 389 К) | ||
| Нерастворим в воде | |||
| Кислотность ( pK a ) | 36 | ||
| Опасности | |||
| Маркировка СГС : | |||
    | |||
| Опасность | |||
| Н225 , Н301 , Н304 , Н311 , Н315 , Н319 , Н335 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P270 , P271 , P280 , P301+P310 , P302+P352 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P312 , P321 , P322 , P330 , P331 , P332+P313 , P337+P313 , P361 , P362 , P363 , P370+P378 , P403+P233 , P403+P235 , P405 , П501 | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
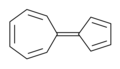
Циклогептатриен ( CHT ) — органическое соединение с формулой C7H8 . Это замкнутое кольцо из семи атомов углерода, соединенных тремя двойными связями (как следует из названия) и четырьмя одинарными связями. Эта бесцветная жидкость вызывает повторяющийся теоретический интерес в органической химии . Это лиганд в металлоорганической химии и строительный блок в органическом синтезе . Циклогептатриен не является ароматическим , о чем свидетельствует непланарность метиленового мостика (-CH2- ) по отношению к другим атомам; однако родственный катион тропилия является.
Синтез
Альберт Ладенбург впервые получил циклогептатриен в 1881 году путем разложения тропина . [2] [3] Структура была окончательно доказана синтезом Рихарда Вильштеттера в 1901 году. Этот синтез начался с циклогептанона и установил семичленную кольцевую структуру соединения. [4]
Циклогептатриен может быть получен в лаборатории путем фотохимической реакции бензола с диазометаном или пиролиза аддукта циклогексена и дихлоркарбена . [5] Связанный классический синтез для производных циклогептатриена, расширение кольца Бюхнера , начинается с реакции бензола с этилдиазоацетатом , чтобы получить соответствующий этиловый эфир норкарадиена, который затем подвергается термически разрешенному электроциклическому расширению кольца , чтобы получить этиловый эфир 1,3,5-циклогептатриена 7-карбоновой кислоты. [6] [7]

- Отдельные производные циклогептатриена
- Гептален – состоит из двух конденсированных циклогептатриеновых колец.
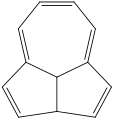
- Азулен – состоит из конденсированных циклопентадиеновых и циклогептатриеновых колец.
- Сесквифульвален – состоит из связанных циклопентадиеновых и циклогептатриеновых колец.
- Элассовален – состоит из одного циклогептатриена и двух конденсированных циклопентеновых колец.
- Тропон – состоит из циклогептатриенового кольца и карбонильной группы .
- Хинокитиол – состоит из циклогептатриенового кольца, изопропиловой , карбонильной и гидроксигрупп ( изопропилциклогептатриенолон ).
Реакции
Удаление гидрид- иона из метиленового мостика дает плоский и ароматический катион циклогептатриена, также называемый тропилиевым ионом. Практический путь к этому катиону использует PCl 5 в качестве окислителя. [8] CHT ведет себя как диен в реакциях Дильса-Альдера , например, с малеиновым ангидридом : [9]
Известно много металлических комплексов циклогептатриена , включая Cr(CO) 3 ( C7H8 ) [10] и циклогептатриенмолибдентрикарбонил . [ 11]

Циклооктатетраен и циклогептатриен используются в качестве триплетного гасителя для лазеров на красителе родамин 6G . [12] [13]
Смотрите также
Ссылки
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 223. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ А. Ладенбург (1883). «Конституция атропинов». «Анналы химии» Юстуса Либиха . 217 (1): 74–149 . doi :10.1002/jlac.18832170107.
- ^ А. Ладенбург (1881). «Цветок Тропинов». Berichte der Deutschen Chemischen Gesellschaft . 14 (2): 2126–2131 . doi :10.1002/cber.188101402127.
- ^ Ричард Вильштеттер (1901). «Synthesen in der Tropingruppe. I. Synthese des Tropilidens». «Анналы химии» Юстуса Либиха . 317 (2): 204–265 . doi :10.1002/jlac.19013170206.
- ^ HE Winberg (1959). «Синтез циклогептатриена». Журнал органической химии . 24 (2): 264– 265. doi :10.1021/jo01084a635.
- ^ Бухнер и др., Бер., 18, 2377 ( 1885 );
- ↑ Для вариации: Irvin Smith Lee; Tawney Pliny O (1934). «Исследования полиметилбензолов. IX. Добавление этилдиазоацетата к дурену». J. Am. Chem. Soc. 56 (10): 2167– 2169. doi :10.1021/ja01325a054.
- ^ Conrow, K. (1973). "Tropylium Fluoroborate". Organic Syntheses, Collected Volume . 5 : 1138. doi :10.15227/orgsyn.043.0101.
- ^ Ишитоби, Хироюки; Танида, Хироси; Тори, Казуо; Цудзи, Терудзи (1971). «Повторное рассмотрение циклоприсоединения циклогептатриена с малеиновым ангидридом». Бюллетень химического общества Японии . 44 (11): 2993– 3000. doi : 10.1246/bcsj.44.2993 .
- ^ Джеймс Х. Ригби, Кевин Р. Фейлз (2004). "7α-АЦЕТОКСИ-(1Hβ, 6Hβ)-БИЦИКЛО[4.4.1]УНДЕКА-2,4,8-ТРИЕН ЧЕРЕЗ ОПОЗДАННУЮ ХРОМОМ ВЫСШУЮ ЦИКЛОПРИСОЕДИНЕНИЮ". Органические синтезы; Собрание томов , т. 10, стр. 1.
- ^ Грин, Малкольм Л. Х.; Нг, Деннис КП (1995). «Циклогептатриеновые и -енильные комплексы ранних переходных металлов». Chemical Reviews . 95 (2): 439– 473. doi :10.1021/cr00034a006.
- ^ Томи Нат Дас; К. Индира Приядарсини (1994). «Триплет циклооктатетраена: реакционная способность и свойства». Журнал химического общества, Faraday Transactions . 90 (7): 963– 968. doi :10.1039/ft9949000963.
- ^ Р. Паппалардо; Х. Самельсон; А. Лемпицки (1970). «Длинноимпульсное лазерное излучение из родамина 6G с использованием циклооктатетраена». Applied Physics Letters . 16 (7): 267– 269. Bibcode : 1970ApPhL..16..267P. doi : 10.1063/1.1653190.