Азид цезия
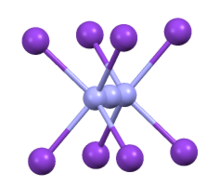 Координационная сфера азида в CsN 3 | |
| Имена | |
|---|---|
| Название ИЮПАК азид цезия | |
| Другие имена азид цезия | |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.041.072 |
| Номер ЕС |
|
CID PubChem |
|
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Свойства [1] | |
| CSN 3 | |
| Молярная масса | 174,926 г/моль |
| Появление | бесцветные иглы |
| Плотность | 3,5 г/см 3 |
| Температура плавления | 310 °C (590 °F; 583 К) |
| 224,2 г/100 мл (0 °C) | |
| Структура [2] | |
| четырехугольный | |
| I4/mcm, № 140 | |
а = 6,5412 Å, с = 8,0908 Å | |
Формульные единицы ( Z ) | 4 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Азид цезия или цезиевый азид — неорганическое соединение цезия и азота . Это соль азида с формулой CsN3 .
Структура
CsN 3 принимает ту же структуру, что и KN 3 , RbN 3 и TlN 3 , кристаллизуясь в тетрагональной искаженной структуре хлорида цезия, где каждый ион азида координируется с восемью катионами металла, а каждый катион металла координируется с восемью конечными центрами N. [2] При нагревании до 151 °C он переходит в кубическую структуру. [3]
Приготовление и реакции
Азид цезия можно получить реакцией нейтрализации между азотистоводородной кислотой и гидроксидом цезия : [4]
CsOH + HN3 → CsN3 + H2O
В качестве основания также можно использовать карбонат цезия:
Cs 2 CO 3 + HN 3 → CsN 3 + CO 2 + H 2 O
Сульфат цезия реагирует с азидом бария с образованием нерастворимого сульфата бария и азида цезия:
Cs 2 SO 4 + Ba(N 3 ) 2 → 2CsN 3 + BaSO 4 ↓
Термическое разложение CsN 3 в вакууме может быть использовано как метод получения металлического цезия высокой чистоты: [5]
2 CsN 3 → 2 Cs + 3 N 2
Ссылки
- ^ Перри, Дейл Л. (18 мая 2011 г.). Справочник неорганических соединений . CRC Press. стр. 110. ISBN 978-1-4398-1461-1.
- ^ аб Мюллер, Ульрих (1972). «Verfeinerung der Kristallstrukturen von KN 3 , RbN 3 , CsN 3 и TIN 3 ». Zeitschrift für anorganische und allgemeine Chemie . 392 (2): 159–166 . doi :10.1002/zaac.19723920207.
- ^ Макинтайр, Дж. Э. (ред.). Словарь неорганических соединений, том 3: C 46 – Zr . Chapman & Hill. стр. 3096. ISBN 0-412-30120-2.
- ^ Штойдель, Р.; Шенк, PW (1975). «Стикстофф». Брауэр, Георг (ред.). Handbuch der Präparativen Anorganischen Chemie, 3. Auflage, Band I. Ф. Энке. п. 458. ИСБН 3-432-02328-6.
- ^ Блаттер, Фриц; Шумахер, Эрнст (15 января 1986 г.). «Производство цезия высокой чистоты». Журнал менее распространённых металлов . 115 (2): 307– 313. doi :10.1016/0022-5088(86)90153-0.