Аминоаллил нуклеотид

Аминоаллиловый нуклеотид — это нуклеотид с модифицированным основанием, содержащим аллиламин . Они используются при пост-маркировке нуклеиновых кислот методом флуоресцентной детекции в микрочипах . Они реагируют с группой эфира N-гидроксисукцинимида , которая помогает прикрепить флуоресцентный краситель к первичной аминогруппе нуклеотида. Эти нуклеотиды известны как 5-(3-аминоаллил ) -нуклеотиды, поскольку аминоаллильная группа обычно присоединена к углероду 5 пиримидинового кольца урацила или цитозина . Первичная аминогруппа в аминоаллильном фрагменте является алифатической и, таким образом, более реакционноспособной по сравнению с аминогруппами, которые непосредственно присоединены к кольцам ( ароматическим ) оснований. Общие названия аминоаллиловых нуклеозидов изначально сокращаются до aa- или AA- для обозначения аминоаллила. 5-углеродный сахар указывается с или без строчной буквы «d», что указывает на дезоксирибозу , если она включена, или на рибозу, если нет. Наконец, указаны азотистое основание и количество фосфатов (т.е. аа-УТФ = аминоаллилуридинтрифосфат ).
История

Целью объединения флуоресценции и нуклеиновых кислот было обеспечение неизотопной метки , которая может быть обнаружена для изучения ДНК или РНК . Этот тип маркировки позволяет ученым изучать ДНК или РНК в их структуре, функции или образовании с другими нуклеиновыми кислотами. [2] Первая базовая модификация для флуоресцентной маркировки произошла в 1971 году с 4-тиоуридином и 4-тиоурацилом. [3] Это исследование наряду с другими, которые включали различные типы прямой и непрямой маркировки через: аналоги , добавление через ферменты или другие методы, сделало маркировку нуклеотидов намного более безопасной для ученых, изучающих ДНК. [2]
По мере того, как приборы и технологии в области ДНК-микрочипов становятся все более продвинутыми , для дальнейших научных исследований потребуются более совершенные реагенты и методы. Было показано, что флуоресцентная маркировка с помощью Cy3 является недостаточной и искажает результаты; вместо этого был выбран метод включения аминоаллиловых нуклеотидов. Использование аминоаллиловых нуклеотидов в качестве непрямой флуоресцентной маркировки, по-видимому, сводит на нет проблемы с чувствительностью, наблюдаемые при цианиновой маркировке . [4]
Синтез
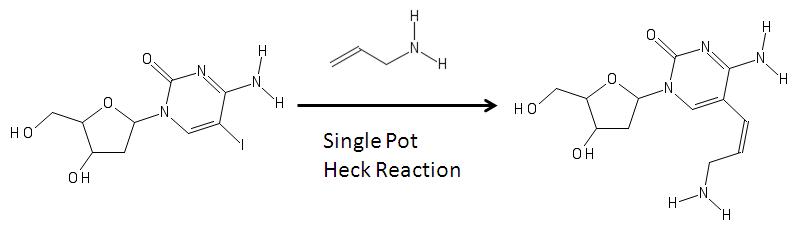
Аминоаллильные нуклеозиды можно синтезировать с помощью реакции Хека , как показано на рисунке ниже. [5]
На изображении выше слева находится модифицированный нуклеозид с йодом (йод добавляется посредством электрофильного галогенирования ) в пятом углероде пиримидинового кольца. Его образование может быть связано с реакцией с аллиламином, и различные реагенты посредством связи Хека способны удалить галогеновую группу из основания и добавить аллиламин, чтобы стать аминоаллиловым нуклеозидом, показанным справа. [5] Продукт справа затем используется в молекулярной биологии для синтеза РНК. [4] [6] [7]
Другие реакции включают использование синтеза в одном сосуде с другими галогенами . [8]
Реакция
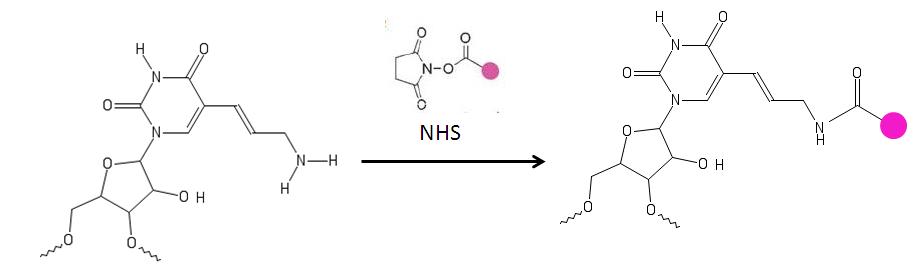
Первичный амин на аминоаллильном нуклеотиде реагирует с аминореактивными красителями [9], такими как цианин и запатентованные красители [10] [11] , которые содержат реактивную уходящую группу, такую как сукцинимидиловый эфир ( NHS ). Аминогруппы, непосредственно присоединенные к кольцу основания, не затрагиваются. Эти нуклеотиды используются для маркировки ДНК. [4] [6] [10] [11] [12]
Использует
Аминоаллил NTP используются для непрямой маркировки ДНК в ПЦР , ник-трансляции , удлинении праймеров и синтезе кДНК . [13] Эти меченые NTP полезны из-за их применения в лабораториях молекулярной биологии, где они не имеют возможности работать с радиоактивным материалом. Например, 5-(3-аминоаллил)-уридин (AA-UTP) более эффективны для высокоплотной маркировки ДНК, чем для предварительной маркировки ДНК. После ферментативного добавления NTP можно добавить флуоресцентные красители аминных реагентов для обнаружения молекулы ДНК. [7] При включении в молекулы ДНК или РНК ДНК/РНК- полимеразой 5-(3-аминоаллил)-UTP обеспечивает реактивную группу для добавления других химических групп. Таким образом, аминоаллил модифицированную ДНК или РНК можно пометить любым соединением, которое имеет аминореактивную группу. aa-NTP, включенные в ДНК/РНК в сочетании с реагентами для связывания вторичного красителя, могут использоваться для анализа массива. [6]
cDNA полагается на аминоаллильную маркировку для целей обнаружения. Хотя прямая маркировка dNTP является самым быстрым и дешевым методом флуоресцентной маркировки, она невыгодна, поскольку последовательность позволяет использовать только один модифицированный нуклеотид. Другим недостатком прямой маркировки являются громоздкие нуклеотиды, однако это можно преодолеть с помощью непрямой маркировки с использованием аминоаллильных модифицированных нуклеотидов. [14] Простым способом проверки успешности маркировки является цвет; Хорошая маркировка приведет к появлению видимого синего (Cy5) или красного (Cy3) цвета в конечном материале. [15]

Другой процесс, который использует аминоаллиловую маркировку, — это NASBA (Nucleic Acid Sequence Based Amplification), высокочувствительная технология амплификации РНК. В этом конкретном случае модифицированные РНК aaUTP были помечены флуоресцентным рынком Cy3. NASBA в сочетании с аминоаллил-UTP-маркировкой очень полезен для многих различных областей микробной диагностики, включая мониторинг окружающей среды , обнаружение биологических угроз, мониторинг промышленных процессов и клиническую микробиологию. [16] ДНК-микрочип — это еще один метод, который использует именно AA-NTP, что делает тестирование ДНК-микрочипов более быстрым и дешевым. [12]
Постсинтезная маркировка позволяет избежать проблем, возникающих при прямом ферментативном включении Cy-меченых dNTP, путем создания зондов с одинаковой эффективностью маркировки. При непрямой маркировке модифицированные амином NTP включаются во время обратной транскрипции , амплификации РНК или ПЦР . Аминоаллил-NTP включаются с такой же эффективностью, как и немодифицированные NTP во время полимеризации. [17] [18]
Проблемы с маркировкой: Аминогруппа в аминоаллил-модифицированном нуклеотиде реагирует с красителями, такими как цианиновый ряд, или другими запатентованными красителями. Проблема возникает, когда красители реагируют с буферными агентами , которые необходимы для надлежащего хранения нуклеотидов. Однако для решения этой проблемы можно использовать карбонатный буфер. [19]
Смотрите также
Ссылки
- ^ Хоган, Дэниел Дж.; Риордан, Дэниел П.; Гербер, Андре П.; Хершлаг, Дэниел; Браун, Патрик О. (2008). «Разнообразные РНК-связывающие белки взаимодействуют с функционально связанными наборами РНК, предполагая обширную регуляторную систему». PLOS Biology . 6 (10): e255. doi : 10.1371/journal.pbio.0060255 . PMC 2573929 . PMID 18959479.
- ^ ab Kricka, LJ; Fortina, P (апрель 2009 г.). «Аналитическая родословная: «первые» в флуоресцентной маркировке нуклеозидов, нуклеотидов и нуклеиновых кислот». Клиническая химия . 55 (4): 670–83 . doi : 10.1373/clinchem.2008.116152 . PMID 19233914.
- ^ Secrist III, John A.; Jorge R. Barrio; Nelson J. Leonard (3 декабря 1971 г.). «Присоединение флуоресцентной метки к 4-тиоурацилу и 4-тиоуридину». Biochemical and Biophysical Research Communications . 45 (5): 1262– 1270. doi :10.1016/0006-291x(71)90154-9. PMID 4332594.
- ^ abc Фаррелл, Роберт (2010-07-22). Методологии РНК: Лабораторное руководство по выделению и характеристике. Elsevier. стр. 597. ISBN 9780080454764.
- ^ ab Реддингтон, Марк; Дэниел Каннинген-Брайант (12 января 2011 г.). «Удобный синтез (E)-5-аминоаллил-2′-дезоксицитидина и некоторых родственных производных». Tetrahedron Letters . 52 (2): 181– 183. doi :10.1016/j.tetlet.2010.10.137.
- ^ abc Biosystems, Applied. "Модифицированный нуклеотид 5-(3-аминоаллил)-UTP" (PDF) .
- ^ ab Biotechnology, Trilink. "Модифицированные нуклеотиды" (PDF) . Архивировано из оригинала (PDF) 2017-02-23 . Получено 2014-04-22 .
- ^ Коре, Анилкумар Р.; Бо Янг; Баласубраманиан Шринивасан (13 ноября 2013 г.). «Синтез (E)-5-[3-аминоаллил]-уридин-5′-трифосфата с использованием фтора». Tetrahedron Letters . 54 (46): 6264– 6266. doi :10.1016/j.tetlet.2013.09.026.
- ^ ДеРизи, Джозеф. "Протокол связывания амино-аллилового красителя" (PDF) . Получено 9 апреля 2014 г.
- ^ ab AnaSpec, Inc. "Hiyte Fluor Brochure" (PDF) . Архивировано из оригинала (PDF) 13 апреля 2014 г. . Получено 9 апреля 2014 г. .
- ^ ab life technologies. "Аминоаллил dUTP" . Получено 24 марта 2014 г.
- ^ ab Xiang, CC; Kozhich, OA; Chen, M; Inman, JM; Phan, QN; Chen, Y; Brownstein, MJ (июль 2002 г.). «Случайные праймеры, модифицированные амином, для маркировки зондов для ДНК-микрочипов». Nature Biotechnology . 20 (7): 738– 42. doi :10.1038/nb0702-738. PMID 12089562.
- ^ Биотехнология, Trilink. «ДНК-маркировка».
- ^ Джибриэль, Абдулла (17 апреля 2012 г.). «Доступные варианты маркировки образцов нуклеиновых кислот в методах обнаружения на основе микрочипов ДНК». Briefings in Functional Genomics . II (4): 311– 318. doi : 10.1093/bfgp/els015 . PMID 22510454.
- ^ Грин, Майкл. «Молекулярное клонирование — лабораторное руководство». Cold Spring Harbor Laboratory Press.
- ^ Отт, Шелер; Барри Глинн (2009). «Флуоресцентная маркировка молекул tmRNA, амплифицированных NASBA, для применения в микрочипах». BMC Biotechnology .
- ^ 'т Хоэн, Пенсильвания; де Корт, Ф; ван Оммен, Дж.Дж.; ден Даннен, JT (1 марта 2003 г.). «Флуоресцентная маркировка кРНК для применения в микрочипах». Исследования нуклеиновых кислот . 31 (5): е20. дои : 10.1093/nar/gng020. ПМК 149842 . ПМИД 12595569.
- ^ Капоши-Новак, П.; Ли, Дж. С.; Микаэлян, А.; Патель, В.; Торгейрссон, СС (октябрь 2004 г.). «Олигонуклеотидный микроматричный анализ аминоаллил-меченых кДНК-мишеней из линейной РНК-амплификации». BioTechniques . 37 (4): 580, 582– 6, 588. doi : 10.2144/04374ST02 . PMID 15517970.
- ^ Soundy, P; Wheeler, C.; Latham, H. (2001). «Подготовка высокофлуоресцентных, равномерно маркированных зондов для гибридизации микрочипов с использованием метода аминоаллила с набором CyScribe Post-Labelling Kit». Life Science News . 9 : 17–19 .
Внешние ссылки
- Пример протокола Холли Беннет и Джо ДеРизи, созданный в Rosetta Informatics и модифицированный Крисом Сайделем. [1]
- ^ Seidel, Chris. "Подготовка флуоресцентного зонда" . Получено 24 марта 2014 г.