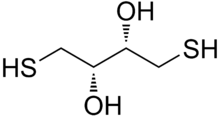
Дитиотреитол
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК (2 S ,3 S )-1,4-Бис(сульфанил)бутан-2,3-диол | |
| Другие имена ( 2S ,3S ) -1,4-Димеркаптобутан-2,3-диол D - трео -1,4-Димеркаптобутан-2,3-диол D - трео -1,4-Димеркапто-2,3-бутандиол 1,4-Дитио- D -треитол Реактив Клеланда Редуктакрил | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Информационная карта ECHA | 100.020.427 |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С4Н10О2S2 | |
| Молярная масса | 154,253 г/моль |
| Появление | Белое твердое вещество |
| Температура плавления | 42–43 °C (108–109 °F; 315–316 K) |
| Точка кипения | от 125 до 130 °C (от 257 до 266 °F; от 398 до 403 K) при 2 мм рт. ст. |
| Растворимый | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Дитиотреитол ( ДТТ ) — это сероорганическое соединение с формулой (CH(OH)CH 2 SH) 2 . Бесцветное соединение, классифицируется как дитиол и диол . ДТТ — это окислительно-восстановительный реагент, также известный как реагент Клеланда , в честь У. Уоллеса Клеланда . [2] Реагент обычно используется в рацемической форме. Его название происходит от четырехуглеродного сахара , треозы . ДТТ имеет эпимерное («сестринское») соединение, дитиоэритритол (ДТЭ).
Синтез
Традиционный путь получения дитиотреитола (и его изомера дитиоэритрита) — сульфидирование чрезвычайно слезоточивого 1,4-дибромбут-2-ена . Современные промышленные синтезы вместо этого используют родственные эпоксиды и сероводород. [3]
Восстановитель
DTT является восстановителем ; после окисления он образует стабильное шестичленное кольцо с внутренней дисульфидной связью . Он имеет окислительно-восстановительный потенциал −0,33 В при pH 7. [1] Восстановление типичной дисульфидной связи происходит посредством двух последовательных реакций обмена тиол-дисульфид и проиллюстрировано ниже. Восстановление обычно не останавливается на смешанных дисульфидных видах, поскольку второй тиол DTT имеет высокую склонность замыкать кольцо, образуя окисленный DTT и оставляя восстановленную дисульфидную связь . Восстановительная способность DTT ограничена значениями pH выше 7, поскольку только отрицательно заряженная тиолатная форма -S − является реакционноспособной (протонированная тиоловая форма -SH не является); pKa тиоловых групп составляет 9,2 и 10,1.

Приложения
DTT используется в качестве восстанавливающего или «снимающего защиту» агента для тиолированной ДНК. Концевые атомы серы тиолированной ДНК имеют тенденцию образовывать димеры в растворе, особенно в присутствии кислорода. Димеризация значительно снижает эффективность последующих реакций связывания, таких как иммобилизация ДНК на золоте в биосенсорах. Обычно DTT смешивают с раствором ДНК и дают ему прореагировать, а затем удаляют фильтрацией (для твердого катализатора) или хроматографией (для жидкой формы). Процедуру удаления DTT часто называют «обессоливанием». Обычно DTT используется в качестве защитного агента, который предотвращает окисление тиоловых групп .
DTT часто используется для восстановления дисульфидных связей белков и, в более общем плане, для предотвращения образования внутримолекулярных и межмолекулярных дисульфидных связей между остатками цистеина белков. Однако даже DTT не может восстановить скрытые (недоступные для растворителя) дисульфидные связи, поэтому восстановление дисульфидных связей иногда проводят в денатурирующих условиях (например, при высоких температурах или в присутствии сильного денатуранта, такого как 6 М гуанидинхлорид , 8 М мочевина или 1% додецилсульфат натрия ). DTT часто используется вместе с додецилсульфатом натрия в SDS-PAGE для дальнейшей денатурации белков путем восстановления их дисульфидных связей, чтобы обеспечить лучшее разделение белков во время электрофореза . Благодаря способности восстанавливать дисульфидные связи DTT можно использовать для денатурации CD38 на эритроцитах. DTT также денатурирует антигены в системах групп крови Kell, Lutheran, Dombrock, Cromer, Cartwright, LW и Knops. Наоборот, воздействие растворителя на различные дисульфидные связи можно оценить по скорости их восстановления в присутствии DTT.
DTT также может использоваться в качестве окислителя . Его главное преимущество заключается в том, что фактически не заселяются смешанные дисульфидные виды, в отличие от других агентов, таких как глутатион . В очень редких случаях может образовываться аддукт DTT , т. е. два атома серы DTT могут образовывать дисульфидные связи с различными атомами серы; в таких случаях DTT не может циклизоваться, поскольку у него нет таких оставшихся свободных тиолов.
Характеристики
DTT окисляется воздухом. Поэтому его обычно хранят и обрабатывают в инертной атмосфере, чтобы минимизировать окисление. Скорость окисления воздухом ниже при низких температурах. [4] Окисленный DTT демонстрирует сильный пик поглощения при 280 нм. Поскольку тиолы менее нуклеофильны, чем их сопряженные основания, тиоляты , DTT становится менее сильным нуклеофилом по мере снижения pH. (2 S )-2-амино-1,4-димеркаптобутан ( дитиобутиламин или DTBA), родственный дитиоловый восстанавливающий агент, несколько преодолевает это ограничение DTT. [5] Трис(2-карбоксиэтил)фосфин ( TCEP ) является альтернативным восстанавливающим агентом, который более стабилен и эффективен при низком pH, но он громоздкий и восстанавливает цистины в сложенных белках только медленно. [6]
Период полураспада DTT составляет 40 часов при pH 6,5 и 1,4 часа при pH 8,5 и 20 °C; его период полураспада еще больше уменьшается с ростом температуры. Присутствие EDTA (этилендиаминтетрауксусной кислоты) для хелатирования двухвалентных ионов металлов значительно продлевает период полураспада DTT в растворе. [7]
Смотрите также
- Дитиобутиламин (ДТБА)
- 2-меркаптоэтанол (БМЭ)
- TCEP
Ссылки
- ^ ab O'Neil MJ, ed. (2001). Merck Index: энциклопедия химикатов, лекарств и биологических препаратов (13-е изд.). Соединенные Штаты: Merck & Co, Inc. ISBN 0-911910-13-1.
- ^ Cleland WW (апрель 1964). «Дитиотреитол, новый защитный реагент для SH-групп». Биохимия . 3 (4): 480– 2. doi :10.1021/bi00892a002. PMID 14192894.
- ^ Гергель, Макс Г. Нестареющий Гергель (PDF) . С. 76–78 .
- ^ "NLM PubChem CID Index", Справочник по витамину D , John Wiley & Sons, Inc., стр. 239–244 , 2007, doi : 10.1002/9780470238165.indsp1 , ISBN 978-0-470-23816-5
- ^ Lukesh JC, Palte MJ, Raines RT (март 2012 г.). «Мощный, универсальный дисульфид-восстанавливающий агент из аспарагиновой кислоты». Журнал Американского химического общества . 134 (9): 4057– 9. doi :10.1021/ja211931f. PMC 3353773. PMID 22353145 .
- ^ Cline DJ, Redding SE, Brohawn SG, Psathas JN, Schneider JP, Thorpe C (декабрь 2004 г.). «Новые водорастворимые фосфины как восстановители пептидных и белковых дисульфидных связей: реакционная способность и проницаемость мембран». Биохимия . 43 (48): 15195– 203. doi :10.1021/bi048329a. PMID 15568811.
- ^ Стивенс Р., Стивенс Л., Прайс NC (1983). «Стабильность различных тиоловых соединений, используемых при очистке белков». Биохимическое образование . 11 (2): 70. doi :10.1016/0307-4412(83)90048-1.



