Викривирок
 | |
| Имена | |
|---|---|
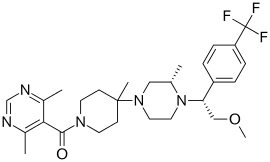
| Название ИЮПАК 5-({4-[(3 S )-4-{2-метокси-1-[4-(трифторметил)фенил]этил}-3-метилпиперазин-1-ил]-4-метилпиперидин-1-ил}карбонил)-4,6-диметилпиримидин | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChEMBL | |
| ChemSpider | |
| |
| МеШ | Викривирок |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С28Н38Ф3Н5О2 | |
| Молярная масса | 533,629 г/моль |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Vicriviroc , ранее называвшийся SCH 417690 и SCH-D, является ингибитором проникновения пиримидина CCR5 ВИЧ -1 . Он был разработан фармацевтической компанией Schering-Plough . Merck решила не добиваться одобрения регулирующих органов для использования у пациентов, ранее проходивших лечение, поскольку препарат не достиг первичных конечных точек эффективности на поздних стадиях испытаний. Клинические испытания продолжаются у пациентов, ранее не проходивших лечение от ВИЧ.
ВИЧ-1 фон
Механизмы ряда доступных анти-ВИЧ-препаратов предотвращают либо вирусный фермент обратной транскриптазы, либо фермент протеазы, позволяя вирусу проникнуть в клетку до того, как эти препараты подействуют. Однако ингибиторы CCR5, такие как викривирок, а также другие ингибиторы проникновения ВИЧ-1, подавляют начальные стадии жизненного цикла вируса. [1]
ВИЧ-1 запись
ВИЧ связывается и сливается с целевыми Т-клетками или макрофагами с помощью gp120 и gp41 , единственных двух белков, которые, как известно в настоящее время, присутствуют на поверхности вирусной оболочки . [2] Одна молекула каждого белка нековалентно связывается с другой на вирусной мембране, и три из этих единиц объединяются, образуя гетеротример gp120/gp41 , который удерживает gp41 в конформационно метастабильном состоянии . [2]
Слияние мембран начинается со связывания gp120 с CD4 , гликопротеином, который экспрессируется на поверхности клетки-мишени. [1] После связывания gp120 претерпевает конформационное изменение, которое вызывает образование сайта связывания корецептора на gp120. [2] Все штаммы ВИЧ-1 используют один из двух корецепторов: CCR5 или CXCR4; специфичность корецептора будет описана ниже. Как только gp120 связывается с корецептором, gp41 претерпевает конформационное изменение, которое высвобождает его из некогда метастабильного положения. [2] Это изменение заставляет гидрофобный N-конец белка gp41, также известный как домен слияния, встраиваться в мембрану клетки-хозяина и закреплять вирус на месте. [1] [2] Вставка gp41 в целевую клетку вызывает тонкую перестройку в белке gp41, которая объединяет две тримерные спиральные спирали, HR1 и HR2, образуя шестиспиральный пучок. [2] Пучок позволяет вирусной и клеточной мембранам сближаться и в конечном итоге сливаться вместе, что приводит к высвобождению вирусного генома в цитоплазму целевой клетки. [2]
Корецепторы и тропизм
Два корецептора, участвующих во входе ВИЧ-1, CCR5 и CXCR4 , принадлежат к большему семейству рецепторов, сопряженных с G-белком 7-трансмембранного сегмента ( 7TM ). [2] Таким образом, ВИЧ-1 можно классифицировать в соответствии со специфичностью к одному или другому корецептору. Вирус R5, также известный как М-тропный ВИЧ-1, нацелен на макрофаги и использует CCR5 в качестве корецептора. Вирус X4, или Т-тропный ВИЧ-1, нацелен на Т-клетки и использует CXCR4 в качестве корецептора. Также существуют штаммы ВИЧ-1 с двойной тропностью, которые используют оба рецептора. [1] Селективность к одному или другому корецептору особенно зависит от петли V3, высокоизменчивой и структурно гибкой области gp120, которая состоит приблизительно из 35 аминокислот. Тропизм можно предсказать с помощью метода 11/25, который ищет основные аминокислоты в положениях 11 и 25 в петле V3 и предполагает присутствие вируса X4. [2]
Однако использование корецепторов может меняться в течение инфекции. У 90% пациентов на ранних стадиях инфекции ВИЧ-1 есть вирус R5. Однако после пяти лет инфекции около 50% всех пациентов имеют определяемые количества вируса X4. [2] Причины этого переключения в настоящее время неясны. Однако вирусные изменения с использования корецепторов CCR5 на использование корецепторов CXCR4 связаны с более высокой скоростью потери Т-клеток CD4+, быстрой вирусной прогрессией и повышенной скоростью развития СПИДа и смерти. [1] [2]
CCR5-Δ32
Внимание к корецептору CCR5 как потенциальной мишени для лекарств от ВИЧ началось в 1996 году с открытием CCR5-Δ32, или CCR5 delta-32, мутационного варианта гена, кодирующего CCR5. [1] Делеция 32 пар оснований в этом гене приводит к нефункциональным рецепторам CCR5. [1] Хотя частота этой мутации среди популяций европеоидной расы составляет 0,0808, люди африканского или азиатского происхождения, по-видимому, не обладают этим аллелем. [1] Гомозиготы Δ32 или лица, обладающие двумя копиями варианта Δ32, не имеют функциональных рецепторов CCR5 и, следовательно, обладают высокой устойчивостью к ВИЧ-инфекции. [1] Лица, которые наследуют одну копию варианта Δ32 и одну копию нормального гена CCR5, являются гетерозиготами CCR5. [1] Гетерозиготы Δ32 по-прежнему восприимчивы к инфекции ВИЧ-1, но прогрессирование заболевания значительно замедлено по сравнению с теми, у кого две нормальные копии гена CCR5. Были разработаны антагонисты CCR5, которые вызывают деформацию корецептора CCR5, что приводит к неспособности клетки связываться с белком gp120 ВИЧ. [1]
SCH-C и викривирок
В 2001 году компания Schering-Plough разработала один из первых антагонистов CCR5 на основе малых молекул, SCH-C или SCH 351125, который подавлял репликацию ряда изолятов ВИЧ-1, которые использовали CCR5 в качестве корецептора для связывания. [3] Однако SCH-C вызывал умеренное, но дозозависимое удлинение скорректированного сердечного интервала QT ( QTc ), [4] что привело к изучению альтернативных соединений, чьи противовирусные и фармакокинетические свойства превосходили свойства соединений первого поколения, таких как SCH-C. Викривирок был обнаружен в ходе высокопроизводительного скрининга и анализа взаимосвязей структура-активность (SAR). [5] По сравнению с SCH-C, викривирок последовательно и более активно подавляет репликацию вируса, связывается с CCR5 с более высокой аффинностью, чем SCH-C, и обладает более низкой аффинностью к ионному каналу транскрипции гена человека ether-a-go-go , что может указывать на меньший риск сердечных эффектов. [4]
Метод действия
Викривирок является неконкурентным аллостерическим антагонистом CCR5. [6] Он принимается перорально и, поскольку эффективен в наномолярных концентрациях, его можно вводить один раз в день. [1] [6] Викривирок связывается с небольшим гидрофобным карманом между трансмембранными спиралями вблизи внеклеточной поверхности рецептора CCR5. [1] Связывание с этим карманом вызывает конформационное изменение внеклеточного сегмента CCR5 и предотвращает связывание gp120 с целевой клеткой, следовательно, предотвращая проникновение вируса в целевую клетку вообще. [ необходима цитата ]
Специфические связывающие взаимодействия между CCR5 и викривироком были впервые описаны в 2008 году. [7] В частности, трифторметилфенильная группа викривирока может сильно взаимодействовать с остатком I198 на пятой трансмембранной спирали (TM5) CCR5 посредством гидрофобных взаимодействий. Кроме того, электростатические взаимодействия могут образовываться между положительно заряженной третичной азотной группой викривирока и гидрофильной областью, обеспечиваемой остатком E238 на TM7 CCR5. Другие сильные взаимодействия, предсказанные группой, включают остаток Y108 на TM3 и Y251 на TM6. [ необходима цитата ]
Клинические испытания
В настоящее время викривирок проходит критические испытания. Викривирок продемонстрировал значительное снижение РНК ВИЧ у инфицированных R5 субъектов. Среднее снижение РНК ВИЧ от исходного уровня достигло 1,5 log 10 или более во всех группах лечения (10, 25, 50 мг, дважды в день ) в 14-дневном монотерапевтическом испытании у ВИЧ-инфицированных взрослых. [8]
Испытание фазы II на ВИЧ-1-инфицированных субъектах, не получавших лечения, было прекращено после того, как частота вирусологического рецидива у тех субъектов, которым вводили викривирок, увеличилась по сравнению с контрольными субъектами; однако дальнейшие исследования показывают, что вводимая доза викривирока могла быть слишком низкой. [2] В настоящее время проводится новое испытание фазы II на ВИЧ-1-инфицированных пациентах, не получавших лечения. [ необходима ссылка ]
48-недельное исследование фазы II (ACTG5211), изучающее безопасность и эффективность доз викривирока 5, 10 и 15 мг, показало, что у пациентов в группах лечения викривироком 10 мг и 15 мг было достигнуто медианное снижение вирусной нагрузки на 1,92 и 1,44 (log 10 копий/мл) и медианное увеличение количества клеток CD4 на 130 и 96 (клеток/мкл) от исходного уровня соответственно. У большего количества пациентов в группах викривирока вирус не поддавался обнаружению через 48 недель (РНК ВИЧ-1 <400/<50 копий/мл) по сравнению с пациентами в группе плацебо (57/37 процентов и 43/27 процентов против 14/11 процентов соответственно). [9]
Результаты 48-недельного исследования фазы II (VICTOR-E1), в котором изучалось применение доз викривирока 20 или 30 мг в дополнение к оптимизированной фоновой терапии (ОБТ) из более чем 3 препаратов, которая включала ингибитор протеазы, усиленный ритонавиром, были опубликованы в феврале 2008 года. Исследователи пришли к выводу, что «Викривирок 30 или 20 мг один раз в день плюс содержащее ритонавир ОБТ обеспечивали устойчивое подавление вируса у пациентов, ранее проходивших лечение, и увеличивали количество клеток CD4 независимо от количества активных препаратов в ОБТ». [10]
По состоянию на май 2008 года были начаты два исследования фазы III (VICTOR-E3 и VICTOR E4) с участием пациентов, ранее проходивших лечение. [11] Клинические испытания на поздней стадии не достигли своих основных конечных точек эффективности, и в январе 2010 года компания Merck решила не добиваться одобрения препарата регулирующими органами. [12] [13]
Опасения, связанные с антагонистами CCR5
Доступные данные клинических испытаний предполагают, что новый метод борьбы с ВИЧ-1 может быть найден в антагонистах CCR5. Исследования викривирока продолжаются, и другой антагонист CCR5, маравирок , в настоящее время находится на рынке. Однако возникли опасения относительно использования антагонистов CCR5 в качестве лечения ВИЧ, поскольку такие препараты могут способствовать появлению резистентных штаммов ВИЧ-1. Были выдвинуты две гипотезы о возможности такой резистентности: ВИЧ-1 может эволюционировать, чтобы использовать только CXCR4 в качестве корецептора; или ВИЧ-1 может мутировать таким образом, что он все еще способен взаимодействовать с CCR5, несмотря на присутствие антагониста рецептора. [1] Фактически, устойчивые к маравироку варианты ВИЧ-1 уже были получены in vitro путем мутации остатков в петле V3 gp120. [2]
Смотрите также
Ссылки
- ^ abcdefghijklmn Idemyor V (2005). «Ингибиторы проникновения вируса иммунодефицита человека (ВИЧ) (специфичные блокаторы CCR5) в разработке: являются ли они следующими новыми методами лечения?». HIV Clin Trials . 6 (5): 272– 7. doi : 10.1310/979L-39QP-NC9G-WFTF . PMID 16306033. S2CID 31384269.
- ^ abcdefghijklm Tsibris A (2007). "Обновление ингибиторов CCR5: научное обоснование, клинические доказательства и ожидаемое использование". Physicians' Research Network . Получено 2008-05-11 .
- ^ Palani A, Shapiro S, Clader JW, Greenlee WJ, Cox K, Strizki J, Endres M, Baroudy BM (2001). «Открытие 4-[(Z)-(4-бромфенил)-(этоксиимино)метил]-1'-[(2,4-диметил-3-пиридинил)карбонил]-4'-метил-1,4'-бипиперидина N-оксида (SCH 351125): перорально биодоступного человеческого антагониста CCR5 для лечения ВИЧ-инфекции». J Med Chem . 44 (21): 3339– 42. doi :10.1021/jm015526o. PMID 11585437.
- ^ ab Strizki JM, Tremblay C, Xu S, Wojcik L, Wagner N, Gonsiorek W, Hipkin RW, Chou CC, Pugliese-Sivo C, Xiao Y, Tagat JR, Cox K, Priestley T, Sorota S, Huang W, Hirsch M, Reyes GR, Baroudy BM (2005). "Открытие и характеристика Vicriviroc (SCH 417690), антагониста CCR5 с мощной активностью против вируса иммунодефицита человека типа 1". Antimicrobial Agents and Chemotherapy . 49 (12): 4911– 4919. doi :10.1128/AAC.49.12.4911-4919.2005. PMC 1315929 . PMID 16304152.
- ^ Tagat JR, McCombie SW, Nazareno D, Labroli MA, Xiao Y, Steensma RW, Strizki JM, Baroudy BM, Cox K и др. (2004). «Пиперазино-основанные антагонисты CCR5 как ингибиторы ВИЧ-1. IV. Открытие 1-[(4,6-диметил-5-пиримидинил)карбонил]-4-[4-[2-метокси-1(R)-4-(трифторметил)фенил]этил-3(S)-метил-1-пиперазинил]-4-метилпиперидина (Sch-417690/Sch-D), мощного, высокоселективного и перорально биодоступного антагониста CCR5». J Med Chem . 47 (10): 2405– 8. doi :10.1021/jm0304515. PMID 15115380.
- ^ ab AIDSinfo (2007). "Викривирок малеат". NIH . Получено 2008-05-11 .
- ^ Кондру Р., Чжан Дж., Цзи С., Мирзадеган Т., Ротштейн Д., Санкуратри С., Диосеги М. (2008). «Молекулярные взаимодействия CCR5 с основными классами низкомолекулярных антагонистов CCR5 против ВИЧ». Мол. Фармакол . 73 (3): 789–800 . doi :10.1124/mol.107.042101. PMID 18096812. S2CID 16267853.
- ^ Шюрманн Д. и др. (2007). «Противовирусная активность, фармакокинетика и безопасность викривирока, перорального антагониста CCR5, в течение 14-дневной монотерапии у ВИЧ-инфицированных взрослых». AIDS . 21 (10): 1293– 9. doi :10.1097/QAD.0b013e3280f00f9f. PMID 17545705. S2CID 6752651.
- ^ Бейкер Р. (2007). «Безопасность и эффективность экспериментального антагониста CCR5 Викривирока у пациентов с ВИЧ, прошедших лечение: 48-недельные результаты ACTG 5211». HIVandHepatitis.com. Архивировано из оригинала 23 августа 2007 г. Получено 11 мая 2008 г.
- ^ Highleyman L (2008). «Антагонист CCR5 Викривирок демонстрирует непрерывные преимущества и хорошую переносимость в течение 48 недель: испытание VICTOR-E1». HIVandHepatitis.com . Получено 11 мая 2008 г.
- ^ Бейкер Р. (2008). «Schering-Plough открывает набор на 2 фазы III испытаний экспериментального антагониста CCR5 Викривирока». HIVandHepatitis.com. Архивировано из оригинала 2007-11-12 . Получено 2008-05-11 .
- ^ Лофтус П. (2010). «Merck не будет добиваться одобрения FDA для препарата от ВИЧ». Wall Street Journal . wsj.com . Получено 21.01.2010 .
- ^ Пирсон Р. (2010-01-20). "Препарат Merck HIV от слияния Schering провалил испытания". reuters.com . Получено 2010-01-21 .


