Триэтилалюминий
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Триэтилалюман | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| Сокращения | ЧАЙ, [1] ЧАЙА, [2] ЧАЙА [3] |
| ChemSpider | |
| Информационная карта ECHA | 100.002.382 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
| Номер ООН | 3051 |
Панель инструментов CompTox ( EPA ) |
|
| |
| Характеристики | |
| С12Н30А12 | |
| Молярная масса | 228,335 г·моль −1 |
| Появление | Бесцветная жидкость. |
| Плотность | 0,8324 г/мл при 25 °C |
| Температура плавления | −46 °C (−51 °F; 227 K) |
| Точка кипения | от 128 до 130 °C (от 262 до 266 °F; от 401 до 403 K) при 50 мм рт. ст. |
| Реагирует | |
| Растворимость | Эфир, углеводороды, ТГФ |
| Опасности | |
| Охрана труда и техника безопасности (OHS/OSH): | |
Основные опасности | пирофорный |
| Маркировка СГС : | |
  | |
| Опасность | |
| Н250 , Н260 , Н314 | |
| Р210 , Р222 , Р223 , Р231+Р232 , Р260 , Р264 , Р280 , Р301+Р330+Р331 , Р302+Р334 , Р303+Р361+Р353 , Р304+Р340 , Р305+Р351+Р338 , Р310 , Р321 , Р335+Р334 , Р363 , Р370+Р378 , Р402+Р404 , Р405 , Р422 , Р501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | −18 °C (0 °F; 255 K) |
| Родственные соединения | |
Родственные соединения | Триметилалюминий Триизобутилалюминий |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Триэтилалюминий является одним из простейших примеров алюминийорганического соединения . Несмотря на свое название, соединение имеет формулу Al 2 ( C 2 H 5 ) 6 (сокращенно Al 2 Et 6 или TEA). Эта бесцветная жидкость является пирофорной . Это промышленно важное соединение, тесно связанное с триметилалюминием . [4] [5]
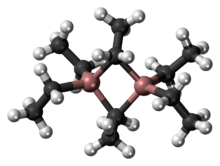
Структура и связь
Структура и связь в Al 2 R 6 и диборане аналогичны (R = алкил). Что касается Al 2 Me 6 , расстояния Al-C(концевой) и Al-C(мостиковый) составляют 1,97 и 2,14 Å соответственно. Центр Al является тетраэдрическим. [6] Атомы углерода мостиковых этильных групп окружены пятью соседями: углеродом, двумя атомами водорода и двумя атомами алюминия. Этильные группы легко взаимозаменяются внутримолекулярно. При более высоких температурах димер расщепляется на мономерный AlEt 3 . [7] [8]
Синтез и реакции
Триэтилалюминий может быть образован несколькими путями. Открытие эффективного пути стало значительным технологическим достижением. Многоступенчатый процесс использует алюминий, водородный газ и этилен , что можно резюмировать следующим образом: [4]
- 2 Al + 3 H 2 + 6 C 2 H 4 → Al 2 Et 6
Благодаря такому эффективному синтезу триэтилалюминий является одним из наиболее доступных алюминийорганических соединений.
Триэтилалюминий также может быть получен из сесквихлорида этилалюминия (Al 2 Cl 3 Et 3 ), который возникает при обработке алюминиевого порошка хлорэтаном . Восстановление сесквихлорида этилалюминия щелочным металлом , таким как натрий, дает триэтилалюминий: [9]
- 6 Al 2 Cl 3 Et 3 + 18 Na → 3 Al 2 Et 6 + 6 Al + 18 NaCl
Реактивность
Связи Al–C триэтилалюминия поляризованы до такой степени, что углерод легко протонируется , высвобождая этан: [10]
- Al2Et6 + 6HX → 2AlX3 + 6EtH
Для этой реакции можно использовать даже слабые кислоты, такие как терминальные ацетилены и спирты.
Связь между парой алюминиевых центров относительно слаба и может быть расщеплена основаниями Льюиса (L) с образованием аддуктов с формулой AlEt 3 L:
- Al2Et6 + 2L → 2 LAlEt3
Приложения
Предшественники жирных спиртов
Триэтилалюминий используется в промышленности в качестве промежуточного продукта в производстве жирных спиртов , которые преобразуются в моющие средства . Первый шаг включает олигомеризацию этилена по реакции Ауфбау , которая дает смесь соединений триалкилалюминия (упрощенно здесь как октильных групп): [4]
- Al 2 (C 2 H 5 ) 6 + 18 C 2 H 4 → Al 2 (C 8 H 17 ) 6
Затем эти триалкильные соединения окисляются до алкоксидов алюминия , которые затем гидролизуются:
- Al 2 (C 8 H 17 ) 6 + 3 O 2 → Al 2 (OC 8 H 17 ) 6
- Al2 ( OC8H17 ) 6 + 6H2O → 6C8H17OH + 2Al ( OH ) 3
Сокатализаторы в полимеризации олефинов
Большое количество TEAL и родственных алюминиевых алкилов используется в катализе Циглера-Натта . Они служат для активации катализатора переходного металла как восстановителя и алкилирующего агента . TEAL также выполняет функцию очистки воды и кислорода. [11]
Реагент в органической и металлоорганической химии
Триэтилалюминий имеет узкоспециализированное применение в качестве предшественника других алюминийорганических соединений, таких как диэтилалюминийцианид : [12]
Пирофорный агент
Триэтилалюминий воспламеняется при контакте с воздухом и воспламеняется и/или разлагается при контакте с водой и любым другим окислителем [13] — это одно из немногих веществ, достаточно пирофорных, чтобы воспламениться при контакте с криогенным жидким кислородом . Энтальпия сгорания , Δ c H°, составляет –5105,70 ± 2,90 кДж / моль [ 14] (–22,36 кДж/ г ). Его легкое воспламенение делает его особенно желательным в качестве воспламенителя ракетного двигателя . Ракета SpaceX Falcon 9 использует смесь триэтилалюминия и триэтилборана в качестве воспламенителя первой ступени. [1]
Триэтилалюминий , загущенный полиизобутиленом , используется в качестве зажигательного оружия , как пирофорная альтернатива напалму ; например, в обойме M74, удерживающей четыре ракеты для пусковых установок M202A1 . [15] В этом применении он известен как TPA, для загущенного пиротехнического агента или загущенного пирофорного агента . Обычное количество загустителя составляет 6%. Количество загустителя может быть уменьшено до 1%, если добавлены другие разбавители. Например, н -гексан может использоваться с повышенной безопасностью, делая соединение непирофорным до тех пор, пока разбавитель не испарится, после чего из паров триэтилалюминия и гексана образуется комбинированный огненный шар. [16] M202 был снят с вооружения в середине 1980-х годов из-за проблем с безопасностью, транспортировкой и хранением. Некоторые из них ограниченно применялись в войне в Афганистане против пещер и укрепленных соединений.
Смотрите также
- Триэтилборан , используемый в качестве воспламенителя в турбореактивных / прямоточных двигателях Pratt & Whitney J58 .
- Триметилалюминий
Ссылки
- ^ ab Mission Status Center, 2 июня 2010 г., 19:05 GMT, SpaceflightNow , дата обращения 2010-06-02, Цитата: «Фланцы соединят ракету с наземными резервуарами для хранения, содержащими жидкий кислород, керосиновое топливо, гелий, газообразный азот и источник воспламенителя первой ступени, называемый триэтилалюминий-триэтилборан, более известный как TEA-TEB».
- ^ "Gulbrandsen Chemicals, Металлические алкилы: триэтилалюминий (TEAl)". Gulbrandsen. Архивировано из оригинала 13 декабря 2017 г. Получено 12 декабря 2017 г.
Триэтилалюминий (TEAl) — это пирофорная жидкость...
- ^ Malpass, Dennis B.; Band, Elliot (2012). Введение в промышленный полипропилен: свойства, катализаторы, процессы. John Wiley & Sons. ISBN 9781118463208.
- ^ abc Krause, Michael J.; Orlandi, Frank; Saurage, Alfred T.; Zietz, Joseph R. (2000). "Aluminum Compounds, Organic". Энциклопедия промышленной химии Ульмана . Weinheim: Wiley-VCH. doi :10.1002/14356007.a01_543. ISBN 978-3527306732.
- ^ C. Elschenbroich (2006). Металлоорганические соединения . VCH. ISBN 978-3-527-29390-2.
- ^ Холлеман, А. Ф.; Виберг, Э. (2001). Неорганическая химия . Сан-Диего: Academic Press. ISBN 0-12-352651-5.
- ^ Васс, Габор; Тарчай, Дьёрдь; Мадьярфалви, Габор; Бёди, Андраш; Сепеш, Ласло (2002). «HeI-фотоэлектронная спектроскопия соединений триалкилалюминия и диалкилалюминия гидридов и их олигомеров». Металлоорганические соединения . 21 (13): 2751–2757. дои : 10.1021/om010994h.
- ^ Смит, Мартин Бристоу (1967-01-01). "Мономерно-димерные равновесия жидких алюминиевых алкилов. I. Триэтилалюминий". Журнал физической химии . 71 (2): 364–370. doi :10.1021/j100861a024. ISSN 0022-3654.
- ^ Краузе, М. Дж.; Орланди, Ф.; Сораж, А. Т.; Циц, Дж. Р., «Органические соединения алюминия» Wiley-Science 2002.
- ^ Эльшенбройх, К. «Металлоорганические соединения» (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ^ Деннис Б. Малпасс (2010). «Коммерчески доступные алкилы металлов и их использование в катализаторах полиолефинов». В Ray Hoff; Robert T. Mathers (ред.). Справочник по катализаторам полимеризации переходных металлов . John Wiley & Sons, Inc. стр. 1–28. doi :10.1002/9780470504437.ch1. ISBN 9780470504437.
- ^ Ватару Нагата и Ёсиока Мицуру (1988). «Цианиды диэтилалюминия». Органические синтезы; Собрание томов , т. 6, стр. 436.
- ^ Паспорт безопасности материала TEA Архивировано 14 ноября 2006 г. на Wayback Machine , просмотрено 27 марта 2007 г.
- ^ «Триэтилалюминий (CAS 97-93-8) — Химические и физические свойства по Cheméo».
- ^ M202A1 Flame Assault Shoulder Weapon (Flash), inetres.com
- ↑ Энциклопедия взрывчатых веществ и связанных с ними предметов , том 8, Армия США




![{\displaystyle {\ce {{1/2Al2Et6}+ HCN ->}}\ {\tfrac {1}{n}}{\ce {[Et2AlCN]}}_{n}+{\ce {C2H6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b73bebe835386dae4e699b7a9b65a76a0f6853f3)